生本高效课堂模式下整合信息技术探究氢氧化亚铁的制备
张 毅 何爱玲
2003年全国高考理综33题(22分)考查了氢氧化亚铁的制备,有很多专家也在不断探究氢氧化亚铁制备的方案、可行性、原理等,笔者在这里呈现的是组织学生在生本高效课堂模式下整合信息技术对该实验进行探究的过程。
一、呈现制备氢氧化亚铁的常规方案
1.多媒体投出,学生回答,师生共选定
反应原理:盐+碱→新碱+新盐。试剂:可溶性亚铁盐溶液—FeCl2溶液、FeSO4溶液等;可溶性碱溶液—NaOH溶液、KOH溶液、氨水等。师生选定FeSO4+2NaOH=Fe(OH)2↓+Na2SO4;Fe2++2OH-=Fe(OH)2↓。
实验操作:将NaOH溶液滴入FeSO4溶液中,先演示并讲解,力求规范基本操作,然后各组实验,强化试管、胶头滴管的使用及液体药品的取用等基本操作。
2.结合实验,学生描述实验现象,多媒体投出
有白色沉淀生成,迅速变成灰绿色,震荡后灰绿色变深,试管壁上生成红褐色物质。
二、呈现教师引领下学生设计、展示并交流制备氢氧化亚铁的改进方案
1.小组内讨论出现上述现象的原因
氢氧化亚铁很不稳定、极易被氧化,空气中的氧气很快将其部分氧化:4Fe(OH)2+O2+2H2O=4Fe(OH)3↓。因此制备实验的关键是创造“无Fe3+、无O2”的环境,防止氢氧化亚铁被氧化。改进措施:分析可能有氧气的各种情况,除去Fe3+、驱逐O2,想方设法避免与空气接触。
2.给出学生分组设计实验方案的要求
以小组为单位,各抒己见提出实验方案,全组讨论,最后统一方案,全组分工协作,记录实验现象和实验中遇到的问题。然后各组根据实验制成小课件展示设计的方案:一生结合多媒体课件和实物投影仪讲解实验装置、实验现象及结果处理,一生展示实物,一生在黑板上画装置图,其他学生质疑交流。
3.小课件1,多媒体投出方案一(如图1所示)
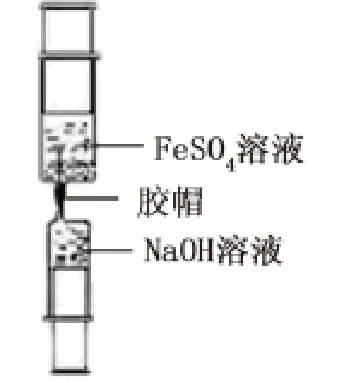
图1 Fe(OH)2的制备方案一
仪器药品:石棉网、烧杯、三脚架、玻璃棒、药匙、注射器、酒精灯、浓硫酸、NaOH固体、铁粉。
操作步骤:
①煮沸蒸馏水50 mL备用。
②稀释浓硫酸,稍冷趁热吸少量于已有1 g还原铁粉的10 mL针筒中,震荡,缓慢推动活塞至挤出少量液体。
③取约1 gNaOH固体送入另一针筒内,吸入煮沸过的蒸馏水5 mL,使其充分溶解,利用溶解放出的热气把空气排除,缓慢推动活塞至挤出少量液体。
④把针头插入②中的注射器内,慢慢挤压活塞,使FeSO4溶液和NaOH溶液充分接触,发现有白色絮状沉淀,黑色铁粉继续溶解并伴随着大量气泡冒出。
相关反应:F e+H2S O4=F e S O4+H2↑;FeSO4+2NaOH=Fe(OH)2↓+Na2SO4
优点:①尽量避免了Fe3+的生成。②尽量赶走O2,防止了与O2的接触,白色沉淀可保存2~3天。③废物(注射器)回收再利用,环保,密封性好。
缺点:铁粉难以完全溶解,影响白色沉淀的观察。
4.小课件2,多媒体投出方案二(如图2所示)
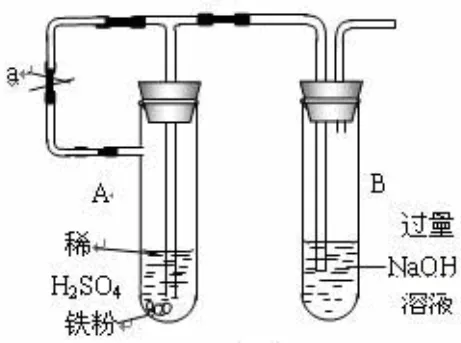
图2 Fe(OH)2的制备方案二
仪器药品:试管、量筒、酒精灯、胶头滴管、试管夹、药匙、镊子、纸槽、还原铁粉、稀硫酸(1:5)、NaOH固体。
有关操作与步骤及注意事项:
①首先向左端洁净的具支试管中加入适量的还原铁粉,加入6 mL稀硫酸(1:5),如图2所示组装好仪器,打开止水夹a,微微加热。
②反应后有气泡冒出,用一条燃着的木条靠近B短管部分,产生蓝色火焰说明气体是H2,则整套装置充满H2。
③夹紧止水夹,A试管中继续反应产生的气体将FeSO4溶液压入B中,产生白色沉淀。
优点:现象明显,反应放出的H2可以较长时间阻碍空气的进入,长时间保持Fe(OH)2不变色。
缺点:操作复杂,装置对气密性要求高,H2直接进入空气中,没有得到较好的回收利用。
学生情绪高涨,纷纷提出改进方案,如有的学生提出:此实验中H2携带杂质直接进入空气中会产生刺鼻气味且浪费,可以在试管口加一个气球用来收集H2,正符合当下“废物利用,绿色环保”的主题。学生现场制作Flash动画进行模拟,激发了学生用信息技术解决化学问题的欲望。
5.小课件3,多媒体投出方案三(如图3所示)
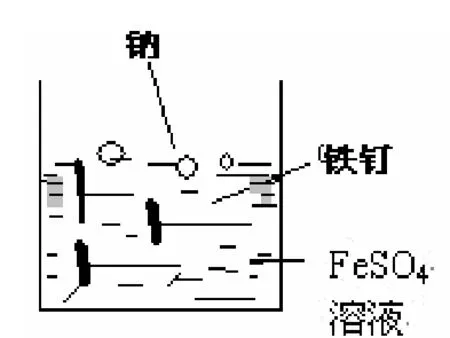
图3 Fe(OH)2的制备方案三
仪器药品:稀盐酸、稀硫酸、FeSO4晶体、镊子、滤纸、小刀、铁钉数枚、烧杯2只、胶头滴管。
操作步骤:
①提前一天将铁钉放入盛有稀盐酸的小烧杯中,以除去铁锈。
②向另一烧杯中加入约3 gFeSO4晶体,加水溶解,并将①中已除去铁锈的铁钉(防止FeSO4水解)放入其中,再滴入8滴稀硫酸。
③待无气泡冒出时向烧杯中加入钠,观察到溶液底部有大量白色沉淀,与液面接触的烧杯壁上出现灰绿色、红褐色。
相关反应:2 N a+2 H2O=2 N a O H+H2↑;FeSO4+2NaOH=Fe(OH)2↓+Na2SO4
学生求助其他组员:本实验反应时间长,液面与空气接触,部分沉淀被氧化,请大家提出改进措施。
学生讨论交流后确定改进方案:可在试管中进行该反应,加橡皮塞,用导管导出产生的H2并用气球收集备用,避免O2进入。问题是在试管中钠反应剧烈,容易引起爆炸。经上网查阅资料得知:钠球上方的空气被H2赶走至极稀少时,这种燃烧将难于进行,爆炸便无从发生。因此上述改进措施可行。
6.小课件4,多媒体投出方案四(如图4所示)

图4 Fe(OH)2的制备方案四
仪器药品:铁片、碳棒、电解槽、酒精灯、学生电源、三脚架、石棉网、导线、Na2SO4溶液、稀盐酸、植物油、火柴。
操作步骤:
(1)加热Na2SO4溶液,除去O2。
(2)将电极放入稀盐酸溶液中除去氧化层。
(3)将Na2SO4溶液倒入电解槽加入几滴植物油,以隔绝O2。
(4)按图4所示装置接通直流电源,将电压调至4~6 V,打开电源。
现象:两极间产生了白色沉淀,碳棒上有大量气体冒出,铁片逐渐溶解且下部出现黑色不溶物。
相关反应:
阴极:2H2O+2e-=H2↑+ 2OH-,阳极:Fe-2e-=Fe2+,阴极附近产生的OH-与阳极溶解产生的Fe2+结合生成Fe(OH)2,Fe2++2OH-= Fe(OH)2↓。
优点:阴极产生的还原性气体H2排出了溶液中的O2且阻止了空气中的O2进入溶液,可以较长时间保留Fe(OH)2白色沉淀。
缺点:铁片杂质较多,电极下有黑色物质,现象不明显。
三、结束语
学生是学习的主人,结合信息技术手段增大了课堂容量,学生的动手能力、观察能力、总结概括能力、表达能力、协作能力都有所提高。课代表根据课堂表现公布最佳小组团队,信息技术社团用摄像机镜头记录精彩的课堂,同步投放在大屏幕上,激起了学生的自豪感和荣誉感。教师及时表扬激励学生,鼓励他们以课堂为舞台,努力学习,不断探究。
[1] 宋心琦.普通高中课程标准实验教科书化学必修1[M].北京:人民教育出版社,2010.
[2] 乔国才.普通高中课程标准实验教科书化学必修1:教师教学用书[M].北京:人民教育出版社,2010.
[3] 吴明胜.探究制备氢氧化亚铁的实验方法[J].化学教育,2010(9):79.
[4] 矫可庆.金属钠与水反应的发散探究[EB/OL].[2011-11-07].http://www.pep.com.cn/gzhx/gzhxjs/jxyj_1/czsxjxyjjscg/201111/t20111107_1078804.htm.

