舒芬太尼联合右美托咪啶在22例骨科术后患者自控静脉镇痛中的效果观察
秦洪猛
(河南省南阳市中心医院麻醉科 473000)
手术后患者自控静脉镇痛(patient-controlled intravenous analgesia,PCIA)临床应用范围和适应证较为广泛,在术后急性疼痛的治疗中发挥着重要作用[1]。研究结果显示,PCIA多使用单一的阿片类药物,由于个体间的差异,部分患者镇痛效果不完善、不满意,为达到良好镇痛效果而增加剂量又会引起一系列不适,且存在多种不良反应如嗜睡、恶心呕吐、皮肤瘙痒、呼吸抑制等[2]。右美托咪啶为新一代高度选择性的α2肾上腺受体激动剂,同时具有较好的镇静、镇痛作用,且无明显的呼吸抑制等药物不良反应,临床上日益受到重视,已经在重症监护室(ICU)及麻醉诱导等得到广泛使用[3]。本研究选取单纯舒芬太尼和舒芬太尼联合右美托咪啶的2种不同药物配伍用于骨科术后患者,观察两组患者的镇痛、镇静效果,探讨其有效性、安全性、可行性,为手术术后镇痛提供最佳的药物配伍给药方案。
1 资料与方法
1.1 一般资料 选择2010年1月至2011年6月接受下肢骨科手术的患者44例,年龄51~72岁,平均(62.3±5.7)岁。采用随机数字法分为对照组和观察组,各22例,所有患者都在L2~3间隙穿刺行椎管内麻醉后进行手术,术后立即开启PCIA。纳入标准:择期下肢骨科手术、ASAⅠ~Ⅱ级、体质量65~75kg,手术时间3~4h;排除标准:糖尿病、高血压、冠心病等;急慢性呼吸系统疾病及血液系统疾病等;肝肾功、血脂、血常规、凝血功能异常等。本试验为双盲研究,研究者和患者对分组情况均不知情,很好地控制了受试者与观察者的偏倚。两组患者间的性别、年龄、体质量、并发症及患者身体状况等一般情况比较差异无统计学意义(P>0.05)。
1.2 方法 所有患者常规术前禁食、禁水8h,入室后小流量吸氧(2L/min),建立上肢静脉通道,连接多功能监护仪(Detex Ohmeda,美国),术中及术后用生命指标监护仪持续监测收缩压(SBP)、舒张压(DBP)、心率(HR)、血氧饱和度(SPO2)。在侧卧位下行蛛网膜下隙与硬脊膜外联合阻滞麻醉,穿刺点选择在L2~3腰硬联合置管,穿刺成功后注入试验量3~5mL,蛛网膜下麻醉的麻醉药选择0.5%布比卡因的重比重液8~12mg,硬脊膜外麻醉的麻醉药选择1%盐酸利多卡因和0.5%甲磺盐酸罗哌卡因的混合液。麻醉过程中每隔5min检测麻醉平面,控制在T10~S,手术中未使用镇静药物。按照补液规范术中补液2 400~2 500mL,其中晶体液1 600mL,胶体液750~900mL。手术结束前30min停止硬脊膜外给药,两组患者均在手术结束即刻开启PCIA(CBL+PCA,新乡市驼人医疗器械有限公司)。背景输注速率为2mL/h,单次自控PCA的量为0.5mL,锁定时间为10min,维持镇痛48h。对照组:采用单纯舒芬太尼(宜昌人福药业有限责任公司,批号:2110401)的PCIA药物配方,将舒芬太尼150μg用0.9%生理盐水稀释至100mL;观察组:采用舒芬太尼复合右美托咪啶(江苏恒瑞医药股份有限公司,批号:10020234)的PCIA药物配方,将舒芬太尼150μg和右美托咪啶500μg用0.9%生理盐水稀释至100mL。
1.3 观察指标
1.3.1 镇痛效果观察 从连接PCIA开始记录整个镇痛过程中的并发症及不良反应的种类、次数。记录自控PCIA泵的按压次数和其他镇痛药的需要次数。取入室(T1)、PCIA后6h(T2)、12h(T3)、24h(T4)、48h(T5)5个时间段记录SBP、平均动脉压(MAP)、HR、SPO2,观察PCIA镇痛的平稳程度。
1.3.2 患者满意程度测定 分别于 T1、T2、T3、T4、T55个时间段进行评分测定:(1)疼痛视觉模拟评分(pain visual analog test,VAS):在1根长10cm的直线上,0代表完全无疼痛,10代表最剧烈的疼痛,由患者根据其自觉疼痛程度在直线上做标记,记录长度(cm)。(2)Ramsay镇静评分:1分为不安静、烦躁;2分为安静合作;3分为嗜睡,能听从指令;4分为睡眠状态,但可唤醒;5分为呼唤反应迟钝;6分为深睡状态,呼唤不醒。其中2~4分镇静满意,5~6分镇静过度。(3)舒适度(bruggrmann comfort scale,BCS)评分:0分为持续疼痛;1分为安静时无痛,深呼吸或咳嗽时疼痛严重;2分为平卧安静时无痛,深呼吸或咳嗽时轻微疼痛;3分为深呼吸时也无痛;4分为咳嗽时也无痛。
1.4 统计学处理 采用SPSS18.0软件对所得数据进行分析,计量资料以±s表示。VAS疼痛评分属于等级资料,各组件采用非参数检验;组间采用单因素方差分析、组内比较采用两两比较的SNK(S)检验,与正常值比较应用单样本t检验;组间不良反应的发生率采用χ2检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 镇痛效果观察 (1)自控PCIA泵的按压次数及其他镇痛药的需要次数(中位数):按压次数(中位数)观察组为4次,对照组为8次,组间比较差异有统计学意义(P<0.05);额外使用镇痛药次数(中位数)观察组为1次,对照组为2次,两组间比较差异有统计学意义(P<0.05)。(2)并发症及不良反应:观察组不良发应发生率为9.1%(2/22),其中1例出现低血压(低血压标准:收缩压小于90mm Hg,舒张压小于60 mm Hg)。但经查为一过性的,恢复平稳,显著低于对照组的54.5%(12/22),两组比较差异有统计学意义(P<0.05),见表1。(3)血流动力学指标:观察组在5个时间点上SBP、MAP、HR、SPO2很平稳,组内各时间点比较差异无统计学意义(P>0.05)。观察组在T2时间点即PCIA后6h出现了血压下降且下降幅度较高、心率的变化也超出了正常范围,组间、组内比较差异均有统计学意义(P<0.05),见表2。

表1 两组患者不良反应比较[n(%),n=22]
表2 两组患者血流动力学指标比较(±s,n=22)
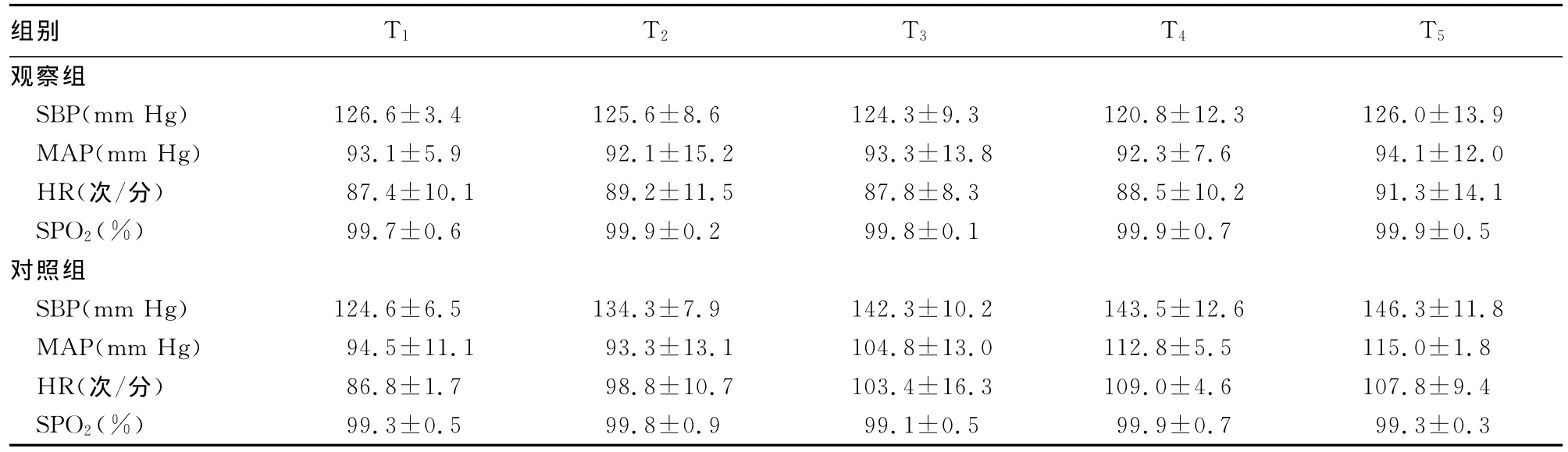
表2 两组患者血流动力学指标比较(±s,n=22)
组别 T1 T2 T3 T4 T5观察组SBP(mm Hg) 126.6±3.4 125.6±8.6 124.3±9.3 120.8±12.3 126.0±13.9 MAP(mm Hg) 93.1±5.9 92.1±15.2 93.3±13.8 92.3±7.6 94.1±12.0 HR(次/分) 87.4±10.1 89.2±11.5 87.8±8.3 88.5±10.2 91.3±14.1 SPO2(%) 99.7±0.6 99.9±0.2 99.8±0.1 99.9±0.7 99.9±0.5对照组SBP(mm Hg) 124.6±6.5 134.3±7.9 142.3±10.2 143.5±12.6 146.3±11.8 MAP(mm Hg) 94.5±11.1 93.3±13.1 104.8±13.0 112.8±5.5 115.0±1.8 HR(次/分) 86.8±1.7 98.8±10.7 103.4±16.3 109.0±4.6 107.8±9.4 SPO2(%) 99.3±0.5 99.8±0.9 99.1±0.5 99.9±0.7 99.3±0.3
表3 两组患者应用PCIA后VAS评分测定指标比较(±s,分)

表3 两组患者应用PCIA后VAS评分测定指标比较(±s,分)
组别 T1 T2 T3 T4 T5 1.0±0.3 4.1±1.1 2.9±1.0 2.0±1.1 1.2±1.1观察组 1.1±0.1 3.5±1.1 2.8±1.2 1.6±1.0 1.2±0.9 t 7.233 2.734 3.598 4.677 3.121 P对照组0.216 0.075 0.114 0.143 0.091
2.2 患者满意程度测定 (1)术后VAS评分测定:观察组与对照组比较术后PCIA镇痛各个时间点VAS评分均低,但两组间比较差异无统计学意义(P>0.05),见表3。(2)Ramsay镇静评分测定:观察组在T2和T3时间点上的Ramsay镇静评分优于对照组,镇静镇痛效果比较差异有统计学意义(P<0.05),见表4。(3)舒适度BCS评分测定:观察组在PCIA使用后24h时间段(T4)BCS评分在4分以上者占63.64%(14/22),明显高于对照的27.27%(6/22),组间比较差异有统计学意义(P<0.05);在其他4个时间段比较差异无统计学意义(P>0.05)。
表4 两组患者应用PCIA后Ramsay评分测定指标比较(±s,分)

表4 两组患者应用PCIA后Ramsay评分测定指标比较(±s,分)
组别 T1 T2 T3 T4 T5 3.5±1.3 5.8±1.6 6.0±0.2 4.2±2.3 3.8±1.6观察组 3.9±2.0 3.2±2.4 3.7±1.1 4.0±3.4 3.6±2.2 t 8.714 13.774 14.669 4.785 7.712 P对照组0.249 0.023 0.014 0.145 0.243
3 讨 论
右美托咪啶是新一代的高效、高选择性(α2∶α1=1 620∶1)[4]的α2肾上腺素受体激动药,为中枢性和外周性的选择性α2受体激动药,可用于临床上降压、镇静、镇痛、抗焦虑、抑制交感神经兴奋等,其受体作用特异性好,显著优于传统的α2肾上腺素受体激动药[5]。
近年来,研究发现该药有较好的麻醉辅助作用,受到临床麻醉科医生的青睐,在全身麻醉、椎管内麻醉、神经阻滞、围术期镇痛、治疗撤药反应等方面得到了广泛的应用[6]。本研究结果显示,舒芬太尼在术后自控PCIA镇痛中联合右美托咪啶,血压低、呕吐等不良反应少,疼痛VAS评分及舒适度评分较好,且额外按压PCIA泵的次数和需要其他镇痛药的次数少,较单独使用舒芬太尼的组别差异有统计学意义,说明右美托咪啶在术后镇痛中有较好的作用,不良反应少且具有较高的安全性。
下肢骨科手术术后疼痛剧烈难忍。为了防止关节僵硬、血栓形成、褥疮等近期术后并发症,需要患者积极配合进行适当的功能锻炼,因而对术后镇痛效果的要求较高,鉴于此,本研究选择在骨科手术术后患者应用自控PCIA镇痛以便进行功能锻炼。要求镇痛效果满意,患者的血流动力学稳定,各种不良反应如恶心呕吐、低血压等较少,完全抑制骨科手术的伤害性刺激引起的术后应激反应,尽量减少应激反应所致的心血管并发症,便于患者进行术后功能锻炼,打造舒适麻醉的理念。而新型α2肾上腺素受体激动药右美托咪啶能抑制交感神经兴奋[7-10],并且与阿片类镇痛药物具有协同作用,其机制是激活了脊髓α2受体亚型从而减弱疼痛信号从外周到中枢的传递,因而有很好的镇痛镇静作用,能较好辅助舒芬太尼用在术后患者自控静脉镇痛中,降低PCIA泵自控按压次数,镇痛效果完善,利于患者进行功能锻炼。
[1]Dahl JB,Moiniche S.Pre-emptive analgesia[J].Br Med Bull,2004,71(1):13-27.
[2]Ruan XC,Xu LX,She SZ,et al.Effects of epidural clonidine pretreatment in epidural patient-controlled analgesia using sufentanil combined with levobupivacaine[J].Zhon-ghua Yi Xue Za Zhi,2008,88(9):583-586.
[3]Hall RI,Sandham D,Cardinal P,et al.Propofol vs midazolam for ICU sedation:a canadian multicenter randomized trial[J].Chest,2009,119(4):1151-1159.
[4]Butkowasa K,Kanpik P,Misiolek A.The effect of dexmedetomdine sedation on brachial plexus block in patients with endstage renal disease[J].Eur J Anaesthesiol,2009,26(10):851-855.
[5]Wijeysundera DN,Bender JS,Beattie WS.Alpha-2adrenergic agonists for the prevention of cardiac complications among patients undergoing surgery[J].Cochrane Database Syst Rev,2011,7(4):841-846.
[6]Guinter JR,Kristeller JL.Prolonged infusions of dexmedetomidine in critically ill patients[J].Am J Health Syst Pharm,2010,67(15):1246-1253.
[7]Talke P,Chen R,Thomas B,et al.The hemodynamic and adrenergic effects of perioperative dexmedetomidine infusion after vascular surgery[J].Anesth Analg,2010,90(4):834-839.
[8]Farag E.Dexmedetomidine in the neurointensive care unit[J].Discov Med,2010,9(1):42-45.
[9]Shehabi Y,Ruettimann U,Adamson H,et al.Dexmedetomidine infusion for more than 24hours in critically ill patients:sedative and cardiovascular effects[J].Intensive Care Med,2004,30(12):2188-2196.
[10]Greening A,Mathews L,Blair J.Apparent dexmedetomidine-induced polyuric syndrome in an achondroplastic patient undergoing posterior spinal fusion[J].Anesth Analg,2011,113(6):1381-1383.

