沉淀法制备磷钼酸铵及其对Cs+的吸附特性研究
黄召亚 张 东 谭昭怡
(中国工程物理研究院核物理与化学研究所 绵阳 621900)
沉淀法制备磷钼酸铵及其对Cs+的吸附特性研究
黄召亚 张 东 谭昭怡
(中国工程物理研究院核物理与化学研究所 绵阳 621900)
采用两种沉淀方法合成了磷钼酸铵(Ammonium Molybdophosphate, AMP, (NH4)3P(Mo3O10)4·xH2O),通过XRD和FT-IR等手段对其进行了表征和比较,获得了具有理想纯度的AMP;研究了温度、时间、竞争离子等条件对AMP吸附Cs+的影响。结果显示,AMP对Cs+的吸附在10 min即可达到动态平衡;Cs+在AMP上的吸附过程可很好地用准二级动力学方程描述(R2>0.999);Na+、K+的存在对吸附容量有明显影响,其中K+的竞争作用更为明显,表明AMP对Cs的吸附为Cs+与[NH4]+的离子交换过程。
AMP, Cs+, 吸附
随着核工业、核技术的发展及核能的开发利用,产生了大量放射性废液(水)。137Cs是高放废液中半衰期较长(T1/2=30 a)的高释热裂变产物核素,在对放射性废液(水)最终处置前将其去除是必不可少的环节。离子交换和吸附法是目前国内外去除溶液中Cs+的主要方法[1,2],沸石、多价金属磷酸盐、杂多酸盐、不溶性亚铁氰化物、硅钛酸盐等无机离子交换剂由于其对Cs+的高选择性、高吸附容量和良好的稳定性而受到广泛关注[3–8]。
AMP是具有Keggin结构的典型十二钼磷杂多酸盐,基本结构是四组三个钼氧八面体,每一组中三个钼氧八面体共用顶角上的氧原子,结合成Mo3O10单元,[NH4]+位于其结构的空隙中。Archer等[9,10]利用水热法合成了AMP,并研究其在弱酸溶液中的溶解度和杂多酸铵盐的阳离子交换性能。其合成过程比较复杂,且受当时表征手段的限制。Lehto[11]研究了多种离子在AMP上的吸附和分离,发现AMP对Cs的吸附容量约为1.0 mmol/g,由此推测形成了Cs2NH4PMo12O40,文献[12]对此进行了验证。田国新等[13]合成了更适于柱操作的AMP粒状结晶,但其对Cs+的静态和动态交换性能仅为0.63和0.55 mmol/g。为进一步研究和验证AMP对Cs+的吸附特性及吸附机理,本文采用两种沉淀方法制备了AMP,并通过XRD和FTIR表征和分析,得到理想的AMP。在此基础上,研究了其对溶液中Cs+的吸附行为及温度、吸附时间和竞争阳离子等对吸附过程的影响。
1 实验材料与方法
1.1试剂与仪器
(NH4)6Mo7O24·4H2O、K4P2O7·3H2O、CsCl、NaCl、KCl等所用试剂均为分析纯,实验用水为去离子水。
主要仪器:Mettler-Toledo SevenMult精密酸度计(瑞士Mettler-Toledo公司生产);AA700原子吸收光谱仪(美国PerkinElmer公司生产);X'Pert Pro MPD X射线衍射仪(荷兰Philips公司生产);Nicolet 6700红外光谱仪(美国Thermo Fisher Scientific公司生产)。
1.2 AMP的制备
AMP-1:将0.025 mol (NH4)6Mo7O24·4H2O溶于180 mL去离子水中;在溶液中缓慢滴加30 mL含有0.0125 mol K4P2O7·3H2O的溶液,边加边搅拌;在混合溶液中滴加浓HNO3至沉淀完全后继续搅拌1 h,陈化18 h后过滤出沉淀,分别用1 mol/L HNO3和去离子水洗涤,在(40±1)ºC下干燥。
AMP-2:将0.018 mol (NH4)6Mo7O24·4H2O溶于300 mL去离子水中;在溶液中缓慢滴加7.5 mL 2 mol/L 的H3PO4,边加边搅拌;用浓HNO3调节混合溶液的pH至1,出现黄色沉淀,在室温下持续搅拌1.5 h后陈化16 h;过滤出沉淀,用1 mol/L 的HNO3溶液洗涤3次,再用去离子水洗涤1次,过滤出沉淀,在(40±1)ºC下干燥,即得黄色粉末状AMP。
1.3吸附实验及吸附动力学
1.3.1 吸附量的确定
吸附实验所用AMP均为AMP-2。按各实验要求称取一定质量的AMP,加入盛有一定体积和浓度的Cs+溶液,在水浴恒温磁力搅拌器中恒温搅拌一定时间后,移取一定体积溶液进行过滤、稀释,然后用原子吸收仪测量吸附前后溶液中Cs+浓度,结果以吸附量q(mg/g)表示为:q = (c0−ct)×V/m。其中,c0为溶液中Cs+的初始浓度(mg/L),ct为吸附后溶液中Cs+的浓度,V为吸附溶液的体积(L),m为AMP质量(mg)。
1.3.2 准二级动力学
准二级动力学方程表达式为t/qt= t/qe+1/kq2e。式中,qt和qe分别为t时刻和平衡时的吸附量(mg/g);k为准二级速率常数(min·g/mg)。利用t/qt对t作线性拟合,可得准二级动力学方程,并由斜率获得理论平衡吸附量。
2 实验结果与讨论
2.1 AMP的表征
图1为所制备的两种AMP的XRD衍射谱图与(NH4)3P(Mo3O10)4·xH2O的标准谱图。由图可见,AMP-1的峰形较尖锐,但杂峰较多,说明含一种或多种杂质,可能是合成过程中形成的磷酸盐或钼酸盐。AMP-2的XRD衍射峰的位置和峰强与标准图谱符合得很好,峰形尖锐且无明显杂峰,说明AMP-2的纯度优于AMP-1。
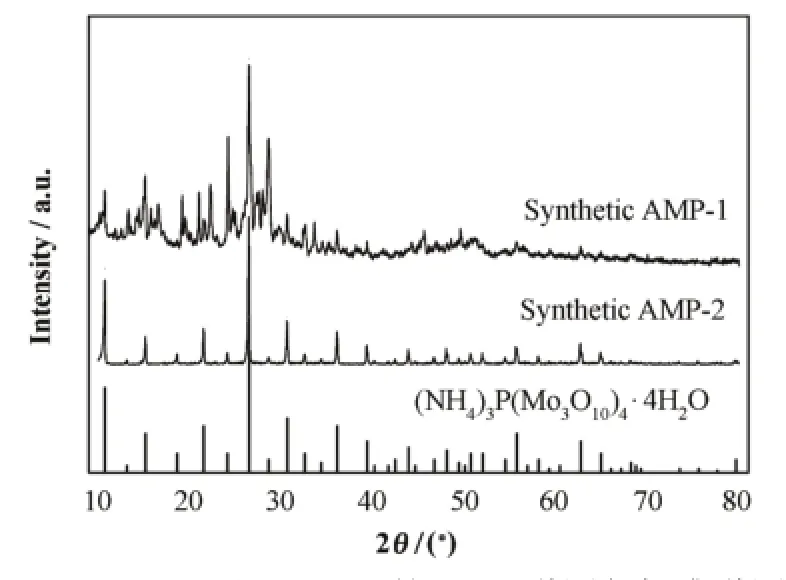
图1 AMP-1和AMP-2的XRD谱图与标准谱图Fig.1 XRD spectra of the synthetic AMP-1, AMP-2 and (NH4)3P(Mo3O10)4·4H2O.
图2 是合成的AMP的FT-IR谱图。分析AMP-2的红外谱图,3430.39 cm–1和1616.15 cm–1处的两个吸收峰分别为H-O-H伸缩振动和弯曲振动引起的吸收峰,说明所合成的磷钼酸铵中含有结晶水;3206.16 cm–1和1404.44 cm–1处的两个吸收峰分别为N-H伸缩振动吸收峰和弯曲振动吸收峰,这表明了[NH4]+的存在;1063.60、962.81、867.91和790.88 cm–1的几个吸收峰分别与[PMo12O40]3–Keggin结构的特征峰(1068、962、869和785 cm–1)[14]吻合较好,说明存在完整的[PMo12O40]3–骨架结构;IR图谱中并没有出现其他杂峰,说明合成的AMP纯度较高。而AMP-1的谱图中,869 cm–1和785 cm–1处两个吸收峰不明显,且在680 cm–1处出现杂质吸收峰,可能是磷酸盐或钼酸盐杂质引起的。结合XRD谱图对比,AMP-2的纯度优于AMP-1。

图2 AMP-1和AMP-2的FT-IR谱图Fig.2 FT-IR spectra of the synthetic AMP-1, AMP-2.
2.2吸附动力学结果
2.2.1 温度和接触时间对吸附的影响
温度和接触时间对吸附的影响示于图3。由图可见,吸附量在前10 min上升明显,其后上升缓慢。可以认为,在120 min时吸附过程达到动态平衡。在Cs+初始浓度为80 mg/g、固液比为400 mg/L条件下,吸附容量最高可达125.7 mg/g,与文献[11]结果相符,高于粒状AMP结晶对Cs+的吸附容量。随着温度升高,AMP对Cs的平衡吸附容量有减小的趋势。

图3 温度和吸附时间对吸附的影响Fig.3 Effect of temperature and contact time on the uptake of Cs+. (c0 = 80 mg/L, V = 0.5 L, m = 200 mg)
2.2.2 准二级动力学拟合
用准二级速率方程对不同温度下吸附过程的拟合结果见图4,拟合曲线的相关系数R2分别为0.99996、0.99975、0.99975。由拟合曲线的斜率计算得到30ºC、40ºC、50ºC下的平衡吸附量分别为125.8、123.9、120.6 mg/g。
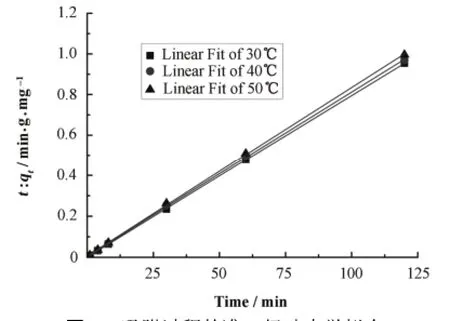
图4 吸附过程的准二级动力学拟合Fig.4 Simulated results using pseudo second-order kinetic equation.(c0 = 80 mg/L, V = 0.5 L, m = 200 mg)
因为吸附过程的活化熵变ΔSo和活化焓变ΔHo受温度的影响可忽略不计[15],根据Arrhenius公式有:lnk = −Ea/rT+c。其中,k为反应速率常数;Ea为吸附活化能(kJ·mol–1);r为理想气体常数(8.314×10–3kJ·K–1·mol–1);T为绝对温度。取k为准二级吸附速率常数,以lnk对1/T作图,由斜率计算得到吸附的表观活化能为Ea= −15.3 kJ·mol–1,说明吸附过程不需通过吸收能量来跨越能垒,吸附现象很容易发生[16]。
2.3 Na+、K+对AMP吸附Cs+的影响
由于放射性废液中存在的主要竞争离子为Na+和K+等,分别考察了其浓度对吸附容量的影响,结果如图5所示。由图可见,Na+和K+的引入均会使AMP吸附Cs+的吸附容量明显降低;随着溶液中Na+浓度的增大,AMP对Cs+的吸附容量缓慢降低,而随着K+浓度的增大,AMP对Cs+的吸附容量明显下降,说明K+与Cs+的竞争作用更明显。磷钼酸铵晶体中存在12个钼氧八面体结构,[NH4]+存在其结构空隙中,因此,原因可能是相对Na+而言,K+与的离子半径更接近,通过置换进入到的位置所引起的晶体结构畸变更小,而更容易与Cs+形成竞争关系。Na+(NaNO3)、K+(KNO3)、[NH4]+、Cs+(CsCl)的离子半径分别为0.095、0.138、0.143、0.169[17]。
3 结语
利用向钼酸铵和磷酸的混合溶液中滴加硝酸的方法制备AMP,方法简便,成品纯度达到理想水平。静态吸附实验结果显示,不同温度下,AMP对Cs+的吸附在10 min内可达到平衡,随着温度升高,吸附容量呈下降趋势;吸附过程可用准二级方程很好描述,根据Arrhenius公式计算得到吸附活化能为−15.3 kJ·mol–1;Na+和K+的竞争作用使吸附容量明显降低,其中K+的竞争作用更为明显,原因可能是K+与[NH4]+的离子半径更接近,通过置换进入到AMP晶体中[NH4]+的位置所引起的晶格畸变更小,也表明AMP对Cs+的吸附是Cs+与[NH4]+的交换过程。但是,合成的AMP为微晶结构,不利于离子交换柱中大量废液的连续除Cs+处理。因此,开展对AMP-复合材料的研究很有必要。

图5 Na+和K+对吸附的影响Fig.5 Effect of concentrations of Na+ and K+ on the uptake of Cs+. (c0 = 80 mg/L, V = 0.5 L, m = 200 mg, t = 90 min)
1 Todd T A, Batcheller T A, Law J D, et al. Cesium and strontium separation technologies literature review[R]. INEEL/EXT-04-01895, Idaho, 2004
2 Naushad M. Inorganic and composite ion exchange materials and their applications[J]. Ion Exchange Letters, 2009,2(1): 1–14
3 徐世平, 张继荣, 宋崇立. 用无机离子交换法从酸性高放废液中去除铯研究进展[J]. 辐射防护通讯, 2000,119: 8–12
XU Shiping, ZHANG Jirong, SONG Chongli. Advance in the study of removing cesium from acidic HLW by inorganic ion exchangers[J]. Radiation Protection Bulletin, 2000,119: 8–12
4 Tranter T, Herbst R S, Todd T A, et al. Evaluation of ammonium molybdophosphate polyacrylonitrile as a cesium selective sorbent for the removal of137Cs from acidic nuclear waste solutions[J]. Advances in Environmental Research, 2002,6(2): 107–121
5 Borai E H, Harjulab R, Malinen L. Efficient removal of cesium from low-level radioactive liquid waste using natural and impregnated zeolite minerals[J]. Journal of Hazardous Materials, 2009,172(1): 416–422
6 Andersen A M K, Norby P. Structural aspects of the dehydration and dehydroxylation of gamma–titanium phosphate, gamma-Ti(PO4)(H2PO4)H2O[J]. Inorganic Chemistry, 1998,37: 4313–4320
7 LI Bing, LIAO Jiali, WU Jiaojiao, et al. Removal of radioactive cesium from solutions by zinc ferrocyanide[J]. Nuclear Science and Techniques, 2008,19(2): 88–92
8 Anthony R G, Dosch R G, Gu D, et al. Use of silicotitanates for removing cesium and strontium from defense Waste[J]. Industrial & Engineering Chemistry Research, 1994,33(11): 2702–2705
9 Archer D W, Heslop R B. The solubility of ammonium 12-Molybdophosphate in dilute acids[J]. Analytica Chimica Acta, 1964,30: 582–589
10 Smit J V R, Robb W, Jacobs J J. Cation exchange properties of the ammonium heteropolyacid salts[J]. Journal of Inorganic Nuclear Chemistry, 1959,12(1–2): 95–103
11 Lehto J, Harjula R. Separation of cesium from nuclear waste solutions with hexacyanoferrate and ammonium phosphomolybdate[J]. Solvent Extraction and Ion Exchange, 1987,5(2): 343–352
12 HUANG Zhaoya, ZHANG Dong, TAN Zhaoyi. Preliminary research on the uptake behavior of ammonium molybdophosphate for cesium and the corresponding structural transformation[C]. Advanced Materials Research, 2012,535–537: 2191–2194
13 田国新, 翁皓珉. 粒状十二磷钼酸铵结晶的合成及对Cs+的交换性能研究[J]. 离子交换与吸附, 1996,12(2): 149–153
TIAN Guoxin, WENG Haomin. Preparation of granular crystal of ammonium molybdophosphate and study on its ion exchange property[J]. Ion Exchange and Adsorption, 1996,12(2): 149–153
14 Katsoulis D E. A survey of applications of polyoxometalates[J]. Chemical Reviews, 1988,98: 359–387
15 沈培友, 徐晓燕, 马毅杰. 无机.有机柱撑蒙脱石吸附对硝基苯酚的热力学与动力学特征研究[J]. 环境保护科学, 2005,6(31): 15–19
SHEN Peiyou, XU Xiaoyan, MA Yijie. Study on characteristics of thermodynamics and kinetics of p-Nitrophenol sorption by inorganic-organic pillared montmorillonite from water[J]. Environmental Protection Science, 2005,6(31): 15–19
16 黄开辉, 万惠霖. 催化原理[M]. 北京: 科学出版社, 1983: 188–189
HUANG Kaihui, WAN Huilin. Catalysis principles[M]. Beijing: Science Press, 1983: 188–189
17 钱庭宝. 离子交换剂应用技术[M]. 天津: 天津科学技术出版社, 1984: 419
QIAN Tingbao. Applition of ion exchangers[M]. Tianjin: Tianjin Science & Technology Press, 1984: 419
CLCTL941
Synthesis of ammonium molybdophosphate and the uptake behavior for cesium
HUANG Zhaoya ZHANG Dong TAN Zhaoyi
(Institute of Nuclear Physics and Chemistry,China Academy of Engineering Physics,Mianyang 621900,China)
Background:An enormous amount of liquid radioactive wastes (LRW) was produced by nuclear power plants operation and the reprocessing of spent nuclear fuel. It is necessary to remove137Cs from LRW to reduce the volumes of waste that require solidification prior to final disposal.Purpose:This paper aimed to study the ion exchange mechanism and uptake behavior for cesium of Ammonium Molybdophosphate (AMP, (NH4)3P(Mo3O10)4·xH2O) in more detail.Methods:Two samples of AMP (AMP-1, AMP-2) were synthesized by different precipitation reactions and they were analyzed by X-ray diffraction (XRD) and Fourier transform infrared spectroscopy (FTIR). The uptake behavior of AMP-2 for Cs+under different conditions, such as temperature, contact time, competing ions was investigated through batch experiments.Results:The results show that the adsorption reaches equilibrium in 10 min. The adsorption kinetics can be described by the pseudo second-order equation quite well (R2>0.999). The existence of Na+and K+have negative effects on the uptake of Cs+, while with K+concentration enrichment, the adsorption capacity of Cs+decreases faster.Conclusions:The results support the theory of isomorphous exchange of Cs ions for ammonium ions. In addition, AMP has the potential to be a very useful ion exchanger in treatment with nuclear waste solution for removal of137Cs.
AMP, Cs+, Uptake
TL941
10.11889/j.0253-3219.2013.hjs.36.020301
中国工程物理研究院科学技术发展基金(2012b0301032)资助
黄召亚,男,1987年出生,2010年毕业于浙江大学,现为中国工程物理研究院硕士研究生,核燃料循环与材料专业
谭昭怡,liu315351@163.com
2012-09-03,
2012-10-31