纳米TiO2/多孔矿物光催化剂与甲基橙染料的作用过程研究
王 程, 黄剑锋
(陕西科技大学 材料科学与工程学院, 陕西 西安 710021)
0 引言
以纳米TiO2为代表的半导体光催化剂及其光催化氧化技术是当前国内外的研究热点.TiO2纳米粉体易团聚、难回收等是限制其实际应用的关键问题之一.采用玻璃、陶瓷和多孔吸附剂等作为载体对TiO2进行固定是解决上述问题的有效途径.近年来的研究表明:将多孔矿物如沸石[1-3,13]、硅藻土[4,5,16]、膨润土[6-7,15,18]、海泡石[8,17]、高岭石[9-11,13]、坡缕石[12,19]等作为载体负载纳米TiO2,一方面可实现TiO2的固定化负载;另一方面具有丰富孔道、高比表面积和强吸附特性的多孔矿物可实现水及空气中污染物的靶向富集,使纳米TiO2与污染物更有效地接触,从而提高材料对污染物的光催化降解效率.
由于多孔矿物载体的引入,纳米TiO2/多孔矿物光催化剂与有机污染物的作用过程必然与单一TiO2之间有所不同.关于上述二者之间的作用过程等方面的研究仍有待深入.本课题组前期在纳米TiO2/多孔矿物光催化剂的制备及性能方面已开展了大量的研究工作[13-19],重点研究了材料结构和性能的影响及其机理等.本文在此基础上,进一步分析纳米TiO2/多孔矿物光催化剂与甲基橙染料的作用过程及相关机理.
1 实验部分
1.1 材料制备
采用静电自组装方法制备TiO2/多孔矿物光催化剂[13-19]:矿物粉体经巯丙基三甲氧基硅烷改性并氧化后,称取一定改性矿物粉体放入三口烧瓶中,加水搅拌,水浴加热70 ℃.移取30 wt%TiO2理论负载量的TiCl4溶液,滴加入矿浆中,采用盐酸和氨水调节pH 在2.0左右,恒温搅拌4 h,陈化12 h,再经过滤,80 ℃干燥,一定温度下焙烧,即得到纳米TiO2/多孔矿物光催化剂.其中,TiO2/沸石、TiO2/膨润土和TiO2/坡缕石光催化剂的焙烧温度分别为200 ℃、500 ℃和300 ℃.
1.2 性能评价
采用甲基橙染料评价材料的光催化性能.配制甲基橙溶液浓度为10 mg/L,甲基橙最大吸收波长464 nm.以1只40 W(主波长253.7 nm)的紫外灯管为照射光源.采用磁力搅拌器使光催化剂与模拟废水混合均匀.紫外线光强约为6.7 mW/cm2,灯管离液面约10 cm.采用紫外-可见光分光光度计评价甲基橙溶液的脱色效果,计算公式为:P=(A0-At)/A0×100%.式中:P为溶液的脱色率;A0为未处理原溶液的吸光度;At为经t时间处理后溶液的吸光度.
1.3 分析表征
采用D/max2550VB3+/PC型X射线衍射仪对材料成分和结构进行分析,2θ°为3°~70°.采用谢乐公式计算纳米TiO2的晶粒尺寸.采用TriStar 3000型比表面积和孔隙度分析仪分析材料的比表面积.
2 结果与讨论
2.1 样品的表征分析
图1分别是三种矿物和TiO2/多孔矿物光催化剂的XRD图谱.图中显示:TiO2/矿物光催化剂的XRD图谱中均出现了明显的锐钛矿的特征峰.采用谢乐公式计算得到TiO2/沸石、TiO2/膨润土和TiO2/坡缕石光催化剂中TiO2晶粒尺寸分别为:5.9 nm、8.7 nm和6.6 nm.

图1 样品的XRD图谱
表1为三种矿物和TiO2/矿物光催化剂的比表面积分析结果.表中显示:TiO2/矿物光催化剂的比表面积较原矿均显著提高.这是由于分散在矿物表面的纳米TiO2具有很大的比表面积,同时纳米TiO2的分布使材料表面呈现凹凸不平的状态,进而增加了材料的比表面积[1].

表1 样品的比表面积
2.2 样品的光催化性能
图2为TiO2/矿物光催化剂对甲基橙溶液的降解曲线.光催化剂用量均为10 g/L.图2显示:光照1 h,甲基橙溶液的脱色率迅速上升.随着光照时间的延长,甲基橙溶液的脱色率均缓慢下降,后趋于平缓.
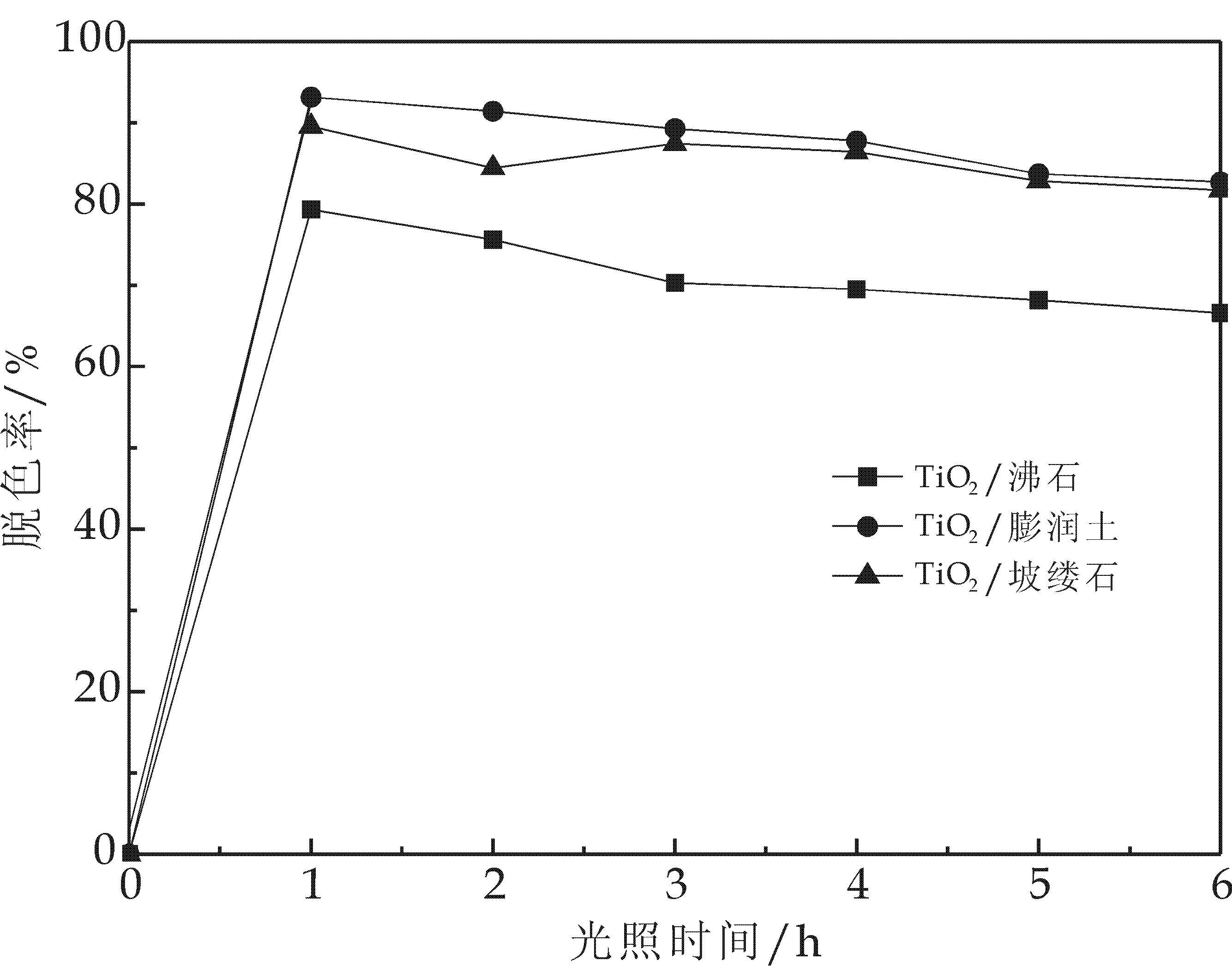
图2 样品对甲基橙溶液的脱色效果
表2分别对比了三种矿物和TiO2/矿物光催化剂对甲基橙溶液的吸附效果.样品的用量均为4 g/L,处理时间均为1 h.表2显示:负载TiO2之后的光催化剂对甲基橙溶液的脱色效果较原矿均有很大提高,这是由于TiO2矿物比表面积较大,导致其吸附性能增强所致.
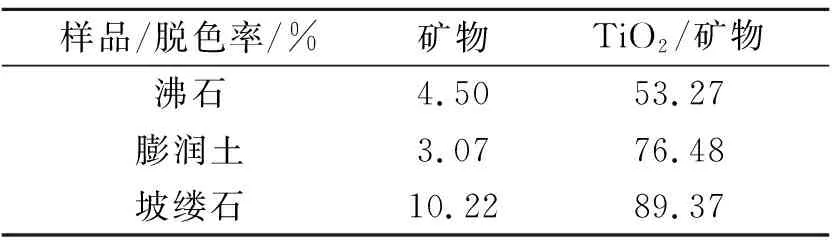
表2 样品的吸附性能
为了进一步考察TiO2/矿物对甲基橙的作用过程,分别在避光和紫外光照射条件下对比光催化剂对甲基橙溶液的脱色效果.为了减少材料吸附作用的影响,材料的用量均为2 g/L,结果如图3所示.图3显示:在避光和光照条件下处理30 min后,光催化剂对甲基橙溶液脱色效果基本相同,表现出一定的吸附性能.随着处理时间的延长,避光条件下,溶液的脱色率基本保持一致;而光照条件下,溶液的脱色率缓慢上升,且与避光条件下甲基橙溶液的脱色率相比均有所提高,表明材料具有一定的光催化性能.
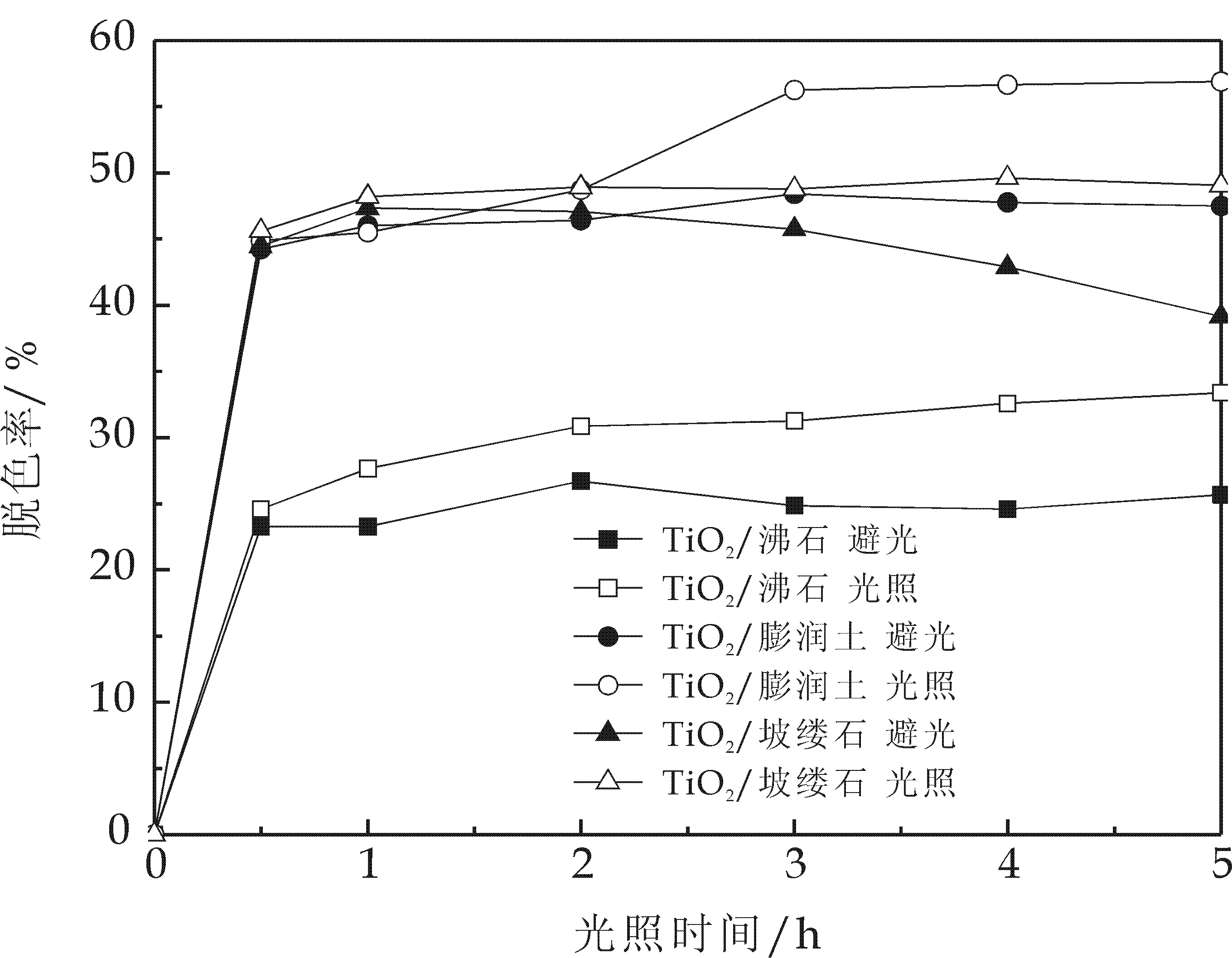
图3 避光和光照条件下样品对甲基橙溶液的脱色效果
图4为重复利用过程中TiO2/矿物对甲基橙的降解曲线.样品的用量均为10 g/L,光照时间均为5 h.图4显示:经重复利用后,TiO2/多孔矿物光催化剂对甲基橙溶液的脱色效果显著下降.重复利用三次后,TiO2/沸石、TiO2/膨润土和TiO2/坡缕石光催化剂对甲基橙溶液的脱色效果分别从第一次的82.78%、90.25%和89.32%降低到3.63%、35.87%和69.43%.这可能是由于本试验所采用的紫外光光强太弱,吸附于材料表面的甲基橙染料得不到充分降解,循环利用过程中,甲基橙染料在材料表面不断累积,导致材料对甲基橙溶液的脱色效果急剧下降.

图4 样品的重复利用性能
2.3 光催化剂与甲基橙染料的作用过程
在紫外光的照射下,纳米TiO2/矿物光催化剂与甲基橙染料作用过程如图5所示:将催化剂颗粒与甲基橙溶液混合后,催化剂颗粒在溶液中处于悬浮状态;在催化剂颗粒中具有优异吸附性能的多孔矿物的作用下,甲基橙染料分子被迅速吸附至催化剂颗粒表面;催化剂颗粒表面的部分甲基橙染料在光照作用下被其表面的TiO2所分解,同时部分甲基橙染料在不断搅拌过程中在颗粒表面发生脱附;持续光照,催化剂表面的染料分子不断发生分解.但如果光强太弱,催化剂颗粒表面的染料分子无法充分降解,将会在颗粒表面不断累积,进而影响材料的光催化及重复利用性能.

图5 纳米TiO2/多孔矿物光催化剂与甲基橙染料的作用过程示意图
3 结论
采用静电自组装方法制备了纳米TiO2/多孔矿物光催化剂.TiO2纳米晶粒均为锐钛矿结构.纳米TiO2的负载显著增加了材料的比表面积及其对甲基橙染料的吸附性能.光催化剂对甲基橙染料表现出吸附和光催化的共同作用.经重复利用后,光催化剂对甲基橙溶液的处理效果明显降低.
TiO2/多孔矿物光催化剂与甲基橙染料的作用过程为:当光催化剂与甲基橙溶液混合后,甲基橙染料分子被迅速吸附至催化剂颗粒表面;催化剂颗粒表面的部分甲基橙染料在光照作用下被其表面的TiO2所分解,同时部分甲基橙染料在不断搅拌过程中在颗粒表面发生脱附;持续光照,催化剂表面的染料分子不断发生分解.但如果光强太弱,催化剂颗粒表面的染料分子无法充分降解,将会在颗粒表面不断累积,进而影响材料的光催化及重复利用性能.
[1] 李静谊,刘丽娜,斯琴高娃,等.TiO2/斜发沸石光催化降解罗丹明B的研究[J].感光科学与光化学,2007,25(4):284-294.
[2] Li F.F.,Sun S.M.,Jiang Y.S.,et al.Photodegradation of an azo dye using immobilized nanoparticles of TiO2supported by natural porous mineral[J].Journal of Hazardous Materials,2008,152(3):1 037-1 044.
[3] Nikazar M.,Gholivand K.,Mahanpoor K.Photocatalytic degradation of azo dye Acid Red 114 in water with TiO2supported on clinoptilolite as a catalyst[J].Desalination,2008,219(1-3):293-300.
[4] Jia Y.X.,Han W.,Xiong G.X.,et al.Layer-by-layer assembly of TiO2colloids onto diatomite to build hierarchical porous materials[J].Journal of Colloid and Interface Science,2008,323(2):326-331.
[5] 传秀云,卢先春,卢先初.负载TiO2的硅藻土对亚甲基蓝的光降解性能研究[J].硅酸盐学报,2008,23(4):657-661.
[6] Li J.Y.,Suyoulema,Wang W.B.,et al.A study of photodegradation of sulforhodamine B on Au-TiO2/bentonite under UV and visible light irradiation[J].Solid State Sciences,2009,11(12):2 037- 2 043.
[7] Pichat P.,Khalaf H.,Tabet D.,et al.Ti-montmorillonite as photocatalyst to remove 4-chlorophenol in water and methanol in air[J].Environmental Chemistry Letters,2005,2(4):191-194.
[8] Neren Ökte A.,Saynsöz E.Characterization and photocatalytic activity of TiO2supported sepiolite catalysts[J].Separation and Purification Technology,2008,62(3):535-543.
[9] Lei S.M.,Gong W.Q.,Bai C.H.,et al.Preparation of TiO2/kaolinite nanocomposite and its photocatalytical activity[J].Journal of Wuhan University of Technology (Materials Science Edition), 2006,21(12):12-15.
[10] Chong M.N.,Vimonses V.,Lei S.M.,et al.Synthesis and characterisation of novel titania impregnated kaolinite nano-photocatalyst[J].Microporous and Mesoporous Materials,2009,117(1-2):233-242.
[11] Wang C.,Shi H.S.,Zhang P.,et al.Synthesis and characterization of kaolinite/TiO2nano-photocatalysts[J].Applied Clay Science,2011,53(4):646-649.
[12] Zhao D F,Zhou J,Liu N.Surface characteristics and photoactivity of silver-modified palygorskite clays coated with nanosized titanium dioxide particles[J].Materials Characterization,2007, 58(3):249-255.
[13] 王 程,施惠生,李 艳,等.静电自组装制备镧掺杂高岭石基纳米TiO2光催化材料研究[J].人工晶体学报,2010,39(6):1 381-1 385.
[14] 李 艳,王 程.静电自组装制备斜发沸石负载纳米TiO2吸附及光催化降解甲基橙染料研究[J].岩石矿物学,2011,30(2):286-290.
[15] 王 程,施惠生,李 艳.静电自组装制备纳米TiO2/膨润土复合材料及其光催化性能研究[J].化工新型材料,2011,39(1):55-57.
[16] 李 艳,王 程.静电自组装制备硅藻土负载纳米TiO2光催化材料[J].纳米技术与精密工程,2011,9(6):493-498.
[17] 李 艳,王 程,杜国强.静电自组装制备海泡石负载纳米TiO2复合光催化材料研究[J].高校化学工程学报,2011,25(5):871-876.
[18] Wang C.,Shi H.S.,Li Y.Preparation of bentonite supported nano titanium dioxide photocatalysts by electrostatic self-assembly method[J].Journal of Wuhan University of Technology (Materials Science Edition),2012,27(4):603-607.
[19] 王 程,施惠生,李 艳.静电自组装制备坡缕石负载纳米TiO2光催化材料研究[J].同济大学学报(自然科学版),2012,40(4):578-582.

