Nb5+掺杂LiFePO4/C的反应挤出合成
刘旭恒 ,黄少波,赵中伟,王德志
(1.中南大学 材料科学与工程学院,长沙 410083;2.中南大学 冶金科学与工程学院,长沙 410083)
环保和能源危机日益凸显,LiFePO4因其环境友好、原料价格低、循环寿命长和高温稳定性好等优点,在锂离子动力电池方面显示出良好的应用前景,倍受广大研究者的关注,被认为是最具发展潜力的动力型正极材料[1-2]。但LiFePO4较低的电导率制约了它的推广应用。目前,通过碳包覆可以提高LiFePO4颗粒间的电导率[3-5],但并不能改善LiFePO4的本征电导率,同时还会降低材料的体积比能量密度[6-8];而金属离子掺杂可以改变LiFePO4的内部结构来提高其本征电导率[9-11]。CHUNG等[12]通过掺杂少量金属离子取代Li+位,使掺杂后的 LiFePO4的电导率在室温下达到4.1×10-2S/cm,提高了8个数量级,引起了极大的关注。
在聚合物工业中有一种反应挤出工艺[13]。在反应挤出时,物料受到螺杆强烈的研磨、挤压和剪切作用,实现原子级的混合均匀度,并发生局部的化学反应;同时,外热系统促使物料塑化熔融,加快反应速度[14-15]。在磷酸铁锂的合成过程中,物料的混合均匀度对最终产品的性能有着很大的影响,而反应挤出在这方面具有非常明显的优势。因此,本文作者提出采用反应挤出的方法来合成磷酸铁锂材料,在采用少量碳包覆的同时掺杂少量金属离子,使掺杂源物质在反应挤出过程中弥散在前驱物中,实现很好的微观混合均匀度,使材料的电导率得到整体提高。
1 实验
1.1 Li1-5xNbxFePO4/C的合成
以草酸铌为离子掺杂源,按照化学计量比称取LiOH·H2O、FeC2O4·2H2O、P2O5和草酸铌,按 3%(质量分数)的理论碳含量添加葡萄糖,置于搅拌球磨机中混合10 min;将球磨后的混合物置于螺杆喂料机中,以5 g/S的速度将混合物加入到32-Ⅱ型双螺杆挤出机的进料口,控制机筒温度100℃、螺杆转速250 r/min,在此条件下进行混合物的反应挤出;将挤出产物置于管式电炉中,在高纯氮气的保护下,于680 ℃保温10 h,随炉冷却后得到Li1-5xNbxFePO4/C样品。
1.2 材料表征
采用日本理学 D/RAX射线衍射仪对样品进行物相分析,Cu Kα辐射源,管电压为50 kV,管电流为100 mA,扫描速度为8(°)/min;采用日本电子JSM-6360LV型扫描电子显微镜观察样品的颗粒尺寸和表面形貌。
1.3 电池组装与测试
以涂布法制备电极,按m(活性物质):m(碳黑):m(PVDF(聚偏氟乙烯))=90:5:5的比例配料混合均匀,采用NMP (N-甲基-吡咯烷酮)为溶剂调成正极浆液,将浆液均匀涂布在预处理过的铝箔上,置于真空干燥箱中,在120 ℃下干燥12 h后用圆孔器敲取正极片;以锂片为对电极,电解液为1 mol/L的LiPF6(V(EC):V(DMC):V(EMC)=1:1:1)混合溶液,采用 Celgerd2400聚丙烯多孔隔膜,在高纯氩气(纯度>99.999%)保护的手套箱里组装成2025型扣式电池,静置24 h后,在CT2001A电池性能测试系统上进行充放电测试,电压范围为2.3~4.1 V,用CHI660A电化学工作站进行循环伏安测试,电压范围为2.8~4.2 V。
2 结果与讨论
2.1 Nb5+对材料结构的影响
图1所示为Li1-5xNbxFePO4/C材料的XRD谱。由图1可知,当Nb5+加入量x为0~0.008时,不同样品与LiFePO4的标准衍射谱基本一致,由于Nb5+的半径(0.068 nm)与Li+的半径(0.069 nm)很接近,因此,Nb5+很容易占据Li位进入晶格中,形成Li1-5xNbxFePO4/C固溶体,所以样品仍保持着完整的橄榄石型结构,同时也说明采用反应挤出工艺合成磷酸铁锂材料这一方法是可行的;当Nb5+加入量x为0.01时,XRD谱表明,样品中出现了一个微小的杂相峰,如图1中箭头所示;由于衍射峰的峰位单一且强度不高,通过与标准衍射数据库对比后未能确定具体的物相组成,通过对比分析,极可能是草酸铌加入量过多而受热分解所残留的氧化物。
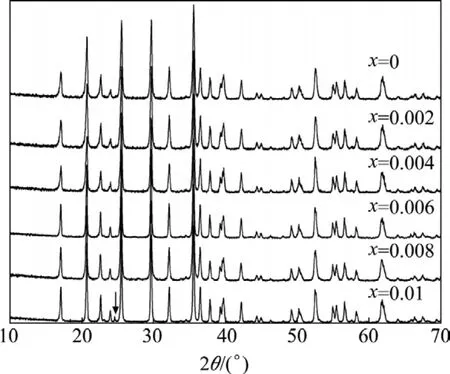
图1 Li1-5xNbxFePO4/C(x=0,0.002,0.004,0.006,0.008,0.01)的XRD谱Fig.1 XRD patterns of Li1-5xNbxFePO4/C (x=0, 0.002, 0.004,0.006, 0.008, 0.01)
掺杂Nb5+后样品的晶胞参数如表1所列。掺杂后样品的晶胞参数都发生了变化,这表明掺杂的Nb5+已进入晶格的内部;晶胞参数随掺杂量的增加逐渐减小,这是由于 Nb5+取代 Li+产生的空位导致晶体的晶胞发生收缩,且掺杂量越大,晶胞参数越小,虽然Li+空位的产生能提供更多的Li+扩散通道,但掺杂量过大时,晶胞参数的过度萎缩会导致扩散通道横截面积的减小,对Li+的嵌入/脱嵌过程造成一定的阻碍。
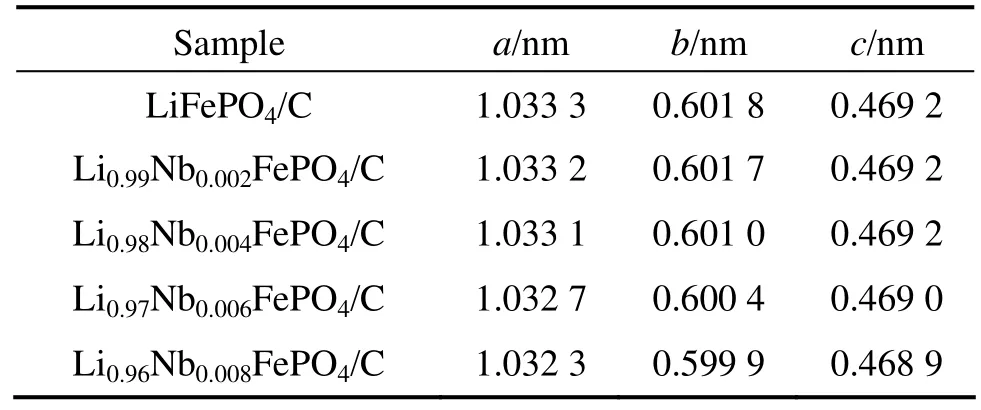
表1 Li1-5xNbxFePO4/C(x=0,0.002,0.004,0.006,0.008)的晶胞参数Table 1 Lattice parameters of Li1-5xNbxFePO4/C (x=0, 0.002,0.004, 0.006, 0.008)
2.2 Nb5+对材料形貌的影响
图2所示为Li1-5xNbxFePO4/C(x=0,0.002,0.004,0.006,0.008)的SEM像。由图2可知,Nb5+的加入对颗粒的形貌没有明显的影响,不同掺杂量的Li1-5xNbxFePO4/C样品的表观形貌基本一致,颗粒表面光滑致密,大小比较均匀,单颗粒粒径在1 μm左右;当掺杂量为0.008时,颗粒略有长大,且团聚也有所加剧,表明掺杂量过大不利于Li+的扩散。
2.3 Nb5+掺杂对材料电化学性能的影响
图3所示为Li1-5xNbxFePO4/C的循环伏安曲线。图3中的每条曲线上都有一对氧化还原峰,分别对应Li+的脱嵌/嵌入过程。与未掺杂的LiFePO4/C相比,掺杂后的Li1-5xNbxFePO4/C的峰型更好,LiFePO4/C氧化峰与还原峰的电位差为0.66 V,表明此时Li+的脱嵌/嵌入过程电极极化较强;Li0.99Nb0.002FePO4/C、Li0.98-Nb0.004FePO4/C、Li0.97Nb0.006FePO4/C和 Li0.96Nb0.008-FePO4/C的氧化还原峰对应的电位差分别为 0.56、0.38、0.37和0.39 V,以Li0.97Nb0.006FePO4/C的电位差最小,表明此样品在电化学反应时极化最弱,材料具有更好的可逆循环性能。另外,由图3还可以看出,峰强随着 Nb5+加入量的增加也有所提高,表明 Li+在掺杂样品中的扩散速率也得到了提高。

图2 Li1-5xNbxFePO4/C(x=0,0.002,0.004,0.006,0.008)的SEM像Fig.2 SEM images of Li1-5xNbxFePO4/C(x=0,0.002, 0.004, 0.006, 0.008): (a)—x=0;(b)—x=0.002; (c)—x=0.004; (d)—x=0.006;(e)—x=0.008

图3 扫描速率为0.2 mV/s时Li1-5xNbxFePO4/C的循环伏安曲线Fig.3 CV curves of Li1-5xNbxFePO4/C at scan velocity of 0.2 mV/s
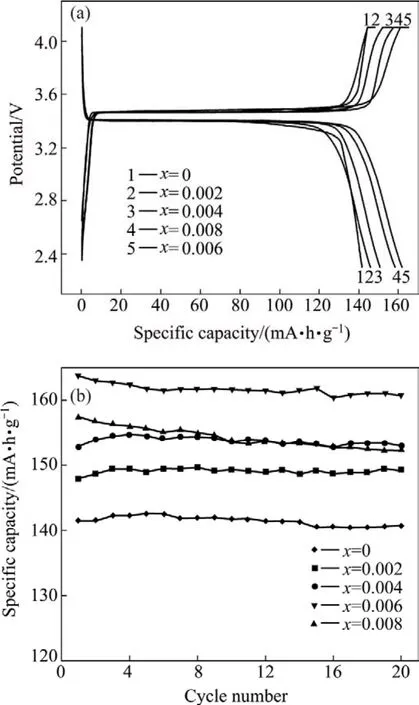
图4 Li1-5xNbxFePO4/C在0.2 C倍率下的首次充放电曲线和循环性能曲线Fig.4 Initial charge-discharge curves (a)and cycle performance (b)of Li1-5xNbxFePO4/C at 0.2C rate
图4所示为Li1-5xNbxFePO4/C在0.2C倍率下的首次充放电曲线和循环性能曲线。由图4可知,样品充放电平台都非常平坦。未掺杂Nb5+的LiFePO4/C的放电比容量为141.5 mA·h/g;Nb5+的掺入使材料的电化学性能有明显的改善,Nb5+掺杂量为0.002和0.004的Li1-5xNbxFePO4/C样品的放电比容量分别为 147.0和152.9 mA·h/g;Li0.97Nb0.006FePO4/C具有最高的放电比容量,达到162.9 mA·h/g;Li0.96Nb0.008FePO4/C的放电比容量与 Li0.97Nb0.006FePO4/C的相比有所降低,为157.2 mA·h/g。经过 20次循环后,LiFePO4/C、Li0.99Nb0.002FePO4/C、Li0.98Nb0.004FePO4/C、Li0.97Nb0.006-FePO4/C和 Li0.96Nb0.008FePO4/C的放电比容量分别为140.8、148.7、152.0、160.8 和 152.3 mA·h/g,容量保持率分别为99.5%、101.2%、99.4%、98.7%和96.9%。Nb5+掺杂的作用可以从空位的角度来解释。Nb5+的加入取代了Li+位,由于离子价态的不同,根据电荷守恒的原则,Nb5+掺杂后晶体中会产生大量的Li空位,也就提供了更多的Li+的扩散通道,减小了Li+扩散的障碍,因此,掺杂Nb5+样品的电化学性能更优。
图5所示为Li0.97Nb0.006FePO4/C在不同倍率下的电化学性能图。由图5可以看出,Li0.97Nb0.006FePO4/C在 0.2C、0.5C、1C和 2C倍率的放电比容量分别为162.9、148.9、141.7和137.1 mA·h/g;经过10次循环后的容量衰减程度很小,容量分别为 162.1、146.9、140.4和 135.8 mA·h/g,容量保持率分别为 99.5%、99.0%、99.1%和99.0%,表现出较好的倍率性能和循环性能。

图5 Li0.97Nb0.006FePO4/C在不同倍率下的首次充放电曲线和循环性能图曲线Fig.5 Initial charge-discharge curves (a)and cycle performance (b)of Li0.97Nb0.006FePO4/C at different rates
3 结论
1)采用反应挤出法合成了 Li1-5xNbxFePO4/C材料。XRD结果表明,适量掺杂 Nb5+能有效取代LiFePO4中的Li+,形成固溶体;随着掺杂量的增加,固溶体的晶胞参数减小。
2)Nb5+掺杂量的改变对材料颗粒形貌没有明显影响;掺杂适量的Nb5+能有效降低氧化还原峰之间的电位差,其中最小的电位差为0.37 V,表明Nb5+的掺杂改善了Fe3+/Fe2+电对的氧化还原动力学性能,减小了电化学过程的电极极化。
3)当Nb5+掺杂量为x为0.006时,样品具有最优的电化学性能,其首次放电比容量达到162.9 mA·h/g,与LiFePO4/C的相比提高了21.4 mA·h/g。
4)Li0.97Nb0.006FePO4/C在0.2C、0.5C、1C和2C倍率下的放电比容量分别为 162.9、148.9、141.7和137.1 mA·h/g;经过 10次循环后容量保持率分别为99.5%、99.0%、99.1%和 99.0%,倍率性能和循环性能良好。
[1]蒋志君.锂离子电池正极材料磷酸铁锂:进展与挑战[J].功能材料, 2010, 41(3): 365-368 JIANG Zhi-jun.Development and challenge of LiFePO4cathode materials for Li-ion batteries[J].Journal of Functional Materials,2010, 41(3): 365-368.
[2]任志国, 冉龙国.磷酸铁锂电池材料研究进展[J].船电技术,2009, 29(11): 31-35.REN Zhi-guo, RAN Long-guo.Recent development for materials of LiFePO4cell[J].Marine Electric & Electronic Engineering, 2009, 29(11): 31-35.
[3]WANG G X, YANG L, CHEN Y, WANG J Z, BEWLAY S, LIU H K.An investigation of polypyrrole-LiFePO4composite cathode materials for lithium-ion batteries[J].Electrochimica Acta, 2005, 50(24): 4649-4654.
[4]LIU Xu-heng, ZHAO Zhong-wei.Synthesis of LiFePO4/C by solid-liquid reaction milling method[J].Powder Technology,2010, 197: 309-313.
[5]刘旭恒, 赵中伟.碳源和铁源对LiFePO4/C材料的制备及性能的影响[J].中国有色金属学报, 2008, 18(3): 541-545.LIU Xu-heng, ZHAO Zhong-wei.Effects of carbon source and iron source on preparation and performance of LiFePO4/C[J].The Chinese Journal of Nonferrous Metals, 2008, 18(3):541-545.
[6]夏继才, 王殿龙, 张若昕, 伊廷峰.Ni2+掺杂对LiFePO4正极材料电化学性能的影响[J].稀有金属快报, 2008, 27(11): 23-26.XIA Ji-cai, WANG Dian-long, ZHANG Ruo-xin, YI Ting-feng.Influence of the Ni-doped on the electrochemical performance of LiFePO4[J].Rare Metals Letters, 2008, 27(11): 23-26.
[7]WANG G.X, BEWLAY S, YAO J, AHN J H, DOU S X, LIU H K.Characterization of LiMxFe1-xPO4(M=Mg, Zr, Ti)cathode materials prepared by the sol-gel method[J].Electrochemical and Solid-State Letters, 2004, 7(12): A503-A506.
[8]张胜利, 杨胜杰, 宋延华, 李 维.锂离子电池正极材料LiFePO4掺杂改性研究进展[J].电源技术, 2010, 134(3):299-302.ZHANG Sheng-li, YANG Sheng-jie, SONG Yan-hua, LI Wei.Research progress of ion-doped cathode materials LiFePO4for lithium ion batteries[J].Chinese Journal of Power Sources, 2010,134(3): 299-302.
[9]WU She-huang, CHEN Mao-sung, CHIEN Chao-jung, FU Yen-pei.Preparation and characterization of Ti4+-doped LiFePO4cathode materials for lithium-ion batteries[J].Journal of Power Sources, 2009, 189(1): 440-444.
[10]PARK K S, SON J T, CHUNG H T, KIM S J, LEE C H, KANG K T, KIM H G.Surface modification by silver coating for improving electrochemical properties of LiFePO4[J].Solid State Communications, 2004, 129(5): 311–314.
[11]NI J F, ZHOU H H, CHEN J T, ZHANG X X.LiFePO4doped with ions prepared by co-precipitation method[J].Materials Letters, 2005, 59(18): 2361-2365.
[12]CHUNG S Y, BLOCKING J T, CHIANG Y M.Electronically conductive phospho-olivines as lithium storage electrodes[J].Nature Materials, 2002, 1: 123-128.
[13]李 柱, 苑会林.CO2与环氧丙烷共聚物的反应挤出[J].合成树脂及塑料, 2010, 27(5): 71-73.LI Zhu, YUAN Hui-lin.Reactive extrusion processing of carbon dioxide-epoxide copolymers[J].China Synthetic Resin and Plastics, 2010, 27(5): 71-73.
[14]于人同, 方显力, 张云灿, 陈贤益.反应挤出法制备马来酸酐接枝聚乳酸[J].高分子材料科学与工程, 2009, 25(3): 85-88.YU Ren-tong, FANG Xian-li, ZHANG Yun-can, CHEN Xian-yi.Preparation and properties of PLA grafted with maleic anhydride through reactive extrusion[J].Polymer Materials Science and Engineering, 2009, 25(3): 85-88.
[15]郭 林, 李 艳, 杨建华, 廖勇胜, 文光俊.反应挤出制备钢带管粘接树脂的研究[J].塑料工业, 2010, 38(S): 147-150.GUO Lin, LI Yan, YANG Jian-hua, LIAO Yong-sheng, WEN Guang-jun.Study on the preparation of steel pipe adhesion resin by reaction extrusion[J].China Plastics Industry, 2010, 38(S):s147-s150.

