锈蚀法提取预还原红土镍矿中镍和钴
赵玉先,胡启阳,李新海,王志兴,郭华军
(中南大学 冶金科学与工程学院,长沙 410083)
镍是一种银白色金属,具有良好的延展性、较高的机械强度和较好的化学稳定性,在日常生活和国防建设中占据重要的地位[1]。可供开采的陆地镍资源主要分为硫化镍矿和红土镍矿两类[2]。目前,世界上70%(质量分数)的镍产量来源于占全球镍储量 30%的硫化镍矿。然而,随着硫化镍矿的逐渐枯竭,从占全球镍储量70%的红土镍矿中提取镍是未来镍产业的发展趋势[3-4]。
红土镍矿是含镍岩石经长期风化淋滤变质而形成的,是一种由铁和硅等含水氧化物组成的氧化镍矿,镍含量低,成矿结构复杂,一般由如下3层组成:褐铁矿层、过渡层和腐殖质层。目前,世界上红土镍矿的处理工艺主要有火法工艺[4-5](还原熔炼和锍化熔炼)、湿法工艺[6-11](常压酸浸、高压酸浸、还原焙烧-氨浸、生物浸出、碱系脱硅等)、火法-湿法联合工艺[12-13](还原焙烧-磁选、还原焙烧-浮选)。由于火法工艺能耗高,污染严重,所以湿法工艺受到越来越多学者的关注。尹飞等[14]采用选择性还原焙烧-氨浸工艺从低品位红土镍矿中综合提取镍和钴,在常温常压下采用氨浸法浸出镍和钴,其浸出率分别为89.87%和62.2%,而且浸出剂可以循环使用,但是氨浸工艺的钴浸出率很低,经济价值不高。GUO等[15]研究了高压酸浸工艺处理红土镍矿过程中金属元素的浸出行为,结果表明,镍、钴、锰和镁的浸出率分别达到97%、96%、93%和95%以上,铁的浸出率控制在1%以内。采用高压酸浸工艺钴浸出率达到96%,远高于其他工艺的钴浸出率,同时简化了后续除铁工序,但是该工艺在高温、高压和高盐度的环境下进行,对设备腐蚀严重,且过程中有结垢现象产生,使成本增大。
据报道,在海洋锰结核的综合利用和钛精矿制取富钛料或金红石中采用锈蚀法来提取有价元素和去除杂质[15-18]。锈蚀法具有生产工艺简单,成本低,金属分离效果好及易于工业化等优点。李光辉等[19]采用锈蚀法处理锌浸渣还原铁粉提取镓和锗,结果表明,通过控制溶液pH值和电位φ,可使金属铁生成FeOOH沉淀,而镓和锗以离子形式进入溶液,实现铁与镓和锗分离的目的,且镓和锗浸出率均达到90%以上。红土镍矿经还原焙烧后,镍、钴和铁主要以合金态或金属态存在,所以有望采用锈蚀法实现铁与镍和钴的分离。
本文作者以经氯化离析法预还原处理的红土镍矿为原料,采用锈蚀法提取预还原红土镍矿中镍和钴,实现铁与镍和钴的分离,为红土镍矿的开发利用提供一条新途径。
1 实验
1.1 实验原理
锈蚀法是通过控制溶液pH值和电位φ,使金属在特定的条件下发生电化学腐蚀反应,从而达到分离金属元素的目的。根据冶金热力学数据和能斯特方程计算,绘制出镍、铁和钴在水溶液中电位φ—pH图,如图1所示。
由图1可知,在以空气为氧化剂的情况下,如果溶液 pH值控制在 0.685~4.6,铁将被氧化生成FeOOH,而镍和钴将以Ni2+和Co2+的形式稳定存在,从而达到铁与镍和钴分离的目的。以下反应式说明了在弱酸性溶液中采用锈蚀法提取镍、钴和去除杂质铁的过程。
1)还原矿表面主要发生以下反应:
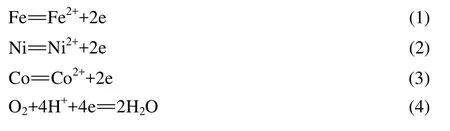
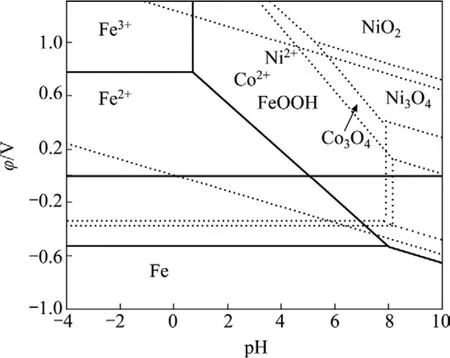
图1 Fe-H2O、Ni-H2O和Co-H2O系的φ—pH图(25 ℃,Fe2+、Fe3+、Ni2+和Co2+的浓度均为1 mmol/L)Fig.1 φ—pH equilibrium diagrams of Fe-H2O, Ni-H2O,Co-H2O systems (25 ℃, concentrations of Fe2+ , Fe3+, Ni2+ and Co2+ are all 1 mmol/L)
2)液相中主要发生以下反应:
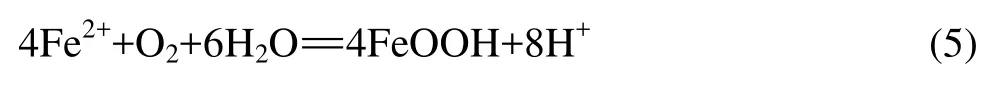
1.2 实验原料
本研究以国外某红土镍矿经氯化离析预还原后的还原矿为实验原料,其主要化学成分如表1所列。所用硫酸为分析纯,水为去离子水。

表1 预还原红土镍矿的主要化学成分Table 1 Chemical compositions of reductive laterite (mass fraction, %)
对预还原红土镍矿进行物相分析,其 XRD谱如图2所示。由图2可以看出,预还原红土镍矿中主要物相为游离二氧化硅、铁橄榄石、镍铁合金和单质铁等。
1.3 实验方法
量取一定酸度的水溶液置于三口烧瓶中,采用水浴加热到一定温度,启动搅拌装置(搅拌叶轮直径为50 mm),通入压缩空气,加入一定量的预还原红土镍矿,浸出一段时间后,过滤、洗涤。将浸出渣烘干称量,并采用王水-氢氟酸-高氯酸法溶解浸出渣。溶液定容后,采用 Tas-990F型原子吸收分光光度计分析溶液中各金属元素的含量。
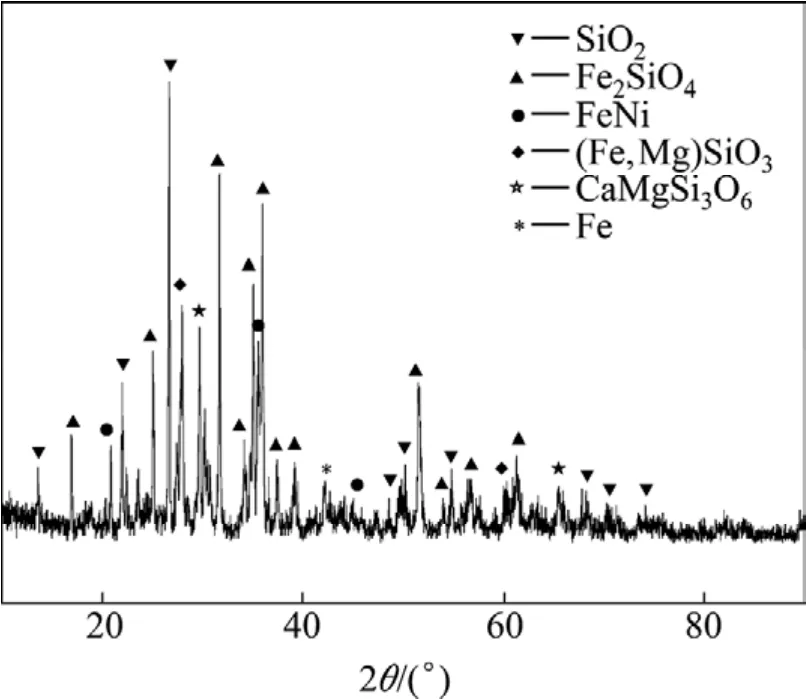
图2 预还原红土镍矿的XRD谱Fig.2 XRD pattern of reductive laterite
2 结果与讨论
2.1 酸矿质量比对镍、钴和铁浸出率的影响
在空气流量5 L/min、锈蚀温度80 ℃、锈蚀时间12 h、搅拌速率300 r/min,固液比1:20和预还原红土镍矿10 g的条件下,分别研究酸矿质量比为0.06:1、0.10:1、0.14:1和 0.18:1时对镍、钴和铁浸出率的影响,结果如图3所示。
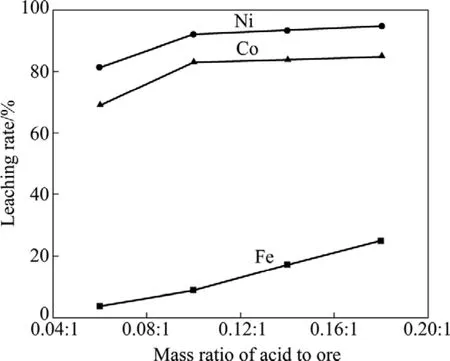
图3 酸矿质量比对各元素浸出率的影响Fig.3 Effect of mass ratio of acid to ore on leaching rate of elements
从图3可以看出,随着酸矿质量比的增大,铁浸出率逐渐增大,这是因为酸矿质量比的提高使体系中H+浓度增高,由反应式(5)可知,提高 H+浓度会抑制FeOOH的生成。同时,图3显示镍和钴的浸出率随酸料质量比的增大迅速增大,当酸料质量比大于 0.10:1时,镍和钴浸出率曲线趋于缓和。由图1可知,增大体系pH值可促进FeOOH的生成,提高Fe2+的氧化速率;当酸料质量比较低时,体系 pH值偏高,导致部分Ni2+和Co2+来不及扩散,被夹杂在FeOOH沉淀中;随着酸料质量比的提高,体系 pH值逐渐降低,抑制了FeOOH的生成,使溶解的Ni2+和Co2+能够及时扩散到浸出液中,当Ni2+和Co2+的扩散与FeOOH的生成达到平衡时,继续降低 pH值对镍和钴浸出率影响不大。综合考虑,本实验选用酸矿质量比为0.10:1。
2.2 空气流量对镍、钴和铁浸出率的影响
当酸料质量比0.1:1、预还原红土镍矿10 g、锈蚀温度80 ℃、锈蚀时间12 h、搅拌速率300 r/min和固液比1:20时,分别研究空气流量为0、0.5、1、2、3、4和5 L/min时对镍、钴和铁浸出率的影响,结果如图4所示。

图4 空气流量对各元素浸出率的影响Fig.4 Effect of air flux on leaching rate of elements
由图4可以看出,随着空气流量的增大,镍和钴的浸出率迅速增大,铁浸出率逐渐下降,这是因为空气流量增大导致体系溶解氧浓度增大,促进了镍、钴和铁的溶解,同时溶解氧浓度的提高也促进了Fe2+的氧化,在一定程度上降低了铁的浸出率。当空气流量高于1 L/min时,铁、镍和钴浸出率均无显著变化。其原因归结于体系中氧的溶解达到平衡,继续增大空气流量,溶解氧浓度不再提高,所以,继续增大空气流量对铁、镍和钴浸出率没有显著影响。综合考虑,选择空气流量为1 L/min,此时铁、镍和钴浸出率分别为8.8%、92.2%和83.4%。
2.3 锈蚀温度对镍、钴和铁浸出率的影响
当酸料质量比0.1:1、预还原红土镍矿10 g、空气流量1 L/min、锈蚀时间12 h、搅拌速率300 r/min和固液比1:20时,分别研究锈蚀温度(25、60、80和90℃)对镍、钴和铁浸出率的影响,结果如图5所示。
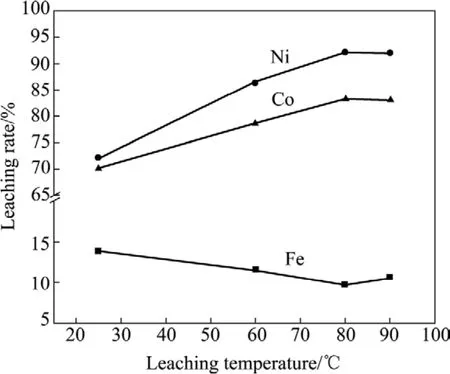
图5 浸出温度对各元素浸出率的影响Fig.5 Effect of leaching temperature on leaching rate of elements
由图5可以看出,随着温度的升高,镍和钴浸出率显著增大,在80 ℃时达到最大值,继续提高温度,镍和钴浸出率呈下降趋势,铁浸出率与之相反。80 ℃时铁、镍和钴浸出率分别为8.8%、92.2%和83.4%。由阿累尼乌斯公式k=Aexp[-E/(RT)]可知:升高温度,表观速率常数k增大,铁、镍和钴的溶解速率增大,同时也提高了Fe2+被氧化生成FeOOH的速率,所以,镍和钴浸出率随温度的升高迅速提高,铁浸出率在一定程度上呈下降趋势。当锈蚀温度高于 80 ℃时,体系中氧的溶解度下降,抑制了反应的进行,所以,镍和钴浸出率呈下降趋势,铁浸出率呈上升趋势。
2.4 锈蚀时间对镍、钴和铁浸出率的影响
当酸料质量比0.1:1、红土镍矿还原矿10 g、空气流量1 L/min、锈蚀温度80 ℃、搅拌速率300 r/min和固液比 1:20时,分别研究锈蚀时间(2、4、6、8、10、12 h)对镍、钴和铁浸出率的影响,结果如图6所示。
由图6可以看出,随时间的延长,镍和钴浸出率迅速增大,当锈蚀时间超过4 h后,镍和钴浸出率曲线趋于缓和,而铁浸出率随时间延长持续下降,且下降速度逐渐减小。这是因为反应初期随着时间的延长,铁、镍和钴迅速溶解,而随着反应的进行,易溶镍和钴几乎完全溶解,导致镍和钴的溶解速率下降,而体系中的Fe2+氧化生成FeOOH是产酸过程,使体系H+活度增大,抑制FeOOH的生成。综合考虑,本实验选用8 h为后续实验的锈蚀时间。

图6 浸出时间对各元素浸出率的影响Fig.6 Effect of leaching time on leaching rate of elements
2.5 搅拌速率对镍、钴和铁浸出率的影响
当酸料质量比0.1:1、预还原红土镍矿10 g、空气流量1 L/min、锈蚀温度80 ℃、锈蚀时间8 h和固液比 1:20时,分别研究搅拌速率(100、300、500、700 r/min)对镍、钴和铁浸出率的影响,结果如图7所示。
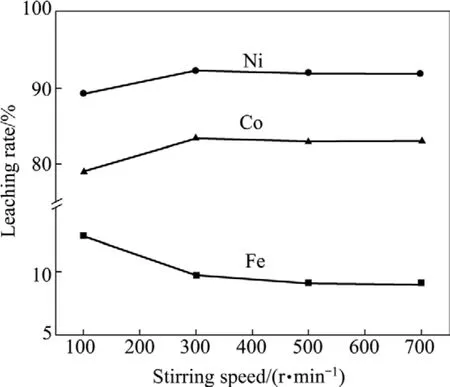
图7 搅拌速率对各元素浸出率的影响Fig.7 Effect of stirring speed on leaching rate of elements
从图7可以看出,随着搅拌速率的增大,镍和钴浸出率呈上升趋势,而铁浸出率呈下降趋势,当搅拌速率大于300 r/min时,铁、镍和钴浸出率均无显著变化。液-固反应体系主要控制步骤为扩散控制、化学反应控制和混合控制。增大搅拌速率导致液固相对运动加快,液固膜厚度降低,扩散速率加快,增大体系中溶解氧和固体颗粒接触的几率,能促进铁、镍和钴的溶解;同时,增大搅拌速率会提高溶液与空气的接触几率,导致溶解氧浓度增高,促进Fe2+的氧化,在一定程度上使铁的浸出率降低。当搅拌速率达到一定程度后,反应不再受扩散控制,而受化学反应速率控制,所以,继续增大搅拌速率,铁、镍和钴浸出率几乎没有变化。
2.6 固液比对镍、钴和铁浸出率的影响
在酸料质量比0.1:1、预还原红土镍矿10 g、空气流量1 L/min、锈蚀温度80 ℃、锈蚀时间8 h和搅拌速率300 r/min的条件下,分别研究固液比(1:5、1:10、1:15、1:20)对镍、钴和铁浸出率的影响,结果如图8所示。
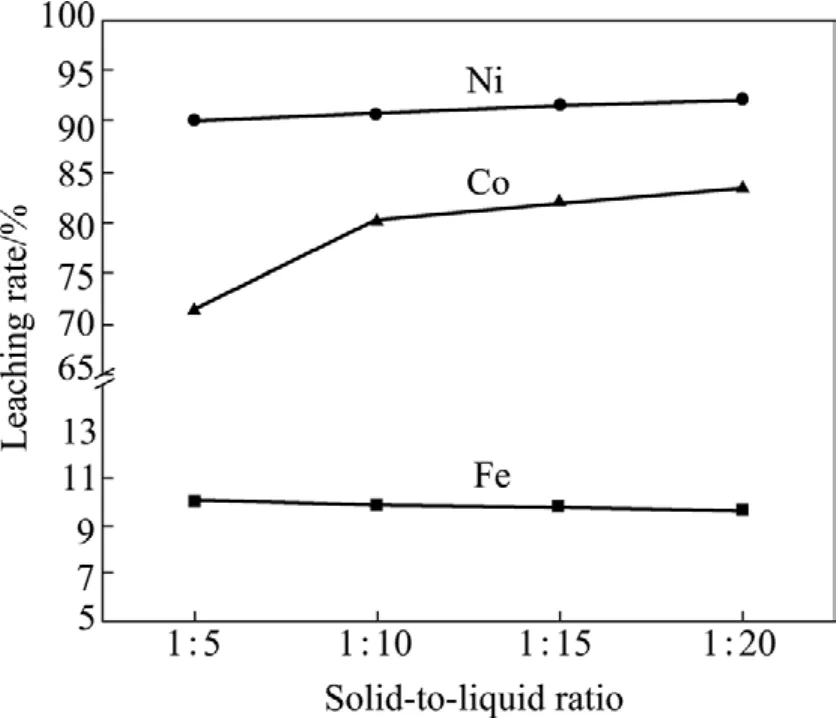
图8 固液比对各元素浸出率的影响Fig.8 Effect of solid-to-liquid ratio on leaching rate of elements
从图8可以看出,在所研究的范围内固液比变化对镍和铁浸出率的影响不大,钴浸出率随固液比降低迅速上升,当固液比降低到1:10之后,钴浸出率变化趋于缓和,这是因为固液比增大,浸出液中各离子浓度也随之增大,使Co3O4/Co2+左移,而反应体系的pH值几乎不变,超出了电位φ—pH图中钴以离子态存在于水溶液中的稳定区域,所以,在固液比较高时钴浸出率较低。而在所研究的范围内,体系pH值和Ni2+浓度能使镍以离子形态稳定地存在于水溶液中。
3 结论
1)经预还原处理的红土镍矿中镍和钴以金属态存在,并与金属铁共存;热力学分析表明,在 pH值为 0.685~4.6的酸性溶液中,以空气为氧化剂,可使铁产生锈蚀,而金属镍和钴以离子形式进入溶液。
2)采用锈蚀法处理预还原红土镍矿,镍、钴和铁浸出率主要受酸矿质量比、空气流量、锈蚀温度、锈蚀时间和搅拌速率的影响;增加酸矿质量比,镍、钴和铁浸出率增加;增大空气流量、升高温度、增大搅拌速率和延长锈蚀时间,均导致镍和钴浸出率增加,铁浸出率降低。
3)锈蚀法处理预还原红土镍矿的较优实验条件如下:酸矿质量比0.10:1,空气流量1 L/min、锈蚀温度80 ℃、锈蚀时间8 h、搅拌速率300 r/min和固液比1:10,在此条件下处理预还原红土镍矿,镍和钴浸出率分别达到 90.9%和 80.2%,而铁的浸出率仅为9.9%,有效地实现了铁与镍和钴的分离。
4)研究结果将为工艺研究提供指导,通过提高固液比、浸出液循环利用等措施提高浸出液中有价金属镍和钴浓度和镍铁比,便于浸出液的后续处理,降低处理过程的用水量和红土镍矿的处理成本。
[1]彭容秋.镍冶金[M].长沙: 中南大学出版社, 2005: 3-4.PENG Rong-qiu.Metallurgy of nickel [M].Changsha: Central South University Press, 2005: 3-4.
[2]PICKLES C A.Drying kinetics of nickeliferous limonitic laterite ores [J].Minerals Engineering, 2003, 16(12): 18-21.
[3]任洪九, 王立川.有色金属提取冶金手册(铜镍)[M].北京:冶金工业出版社, 2000: 512-514.REN Hong-jiu, WANG Li-chuan.Handbook of extractive metallurgy of nonferrous metals (copper and nickel)[M].Beijing:Metallurgical Industry Press, 2000: 512-514.
[4]及亚娜, 孙体昌, 蒋 曼.红土镍矿提镍工艺进展[J].矿产保护与利用, 2011(2): 43-49.JI Ya-na, SUN Ti-chang, JIANG Man.Advance in extraction of nickel from laterite nickel ore[J].Conservation and Utilization of Mineral Resources, 2011(2): 43-49.
[5]郭学益, 吴 展, 李 栋.镍红土矿处理工艺的现状和展望[J].金属材料与冶金工程, 2009, 37(2): 3–9.GUO Xue-yi, WU Zhan, LI Dong.The status and prospect of the technologies of nickel laterite [J].Metal Materials and Metallurgy Engineering, 2009, 37(2): 3-9.
[6]MCDONALD R G, WHITINGTON B I.Atmospheric acid leaching of nickel laterites review: Part I.Sulphuric acid technologies [J].Hydrometallurgy, 2008, 91(1/4): 35-55.
[7]MCDONALD R G, WHITINGTON B I.Atmospheric acid leaching of nickel laterites review: Part Ⅱ.Chloride and bio-technologies [J].Hydrometallurgy, 2008, 91(1/4): 56-69.
[8]佘宗华, 刘建忠, 宁顺明.从印尼含镍红土矿中浸出镍、钴工艺试验研究[J].湿法冶金, 2011, 30(2): 120-123.SHE Zong-hua, LIU Jian-zhong, NING Shun-ming.Experimental study on technology of leaching nickel and cobalt from lateritic-nickel ore in Indonesia [J].Hydrometallurgy of China, 2011, 30(2): 120-123.
[9]CHANDER S, SHARMA V N.Reduction roasting-ammonia leaching of nickeliferous laterites [J].Hydrometallurgy, 1981,7(4): 315-327.
[10]PLESSIS C A, SLABBERT W, HALLBERG K B, JOHNSON D B.Ferredox: A biohydrometallurgical processing concept for limonitic nickel laterites [J].Hydrometallurgy, 2011, 109(3/4):221-229.
[11]赵昌明, 翟玉春, 刘 岩, 段华美.红土镍矿在 NaOH 亚熔盐体系中的预脱硅[J].中国有色金属学报, 2009, 19(5): 949-954.ZHAO Chang-ming, ZHAI Yu-chun, LIU Yan, DUAN Hua-mei.Pre-desilication of laterite in NaOH sub-molten salt system [J].The Chinese Journal of Nonferrous Metals, 2009, 19(5):949-954.
[12]LI Bo, WANG Hua, WEI Yong-gang.The reduction of nickel from low-grade nickel laterite ore using a solid-state deoxidisation method [J].Minerals Engineering, 2011, 24(14):1556-1562.
[13]KIM J, DODBIBA G, TANNO H, MATSUO S, FUJITA T.Calcination of low-grade laterite for concentration of Ni by magnetic separation [J].Minerals Engineering, 2010, 23(4):282-288.
[14]尹 飞, 阮书锋, 江培海, 王成彦, 陈永强.低品位红土镍矿还原焙烧氨浸实验研究[J].矿冶, 2007, 16(7): 29–32.YIN Fei, RUAN Shu-feng, JIANG Pei-hai, WANG Cheng-yan,CHEN yong-qiang.Experimatal study on roasted ore of poor nickeliferous larerite ore with ammonia leaching technology [J].Mining and Metallurgy, 2007, 16(7): 29-32.
[15]GUO Xue-yi, SHI Wen-tang, LI Dong, TIAN Qing-hua.Leaching behavior of metals from limonitic laterite ore by high pressure acid leaching [J].Trans Nonferrous Met Soc China,2011, 21(1): 191-195.
[16]钟 祥, 贺泽权, 沈裕军, 段兴无, 黄元琼, 毛拥军.熔炼-锈蚀-萃取法从大洋多金属结核提取有价金属: 中国,CN96110871.1[P].1998-02-04.ZHONG Xiang, HE Ze-quan, SHEN Yu-jun, DUAN Xing-wu,HUANG Yuan-qiong, MAO Rong-jun.Extraction of valuable metals from ocean polymetallic noddle by smelting-corrosionextraction process: China, CN96110871.1 [P].1998-02-04.
[17]郭宇峰, 刘水石, 马晓雯, 姜 涛, 邱冠周.盐酸强化还原钛铁矿中金属铁的锈蚀动力学[J].中国有色金属学报, 2010,20(10): 2038–2044.GUO Yu-feng, LIU Shui-shi, MA Xiao-wen, JIANG Tao, QIU Guan-zhou.Rusting kinetics of metallic iron in reduced ilmonite strengthened by hydrochloride [J].The Chinese Journal of Nonferrous Metals, 2010, 20(10): 2038–2044.
[18]GEETHA K S, SURENDER G D.Experimental and modeling studies on the aeration leaching process for metallic iron removal in the manufacture of synthetic rutile [J].Hydrometallurgy, 2000,56(1): 41-62.
[19]李光辉, 董海刚, 姜 涛, 黄柱成, 郭宇峰, 杨永斌.锈蚀法从浸锌渣还原铁粉中分离镓锗的基础与应用[J].中国有色金属学报, 2004, 14(11): 1940–1946.LI Guang-hui, DONG Hai-gang, JIANG Tao, HUANG Zhu-cheng, GUO Yu-feng, YANG Yong-bin.Fundamentals and applications of separating Ga and Ge from ferrous powder reduced from zinc leach residues by corrosion process [J].The Chinese Journal of Nonferrous Metals, 2004, 14(11): 1940-1946.

