探讨复方滴眼剂治疗眼部细菌感染的安全性和有效性
蒋大义,谢守霞,马惠莱,杨宏图,孙业红
(广东省深圳市人民医院 暨南大学第二附属医院药学部,深圳 518020)
第4代氟喹诺酮类是一类针对革兰氏阳性菌的广谱抗菌药,也是治疗未知耐药性病原微生物眼睛感染的一类最佳抗菌药[1]。据报道莫西沙星对肺炎链球菌、流感(嗜血)杆菌、甲氧西林敏感葡萄球菌有效,对肠杆菌、绿脓假单胞菌也有效[2]。国际指南都以局部用抗生素和类固醇作为治疗睑缘炎的首选方案,类固醇主要用于控制眼睛表面和眼睑的炎症。该推荐方案需要患者每天服用抗生素和类固醇药物多次,这对患者依从性不利。含有莫西沙星和地塞米松的复方制剂可提高眼睑炎患者的依从性。据报道莫西沙星和地塞米松复方滴眼液在预防术后感染和炎症安全有效[3],但对已有细菌感染和炎症患者的治疗效果还存在争议。本研究通过对比研究0.5%莫西沙星和0.1%地塞米松复方滴眼液与0.5%莫西沙星和0.1%地塞米松滴眼液同时使用,来评估复方莫西沙星滴眼液治疗眼部细菌感染的安全性和有效性。
1 资料和方法
1.1 一般资料
2007年1月~2011年12月,在我院眼科就诊,年龄18岁以上、诊断为睑缘炎、角膜炎或结膜炎的患者。纳入标准:眼部球结膜充血、眼脸结膜、结膜有渗出液、眼睑红斑、眼睑脱皮结痂且评分≥2分(单侧)。排除标准:研究期间有不可控的青光眼、高眼压、佩戴隐形眼镜。研究前72h内口服或局部服用抗生素患者,研究前14d内服用可影响全身的类固醇药物患者,研究前1周内局部服用类固醇或非类固醇抗炎药物患者,研究前24h服用类固醇药物患者。已知或怀疑对氟喹诺酮类或类固醇过敏的患者,怀孕或哺乳期妇女,有类固醇药物禁忌患者。
1.2 方法
1.2.1 给药方法
该研究采用随机、双盲和平行对照试验。患者6人1组随机分配,以双盲方式给药,治疗持续7d。复方药物组和对照组的给药方式为:复方药物组包含0.5%莫西沙星和0.1%地塞米松复方药物滴眼液一瓶(A瓶)和安慰剂一瓶(B瓶);对照组包含0.5%莫西沙星滴眼液一瓶(A瓶)和0.1%地塞米松滴眼液一瓶(B瓶)。每滴都滴入双侧结膜囊,每天4次连续7d。给药方法是A瓶首先滴入,5min后再滴入B瓶。
1.2.2 评价方法
细菌性睑缘炎、角膜炎、结膜炎患者在入院时和治疗7d后,通过临床观察和荧光角膜染色来确诊。医生依据眼部体征(球结膜充血、睑结膜,结膜渗出液、眼睑红斑和眼睑脱皮结痂)来评分。测量最佳的矫正视力,角膜、前房、结膜和眼睑的评估采用生物显微镜,双眼眼内压采用Goldman眼压计来测量。收集入院和治疗7d后感染部位样本并作微生物检查。样本在需氧或微需氧环境下培养于5%的血琼脂平板和巧克力琼脂平板、同时在胰蛋白酶大豆肉汤(TSB)培养基中培养48h。培养细菌的初步鉴定采用革兰氏染色和常规生化反应鉴定,最终鉴定和亚型采用全自动核糖分型系统鉴定。治疗后4d,医生对包括眼科检查在内的治疗效果进行中期评估。
1.3 统计学分析
两治疗组间连续变量比较采用t检验,分类变量比较采用χ2检验。方差分析用于评估眼部体征、视力和眼内压的治疗效果和时间效应。配对比较采用配对t检验。数据分析采用Spass12.0软件分析,P<0.05有统计学意义。
2 结果
2.1 研究对象总体情况
本研究共纳入102例眼部细菌性炎症患者,其中复方药物组和对照组各51例。5例中途失访,最后评估的有97例,复方药物组49例(98只眼睛),对照组48例(96只眼睛)。对照组有1例患者在治疗4d后因眼部灼伤退出研究。
2.2 研究对象基本特征
复方药物组平均年龄57岁,对照组平均年龄58.5岁。所有眼睛都有睑缘炎而无角膜炎,对照组2只眼睛有结膜炎。在纳入研究时,复方药物组8.2%的患者、对照组6.3%的患者使用了眼药。两研究组眼睛体征相似,但8.3%的复方药物组和16.3%的对照组睑结膜是正常的(P=0.002)(见表1)。
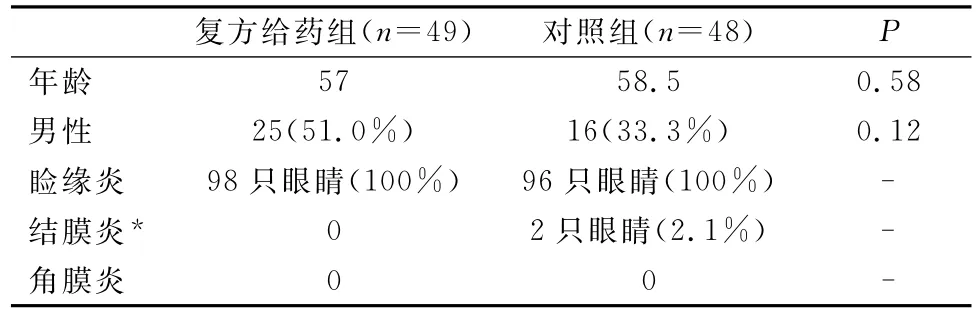
表1 两组患者基本特征
2.3 临床疗效、体征、症状评估
在研究结束时,81.6%的复方药物组和82.3%的对照组患者临床症状消失(P>0.05)(表2)。两组患者眼部体征随着时间显著改善(P<0.0001),但组间无统计学差异(P=0.428)。两组患者的眼睛不适、流泪和畏光等眼部症状都有显著改善,但两组间症状无统计学差异。两组患者的眼部体征改善无统计学差异,但眼睑红斑在复方药物组比对照组改善显著(复方药物组100%;对照组92.7%,P=0.0194)、眼睑脱皮结痂在复方药物组比对照组改善显著(复方药物组98%;对照组89.6%,P=0.0337)。
给药7d后,角膜、眼睑、结膜和前房的活组织显微镜检查或角膜荧光染色显示两组间无显著差异。两组间最佳矫正视力也无显著差异。但复方药物组的改善程度有显著差异(P=0.02,复方药物组:第1d:0.10±0.15,第8d:0.08±0.15)。两组间的眼内压无显著差异,两组患者的眼内压随时间显著增加(复方药物组:P<0.0001,第1d:13.9±2.4mmHg,第8d:15.0±2.7mmHg;对照组:P<0.0001,第1d:13.9±2.8mmHg,第8d:15.5±2.5mmHg)。
笔者从结膜和眼睑样本分离出了850种细菌。治疗前分离出的细菌占总分离的64.5%,革兰氏阳性菌94.3%,革兰氏阴性菌仅5.6%。复方药物组和对照组治疗有效的微生物分别为84%、83%(表2),复方药物组对结膜细菌的有效率是93%,对照组是78%,然而,复方药物组对眼睑细菌的效力与对照组无显著统计学差异。
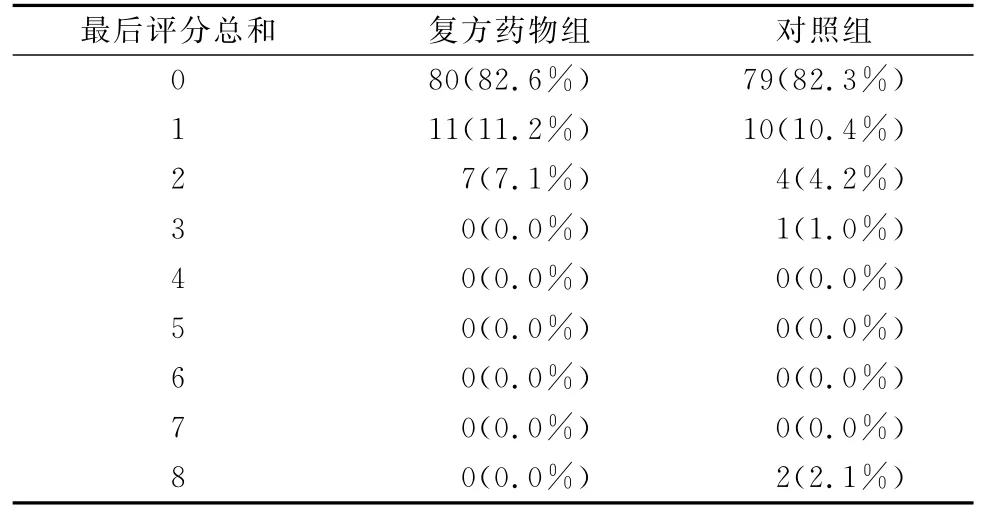
表2 治疗7d后眼部体征评分情况
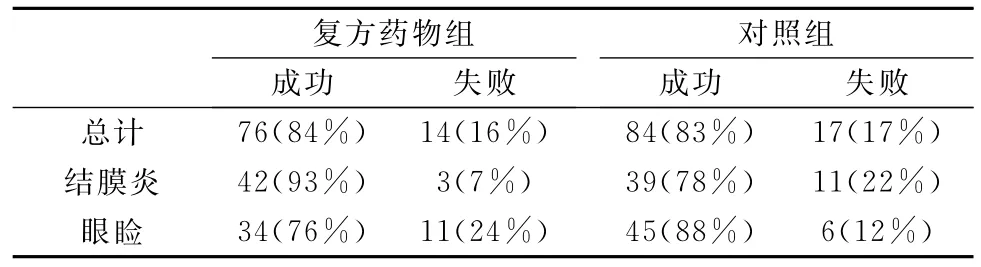
表3 不同治疗组睑缘炎患者微生物治疗效果
2.4 安全性评估
复方药物组有5例不良反应,对照组有7例不良反应。复方药物组1例不良反应(夜间滴加眼药后不能入睡)、对照组2例不良反应(灼伤感和眼内压增加各1位)被认为与药物相关。两组间在不良反应的发生率上没有显著差异(见表4)。
3 讨论
本文探讨30.5%莫西沙星和0.1%地塞米松的复方滴眼液与同时给予0.5%莫西沙星滴眼液和0.1%地塞米松滴眼液治疗眼部细菌性炎症的安全性和有效性。两组给药方式在治疗眼部感染炎症时有很好的临床疗效。两组绝大部分患者临床症状消退、眼部症状和体征明显改善。治疗7d后,组间统计学差异仅存在于复方药物组有更多的眼睛眼睑水肿改善和眼睑红斑改善。与这些临床观察一致的是所有的结膜和眼睑微生物培养结果显示两治疗组间的抗微生物活性无显著差异。
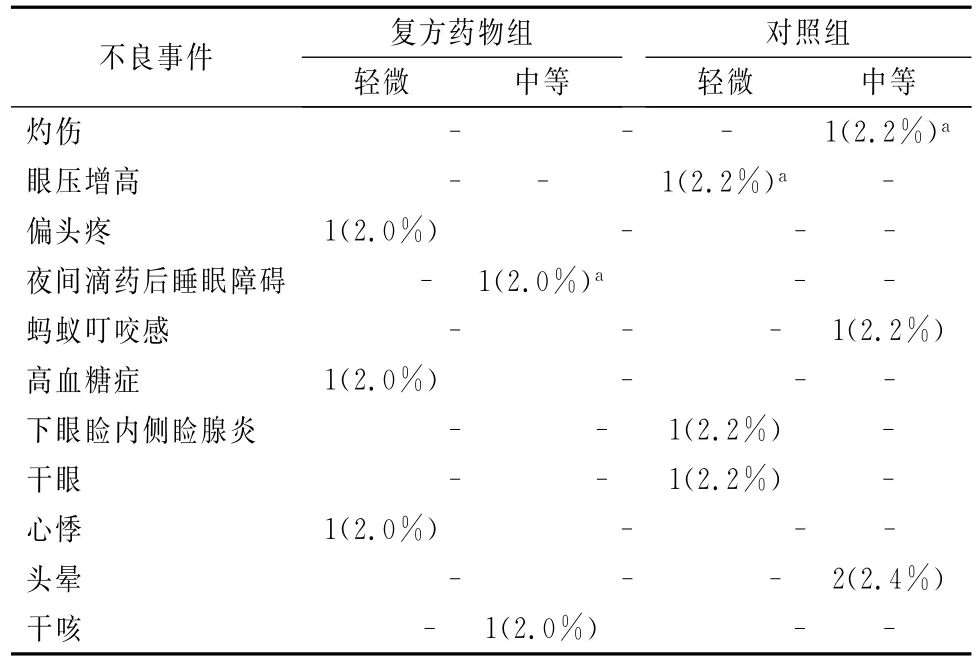
表4 两组患者用药后的不良事件
复方药物组给药方案与对照组给药的安全性和耐受性一致,仅有3例不良反应发生;对照组1例患者出现中等灼伤感,1例患者出现轻微眼内压升高,复方药物组1例出现中等失眠。笔者认为使用滴眼液后失眠或与治疗相关,因为理论上讲,糖皮质激素可以造成睡眠障碍。两组对微生物的抗菌疗效一致。
复方药物滴眼液提供了简单方便的给药方式,增加了患者依从性,避免需要使用多种滴眼液时,常会造成滴加剂量错误[4]。另外,应用单瓶滴眼液更简单方便,且较两瓶滴眼液更经济。
复方药物(复方药物组)比对照组可能效果更好,患者满意度也更高,尽管在本随机对照研究中效果没有差别。为防止本研究的偏倚,复方药物组在复方药物滴眼剂滴入5min后再滴入安慰剂滴眼液。假如患者等不及5min,则有可能将之前滴入的药液冲洗出来。因此,安慰剂滴眼液可能会冲洗出某些复方滴眼剂,从而轻微降低患者药效。
[1]Callegan MC,Ramirez R,Kane ST,et al.Antibacterial activity of the fourth-generation fluoroquinolones gatifloxacin and moxifloxacin against ocular pathogens[J].Adv Ther,2003,20(2):246-252.
[2]Miller D.Review of moxifloxacin hydrochloride ophthalmic solution in the treatment of bacterialeye infections[J].Clin Ophth,2008,2(3):77-91.
[3]Campos M,Avila M,Wallau A,et al.Efficacy and tolerability of a fixed-dose moxifloxacin-dexamethasone formulation for topical prophylaxis in LASIK:a comparative,double-masked clinical tria[J].Clin Ophth,2008,2(4):331-338.
[4]Robin AL,Novack GD,Covert DW,Crockett RS,Marcic TS.Adherence in glaucoma:objective measurements of once-daily and adjunctive medication use[J].Am J Ophthalmol,2007,144(5):533-540.

