硅锌矿在(NH4)2SO4-NH3-H2O体系中高液固比下的浸出动力学
刘志宏,曹志阎,刘智勇,李启厚,李玉虎
(中南大学 冶金科学与工程学院,湖南 长沙,410083)
近年来,随着我国锌产量的高速增长,作为主要炼锌原料的硫化锌矿资源已趋于短缺,开发利用氧化锌矿资源的重要性日益凸显。我国西南、西北等地氧化锌矿资源丰富,但其品位低、难选、硅和碱性脉石含量高,且矿物组成复杂,含锌矿物主要有硅锌矿(Zn2SiO4)、 异 极 矿 (Zn4(Si2O7)(OH)2·H2O)、 菱 锌 矿(ZnCO3)和水锌矿(Zn5(CO3)2(OH)6)等,属典型的难冶资源。采用火法工艺处理,可以实现锌与Fe,Si,Ca和 Mg等杂质的分离[1],但金属回收率低,能耗高,环境污染严重,因此,酸浸、苛性碱浸和氨浸等湿法工艺成为研究的热点。浸出时硅胶的大量生成导致液固分离困难,是酸浸处理氧化锌矿的技术难点。为此,已开发出若干种工艺技术[2−5],主要分为 2类:第 1类是浸出后采用中和絮凝法得到易于分离的矿浆,如中和絮凝法和老山工艺;第2类是在浸出过程中抑制硅的溶解,主要有Redina法、微波辅助法和高压酸浸法等。这些工艺仅适合处理低碱性脉石的高品位氧化锌矿。与酸浸工艺相比,苛性碱浸出工艺选择性较好[6−8],但也存在一些难点:浸出液中硅、铝、铅含量较高,除杂困难;浸出液难以进行有效电积,或电积时只能产出树枝状锌粉。该工艺目前尚处于实验室研究阶段。氨法浸锌工艺简单、高效、原料适应性广、选择性高,并且终端产品灵活,既可生产活性氧化锌,也可电积获得阴极锌。与其他工艺相比,更适合处理高硅高碱性脉石的低品位氧化锌矿。但研究表明,矿石中锌的物相对其浸出率具有决定性的影响,当矿石中硅锌矿等硅酸盐类含锌矿物含量较高时,锌浸出率偏低[9−11]。人们对氧化锌矿氨浸动力学进行了研究,表明浸出速率控制步骤以及表观活化能、反应级数和速率常数等浸出动力学参数,因矿石品位及含锌物相而异[12−16]。由于这些研究所用原料均为天然氧化锌矿石,其矿物组成既包括游离氧化锌,又含有一定量的硅酸盐类锌矿物,因此,并未揭示硅酸盐类锌矿物在氨浸条件下难以浸出的原因。刘智勇等[17]对硅锌矿在(NH4)2SO4-NH3-H2O体系中的浸出机理进行了系统研究,确定其浸出反应为:

总反应为:

式中:i为1,2,3或4。在浸出过程中,Zn2+与NH3形成配合物进入溶液;硅酸根首先形成(NH4)2SiO3进入溶液;(NH4)2SiO3不稳定,发生水解生成 NH3与H4SiO4(aq),当溶液中SiO2浓度达到饱和后会转化为无定形 SiO2沉淀。在低液固质量比下浸出,浸出液中H4SiO4很快达到饱和,速率过程受反应(3)制约,甚至趋于停滞。而在很高的液固比下,硅锌矿浸出缓慢仍是其难以浸出的内在因素。本文作者对硅锌矿在高液固质量比下的浸出动力学进行研究;采用受孔隙扩散控制的粒子模型,对浸出实验数据进行处理,表征浸出过程的控制步骤、表观活化能和反应级数等动力学特性。
1 实验
1.1 实验原料
硅锌矿样品系以云南兰坪的异极矿为原料,于1 100 ℃下煅烧3 h制备得到。煅烧反应方程式为:

异极矿及由其制备的硅锌矿样品XRD图谱如图1所示。硅锌矿样品破碎、筛分后备用,如无特别说明,浸出实验样品粒度为96~109 μm。表1所示为该样品的主要成分、比表面积、孔隙率及平均孔径等,图2所示为其SEM照片。
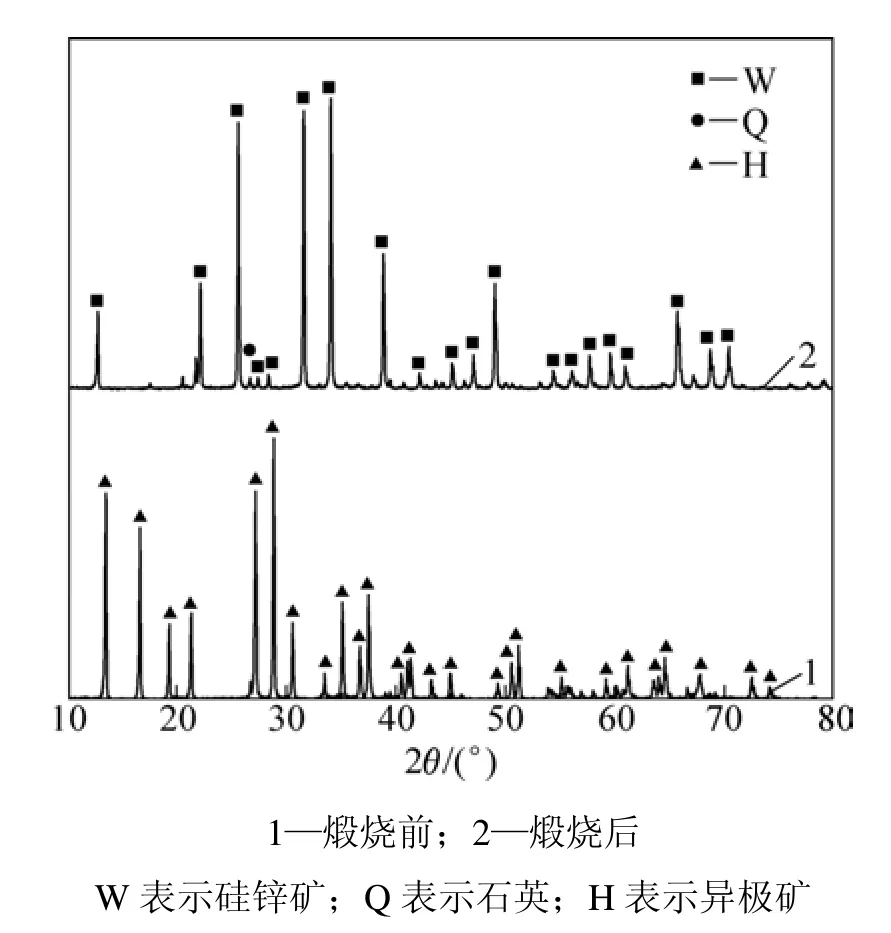
图1 样品的XRD图谱Fig.1 XRD patterns of ore samples

表1 硅锌矿物理化学性质Table 1 Physicochemical properties of willemite sample
由图1和表1可知:异极矿样品煅烧后,已完全脱水转化为硅锌矿,杂质含量很低,基本为硅锌矿纯矿物,其 XRD图谱及化学成分与文献[6,18]中的一致。由图2可见:硅锌矿样品形貌为类球形,颗粒粒径均匀,疏松多孔,是由粒度为1 μm左右的微细粒子组成的多孔团聚体。
实验试剂为氨水(AR,湖南株洲石英化玻有限公司生产)、硫酸铵(AR,上海国药集团生产)、硅酸钠(AR,广东汕头西陇化工有限公司生产);水为去离子水。

图2 硅锌矿样品SEM分析结果Fig.2 SEM photographs of willemite sample with particle size of 96−109 μm
1.2 浸出实验
浸出液根据设定的总氨浓度、NH4+与 NH3摩尔比,由(NH4)2SO4,NH3·H2O和去离子水配制而成。浸出实验在2 L三口瓶中进行,瓶上3个开口分别装设温度计、机械搅拌器(2片半径为50 mm桨叶)。三口瓶置于恒温水浴中,水浴温度在−1~1 ℃波动。每次配制1 L浸出液,置于三口瓶中,预热到实验温度,加入5 g样品开始浸出。每隔一定时间,取10 mL矿浆离心分离,分别取浸出液及渣样进行分析检测。
1.3 分析检测
用EDTA络合滴定法测定浸出液中锌浓度,据此计算锌浸出率;采用日本RIGAKU−TTRⅢ型X 线衍射仪(Cu靶,波长λ=0.154 06 nm)对样品进行物相分析;用日本JSM−6360LV 型扫描电镜(SEM)观察样品形貌;采用低温氮吸附法分析矿石样品比表面积和孔隙结构,仪器为美国ASAP2010型比表面积及孔径测定仪。
2 结果与讨论
2.1 搅拌速度对浸出率的影响
在总氨浓度为7 mol/L,NH4+与NH3摩尔比为1,温度为323 K,液固质量比为200的条件下,考察搅拌速度对锌浸出率影响,结果如图3所示。由图3可见:当搅拌速度低于250 r/mim时,浸出速率随搅拌强度增大而增加;当搅拌速度大于250 r/mim后,浸出速率的增长趋于平稳,说明在该搅拌强度下,已足以消除外扩散对浸出速率的影响。在随后的实验中,搅拌速度固定为350 r/min。
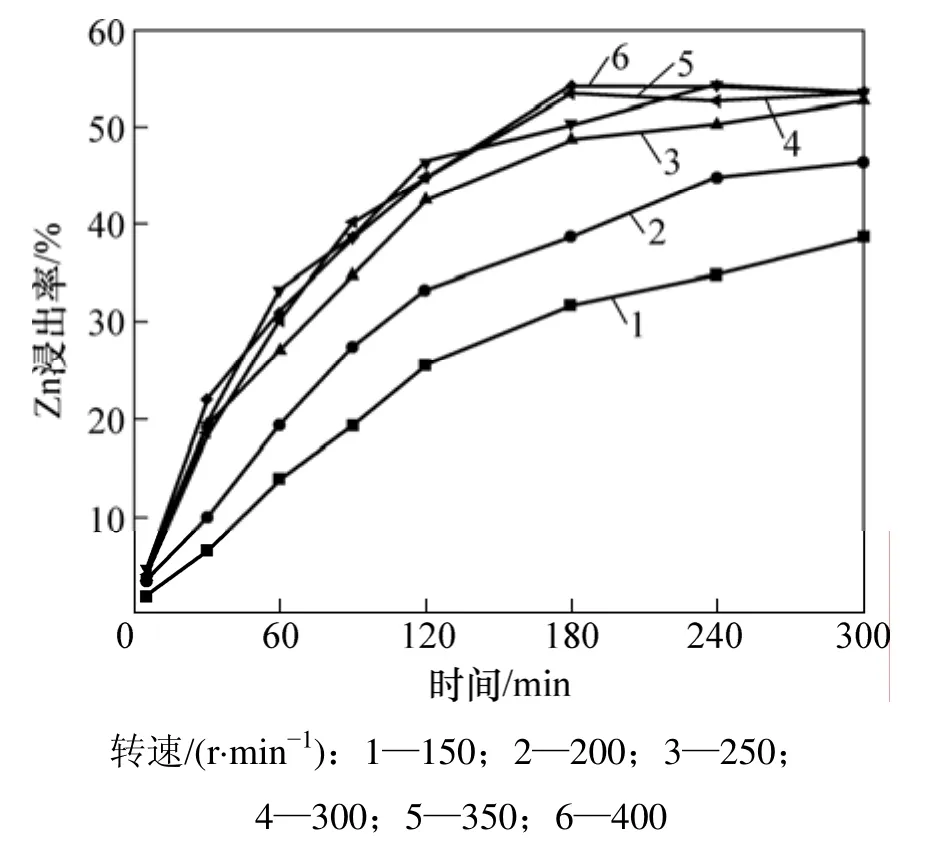
图3 搅拌速度对浸出率的影响Fig.3 Effect of stirring speed on zinc leaching efficiency
2.2 温度对浸出率的影响

图4 温度对Zn浸出率的影响Fig.4 Effect of temperature on zinc leaching efficiency
2.3 总氨浓度对浸出率的影响
在NH4+与NH3摩尔比为1、温度为323 K、液固质量比为200、搅拌速率为350 r/min的条件下,考察总氨浓度对锌浸出率的影响,结果如图5所示。由图5可见:总氨浓度对锌浸出率的影响非常显著。在总氨浓度为7 mol/L时,锌浸出率随着浸出时间的延长快速增大,经180 min浸出,Zn的浸出率达到53.31%,之后停止增大;而当总氨浓度降低到4 mol/L时,锌的浸出率随浸出时间的延长变化缓慢,浸出 300 min后,锌浸出率只有22.79%。
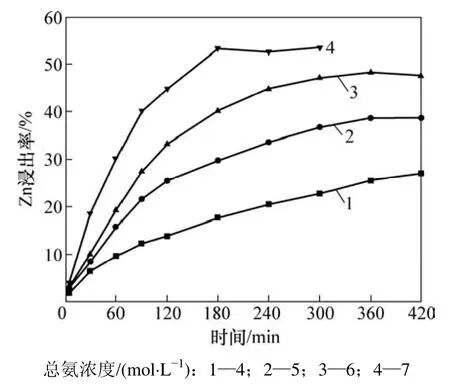
图5 总氨浓度对Zn浸出率的影响Fig.5 Effect of total ammonium concentration on zinc leaching efficiency
2.4 结果分析
2.4.1 动力学模型
实验所用硅锌矿样品为多孔球形颗粒(见图2、表1),液相反应物会扩散到固体内部,扩散与化学反应不是仅仅发生在颗粒外表面,而是同时发生在整个扩散区域内,在动力学数据处理中,不可简单地使用收缩未反应核模型。目前,多孔颗粒非催化反应动力学模型主要有均匀模型[19]、随机分布模型[20−22]和粒子模型[23−25]。分析结果表明:均匀模型及随机分布模型与样品孔隙结构及实验数据难以吻合,不适用于对本研究所得实验数据进行处理。
粒子模型最初用于描述多孔氧化物气体还原过程。该模型假设矿石颗粒是一些性质相同的微小粒子集合体,这些粒子致密且形状单一,在浸出过程中皆遵循收缩未反应核模型。液相反应物通过粒子间的孔隙向颗粒中心扩散,并与粒子反应;固体反应物含量随着反应进行而减少。粒子模型示意图如图6所示。研究表明:该模型也适用于多孔颗粒湿法浸出过程[18, 26]。

图6 粒子模型Fig.6 Grain model
当孔隙扩散不可忽略时,浸出过程类似于受内扩散控制的致密颗粒收缩核反应。在这种情况下,对于球体或类球体矿石颗粒的反应,粒子模型数学表达式如下:
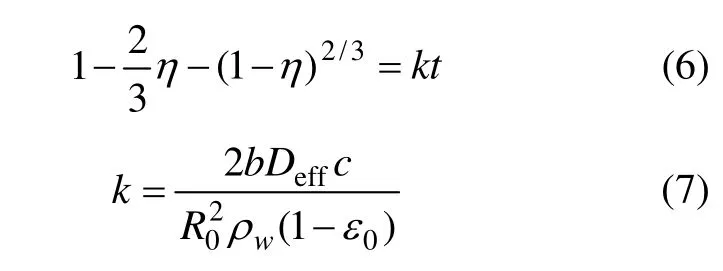
式中:c为总氨浓度,mol/L;R0为颗粒的起始半径,cm;ρw为矿石的密度,mol/cm3;ε0为矿石颗粒初始孔隙率,%;Deff为扩散系数,cm2/s;b为化学计量数。
将图4和图5 所示数据转化为锌浸出率的函数1−2/3η−(1−η)2/3与浸出时间 t的关系图,分别见图7 和图8。

图7 不同温度下 1−2/3η−(1−η)2/3与时间关系图Fig.7 Relationship between 1−2/3η−(1−η)2/3 and time at various temperatures
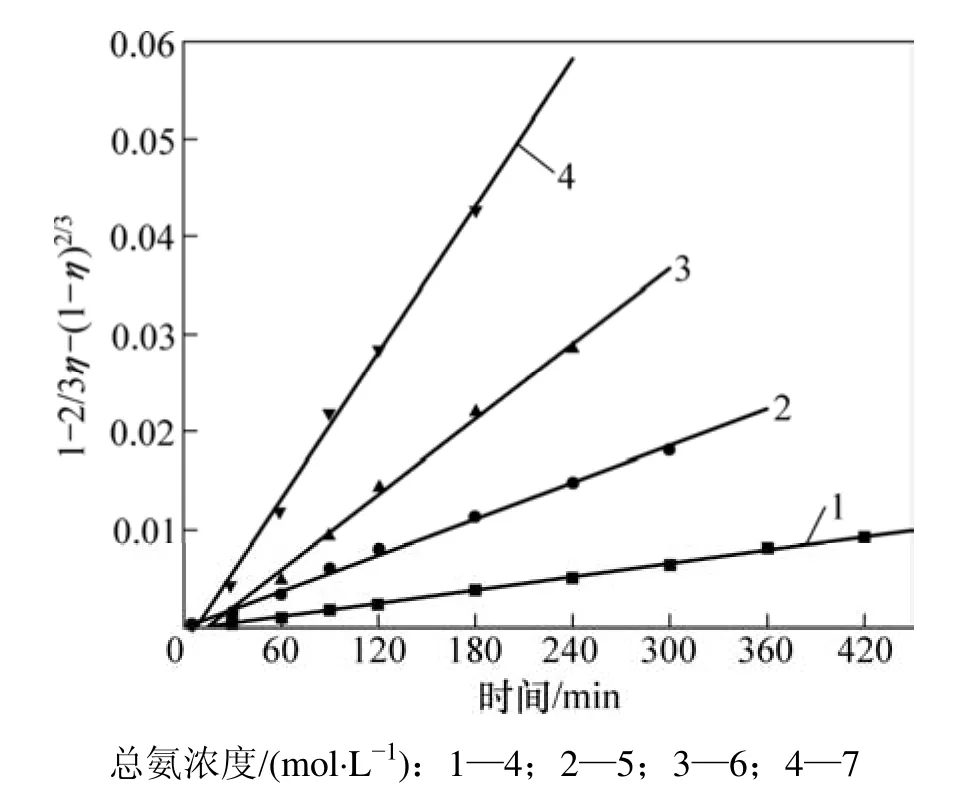
图8 不同总氨浓度下1−2/3η−(1−η)2/3与时间关系图Fig.8 Relationship between 1−2/3η−(1−η)2/3 and time at various total ammonium concentrations
由图7 和图8 可见:1−2/3η−(1−η)2/3与时间 t呈很好的线性关系,在浸出实验条件下式(6)均成立。表明浸出过程符合孔隙扩散控制的粒子模型。
2.4.2 表观活化能与表观反应级数
将图7 中各温度下 1−2/3η−(1−η)2/3与 t之间的关系进行线性回归,所得直线斜率即为不同浓度下的k。以ln k 对1/T作图,如图9所示。根据阿累尼乌斯方程,由图9中所得直线斜率,可得实验条件下,浸出反应表观活化能为71.35 kJ/mol。
同理,将图8中不同总氨浓度下 1−2/3η−(1−η)2/3与t之间的关系进行线性回归,所得直线斜率即为不同总氨浓度下的k。以ln k对ln c作图,如图10所示。由图10所得直线斜率,可得实验条件下,浸出反应表观级数为4.27。

图9 硅锌矿浸出的阿累尼乌斯图Fig.9 Arrhenius plot for leaching of willemite
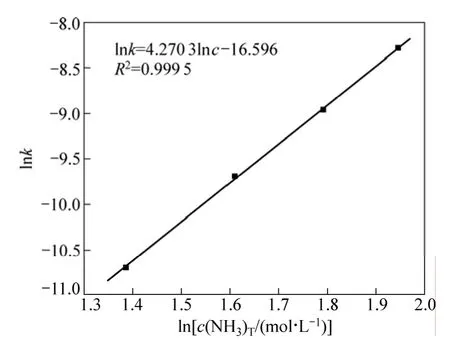
图10 总氨浓度与k关系图Fig.10 Relationship between ln k and total ammonium concentration
须指出的是:由于受孔隙扩散的影响,多孔颗粒反应动力学会不适用,实验得到的仅为活化能和反应级数的表观值。当受孔隙扩散影响时,浸出反应的表观活化能普遍较大。而反应级数大于3的化学反应亦仅在理论上存在,在自然界中尚未发现[18]。
3 结论
(1) 通过实验研究了多孔硅锌矿样品在(NH4)2SO4-NH3-H2O体系中液固质量比为200时的浸出。当搅拌速度大于250 r/min时,外扩散对浸出过程的影响已基本消除;温度和总氨浓度对浸出速率影响显著。
(2) 浸出过程符合孔隙扩散控制的粒子模型,表明反应不只是发生在颗粒外表面,而是发生在包含孔隙内部的整个扩散区域。反应表观反应活化能为71.35 kJ/mol,表观反应级数为4.27。
[1]Matthew I G, Elsner D. The processing of zinc silicate ores: A review[J]. Metallurgical and Materials Transactions B, 1977,8(1): 85−91.
[2]Matthew I G, Elsner D. The hydrometallurgical treatment of zinc silicate ores[J]. Metallurgical and Materials Transactions B, 1977,8(1): 73−83.
[3]Bodas M G. Hydrometallurgical treatment of zinc silicate ore from Thailand[J]. Hydrometallurgy, 1996, 40: 37−49.
[4]Hua Y, Lin Z, Yah Z. Application of microwave irradiation toquick leach of zinc silicate ore[J]. Minerals Engineering, 2002,15: 451−456.
[5]李存兄, 魏昶, 樊刚, 等. 高硅氧化锌矿加压酸浸处理[J]. 中国有色金属学报, 2009, 19(9): 1678−1683.LI Cun-xiong, WEI Chang, FAN Gang, et al. Pressure acid leaching of high silicon zinc oxide ore[J]. The Chinese Journal of Nonferrous Metals, 2009, 19(9): 1678−1683.
[6]Santos F M F, Pina P S, Porcaro R, et al. The kinetics of zinc silicate leaching in sodium hydroxide[J]. Hydrometallurgy, 2010,102: 43−49.
[7]CHEN Ai-liang, ZHAO Zhong-wei, JIA Xi-jun, et al. Alkaline leaching Zn and its concomitant metals from refractory hemimorphite zinc oxide ore[J]. Hydrometallurgy, 2009, 97:228−232.
[8]ZHAO Zhong-wei, LONG Shuang, CHEN Ai-liang, et al.Mechanochemical leaching of refractory zinc silicate(hemimorphite) in alkaline solution[J]. Hydrometallurgy, 2009,99: 255−258.
[9]Harvey T G. The hydrometallurgical extraction of zinc by ammonium carbonate: A review of the Schnabel process[J].Mineral Processing and Extractive Metallurgy Review, 2006, 27:231−279.
[10]唐谟堂, 欧阳民. 硫铵法制取等级氧化锌[J]. 中国有色金属学报, 1998, 8(1): 118−121.TANG Mo-tang, OUYANG Min. Preparation of grade zinc oxide by using ammonium sulfate and ammonia complex leaching process[J]. The Chinese Journal of Nonferrous Metals,1998, 8(1): 118−121.
[11]张保平, 唐谟堂, 杨声海. 氨法处理氧化锌矿制取电锌[J]. 中南工业大学学报:自然科学版, 2003, 34(6): 619−623.ZHANG Bao-ping, TANG Mo-tang, YANG Sheng-hai. Treating zinc oxide ores using ammonia-ammonium chloride to produce electrolysis zinc[J]. Journal of Central South University of Technology: Natural Science, 2003, 34(6): 619−623.
[12]FENG Lin-yong, YANG Xian-wan, SHEN Qing-feng, et al.Pelletizing and alkaline leaching of powdery low grade zinc oxide ores[J]. Hydrometallurgy, 2007, 89: 305−310.
[13]朱云, 胡汉, 苏云生, 等. 难选氧化锌矿氨浸动力学[J]. 过程工程学报, 2002, 2(1): 81−85.ZHU Yun, HU Han, SU Yun-sheng, et al. Kinetics of leaching poorly-floated zinc-oxide-ore with ammonia[J]. The Chinese Journal of Process Engineering, 2002, 2(1): 81−85.
[14]JU Shao-hua, TANG Mo-tang, YANG Sheng-hai, et al.Dissolution kinetics of smithsonite ore in ammonium chloride solution[J]. Hydrometallurgy, 2005, 80: 67−74.
[15]WANG Rui-xiang, TANG Mo-tang, YANG Sheng-hai, et al.Leaching kinetics of low grade zinc oxide ore in NH3-NH4Cl-H2O system[J]. Journal of Central South University of Technology, 2008, 15(5): 679−683.
[16]刘晓丹, 张元福. 铵盐浸出氧化锌矿动力学的研究[J]. 贵州工业大学学报: 自然科学版, 2004, 33(2): 82−84.LIU Xiao-dan, ZHANG Yuan-fu. Study on kinetics of ammonium salt leaching on znicite[J]. Journal of Guizhou University of Technology: Natural Science Edition. 2004, 33(2):82−84.
[17]刘智勇, 刘志宏, 曹志阎, 等. 硅锌矿在(NH4)2SO4-NH3-H2O体系中的浸出机理[J]. 中国有色金属学报, 2011, 21(11):2929−2935.LIU Zhi-yong, LIU Zhi-hong, CAO Zhi-yan, et al. Leaching mechanism of willemite in (NH4)2SO4-NH3-H2O system[J]. The Chinese Journal of Nonferrous Metals, 2011, 21(11):2929−2935.
[18]Souza A D, Pina P S, Lima E V O, et al. Kinetic of sulphuric acid leaching of a zinc silicate calcine[J]. Hydrometallurgy, 2007, 89:337−345.
[19]Ishida M, Wen C Y. Comparison of kinetic and diffusional models for solid-gas reactions[J]. AICHE Journal, 1968, 14(2):311−317.
[20]Bhatia S K, Perlmutter D D. A random pore model for fluid-solid reactions: I. Isothermal, kinetic control[J]. AICHE Journal, 1980,26(3): 379−386.
[21]Bhatia S K, Perlmutter D D. A random pore model for fluid-solid reactions: II. Diffusion and transport effects[J]. AICHE Journal,1981, 27(2): 247−254.
[22]Petersen E E. Reaction of porous solids[J]. AICHE Journal, 1957,3(4): 443−448.
[23]Szekely J, Evans J W. Studies in gas-solid reactions: Part I. A structural model for the reaction of porous oxides with a reducing gas[J]. Metallurgical and Materials Transactions B,1971, 2(6): 1691−1698.
[24]Szekely J, Evans J W. Studies in gas-solid reactions: Part II. An experimental study of nickel oxide reduction with hydrogen[J].Metallurgical and Materials Transactions B, 1971, 2(6):1699−1710.
[25]Evans J W, Song S. A model for the design of gas-solid reactors[J]. Metallurgical and Materials Transactions B, 1973,4(7): 1701−1707.
[26]Georgiou D, Papangelakis V G. Sulphuric acid pressure leaching of a limonitic laterite: chemistry and kinetics[J].Hydrometallurgy, 1998, 49: 23−46.

