高效液相色谱法测定小儿清热口服液中绿原酸的含量
王新晓 卢建峰 河南省叶县中医院(河南叶县467200)
小儿清热口服液是本院主任中医师宋耀民近65年行医之验方,为医院制剂室生产的院内制剂,由金银花、青蒿、薄荷、连翘、冰片5味药材组成。临床上对小儿高热效果明显,为了控制其质量,本文采用了高效液相色谱法对绿原酸进行含量测定,现报道如下。
1 仪器与试药 采用美国Waters510高效液相谱泵;Waters490E检测仪;Waters745数据处理机。绿原酸对照品由中国药品生物制品检定所提供,批号110753-200608。各种药材均经漯河市药检所中药鉴定专家吕斌教授鉴定。所用试剂均为分析纯。
2 绿原酸的含量测定 2.1色谱条件 YWGC18柱(4.0mm×150mm,10μm);流动相甲醇-水-四氢呋喃-冰醋酸(2.5:97:5:1.5);流速1.5mm·min-1;检测波长327nm;灵敏度0.05AUFS;纸速0.1mm·min-1。
2.2 绿原酸对照品溶液的配制 精密称取绿原酸对照品10.1mg,置10mL容量瓶中,加入50%甲醇稀释至刻度,摇匀即得Ⅰ号液。精密量取Ⅰ号液1mL置10mL容量瓶中,加入50%甲醇稀释至刻度,摇匀即得Ⅱ号液。
2.3 供试样品液的配制 精密量取样品试液1mL,置50mL容量瓶中,加入50%甲醇稀释至刻度,摇匀即得。
2.4 阴性液的配制 取除金银花外的其余药材,按制剂工艺制成阴性样品,并按样品供试液方法制成阴性药液,再精密量取阴性药液1mL,置50mL容量瓶中,加入50%甲醇稀释至刻度,摇匀即得。
2.5 药材液的配制 精密称取药材0.15g,置具塞锥形瓶中,精密加入50%甲醇50mL,称定重量,超声处理30min,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀即得。
2.6 标准曲线的绘制 精密量取绿原酸对照品Ⅱ号溶液2、4、5、6、8μl进样测定,以绿原酸进样量(μg)为横坐标,峰面积积分值为纵坐标绘图。其回归方程为:Y=781483.90,X-15316.87,r=0.9999,绿原酸标准品在0.201~0.807μg与峰面积有良好的线性关系。
2.7 精密度试验 按照测定方法重复进样5次,绿原酸峰面积积分值相对标准偏差RSD=1.33%。
2.8 重现性试验 按照测定方法重复测定5份样品,绿原酸含量的相对标准偏差RSD=0.4%
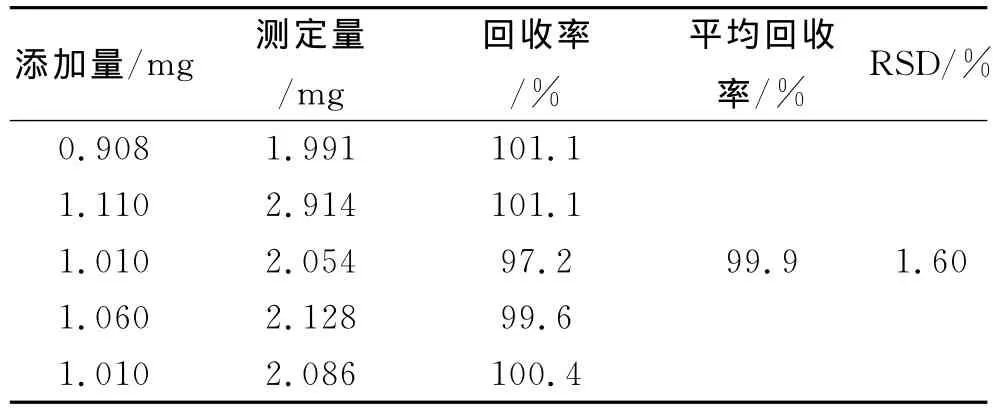
表1 小儿清热口服液中绿原酸的回收率测定结果
2.9 加样回收率试验 精密量取5份样品(批号:110618)各0.5mL,置50mL容量瓶中,精密吸取各样品液,分别精密加入绿原酸对照品Ⅱ号溶液0.90、1.09、1.00、1.04、1.00mL,用50%甲醇定容至刻度,摇匀即得。按上述色谱条件测定,以下式计算回收率,结果如表1结果表明,本方法具有良好的回收率。
2.10 样品测定 精密量取样品液10μL进样,依照上述色谱条件进行含量测定,结果见表2。
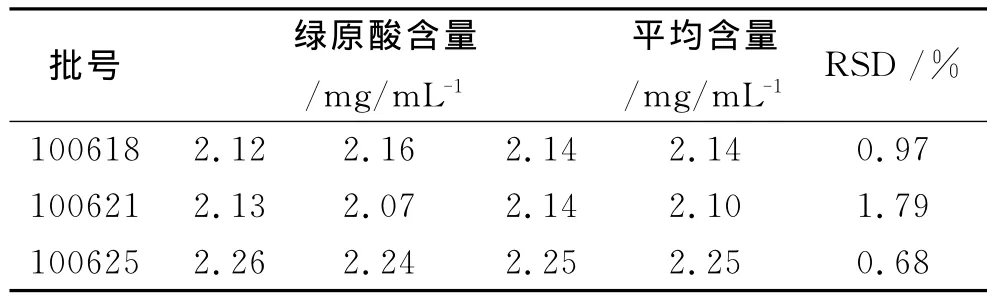
表2 绿原酸含量测定结果
3 结 论 3.1 绿原酸的HPLC的含量测定中曾用甲醇-水-乙腈-冰醋酸(3∶97∶12∶3)为流动相
但在测定过程中发现样品分离不好,绿原酸峰拖尾现象比较严重,故调整流动相中各组分比例,把乙腈改为四氢呋喃,分离效果良好。
3.2 试验中绿原酸的含量测定方法结果较好,与其它成分均可基线分离。
[1]国家药典委员会.中华人民共和国药典一部[M].北京:中国医药科技出版社,2010:205-206.
[2]韩长柏,王静竹.黄栀花口服液质量标准研究[J].中药新药与临床药理,1996,(7)4:34.
[3]康庭国.中成药薄层色谱鉴别[M].北京:人民卫生出版社,1995:142.
[4]孙 莹,吕 洁.药物分析[M].北京:人民卫生出版社,2010:81-85.
——一个解释欧姆表刻度不均匀的好方法

