RP-HPLC法测定注射用重组人B淋巴细胞刺激因子受体-抗体融合蛋白的含量
姚雪静,李壮林(烟台荣昌生物工程有限公司,山东烟台 264006)
RP-HPLC法测定注射用重组人B淋巴细胞刺激因子受体-抗体融合蛋白的含量
姚雪静*,李壮林(烟台荣昌生物工程有限公司,山东烟台 264006)
目的:建立测定注射用重组人B淋巴细胞刺激因子受体-抗体融合蛋白(简称TACI-Fc)含量的方法。方法:采用反相高效液相色谱法。色谱柱为Vydac C18,流动相A液为含0.1%三氟乙酸的水溶液,流动相B液为含0.1%三氟乙酸的乙腈溶液,梯度洗脱,流速为1.3mL·min-1,检测波长为280nm。结果:TACI-Fc进样量在5.0~20.0µg范围内与峰面积积分值呈良好线性关系(r=0.9997);方法平均回收率为99.71%,RSD=1.14%(n=9)。结论:本方法操作简便、重复性好、结果准确,适用于测定注射用TACI-Fc的含量。
反相高效液相色谱法;重组人B淋巴细胞刺激因子受体-抗体;融合蛋白;含量
重组人B淋巴细胞刺激因子受体-抗体融合蛋白是将人B淋巴细胞刺激因子的受体TACI(一种穿膜蛋白活化物)的胞外特定可溶性部分,与人IgG1的Fc部分构建成的融合蛋白(以下简称TACI-Fc),用于类风湿性关节炎和系统性红斑狼疮等自身免疫性疾病的治疗[1~3],目前国内正处于临床研究阶段。注射用TACI-Fc中含有精氨酸、组氨酸、甘露醇等辅料,由于辅料的干扰,采用《中国药典》[4]中常规的蛋白质含量测定方法无法对药物活性成分进行含量测定。为控制TACI-Fc成品质量,笔者拟建立TACI-Fc含量的反相高效液相色谱(RP-HPLC)测定方法,为注射用TACI-Fc的质量评价提供依据。
1 仪器与试药
1.1 仪器
1200型HPLC仪,包括紫外检测器、四元泵、在线脱气机、柱温箱、自动进样器、Chemstation色谱工作站(美国Agilent公司)。
1.2 试药
TACI-Fc对照品(批号:BZ 2010001,溶液浓度:5.42mg·mL-1,纯度:>99.5%)、注射用 TACI-Fc(批号:20091201、20100101、20100301,规格:每支80mg)均由烟台荣昌生物工程有限公司提供;乙腈为色谱纯,水为蒸馏水,其余试剂均为分析纯。
2 方法与结果
2.1 色谱条件与系统适用性试验
色谱柱:Vydac C18(250mm×4.6mm,5μm);流动相A液:含0.1%三氟乙酸的水溶液,流动相B液:含0.1%三氟乙酸的乙腈溶液,梯度洗脱(A液从75%渐变至60%,同时B液从25%渐变至40%),洗脱时间:15min,流速:1.3mL·min-1;柱温:25℃;检测波长:280nm;进样量:25.0μL。在此色谱条件下,取“2.2”项下对照品、供试品溶液、阴性对照溶液进样分析,结果前2种溶液在相同的保留时间处出现吸收峰,而阴性对照溶液在此无吸收峰,说明阴性对照对试验无干扰。色谱见图1。

图1 高效液相色谱图A.对照品;B.供试品;C.阴性对照;1.TACI-FcFig 1 HPLC chromatogramsA.substance control;B.test sample;C.negative control;1.TACI-Fc
2.2 溶液的制备
用微量移液器精密吸取TACI-Fc对照品9.23mL,置于50mL量瓶中,加水定容,得TACI-Fc对照品贮备液(1.0mg·mL-1)。精密吸取贮备液5.0mL,置于10mL量瓶中,水定容,得TACI-Fc对照品溶液(0.5mg·mL-1)。
取注射用TACI-Fc内容物,精密称取适量(约相当于TACI-Fc 25mg),置于50mL量瓶中,水定容,得供试品溶液。
取缺TACI-Fc的阴性样品,精密称取适量,置于50mL量瓶中,水定容,得阴性对照溶液。
2.3 线性关系考察
分别精密吸取TACI-Fc对照品贮备液2.0、3.0、4.0、5.0、6.0、7.0、8.0mL,置于10mL量瓶中,水定容,制备成质量浓度分别为0.2、0.3、0.4、0.5、0.6、0.7、0.8mg·mL-1的系列浓度对照品溶液,进样测定,以峰面积积分值(Y)为纵坐标,质量浓度(X)为横坐标,进行线性回归,得回归方程为Y=47.016X-8.4679(r=0.9997)。结果表明,TACI-Fc进样量在5.0~20.0μg范围内与峰面积积分值呈良好线性关系。
2.4 精密度试验
制备低、中、高浓度(0.3、0.5、0.7mg·mL-1)对照品溶液,分别进样,计算含量。同日内重复测定5次,计算日内RSD值,结果分别为0.66%、0.79%、0.72%;连续5d制备并测定,计算日间RSD值,结果分别为1.00%、0.80%、0.86%,表明本法精密度好。
2.5 稳定性试验
取同一供试品溶液25.0μL,分别在0、4、8、12、24h 后进样,测定峰面积。结果,RSD=1.45%(n=5),表明供试品溶液在24h内基本稳定。
2.6 重复性试验
取同一批样品,平行制备6份供试品溶液,进样测定。结果,RSD=0.90%(n=6),表明方法重复性良好。
2.7 加样回收率试验
精密称取已知含量的同一批样品适量,置于50mL量瓶中,加入不同浓度的对照品溶液,定容。分别取样,测定峰面积,计算加样回收率,结果见表1。
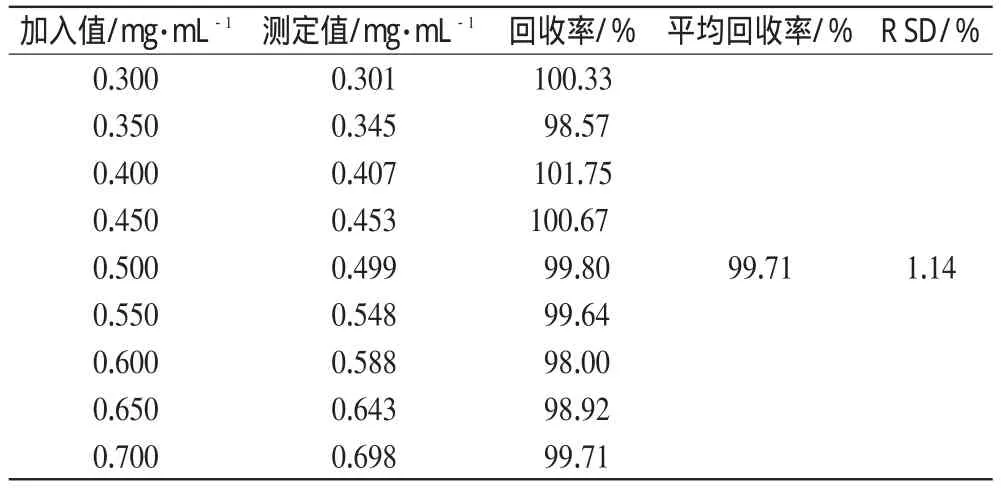
表1 回收率试验结果(n=9)Tab 1Results of recovery test(n=9)
2.8 样品含量测定
取3批样品,制备成供试品溶液,分别进样,测定样品含量。结果,3批样品占标示含量百分率分别为97.03%、97.28%、96.55%(n=3)。
3 论
注射用TACI-Fc为正处于临床研究阶段的一类新药,目前尚无药物含量测定方法的相关报道。TACI-Fc是分子量为80kD的糖蛋白,笔者试验了测定蛋白质含量常用的酶联免疫吸附(ELISA)法和Lowry法[4]。ELISA法虽然检测精密度较高,但测试过程中重复性较差,检测步骤烦琐,检测时间通常在20h以上,因此不适合作为TACI-Fc含量测定的质控方法;而由于注射用TACI-Fc中辅料的干扰,采用Lowry法测定无法得到准确的结果。
笔者以RP-HPLC法测定注射用TACI-Fc的含量,先将TACI-Fc对照品溶液进行连续波段扫描,发现其特征吸收峰在280nm波长处,故采用此波长进行检测。通过调整流动相A液和B液的比例,使TACI-Fc的保留时间合适,所得到的色谱峰与其他杂质峰分离度较好。在流动相中加入0.1%三氟乙酸,改善了主峰拖尾现象,使主峰尖锐对称。另外,笔者还试验了不同流速对分析结果的影响,发现流速在1.0~1.3mL·min-1范围内结果较一致,因此最后选择流速为1.3mL·min-1,可减少分析时间。
综上所述,本文建立的方法操作简便、重复性好、结果准确,适用于测定注射用TACI-Fc的含量。
[1] Nestorov I,Munafo A,Papasouliotis O,et al.Pharmacokinetics and biological activity of atacicept in patients with rheumatoid arthritis[J].J Clin Pharmacol,2008,48(4):406.
[2] Bracewell C,Isaacs JD,Emery P,et al.Atacicept,a novel B cell-targeting biological therapy for the treatment of rheumatoid arthritis[J].Expert Opin Biol Ther,2009,9(7):909.
[3] Dall’Era M,Chakravarty E,Wallace D,et al.Reduced B lymphocyte and immunoglobulin levels after atacicept treatment in patients with systemic lupus erythematosus:results of a multicenter,phaseⅠb,double-blind,placebo-controlled,dose-escalating trial[J].Arthritis Rheum,2007,56(12):4142.
[4] 国家药典委员会.中华人民共和国药典(三部)[S].2010年版.北京:中国医药科技出版社,2010:附录34.
Content Determination of Recombinant Human B Lymphocyte Stimulator Receptor-IgG Fc Fusion Protein for Injection by RP-HPLC
YAO Xue-jing,LI Zhuang-lin(Yantai RC Biotechnologies,Co.,Ltd.,Shandong Yantai 264006,China)
OBJECTIVE:To establish the method for the content determination of recombinant human B lymphocyte stimulator receptor-IgG Fc fusion protein(TACI-Fc)for injection.METHODS:RP-HPLC method was adopted.The chromatographic column was Vydac C18column with 0.1%trifluoroacetic acid in water as mobile phase A and 0.1%trifluoroacetic acid in acetonitrile as mobile phase B(gradient elution)at the flow rate of 1.3mL·min-1.The detection wavelength was set at 280nm.RESULTS:The linear range of TACI-Fc was 5.0~20.0µg(r=0.9997)with an average recovery of 99.71%(RSD=1.14%,n=9).CONCLUSION:The method is simple,reproducible and accurate for the content determination of TACI-Fc for injection.
RP-HPLC;Recombinant human B lymphocyte stimulator receptor-IgG Fc;Fusion protein;Content
R927.2;R977.6
A
1001-0408(2012)33-3144-02
DOI10.6039/j.issn.1001-0408.2012.33.29
*工程师,硕士。研究方向:医药工程。电话:0535-6931915。E-mail:snow8176@sina.com
2011-09-22
2011-12-15)

