奥美拉唑不良反应及其影响因素分析
马丹华1,朱文婷2,徐厚明1*
1江苏省药品不良反应监测中心,南京 210002;2中国药科大学药学院临床药学专业,南京 210009
奥美拉唑为质子泵抑制剂类抗消化性溃疡药物,临床主要用于治疗消化性溃疡、幽门螺杆菌感染、反流性食管炎、胃泌素瘤、卓-艾综合征等消化系统疾病,也可用于预防重症疾病(如脑出血、严重创伤等)手术后预防再出血等。由于其疗效显著、复发率低、应用方便等特点,临床广泛使用。
质子泵抑制剂(PPIs)主要在肝脏经由细胞色素P450酶系进行代谢和清除,其中比较重要的是CYP2C19和CYP3A4,奥美拉唑主要通过CYP2C19代谢。一方面,人群中普遍存在CYP2C19基因的多态性,这种基因多态性导致奥美拉唑在代谢速度和药效学方面存在较大个体差异,甚至还有耐药人群,从而影响了抑酸效果的稳定性。另一方面,CYP是多种药物代谢的共同通路,奥美拉唑的这种代谢方式决定它会与其他多种经该同工酶代谢的药物发生较复杂的相互作用[1],因此不恰当的合并用药也可能导致不良反应的发生或者严重程度加重。本文以奥美拉唑不良反应报告为基础,采用类似病例对照研究方法,对奥美拉唑发生不良反应的影响因素进行分析,考察奥美拉唑合并其他药物是否对药品不良反应有影响,以期为临床提供参考。
1 资料和方法
1.1 资料
病例资料来源于江苏省药品不良反应监测中心报告表数据库,报表一般项目齐全,从中选定奥美拉唑与其他药物合用作为病例组。单一用药作为对照组,筛选的条件为:①病例来源于同一地区(以市为单位);②ADR发生时间相差不超过两周;③为同一民族;④奥美拉唑单一用药。
1.2 分析方法
研究对象均为确定使用奥美拉唑后发生不良反应的患者,应用类似1∶1配对病例对照研究,在有效控制混杂因素的作用的基础上,以合并用药组为病例组,以单一用药为对照组,运用Excel工作表,对病例组与对照组的样本进行初步的整理归纳,然后筛选需要的信息,逐对输入SPSS 18.0建立数据库,分析患者性别、年龄、原患疾病、给药途径、合并用药种类等影响因素。
2 结 果
2.1 患者的基本信息
本研究共筛选病例组与对照组各258例,为江苏省地区病例。病例组男性133例,女性125例,性别比例为1.06∶1;对照组男性151例,女性107例,性别比例为 1.41∶1;两组情况无统计学差异(P>0.05)。两组病例中,男性人数均多于女性,这可能与男性患者本身消化性溃疡的发病率明显高于女性有关[2]。
病例组平均年龄为(49.33±16.88)岁,对照组平均年龄为(46.86±16.26)岁,无统计学差异(P>0.05)。但病例组中50~90岁年龄段的病例数大于对照组。这也许是老年人生理机能的衰退,加上原患疾病较多,更容易患多种慢性疾病,因此服药种类也相对增加,从而更易发生药物相互作用,导致不良反应的发生。
由病例组与对照组原患疾病比较可知,两组病例主要为消化系统疾病,但对病例组而言,预防性用药所占比例相对较大,可能是由于预防性用药多为重症疾病于应激状态下及合并NSAIDS的情况下应用的,因此大多数预防性用药是合并用药,易发生药物相互作用。其中,消化系统肿瘤包括胃癌、食道癌、直肠癌等,消化系统炎症包括胃炎、反流性食管炎等,其他为预防重症疾病应激状态(如脑损伤、非消化系统癌症、术后等)和NSAIDS引起的急性胃黏膜损伤。见表1。
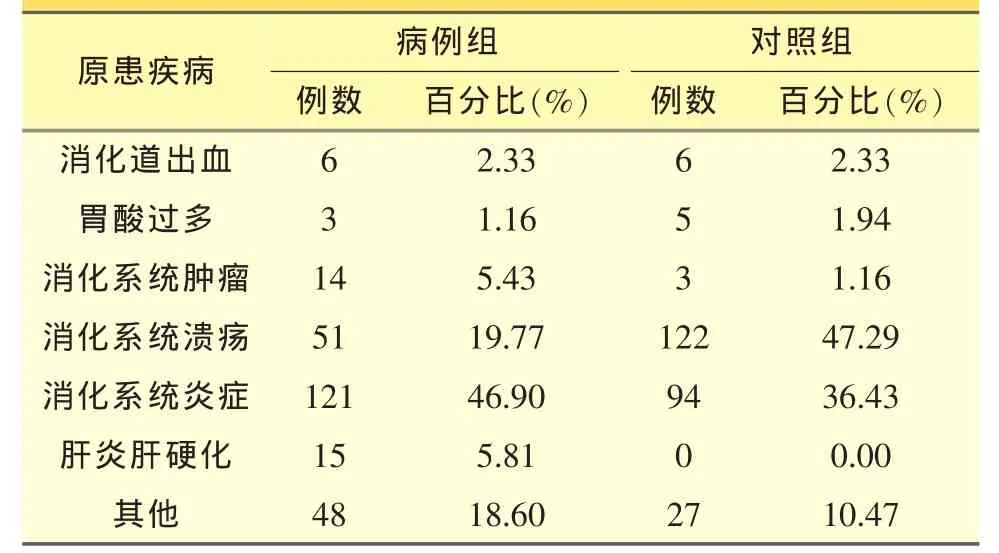
表1 原患疾病状态比较
2.2 用药途径
病例组患者的静脉滴注频率明显高于对照组(43.8%VS.36.36%), 但两组无统计学差异 (P>0.05)。通过两组给药途径的比较发现,口服给药发生不良反应例数较多,这可能与患者总体口服人数多有关。口服给药数日后,可引起造血系统、神经系统的损害以及代谢紊乱,因此用药开始的1周内应加强ADR监测。
2.3 ADR累及的器官、系统
奥美拉唑致ADR以皮肤、胃肠系统、中枢神经及外周神经系统和全身性损害最多,除此以外还有呼吸系统、血液系统、肌肉骨骼系统等较罕见的ADR。见表2。
2.4 合并用药数对ADR累及系统的影响
根据病例组中合并用药数的分类统计,再分别统计其ADR累及的系统数,发现随着用药种类的增加,多系统(≥2)不良反应发生的比率也随之增加。见表3。
2.5 ADR的严重程度及预后
对病例组和对照组的不良反应严重程度以及不良反应的预后进行对比分析,可以明显看出,随着合并用药种类的增加,严重不良反应的发生率明显增加,见表4。奥美拉唑发生ADR的预后较好,大部分可达到好转或治愈,但病例组出现1例死亡,系患者用药后发生呕吐后窒息,属心原性猝死。见表5。
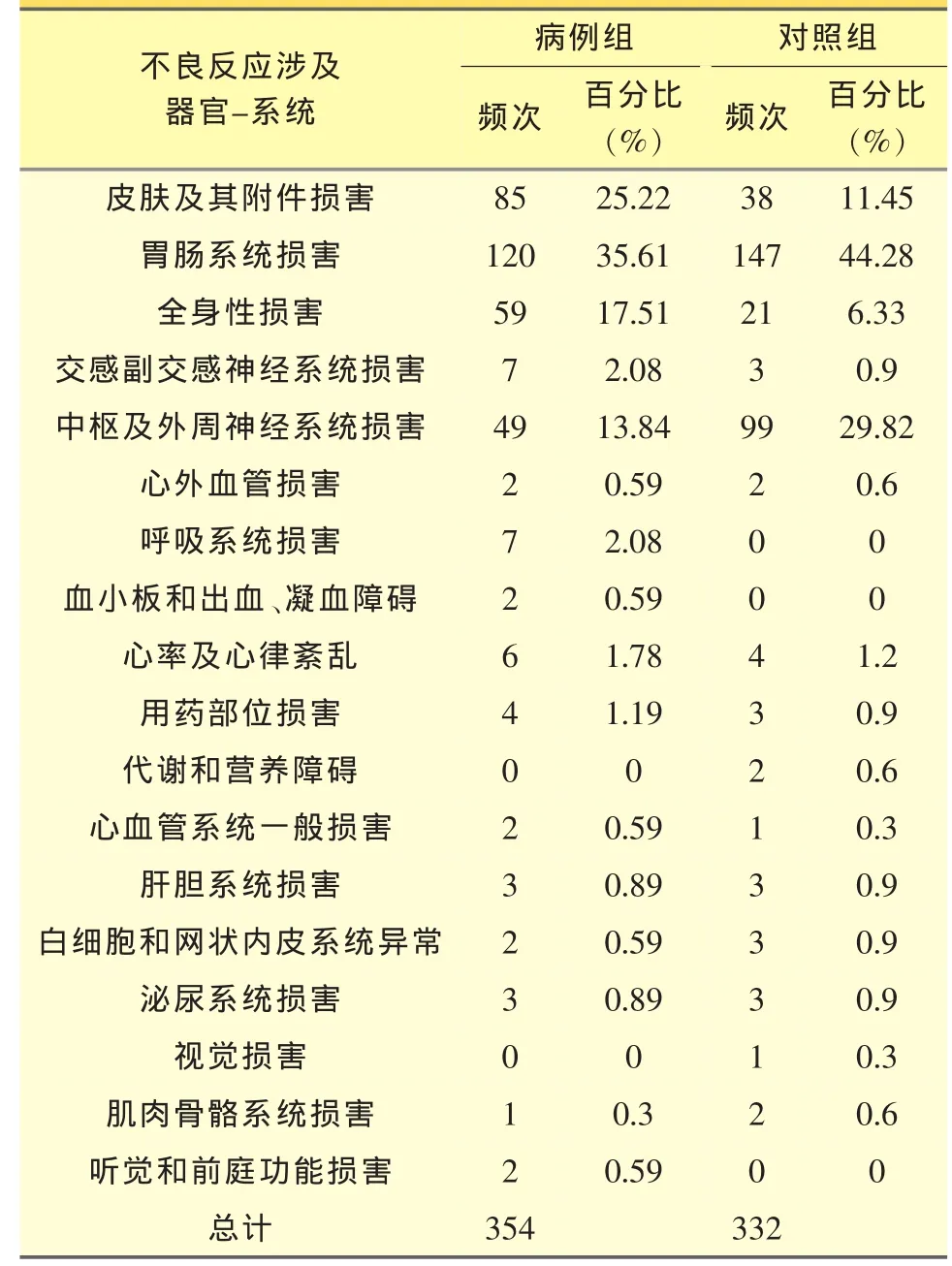
表2 不良反应所涉及的器官、系统比较
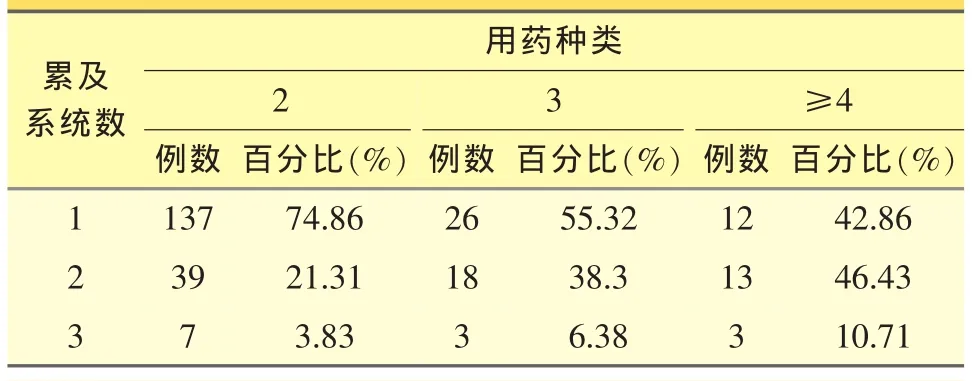
表3 不良反应涉及系统种类与合并用药关系

表4 各组不良反应的严重程度
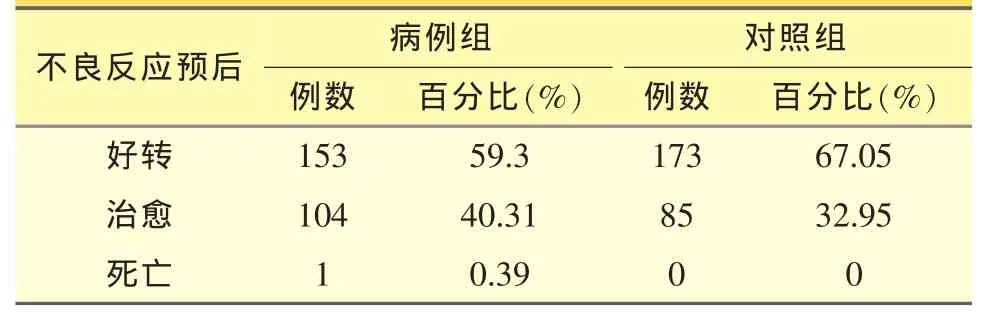
表5 不良反应的预后
3 讨 论
3.1 关注严重和少见的不良反应
本研究发现,奥美拉唑致ADR发生的分布范围较广,其中以皮肤(如皮疹、荨麻疹)、胃肠系统(腹痛、腹泻、腹胀、便秘、恶心、呕吐)等较多,也有严重和少见的ADR值得关注。
病例组与对照组各有1例用药后肝功能异常的报告。动物实验证明,长期服用奥美拉唑(一日400 μmol·kg-1)可引起肝脏重量增加。另据国外报道,本品也有抑制肝脏微粒体P450单氧化酶系统药物代谢作用。服用该药后,人P450IA2免疫活性蛋白及P450IA1酶的活性显著增高,可增加某些药物如醋氨酚对肝脏的毒性作用,可出现严重暴发性肝衰竭[3]。对肝脏的毒性可能是奥美拉唑的特异性反应,肝脏功能不全者应慎用或不用。
全身性损害包括发热、寒战、过敏样反应、过敏性休克等,其中病例组发生3例过敏性休克。奥美拉唑致过敏性休克不良反应在药物说明书中并未明确记载,提醒临床用药时要严密观察患者情况,一旦出现异常,要积极采取有效处置措施。
两组患者均出现了心悸的不良反应,同时病例组还发生1例心律失常,可能因为H+-K+-ATP酶活性被阻断后,胃酸分泌明显减少,血胃泌素的水平明显升高,通过反馈作用,副交感神经的紧张度明显下降,交感神经的兴奋性明显增强,从而导致心率增快产生心悸[4]。此不良反应属于少见并容易被忽略的不良反应,应引起临床医师的注意。
泌尿系统损害主要为尿潴留和蛋白尿。有研究显示,患者口服奥美拉唑后可引起急性尿潴留、血尿及间质性肾炎,临床表现主要为不同程度的发热、皮疹、腰部不适或腰痛,夜尿增多或少尿,个别患者伴有食欲下降、恶心呕吐等胃肠道反应,临床针对老年人与肝肾功能不全患者给药时需慎重,并密切观察[5]。
3.2 合并用药对ADR的影响
本研究发现,病例组患者更易发生多个系统的不良反应,即随着用药种类的增加,患者发生多个ADR的概率也在增加,说明了合并用药可能会改变奥美拉唑的活性或代谢状况,导致不良反应的发生。通过对ADR的严重程度分析,病例组发生严重ADR的概率明显大于对照组,病例组中有1例死亡病例,且随着用药种类的增加,这一比率也可能增加,进一步说明了合并用药对奥美拉唑在体内的药动学及药效学均有影响。
奥美拉唑是目前研究最多的PPIs,其代谢途径主要是通过CYP2C19羟化生成5-羟基奥美拉唑,并经CYP3A4硫化氧化作用生成奥美拉唑砜。可延缓经肝脏细胞色素P450系统代谢的药物 (如双香豆素、安定、苯妥英钠、华法林、硝苯定)在体内的消除,使其半衰期延长,药理作用增强,合用时要注意减量[6]。同时由于基因的多态性,肝药酶CYP2C19存在强代谢型和弱代谢型,增加了个体用药的差异性及合并用药的危险性。因此临床上使用奥美拉唑时,除了关注该药自身可能导致的不良反应,还应根据其代谢特点,在选用合并药物时充分考虑不同药物之间可能存在的相互影响,避免不可预见的不良反应的发生,保障患者的用药安全。
[1]王蔚虹,王小蕾.质子泵抑制剂临床应用进展[J].中国医院用药评价与分析,2011(6):483-7.
[2]徐来风,张玉平,郭秀兰.1386例消化性溃疡的流行病学分析[J]. 中华消化内镜杂志,2000,17(3):184-5.
[3]胡建平.奥美拉唑临床应用过程中的副作用100例分析[J]. 中华消化杂志,1993,13(6):360.
[4]孙成栋,李 真.奥美拉唑致窦性心动过速2例[J].药物不良反应杂志,2007,9(5):373.
[5]张晓东,方敬爱,武明虎.奥美拉唑导致间质性肾炎的临床分析[J].中国中西医结合肾病杂志,2006(9):543.
[6]韩英英.奥美拉唑与其他药物的相互作用[J].山西医药杂志,2011(6):561-2.

