黄铜表面镧转化膜在模拟雨水中的腐蚀行为
范洪强,李淑英,赵宗昌,林乐圣,张琳
(大连理工大学化工与环境生命学部,辽宁 大连 116012)
【腐蚀防护】
黄铜表面镧转化膜在模拟雨水中的腐蚀行为
范洪强,李淑英*,赵宗昌,林乐圣,张琳
(大连理工大学化工与环境生命学部,辽宁 大连 116012)
采用化学浸泡法在黄铜表面制得镧转化膜,转化液组成与工艺条件为:硝酸镧3.5 ~ 5.5 g/L,苯并三氮唑8.0 ~ 12.0 g/L,磺基水杨酸8.0 ~ 12.0 g/L,柠檬酸15.0 g/L,温度60 °C,pH 4,时间3 min。采用原子吸收光谱和电化学法研究了黄铜/镧转化膜在模拟雨水中的腐蚀行为。在相同的浸泡时间内,黄铜/镧转化膜在模拟雨水中溶解的铜离子质量浓度低于黄铜基体。在酸性范围内,模拟雨水的pH越高,黄铜/镧转化膜越不容易被腐蚀。镧转化膜对溶解于雨水中的和Cl−较敏感,Cl−含量的增加使黄铜/镧转化膜的点蚀增强,含量的增加使膜层整体发生严重腐蚀;NO−3含量则对其腐蚀行为的影响不大。黄铜/镧转化膜在pH = 3.29的模拟雨水中的腐蚀经历3个阶段。
黄铜;转化膜;镧;雨水;腐蚀
1 前言
黄铜作为金属材料被广泛应用在众多领域,随酸雨现象日益严重,研究黄铜表面处理技术以提高其耐蚀性能具有重要的意义。稀土对铜及铜合金的缓蚀、转化作用的研究始于20世纪90年代,R. N. Singh等[1]的研究表明,在盐酸溶液中添加 La、Ce、Nd盐,可有效减少701B铝青铜的腐蚀。A. J. Aidykiewicz等[2]采用旋转圆盘电极技术研究铜表面铈转化膜的形成过程,指出O2的还原反应受溶液pH、电极电势及最初形成的铈转化膜形态的影响。韩宝军等[3]研究了稀土铈盐在紫铜缓蚀剂中的应用,进一步证实了稀土盐对铜的缓蚀作用,但过多铈盐的加入不利于钝化膜的性能。近期的研究表明,将硝酸镧和有机缓蚀剂苯并三氮唑(BTA)复配使用,可使黄铜表面膜层在大气、海水和弱酸环境中的耐腐蚀性提高[4-8]。
黄铜在含氧和Cl−的水溶液中常发生电化学腐蚀,生成的腐蚀产物在黄铜表面逐渐沉积,使黄铜表面发生腐蚀产物与无腐蚀产物间的电偶腐蚀(其中,腐蚀产物区为阴极区,无腐蚀产物区为阳极区),从而促进黄铜的溶解[9-11]。D. K. Y. Wong[12]研究了铜在硫酸溶液中溶解的动力学模型。Y. Feng[13-14]等研究了铜在不同pH水溶液中的腐蚀产物、腐蚀机制和黄铜在中性饮水中的腐蚀行为。然而对黄铜及表面稀土转化膜在雨水中的腐蚀行为仍缺乏深刻认识。
本文主要采用电化学方法、原子吸收光谱和扫描电镜研究黄铜表面镧转化膜在模拟上海雨水中的腐蚀行为。
2 实验
2. 1 试验材料
以40 mm × 20 mm × 2 mm的黄铜为基体,其化学成分(以质量分数表示)为:Cu 63.5% ~ 68.0%,Fe 0.10%,Pb 0.03%,Sb 0.005%,Bi 0.002%,P 0.01%,Zn余量。所用化学试剂均为分析纯。
2. 2 稀土镧转化
采用化学浸泡法对基体进行转化处理,工艺流程为:打磨─机械抛光─化学除油─热水清洗─化学抛光─清洗─稀土转化膜工艺─清洗─氮气吹干。
转化液配方与工艺为:

2. 3 模拟雨水组成
根据上海实际降雨组分分析结果[15],用二次蒸馏水和分析纯试剂配制模拟雨水,具体组成见表1。用7 mol/L的HNO3调节模拟雨水的pH。改变模拟雨水中、Cl−的含量,可研究模拟雨水中主要阴离子对黄铜表面镧转化膜腐蚀行为的影响[16]。以表1的模拟雨水为空白液,分别往其中添加 1 μmol/L的Na2SO4、NaCl和NaNO3。

表1 模拟上海雨水的组成Table 1 Composition of artificial rainwater of Shanghai
2. 4 性能测试
采用上海辰华仪器有限公司生产的CHI660B型电化学工作站测试开路电位–时间曲线,以铂片作辅助电极,饱和甘汞电极(SCE)为参比电极,成膜或未成膜的黄铜试片(1 cm × 1 cm)为工作电极。采用美国PRINCETON公司生产的Potentiostat/Galvanostat Model 273电化学系统测定黄铜/镧转化膜(1 cm × 1 cm)的电化学阻抗谱(EIS),pH = 3.29,频率范围为0.01 Hz ~100 kHz,交流干扰幅值为10 mV。电化学测试均以模拟雨水为介质。利用CN63M/CAAM-2001原子吸收光谱仪(北京中西远大科技有限公司)测定试样在模拟雨水中的溶解率。用JSM-5600LV扫描电镜(日本JEOL公司)观察黄铜/镧转化膜在模拟雨水中浸泡30 d后的腐蚀形貌。
3 结果与讨论
3. 1 在模拟雨水中的溶解率
黄铜成膜前后溶解于pH = 3.29的模拟雨水中的铜离子质量浓度由CN63M/CAAM-2001原子吸收光谱仪(北京中西远大科技有限公司)测定,结果见表2。
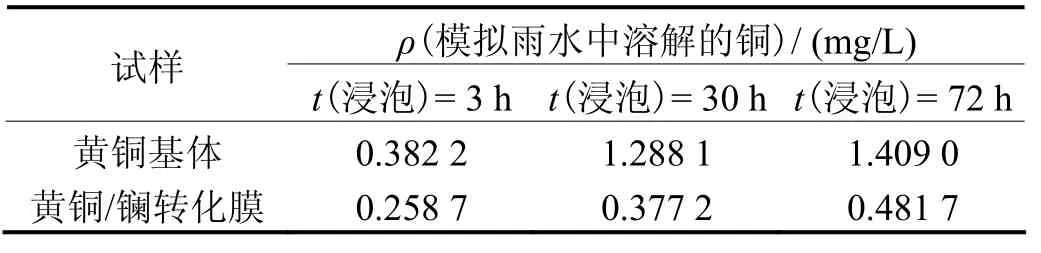
表2 不同试样在模拟雨水中溶解的铜离子质量浓度Table 2 Mass concentration of copper ions dissolved from different samples in artificial rainwater
随浸泡时间的延长,溶解于模拟雨水中的黄铜基体增多,浸泡30 h后模拟雨水中的铜离子质量浓度明显比浸泡3 h时大,变化幅度高达1 mg/L。黄铜/镧转化膜在模拟雨水中的溶解也随浸泡时间的延长而增多,但变化趋势较平缓,且其溶解的量比黄铜基体少,说明镧转化膜有良好的耐蚀性,在一定程度上阻止了铜基体的溶解。
3. 2 pH的影响
图1为黄铜/镧转化膜在不同pH的模拟雨水中的开路电位–时间曲线。
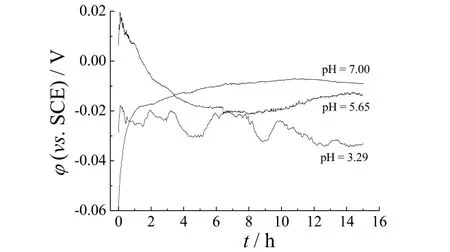
图1 黄铜/镧转化膜在不同pH模拟雨水中的开路电位–时间曲线Figure 1 Open-circuit potential vs. time curves for brass/lanthanum conversion coating in artificial rainwater with different pHs
模拟雨水的pH不同,则试样的腐蚀电位变化也趋势不同。pH = 7时,电位先正移后趋于平稳;pH = 5.65时,曲线变化有2个阶段:浸泡初期,电位逐渐正移随后下降,4 h后进入第2阶段,电位保持在−0.02 V左右,出现平台且持续时间较长;pH = 3.29时,电位曲线变化较大,即使浸泡15 h也未出现平台。另外,浸泡2 h后,黄铜/镧转化膜的腐蚀电位随pH升高而正移,且更稳定。上述结果表明,黄铜/镧转化膜在模拟雨水中的腐蚀与pH有关,在酸性范围内,溶液pH越高,黄铜/转化膜越不容易被腐蚀。
3. 3 主要侵蚀性阴离子的影响
以pH = 3.29的模拟雨水为空白液,分别加入1 μmol/L的Na2SO4、NaCl、NaNO3,浸泡30 d后试样的腐蚀形貌如图2所示。

图2 试样在模拟雨水中浸泡30 d后的腐蚀形貌Figure 2 Corrosion morphology of sample after immersion in artificial rainwater for 30 days
从图2可知,试样在4种模拟雨水中都有一定程度的点蚀。其中,浸于添加了Cl−的模拟雨水中的试样点蚀密度和强度高于浸于空白溶液中的试样;试样在添加溶液中的腐蚀最严重,试样表面膜层遭到严重破坏,除发生一定程度的点蚀外,更接近全面腐蚀;转化膜在加的溶液中的点蚀现象最弱。通常,活性阴离子在铜合金表面的竞争吸附,阴离子与氧化膜和金属基体间的反应较大程度地影响铜合金的腐蚀[17]。、Cl−等对金属材料在雨水中的腐蚀行为主要受其与溶液中O2或OH−的竞争吸附过程及形成的腐蚀产物性质的影响[18]。较多的阴离子吸附在电极表面缺陷部位,由于吸附的阴离子和铜合金的化学反应性质及腐蚀产物性质不同,对铜合金腐蚀过程的影响也就不同。黄铜/镧转化膜对溶解于雨水中的和Cl−较敏感,是因为和Cl−能够纳入转化膜而增加了额外的电荷载体,或直接参与金属基体的溶解反应[19-20]。因而,溶液中或Cl−含量的增加使黄铜/镧转化膜的腐蚀增强。
3. 4 腐蚀过程
图3为黄铜/镧转化膜试样在pH = 3.29的模拟雨水中的电化学阻抗谱。根据阻抗谱特征的变化,黄铜表面镧转化膜试样浸泡的电化学过程可分成初期、中期和后期3个阶段。

图3 黄铜/镧转化膜在pH = 3.29的模拟雨水中浸泡不同时间的电化学阻抗谱Figure 3 EIS diagrams of brass/lanthanum conversion coating immersed in artificial rainwater for different time
从图3a和3b可知,浸泡前期(2.5 ~ 24 h),Nyquist图显示为一段圆弧,表现出明显的电容特征,具有很高的阻抗值,说明转化膜完好,对基体起到屏蔽保护作用。这是因为一方面转化膜的机械阻碍作用阻挡了活性离子的侵蚀,耐点蚀能力大为提高;另一方面,转化膜阻碍了氧和电子的自由传输,抑制了基体铜合金的腐蚀反应,腐蚀电流密度较小。在该浸泡阶段,阻抗谱的圆弧半径变化不大,表明膜层的电阻值基本相同,阻抗值较大说明稀土转化膜层起的电阻作用较强,腐蚀液很难侵入,有效地保护了基体铜。
从图3c和3d可知,浸泡中期(72 ~ 720 h)阻抗图谱发生明显变化,出现2段圆弧,即有2个时间常数,其高频区域的容抗弧对应转化膜的阻抗,而低频区对应电化学反应的阻抗。这说明此时模拟雨水中的侵蚀性介质已渗入膜层并逐渐到达基体表面,稀土镧转化膜逐渐被破坏,性能开始下降。值得注意的是,在浸泡168 ~ 360 h时,阻抗谱的圆弧半径明显减小,膜层低频阻抗值(Zlf)约降低 1个数量级。这说明在 168 ~360 h时,膜层性能下降得最快,即在模拟雨水中,稀土镧转化膜层有效保护时间小于360 h。
从图3e和3f可知,浸泡后期(960 ~ 2 040 h)阻抗谱上出现了3个时间常数,Nyquist图比原来多了1个低频感抗弧,其对应镧转化膜被破坏后黄铜基体发生的氧化还原反应。
4 结论
(1) 在模拟雨水中,成膜后的黄铜溶解量变化较为平缓,均比成膜前的黄铜少,说明镧转化膜有良好的耐蚀效果,在一定程度上阻止了黄铜的阳极溶解。
(2) 黄铜/镧转化膜的腐蚀行为与模拟雨水的 pH有关,在酸性范围内,溶液的pH越高,越不容易发生腐蚀。
(4) 黄铜/镧转化膜在pH = 3.29的模拟雨水中的腐蚀过程有3个阶段:浸泡初期,具有很高的阻抗值,转化膜完好,对基体起到屏蔽保护作用;浸泡中期,出现了2个时间常数,模拟雨水中的侵蚀性介质渗入膜层并逐渐到达基体试样表面;浸泡后期,阻抗谱上出现3个时间常数,黄铜基体发生氧化还原反应。
[1] SINGH R N, TIWARI S K, SINGH W R. Effects of Ta, La and Nd additions on the corrosion behavior of aluminum bronze in mineral acids [J]. Journal of Applied Electrochemistry, 1992, 22 (12): 1175-1179.
[2] ALDYKIEWICZ A J, DAVENPORT A J, ISAACS H S. Studies of the formation of cerium-rich protective films using X-ray absorption near-edge spectroscopy and rotating disk electrode methods [J]. Journal of the Electrochemical Society, 1996, 143 (1): 147-154.
[3] 韩宝军, 徐洲. 稀土 Ce在紫铜缓蚀剂中的应用研究[J]. 表面技术, 2005, 34 (4): 18-20.
[4] 章江洪, 张英杰, 闫宇星. 稀土转化膜在金属材料表面改性中的研究进展[J]. 稀土, 2009 (5): 84-89, 94.
[5] FAN H Q, LI S Y, SHI Z C, et al. Studies of the conversion coatings formed by combined use of lanthanum salt and benzotriazole on commercial brass [J]. Advanced Materials Research, 2011, 239/242: 214-218.
[6] 甘树坤, 吕雪飞. 铜合金表面硝酸镧稀土钝化膜的性能研究[J]. 材料保护, 2008, 41 (8): 35-37.
[7] 吕雪飞, 李淑英. 环保型铜及其合金化学抛光与钝化新工艺[J]. 材料保护, 2006, 39 (9): 25-27.
[8] 李锋, 刘俊, 陈颢. 铜及其合金表面钝化新工艺的研究[J]. 电镀与涂饰, 2005, 24 (2): 15-17.
[9] SCENDO M. The effect of purine on the corrosion of copper in chloride solutions [J]. Corrosion Science, 2007, 49 (2): 373-390.
[10] KOSEC T, MILOŠEV I, PIHLAR B. Benzotriazole as an inhibitor of brass corrosion in chloride solution [J]. Applied Surface Science, 2007, 253 (22): 8863-8873.
[11] RAMJI K, CAIRNS D R, RAJESWARI S. Synergistic inhibition effect of 2-mercaptobenzothiazole and Tween-80 on the corrosion of brass in NaCl solution [J]. Applied Surface Science, 2008, 254 (15): 4483-4493.
[12] WONG D K Y, COLLER B A W, MACFARLANE D R. A kinetic model for the dissolution mechanism of copper in acidic sulfate solutions [J]. Electrochimica Acta, 1993, 38 (14): 2121-2127.
[13] FENG Y, TEO W K, SIOW K S, et al. The corrosion behaviour of copper in neutral tap water. Part I: Corrosion mechanisms [J]. Corrosion Science, 1996, 38 (3): 369-385.
[14] FENG Y, TEO W K, SIOW K S, et al. The corrosion behaviour of copper in neutral tap water. Part II: Determination of corrosion rates [J]. Corrosion Science, 1996, 38 (3): 387-395.
[15] 沙晨燕, 何文珊, 童春富, 等. 上海近期酸雨变化特征及其化学组分分析[J]. 环境科学研究, 2007, 20 (5): 31-34.
[16] 安百刚. 酸雨/雨水环境中典型金属材料的腐蚀行为研究[D]. 天津:天津大学, 2003: 50.
[17] FOLEY R T. The localized corrosion of aluminum alloys—a review [J]. Corrosion, 1986, 42 (5): 277-288.
[18] PYUN S I, HONG M H. The repassivation kinetics of pure nickel in a Na2SO4solution using abrading electrode technique [J]. Electrochimica Acta, 1992, 37 (13): 2437-2442.
[19] AMBAT R, DWARAKADASA E S. Studies on the influence of chloride ion and pH on the electrochemical behavior of aluminum alloys 8090 and 2014 [J]. Journal of Applied Electrochemistry, 1994, 24 (9): 911-916.
[20] PYUN S I, LEE E J. Effect of halide ion and applied potential on repassivation behavior of Al–1 wt.%Si–0.5 wt.%Cu alloy [J]. Electrochimica Acta, 1995, 40 (12): 1963-1970.
Corrosion behavior of lanthanum conversion coating on brass substrate in artificial rainwater //
FAN Hongqiang, LI Shu-ying*, ZHAO Zong-chang, LIN Le-sheng, ZHANG Lin
Lanthanum conversion coating was prepared on brass substrate by chemical immersion. The conversion bath composition and process conditions are as followers: lanthanum nitrate 3.5-5.5 g/L, benzotriazole 8.0-12.0 g/L, sulfosalicylic acid 8.0-12.0 g/L, citric acid 15.0 g/L, temperature 60 °C, pH 4, and time 3 min. The corrosion behavior of brass/lanthanum conversion coating in artificial rainwater was studied by atomic absorption spectroscopy and electrochemical methods. The mass concentration of copper ions dissolved from the brass/lanthanum conversion coating in artificial rainwater is lower than that from brass substrate during the same immersion time. The higher the pH of artificial rainwater under acid condition, the more difficult the corrosion of brass/lanthanum conversion coating will be. Lanthanum conversion coating is sensitive tond Cl−in rainwater. The corrosive pitting of brass/lanthanum conversion coating becomes more serious as the Cl−concentration increases, nearly the whole brass/lanthanum conversion coating corrodes seriously when the
concentration increases, whileconcentration has little effect on the corrosion behavior of brass/lanthanum conversion coating. The corrosion of brass/lanthanum conversion coating in artificial rainwater with a pH of 3.29 proceeds through 3 stages.
brass; conversion coating; lanthanum; rainwater; corrosion
Faculty of Chemical, Environmental and Biological Science and Technology, Dalian University of Technology, Dalian 116012, China
TG174.41
A
1004 – 227X (2012) 01 – 0043 – 04
2011–07–21
2011–09–02
范洪强(1982–),男,福建建瓯人,博士,研究方向为金属材料表面涂装及改性。
李淑英,教授,(E-mail) dllishuying@126.com。
[ 编辑:周新莉 ]

