石墨烯/铂复合材料的制备及电化学性能研究
牛玉莲 肖雪清 顾志国 李在均
(江南大学化学与材料工程学院,无锡 214122)
石墨烯/铂复合材料的制备及电化学性能研究
牛玉莲 肖雪清 顾志国 李在均*
(江南大学化学与材料工程学院,无锡 214122)
采用Hummers法制备氧化石墨,再超声分散于去离子水中形成稳定的氧化石墨分散液。分散液与氯铂酸溶液混合后,氧化石墨烯还原氯铂酸产生大量铂纳米粒子,铂粒子被牢固地锚在氧化石墨烯片上,最后将所得到的氧化石墨烯/铂复合物置于管式炉中在Ar/H2气氛中于800℃下热裂解制备出石墨烯/铂复合材料。形貌与纳米结构分析表明,氧化石墨已被彻底还原成石墨烯,铂纳米粒子均匀分散在褶皱的石墨烯纳米片间。电化学阻抗研究进一步揭示复合材料的电子转移阻抗明显小于石墨烯,呈示铂纳米粒子掺入石墨烯片层大大改善了导电性。石墨烯/铂复合材料应用于对苯二酚的电化学检测,检出限达1.6×10-7mol·L-1,这说明该材料具有优异的电催化性能。
石墨烯;铂;复合材料;电催化
石墨烯是单层碳原子紧密堆积形成的六方蜂巢状晶格结构的晶体[1],它独特的二维结构使其具有优异的电学、热学、力学及化学性质[2-3],但石墨烯片层间存在较大的范德华力,易发生堆积和聚集,从而限制了石墨烯在许多方面的应用。为了解决以上问题,人们采用在石墨烯片层间掺杂金属纳米粒子,这不仅有效避免石墨烯片层因聚集而重新回到石墨晶体,而且大大改善石墨烯材料的电子传导性。贵金属是重要的金属催化剂,应用广泛,而石墨烯具有极大的比表面积,将它们复合即可显著改善贵金属的催化性能和重复利用性。目前,石墨烯/贵金属复合材料已在燃料电池、生物传感器等领域获得较好的应用[4-10]。
目前,石墨烯/贵金属复合材料的制备方法主要有共沉淀法和电化学沉积法。共沉淀法是先将贵金属盐与石墨烯溶液混合,再加入硼氢化钠、水合肼等强还原剂,贵金属盐和氧化石墨同时还原成金属纳米粒子和石墨烯,它们从水溶液中共沉淀析出而制备出石墨烯/贵金属复合材料[11-12]。该方法操作简单,但需大量使用毒性较大的化学试剂,对操作人员健康和环境带来较大危害。此外,氧化石墨和金属前驱体的还原难易程度不同,且还原产物的水溶性差异大,共沉淀得到的石墨烯/贵金属复合材料中贵金属粒子难以均匀分散在石墨烯片层之间,从而导致材料的催化性能并不理想。电化学沉积法常采用将氧化石墨预涂于电极表面,然后电极放在含有贵金属前驱体的电解质溶液中控制电位电解,将金属离子还原成金属纳米粒子并沉积于电极表面[13]。电沉积法简单、绿色环保,但所制得的复合材料金属纳米粒子并没有渗入石墨烯片层中,而是沉积在石墨烯涂层表面。可见,开发一种绿色、高效和可靠的石墨烯/贵金属复合材料制备方法具有非常重要的现实意义。
基于氧化石墨和氯铂酸在氧化还原电位上的差异,我们开发出一种石墨烯/铂复合材料制备新方法。首先,将氧化石墨和氯铂酸溶液均相混合,再利用氧化石墨烯将氯铂酸还原为铂纳米粒子,并牢固地锚于氧化石墨烯纳米片上,最后将收集到的沉淀干燥后置于管式炉中高温热裂解制得石墨烯/铂复合材料。不同于现有文献报道,氧化石墨还原更彻底,氯铂酸在氧化石墨烯纳米片上原位还原和固定,从而使铂粒子能均匀分散于石墨烯片层间。此外,石墨烯/铂复合材料的制备过程中无需使用任何有毒化学试剂,方法非常绿色环保。研究表明,所制备的石墨烯/铂复合材料分散性良好,对对苯二酚的氧化还原表现了显著的电催化行为。
1 实验部分
1.1 试剂和仪器
天然鳞片石墨(质量分数≥99%,500目,青岛天和石墨有限公司);高锰酸钾(分析纯,中国金山区兴塔美兴化工厂);氯铂酸、浓硫酸、硝酸钠、双氧水(均为分析纯,国药集团化学试剂有限公司);实验用水为二次蒸馏水。
JJ-1精密定时电动搅拌器 (江阴市保利科研器械有限公司);HH-S数显恒温水浴锅(江苏金坛医疗仪器厂);SHB-Ⅲ循环水式多用真空泵 (郑州长城科工贸有限公司);超声分散仪(上海新苗医疗器械制造有限公司);电化学工作站CHI660D(上海辰华仪器有限公司);FT-LA 2000型傅立叶红外光谱仪 (加拿大ABB Bomen);S4800型扫描电镜 (日本日立公司);D8 Advance型X-射线衍射仪(德国Bruker AXS公司)。
1.2 材料的制备
取15 mL浓硫酸,5 g过硫酸钾,5 g五氧化二磷置于200 mL烧杯中,加热至80℃后,将10 g天然鳞片石墨加入其中并在此温度下维持6 h,趁热过滤,水洗滤饼至中性,产物在空气中干燥12 h,得初步氧化的氧化石墨[14]。将上述初步氧化产物在机械搅拌下缓慢加入到装有230 mL浓硫酸的2 000 mL大烧杯中,温度维持在(0±1)℃,再缓慢加入5 g硝酸钠与30 g高锰酸钾的混合物,持续搅拌2 h后将恒温水浴锅温度升至 (35±3)℃,搅拌下保温30 min,缓慢加入460 mL水,并升温至98℃,维持15 min。温水稀释到1400 mL后加入适量的H2O2(5%),趁热过滤,用5%HCl(V/V)充分洗涤滤饼,直至滤液中无SO42-(用BaCl2溶液检测)。于50℃在P2O5存在下真空干燥24 h,密封保存得到氧化石墨[3,15]。称取100 mg上述氧化石墨,加入到200 mL水中,超声分散至溶液澄清透明,移取100 mL该氧化石墨烯溶液至250 mL三口烧瓶中,于冰浴下加入3.38 mL浓度为0.029 5 mol·L-1的氯铂酸水溶液,机械搅拌30 min,过滤得到氧化石墨烯/铂复合材料,空气中干燥12 h[16]。最后将此材料置于通有Ar/H2混合气体 (VAr∶VH2=95∶5)的管式炉中,800℃下热裂解10 min,得石墨烯/铂复合材料[17],密封保存待用。
1.3 电化学测试
将氧化石墨、石墨烯、氧化石墨烯/铂复合材料及石墨烯/铂复合材料通过超声分别将其分散于水溶液中,用微量进样器量取10 μL溶液修饰于干净的玻碳电极表面,待晾干后再在其表面修饰5 μL浓度为0.5wt%的壳聚糖溶液,以防止材料脱落。采用三电极系统分别对材料进行循环伏安及交流阻抗测试,其中以玻碳电极为工作电极,银-氯化银电极为参比电极,铂丝为对电极。循环伏安测试:以pH=7的醋酸缓冲溶液配制浓度为0.2 mmol·L-1的对苯二酚为测试溶液,扫描范围为-400~800 mV。电化学阻抗测试:采用含有0.1 mol·L-1KNO3和5.0 mmol·L-1Fe(CN)63-/Fe(CN)64-(1:1)的磷酸盐缓冲溶液(pH=7.0)为测试底液,频率范围在0.1~105Hz。
2 结果与讨论
2.1 合成方法选择与优化
氧化石墨烯/铂复合材料的合成是基于氧化石墨烯与氯铂酸之间的氧化还原反应。由于氧化石墨(0.262 V)的标准电位明显低于氯铂酸(0.771 V),因此氧化石墨可与氯铂酸发生氧化还原反应氯铂酸被氧化石墨烯还原为单质铂[18-19]。当氯铂酸溶液和金黄色的氧化石墨烯混合后,溶液颜色迅速变深,逐渐出现絮状物,最后沉淀析出氧化石墨烯/铂复合物沉淀(图1)。该方法制备氧化石墨烯/铂复合材料操作简单,实验过程不添加任何化学试剂,是非常绿色环保的。由于氧化石墨含有丰富的氧,易溶于水,可确保氧化石墨能与氯铂酸溶液混合均匀,这确保了它们之间的氧化还原反应能在氧化石墨纳米片上进行。扫描电镜研究清楚地证实,铂纳米粒子均匀分散在褶皱的氧化石墨烯片层之间 (图2a)。为了考察氧化石墨与氯铂酸的反应机理,我们还对制得的氧化石墨烯/铂复合材料进行了红外光谱分析(KBr压片法)。从图2b可以看出,氧化石墨烯/铂复合材料的红外光谱图与氧化石墨并无明显差异,含有-OH,-COOH的特征吸收峰,这说明上述反应中氧化石墨的氧并没有得到较好的剥离。考虑到高效、环保、可靠等因素,我们选择用高温固相法还原氧化石墨烯/铂复合材料,目的是使氧化石墨能充分还原成石墨烯。研究表明,当热裂解温度达800℃以上铂纳米粒子可能会在石墨烯表面熔化而发生移动。当煅烧时间超过10 min后,金属粒子也会发生较大迁移。此外,高温煅烧时间对复合材料中金属粒子的大小也有较大影响,继续升高温度铂纳米粒子倾向于彼此聚集成较大颗粒[17]。为了避免铂纳米粒子的聚集和确保氧化石墨得到彻底还原,煅烧温度和时间分别设置为800℃和10 min。

图1 氧化石墨与氯铂酸混合后的变化(a)1 min,(b)10 min,(c)20 min,(d)30 minFig.1 Change after graphite oxide mixed with H2PtCl6for 1 min(a),10 min(b),20 min(c)and 30 min(d)
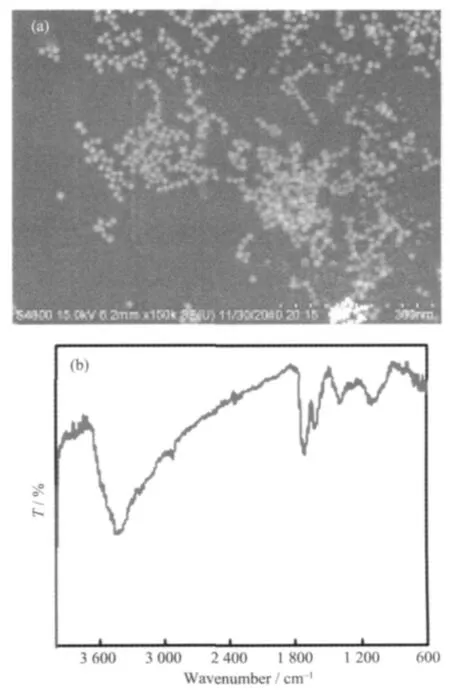
图2 氧化石墨烯/铂复合材料的扫描电镜(a)和红外光谱(b)Fig.2 SEM image(a)and infrared spectrum(b)of the graphene oxide/Pt composite
2.2 结构与形貌表征
分别采用X-射线衍射(XRD)(辐射源:Cu Kα,λ= 0.154 06 nm,功率:1 600 W(40 kV×40 mA),扫描速度:4°·min-1)、红外(IR)(KBr压片法)、拉曼(Raman)(Ar离子激光波长514.5 nm,扫描范围200~2500 cm-1)、扫描电镜(SEM)和透射电镜(TEM)对材料的结构和形貌进行了表征。图3是氧化石墨烯/铂复合材料和石墨烯/铂复合材料的XRD分析结果。图3a呈示,氧化石墨烯/铂复合材料的XRD图在10.9°(2θ)处有一尖锐强峰,它是氧化石墨烯的特征吸收峰[20-21],从而说明氧化石墨烯/铂复合材料中氧化石墨烯并未被彻底还原。另一方面,由于10.9°处的衍射峰太过尖锐,加之金属铂的含量较少,使图3a中金属铂的衍射峰并不突出,但将XRD图放大后,铂纳米粒子的特征晶面衍射峰,可以观察到39.8°(111),46.3° (200),67.5°(220)4个衍射峰[22]。由此可以推断,氯铂酸已被氧化石墨烯还原成铂粒子,从而成功合成了氧化石墨烯/铂复合材料。图3b是石墨烯/铂复合材料的XRD图。在石墨烯/铂复合材料的XRD图中,氧化石墨烯的特征衍射峰消失,而金属铂在39.8° (111),46.3°(200),67.5°(220)处的特征峰变得更加明显。此外,石墨烯/铂复合材料的XRD在26°附近出现了一宽衍射峰,这是典型的石墨结构特征衍射峰,说明在氧化石墨烯在还原过程中出现再次石墨化现象,与文献报导的一致[23-24]。
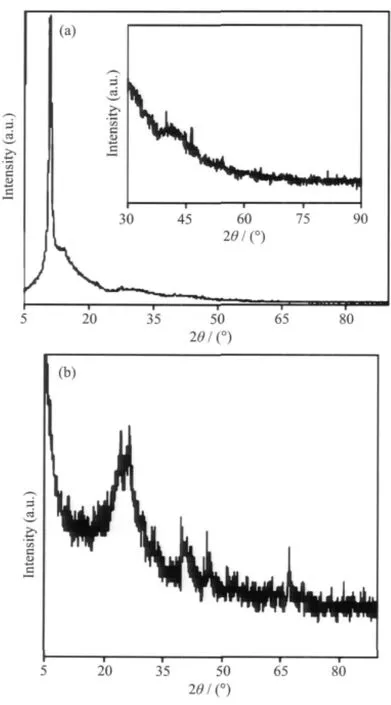
图3 氧化石墨烯/铂复合材料(a)和石墨烯/铂复合材料(b)的XRD图Fig.3 XRD patterns of graphene oxide/Pt composite(a) and graphene/Pt composite(b)
为了方便比较,我们将石墨 (G)、氧化石墨烯(GO)和石墨烯/铂复合材料(GN/Pt)的红外光谱列于图4a。由于天然石墨纯度较高,除了由少量杂质或氧化在3 500 cm-1附近形成的较弱-OH吸收峰外,几乎无明显吸收。石墨经剧烈氧化得到的氧化石墨烯,其红外光谱在3400 cm-1处有较强的-OH吸收峰,在中频区的1710 cm-1位置附近出现较尖锐的氧化石墨边缘羧酸或羰基的C=O伸缩振动吸收峰,1 610 cm-1附近因样品吸收了少量水分子出现-OH的弯曲振动吸收峰,1380 cm-1归属为-COOH中CO的伸缩振动吸收峰,1110 cm-1处的吸收峰是由醇的C-O伸缩振动产生的,以上结果表明氧化石墨烯含有丰富的含氧基团[25-26]。然而,经过高温还原得到的目标产物石墨烯/铂复合材料的红外光谱与石墨非常相似,在氧化石墨烯的红外光谱中出现过的含氧基团的特征吸收峰几乎全部消失,以上事实说明复合材料中的氧化石墨已被深度还原。图4b是石墨烯/铂复合材料的拉曼光谱。石墨烯/铂复合材料的拉曼光谱展现出石墨烯材料典型的特征D峰和G峰,其ID/IG的增加说明碳原子混乱程度较高。
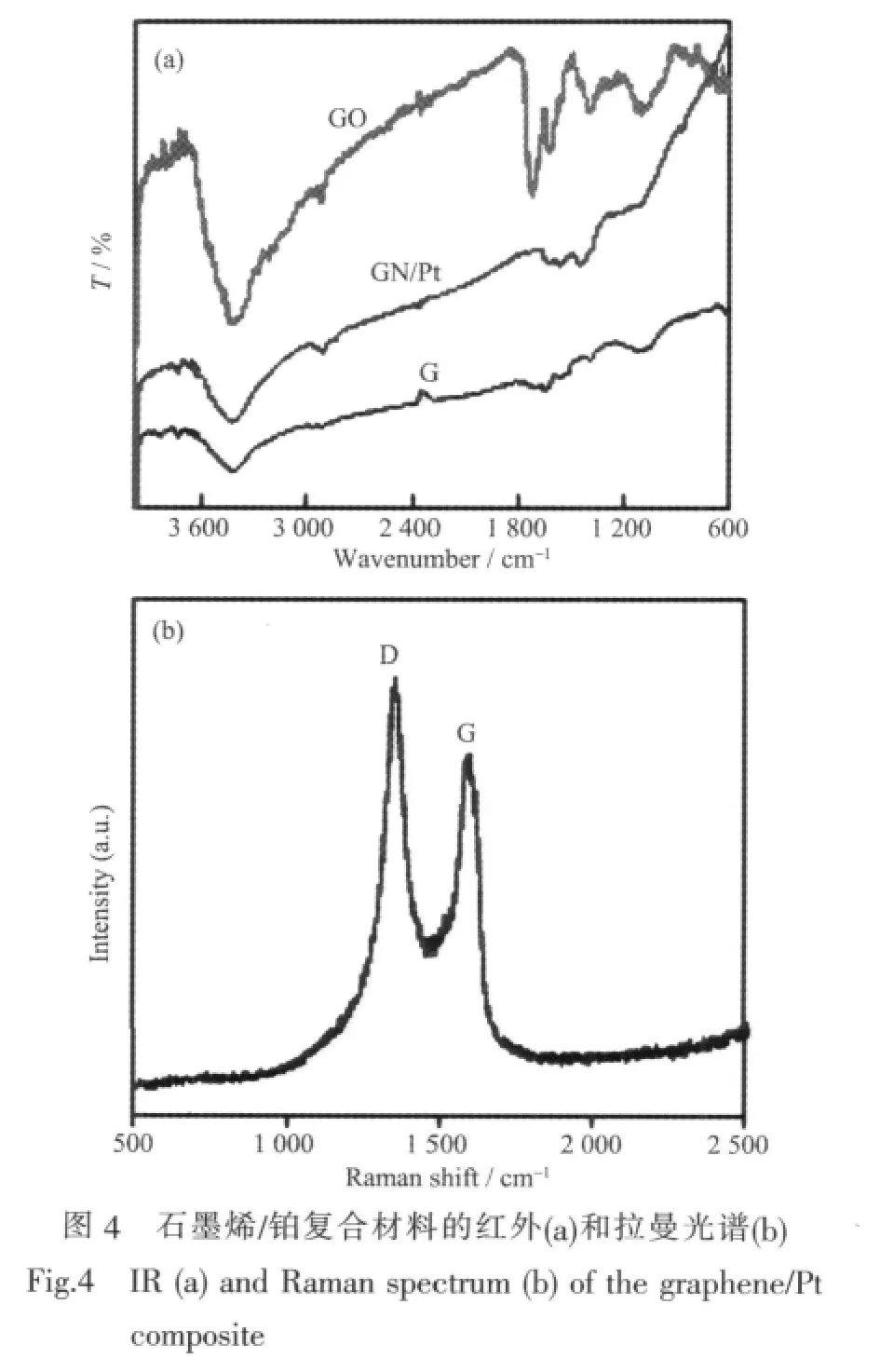
图4 石墨烯/铂复合材料的红外(a)和拉曼光谱(b)Fig.4 IR(a)and Raman spectrum(b)of the graphene/Pt composite
图5是石墨烯/铂复合材料的SEM和TEM。电镜分析显示,褶皱的石墨烯呈片层状结构,整个褶皱面及边缘均能明显看到高度分散的铂纳米粒子。铂纳米粒子呈球形,平均粒径在20 nm左右。以上分析可知,我们成功制备出分散性良好的石墨烯/铂复合材料,经石墨炉原子吸收光度法测定铂负载率为12.3%。
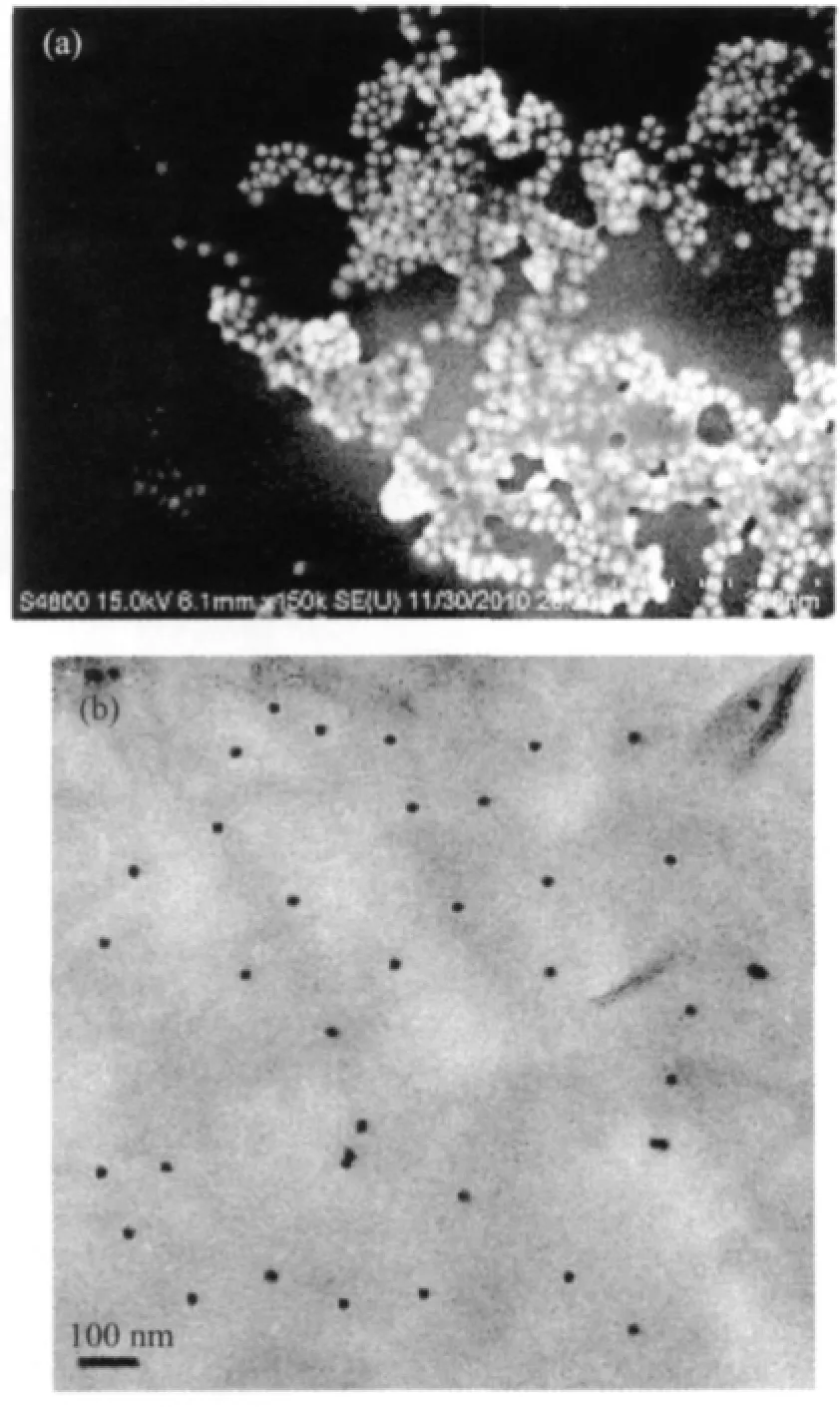
图5 石墨烯/铂复合材料的SEM(a)和TEM(b)Fig.5 SEM(a)and TEM(b)images of the graphene/Pt composite
2.3 电催化性能
电化学交流阻抗(EIS)是研究材料电子传导性的重要工具。石墨烯和石墨烯/铂复合材料交流阻抗列于图6。从图6可以看出,阻抗曲线由两部分组成。其中,半圆部分是表示修饰层的电子转移阻抗,而直线部分是表示电解质在修饰层的扩散电阻。由于导电性良好的铂纳米粒子掺入到石墨烯纳米片层间使材料的传导性大大改善,石墨烯/铂复合材料的电子转移阻抗明显小于石墨烯。石墨烯/铂复合材料优异的传导性为其在电化学方面的应用奠定了基础。为了进一步考察材料在电催化方面的性能,我们分别将氧化石墨、氧化石墨烯/铂复合材料和石墨烯/铂复合材料滴涂在玻碳电极表面制成相应的修饰电极,采用循环伏安法考察对苯二酚在电极表面的氧化还原过程,结果列于图7。从图7可知,由于氧化石墨层不导电,对苯二酚没有电催化作用,其循环伏安曲线几乎没有响应。氧化石墨烯/铂复合材料中铂纳米粒子具有良好的导电性,对对苯二酚氧化还原有一定的催化能力,在循环伏安图上出现一对明显的氧化还原峰,但因材料中的氧化石墨对修饰层与电极之间的电子传递起着阻碍作用,铂纳米粒子的催化作用被大大减弱,这导致对苯二酚氧化还原峰电流的降低和峰电位差增加。然而,石墨烯/铂复合材料修饰电极的氧化还原电流明显高于氧化石墨和氧化石墨烯/铂复合材料,且峰电位更低,这表明石墨烯/铂复合材料对对苯二酚的电化学反应起到了显著的催化作用。石墨烯/铂复合材料修饰电极应用于痕量对苯二酚的差分脉冲伏安法检测 (图8)。结果表明,当对苯二酚的浓度在0~20 μmol·L-1之间,差分脉冲伏安峰电流与对苯二酚浓度呈线性关系,其线性回归方程为:Ip=3.355 7C (μmol·L-1)-0.056 1(R2=0.999 8),方法检出限达1.6× 10-7mol·L-1。可见,所制得的石墨烯/铂复合材料具优异的电催化性能。
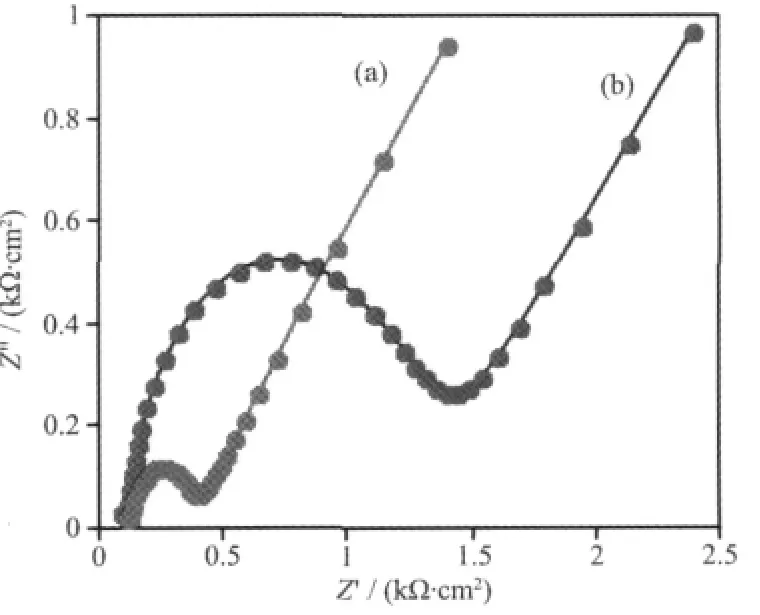
图6 石墨烯(a)和石墨烯/铂复合材料(b)交流阻抗图Fig.6 EIS of graphene(a)and graphene/Pt composite(b)
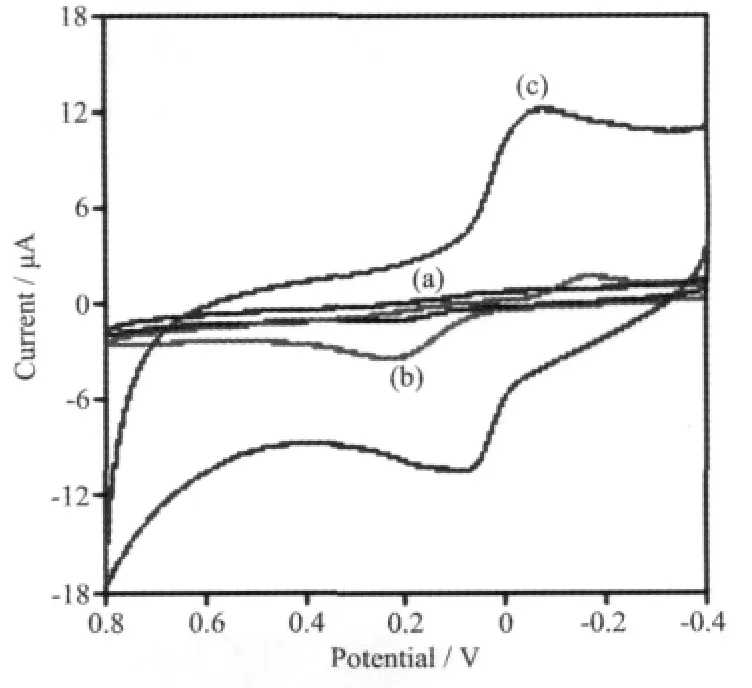
图7 氧化石墨(a)、氧化石墨烯/铂复合材料(b)和石墨烯/铂复合材料(c)的循环伏安图Fig.7 Cyclic voltammograms of graphite oxide(a), graphene oxide/Pt composite(b)and graphene/Pt composite(c)
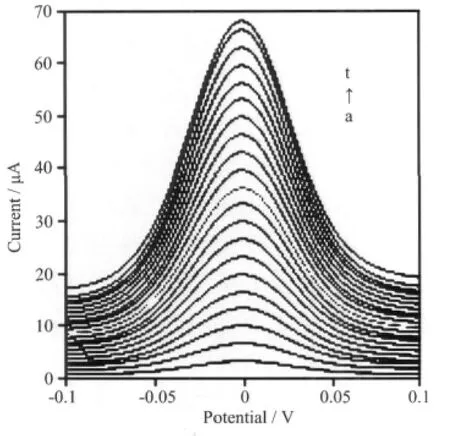
图8 石墨烯/铂复合材料修饰电极的差分脉冲伏安图,对苯二酚:1~20 μmol·L-1(a→t)Fig.8 Differential pulse voltammograms of graphene/Pt modified electrode,hydroquinone:1~20 μmol· L-1(a→t)
3 结 论
利用氧化石墨烯和氯铂酸的原位氧化还原反应不仅实现了氯铂酸的彻底还原,而且所形成的铂纳米粒子被均匀地锚在氧化石墨烯片层上。结合高温固相还原,成功开发出高性能的石墨烯/铂复合材料。新的方法具有简便、绿色和高效等显著特点,可广泛应用于以满足催化剂和电化学传感器需要为目的的铂、金、钯等贵金属的石墨烯复合材料的合成。
[1]Stankovich S,Dikin D A,Dommett G H B,et al.Nature, 2006,442:282-286
[2]YANG Yong-Gang(杨永岗),CHEN Cheng-Meng(陈成猛), WEN Yue-Fang(温月芳),et al.New Carbon Mater.(Xinxing Tan Cailiao),2008,23(3):193-200
[3]HUANG Gui-Rong(黄桂荣),CHEN Jian(陈建).Chin.J. Carbon Techn.(Tansu Jishu),2009,28(4):10-15
[4]Seidel Y E,Schneider A,Jusys Z,et al.Langmuir,2010,26 (5):3569-3578
[5]Wang L,Tian C G,Wang H,et al.J.Phys.Chem.C,2010, 114(19):8727-8733
[6]Yu P,Qian Q,Lin Y Q,et al.J.Phys.Chem.C,2010,114(8): 3575-3579
[7]Shen Q M,Jiang L P,Zhang H,et al.J.Phys.Chem.C, 2008,112(42):16385-16392
[8]Zhang H,Yin Y J,Hu Y J,et al.J.Phys.Chem.C,2010, 114(27):11861-11867
[9]Meng L,Jin J,Yang G X,et al.Anal.Chem.,2009,81(17): 7271-7280
[10]Seger B,Kamat P V.J.Phys.Chem.C,2009,113(19):7990-7995
[11]Muszynski R,Seger B,Kamat P V.J.Phys.Chem.C,2008, 112(14):5263-5266
[12]Dey R S,Raj C R.J.Phys.Chem.C,2010,114(49):21427-21433
[13]Hu Y J,Jin J,Wu P,et al.Electrochimica Acta,2010,56(1): 491-500
[14]Kovtyukhova N I,Ollivier P J,Martin B R,et al.Chem. Mater.,1999,11:771-778
[15]Lee J K,Smith K B,Hayner C M,et al.Chem.Commun., 2010,46:2025-2027
[16]Chen X M,Wu G H,Chen J M,et al.J.Am.Chem.Soc., 2011,133(11):3693-3695
[17]Zhong J,David N,Wei L.Chem.Mater.,2010,22(20):5695-5699
[18]Choi H C,Shim M,Bangsaruntip S.J.Am.Chem.Soc., 2002,124(31):9058-9059
[19]Chen L Y,Tang Y H,Wang K,et al.Electrochem.Commun., 2011,13:133-137
[20]XUE Lu-Ping(薛露平),ZHENG Ming-Bo(郑明波),SHEN Chen-Fei(沈辰飞),et al.Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2010,26(8):1375-1381
[21]DANG Zhi-Min(党志敏).Thesis for the Master of Nanjing University of Science and Technology(南京理工大学硕士学位论文).2010.
[22]Xin Y C,Liu J G,Zhou Y,et al.J.Power Sources,2011, 196:1012-1018
[23]HAN Zhi-Dong(韩志东),WANG Jian-Qi(王建祺).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2003,19(5):459-461
[24]Bourlinos A B,Gournis D,Petridis D,et al.Langmuir, 2003,19(15):6050-6055
[25]HUANG Qiao(黄桥),SUN Hong-Juan(孙红娟),YANG Yong -Hui(杨勇辉).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2011,27(9):1721-1726
[26]YANG Yong-Hui(杨勇辉),SUN Hong-Juan(孙红娟),PENG Tong-Jiang(彭同江).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2010,26(11):2083-2090
Synthesis and Electrochemical Property of the Graphene/Pt Composites
NIU Yu-Lian XIAO Xue-Qing GU Zhi-Guo LI Zai-Jun*
(School of Chemical and Material Engineering,Jiangnan University,Wuxi,Jiangsu214122,China)
Graphite oxide was prepared by Hummers′method and was dispersed in the deionized water with the help of ultrasonic wave to form stable graphene oxide dispersion.After above dispersion was mixed with chloroplatinic acid solution,the graphene oxide rapidly reduced chloroplatinic acid and produce great deal of platinum nanoparticles,which were tightly anchored in the graphene oxide nanosheets.Finally,the obtained graphene oxide/platinum composite was placed in a tube furnace and further reduced in an atmosphere of Ar/H2under 800℃ to graphene/platinum composite.The characterization of morphology and nanostructure shows that the graphite oxide has been thoroughly reduced to graphene and platinum nanoparticles were well dispersed in between draped graphene nanosheets.The electrochemical impedance spectroscopy analysis further revealed the electron transfer impedance of the composite is obviously lower than sole graphene,indicating that the introduction of platinum particles remarkably improve the electrical conductivity.Moreover,the obtained graphene/platinum composite was also applied to electrochemical determination of hydroquinone.The detection limit was found to be 1.6×10-7mol·L-1.This demonstrated the composite is of excellent electrocatalytic property.
graphene;platinum;composite;electrocatalysis
O613.71;O614.82+6
A
1001-4861(2012)04-0751-06
2011-10-10。收修改稿日期:2011-12-01。
国家自然科学基金(No.21176101,No.20771045)资助项目。*
。E-mail:zaijunli@263.net
——庆祝中国共产党成立一百周年贵金属纪念币展

