离体大鼠肠内菌群对知母甾体皂苷代谢研究
张钰哲
(大理学院基础医学院,云南大理 671000)
离体大鼠肠内菌群对知母甾体皂苷代谢研究
张钰哲
(大理学院基础医学院,云南大理 671000)
目的:观察大鼠肠内菌对知母主要活性成分甾体皂苷的代谢及对相应代谢产物进行鉴定。方法:离体培养大鼠肠道菌群,用LC/MS/MS法检测离体肠内菌对甾体皂苷样品的代谢产物。灌胃给予大鼠甾体皂苷样品15 mg·kg-1,于给药后不同时间采集尿样及粪样,用LC/MS/MS法检测甾体皂苷样品的代谢产物。对主要代谢物M1进行结构鉴定。用合成的方法制备代谢物M1标准品进行LC/MS/MS法分析并与大鼠离体和在体样品对比。结果:甾体皂苷样品容易被大鼠消化道菌群代谢,代谢速率很快,其主要代谢产物为代谢物M1,随着代谢时间的延长,代谢物M1的量逐渐增多,而甾体皂苷样品的量则下降迅速。结论:甾体皂苷可被大鼠肠内菌迅速代谢。
甾体皂苷;肠内菌群;代谢物;液-质联用法
甾体皂苷(steroidal saponin)是由螺甾烷类化合物衍生的寡糖苷,是一类重要的中药活性成分,许多常用中药如重楼、黄精、薤白、知母、蒺藜、穿山龙、麦冬等都含有甾体皂苷。研究表明,甾体皂苷具有改善心血管活性,抗癌、抗痴呆、抗病原微生物、降血糖及雌激素样作用。许多主要含甾体皂苷的中成药早已上市,如地奥心血康胶囊、心脑舒通、冠心宁、宫血宁及金刚藤胶囊等。甾体皂苷已成为药物研究开发的重要先导化合物。目前发现中药中含有两个糖链的水溶性甾体皂苷具有显著上调胆碱能n受体数量、改善脑循环、防治老年性痴呆等作用。经构效关系研究,发现呋甾皂苷单体化合物有一定的抗痴呆效果。口服甾体皂苷可显著改善多种拟痴呆模型动物的学习记忆功能,并观察到甾体皂苷对模型动物的脑源性神经生长因子(Brain-derived growth factor,BDNF)、细胞间黏附分子(Intercellular adhesion molecule,ICAM)、血管细胞黏附分子(Vascular cell adhesion molecule,VCAM)、脑组织超氧化物歧化酶(Superoxide dismutase,SOD)活性及丙二醛(Malonaldehyde,MDA)含量的显著调节作用。甾体皂苷改善学习记忆功能的机理,一方面是通过上调胆碱能n及m受体,另一方面是通过扩张血管、抑制血栓形成、改善脑缺血及其损伤实现。经过充分的药效学研究拟将其开发为抗老年性痴呆中药的一类新药。然而药代动力学研究表明,原形药物的生物利用度非常低,小于1%,提示应对其代谢产物进行研究。口服药物的代谢主要通过肝脏和肠道菌群,而中药等天然化合物的代谢与肠道微生菌群关系密切。天然皂苷肠道代谢的研究以日本学者小桥恭一教授为先导者,他先后证明人参皂苷、甘草皂苷等多种中药皂苷口服大多经肠道内细菌转化或代谢后所产生的活性代谢产物入血发挥其疗效。并提出了天然前药的概念〔1〕。本文研究了活体和离体状态下大鼠肠内菌群对甾体皂苷样品的代谢并鉴定其代谢产物,提供主要代谢产物的时-量变化关系。方法采用液-质联用法(LC-MS/MS)。目前文献中对皂苷等天然化合物的代谢研究方法通常为薄层板分离后再用质谱进行检测。此种方法灵敏度较低,测定时基质干扰严重,本研究经过方法摸索,建立了更灵敏的液-质联用法,能够同时提供色谱峰面积和分子量、子离子碎片信息。研究肠内菌群对甾体皂苷样品的代谢及鉴定其代谢产物的结构,对进一步研究代谢产物的活性,阐明其药理作用的真正分子基础有重要意义。
本研究所使用的甾体皂苷样品的分子式为C45H76O19,分子量为920,其结构如图1。
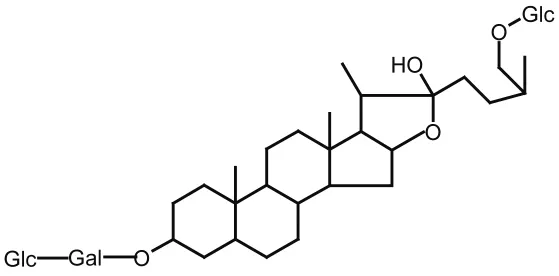
图1 样品甾体皂苷结构式
1 材料与试剂
1.1 实验动物 Wistar大鼠,体重180~200 g,由大理学院动物实验中心提供。
1.2 实验仪器 Finnigan公司LTQ线性离子阱质谱仪,配有离子喷雾离子源以及Xcalibur1.4软件数据处理系统;Agilent 1100高效液相色谱输液泵,Agilent 1100自动进样器;色谱柱为Thermo betabase-18 C18分析柱,I.D.2.1×100 mm,5 mm粒径,美国Thermo公司。
1.3 试剂 知母皂苷化合物BⅡ(规格:HPLC≥ 98%);代谢物M1标准品(萨尔萨皂苷元),购自上海华壹生物科技有限公司;产气袋、密封袋购自Mitsubishi Gas Chemcal Co.Inc;其他化学试剂:磷酸氢二钾、磷酸二氢钾、氯化钠、硫酸铵、氯化钙、硫酸镁、resazurine、L-cysteine、牛肉膏、蛋白胨,以上试剂均为分析纯。为天津福晨化学试剂厂和北京化工厂产品。
1.4 实验方法
1.4.1 厌氧培养液的组成及制备 取37.5 mL溶液A (0.78%K2HPO4);37.5 mL溶 液 B(0.47% KH2PO4,1.18%NaCl,1.2%(NH4)2SO4,0.12%Ca-Cl2,0.25%MgSO4H2O);0.1%resazurine 1 mL;L-cysteine 0.5 g;25%L-ascorbic acid 2 mL;8%Na2CO350 mL;牛肉膏1 g;蛋白胨1 g和营养琼脂1 g;加蒸馏水至1 L;最后调pH 7.5~8.0,其他试剂均为分析纯〔2〕。
1.4.2 离体培养肠内菌群对样品的代谢 取健康大鼠新鲜粪便,按1 g∶4 mL的比例将粪便与生理盐水混合制成悬浊液,取0.5 mL新鲜配制的粪便悬浊液,加入厌氧培养液4.5 mL,混匀,得到5 mL肠菌培养液。取此新鲜配制的肠菌培养液12份,其中6份各加入样品5 mg为实验组。另外6份不加样品,为空白对照组。置于37℃厌氧培养罐(产气袋法:将产气袋打开放入培养袋中就会自动与空气发生化学反应产生CO2,在密闭罐内局部造成缺氧环境,用于肠道厌氧菌培养)中培养,于2、4、8、12、24、36 h取菌群悬液与乙腈按1∶3的比例混合,高速离心10 min,取上清液置高效液相样品瓶中,40 μL进样,LC/MS/MS检测。
1.4.3 大鼠在体肠内菌群对样品代谢粪便及尿样采集与处理〔3-4〕Wistar大鼠6只,雌雄各半,大鼠分别置代谢笼中,实验前禁食12 h,自由饮水,并同时收集空白尿样和粪样;按15 mg·kg-1灌胃给予样品,给药后两小时让大鼠进食。分别收集给药后0~12、12~24、24~48、48~96 h各时间段的尿样及粪样,粪便晾干后研磨混匀,取适量用乙腈浸泡提取过夜。提取液处理同离体菌群悬液。
1.4.4 LC-MS/MS法的分析条件 质谱条件:离子喷射电压4.5 kV;毛细管电压44 V;温度为270℃;鞘气22 L·min-1;辅助气5 L·min-1;扫气2 L·min-1,负离子检测。扫描方式:选择反应监测(SRM)方式。色谱条件:Thermo betabase-18 C18分析柱,I.D.2.1×100 mm,5 mm粒径,梯度洗脱方式。流动相:甲醇-乙腈(50:50,v/v),水,流速0.2 mL·min-1,柱温25℃。流动相梯度变化见表1。

表1 流动相梯度变化
2 实验结果
2.1 离体培养大鼠肠道菌群对知母甾体皂苷化合物的代谢 LC-MS/MS法分析结果显示,样品容易被大鼠肠内菌群代谢。肠内菌悬液与样品在厌氧状态下孵育2 h时,除保留时间为7.9 min的样品色谱峰外,还出现了保留时间为12.3 min的代谢物,称之为M1。M1对应的质谱图显示(见图3),其分子离子峰质荷比m/z∶739.7,二级子离子质荷比m/z∶577.6,根据样品结构推测M1的结构为26位糖链脱去并与22位羟基环合的产物(分子式:C39H64O13结构见图2)。通过化学手段制备的代谢物M1标准品(经过核磁共振分析确证结构),LC-MS/MS法分析,获得的总离子色谱图及二级质谱图(见图4)。图3与图4对比,保留时间及二级质谱图几乎完全一致,佐证M1结构如图3所示。孵育不同时间肠内菌悬液中样品和代谢物M1的色谱峰面积变化如表2所示。代谢物M1自孵育2h时即产生,随后逐渐增多,8 h时峰面积最大,随后缓慢减少。样品在孵育2 h时尚有较高浓度,随后浓度迅速下降,8 h时浓度基本降至谷底。说明样品经口服给药后肠道内转化非常迅速,绝大部分转化为代谢物M1。
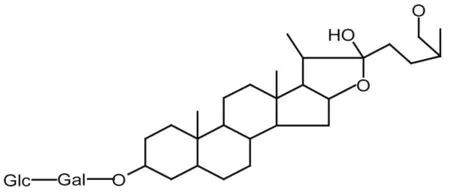
图2 代谢物M1结构式(C39H64O13)

图3 肠内菌群悬液中代谢产物总离子色谱图及M1的对应二级质谱图
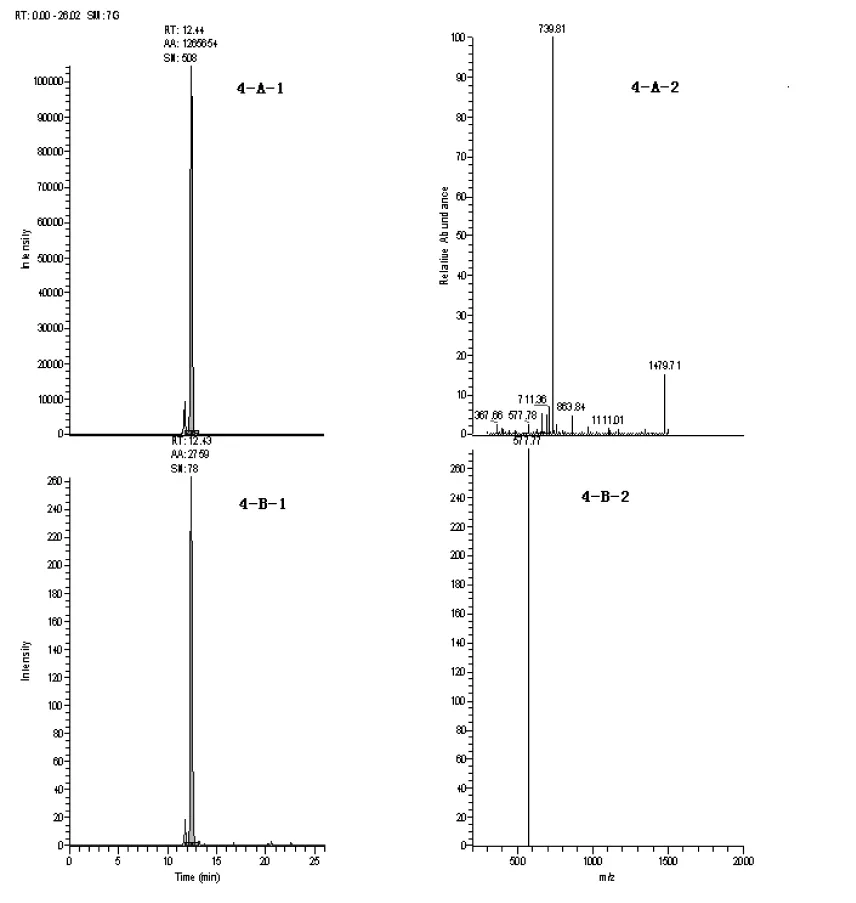
图4 M1标准品色谱图及对应二级质谱图
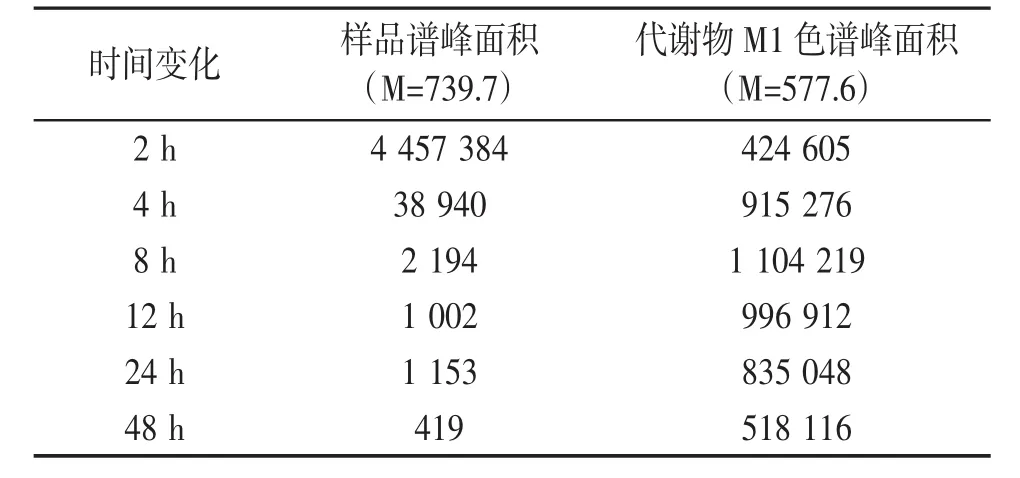
表2 孵育不同时间肠内菌悬液中样品和代谢物M1的色谱峰面积变化
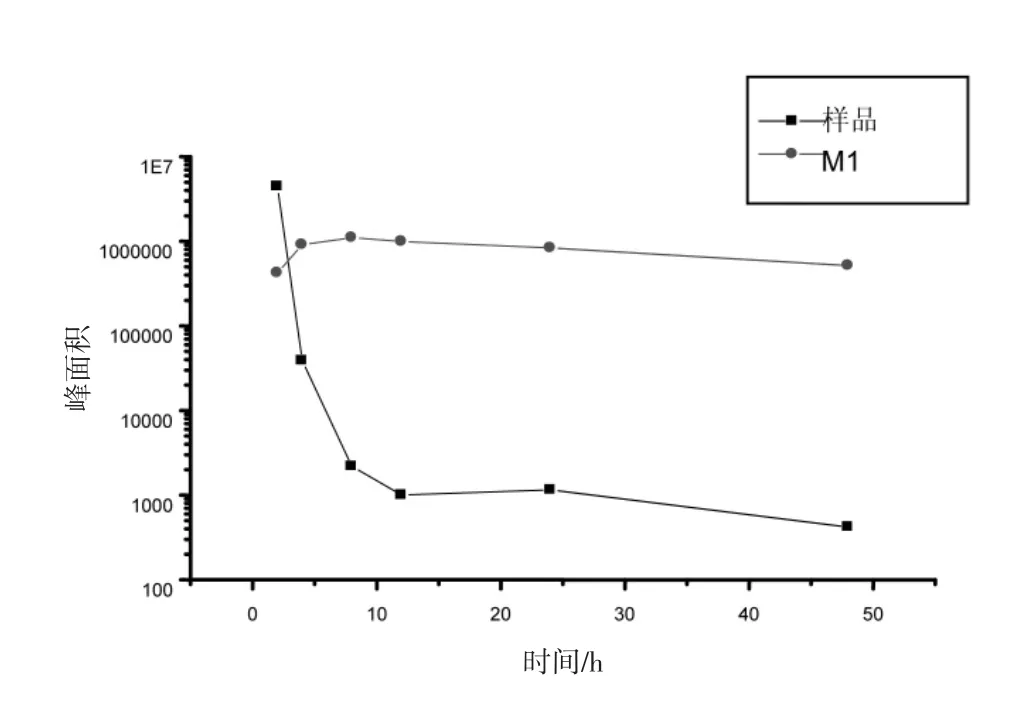
图5 孵育不同时间肠内菌悬液中样品和代谢物M1色谱峰面积曲线
2.2 在体大鼠肠内菌群对样品的代谢 大鼠给药后,分析各个时间段收集的粪便样品色谱及质谱图(典型图谱如图3),样品经肠道菌群代谢后,粪便中已无样品而主要为代谢物M1,与样品经体外培养的肠道菌群代谢后无明显差异,质谱图相似。如图6所示。

图6 体外菌群培养2 h后提取离子在30 min飞行时间内代谢物的典型色谱图及对应质谱图
由2.1及2.2可知样品经体外肠道菌群和在体大鼠肠内菌群的代谢产物均为M1,且随着代谢时间的延长,代谢物M1的量逐渐增多,而甾体皂苷样品的量则下降迅速。
3 讨论
糖类知母甾体皂苷化合物是肠道内细菌重要的碳源,因此,肠道内细菌的苷键水解酶系对具有糖苷键的药物进行水解是肠道内细菌代谢的一大特征〔5-6〕。本研究的结果揭示了样品生物利用度低的原因。样品经口服给药后在肠道内即被菌群迅速转化,主要为代谢物M1。有小部分M1再脱糖的代谢产物,其结构未确定。少量原形被吸收入血,而代谢物M1随后经粪便排出。色谱图中代谢物M1为保留时间非常接近的双峰,双峰对应的质谱图显示分子离子质荷比和子离子质荷比均为739.7及577.6。推测他们是一对结构较为相似的同分异构体。M1是否入血及入血量多少,需再对血样进行代谢物研究。发挥样品药效学的真正活性分子及肠道内具体代谢菌株尚待进一步研究。
〔1〕李艺,蒋建东.中国药用天然产物有效成分的代谢研究进展〔J〕.中国中药杂志,2010,35(23):3223-3232.
〔2〕张怡红,李华冲.离体培养人肠道菌群对黄山药总皂苷的代谢研究〔J〕.中国现代药物应用,2008,2(14):6-8.
〔3〕陈新梅.大鼠肠道酶和菌群对人参皂苷Rg1的代谢转化研究〔J〕.中国实验方剂学杂志,2011,17(11):210-212.
〔4〕徐文,张亚平,张卫东,等.离体大鼠肠道菌群对淫羊藿苷的代谢研究〔J〕.世界科学技术:中医药现代化,2006,8(6):98-106.
〔5〕Akao T,Che Q M,KyoichiK,et al.A Purgative Action of Barbaloin is Induced by Eubacterium sp Strain BAR,a Human Intestinal Anaerobe,Capable of Transforming Barbaloin to Aloeemodin Anthrone〔J〕.Bio Pharm Bull,1996,19(1):136-138.
〔6〕赵钟祥,李美芬,林朝展,等.大鼠肠内菌对毛冬青皂苷ilexsaponin A1的代谢转化〔J〕.中国药科大学学报,2011,42(4):329-332.
In Vitro Study of Rat Coliform Bacteria Metabolism of Steroidal Sponin Extract from Anemarrhena asphodeloides
ZHANG Yuzhe
(Pre-clinical College,Dali University,Dali,Yunnan 671000,China)
Objective:To study the metabolism of steroidal saponins extracted from Anemarrhena asphodeloides in rat intestinal flora in vitro and to identify the major metabolite.Methods:Rat intestinal flora and steroidal saponins extractions were incubated in vitro, and LC/MS/MS method was used to examine metabolites of steroidal saponins.The urine samples and dungs of the rats were collected after the rats were given with steroidal saponins extract in dose of 15 mg·kg-1by gavage.The metabolites of the steroidal saponins were detected with LC/MS/MS,and the structure of the major metabolite M1 was identified.Meanwhile,the M1 obtained from synthesis was compared with the natural M1 both in vitro and in vivo.Results:In vitro,steroidal saponins extracted from A. asphodeloides were metabolized easily by rat intestinal flora,and the metabolic rate was very quickly,and the major metabolite was M1.The metabolite M1 increased gradually with the prolongation of incubation time,but the quantity of steroidal saponins extract were dropped quickly.Conclusion:Steroidal saponins extracted from A.asphodeloides are metabolized easily by rat intestinal flora.
steroidal saponins;intestinal flora;metabolism;LC/MS/MS
R286.2[文献标志码]A[文章编号]1672-2345(2012)03-0005-04
2011-11-18
2012-03-01
张钰哲,硕士,助教,主要从事药代及分子药理学研究.
(责任编辑 毛本勇)

