亲水作用色谱串联质谱同时检测食品接触产品中三聚氰胺和三聚氰酸单体迁移量
吕水源,井 伟,,李小晶,*,江晓芬,刘正才,唐 熙,陈旻实,陈锦权
(1.福建出入境检验检疫局检验检疫技术中心,福建 福州 350001;2.福建农林大学食品科学学院,福建 福州 350002)
亲水作用色谱串联质谱同时检测食品接触产品中三聚氰胺和三聚氰酸单体迁移量
吕水源1,井 伟1,2,李小晶1,*,江晓芬1,刘正才1,唐 熙1,陈旻实1,陈锦权2
(1.福建出入境检验检疫局检验检疫技术中心,福建 福州 350001;2.福建农林大学食品科学学院,福建 福州 350002)
建立一种亲水作用色谱串联质谱技术同时检测食品接触产品中三聚氰胺与三聚氰酸单体迁移量的方法。样品采用水、体积分数4%乙酸溶液、体积分数10%乙醇溶液、异辛烷和橄榄油模拟物进行浸泡。在优化色谱及质谱条件下三聚氰胺和三聚氰酸能很好分离,且分别在1~100ng/mL和2~200ng/mL范围内,峰面积和质量浓度线性关系良好。在50ng/mL添加回收实验结果表明,三聚氰胺和三聚氰酸的平均回收率分别为86.2%~134.0%和78.9%~156.0%,相对标准偏差分别为6.44%~17.93%和5.95%~11.78%。该法简便、快速、准确,可同时测定食品接触产品中三聚氰胺与三聚氰酸单体迁移量。
亲水作用色谱串联质谱;食品接触产品;三聚氰胺;三聚氰酸;迁移
三聚氰胺(melamine,MEL,CAS 108-78-1,C3H6N6)是一种制备塑料,阻燃剂和其他材料的常用化工原料,也是杀虫剂环丙氨嗪在动植物体内代谢产物[1-2]。三聚氰酸(cyanuric acid,CYA,CAS 108-80-5,C3H3N3O3)也是一个重要的工业产品原料,广泛地应用于去污粉、家用漂白剂、工业清洁生产,自动洗碗机清洁粉[3]及游泳池氯稳定剂,防止蒸发和阳光破坏[4]。有研究表明当人体同时摄入三聚氰胺与三聚氰酸时,由于分子间的络合作用,易形成难代谢与分解的大分子化合物[5],其对人体的危害大大于单独摄入某种单体。食品接触产品蜜胺餐具的主要成分为三聚氰胺-甲醛树脂,三聚氰胺易水解为三聚氰酸[6-7],如果生产工艺控制不好,产品中易残留多种单体,接触食品后这些残留单体易迁移到食品中危害健康。
三聚氰胺及三聚氰酸研究在食品领域已有报道[8],但是对于食品接触产品特别是蜜胺餐具中三聚氰胺及其衍生物残留量和迁移量的检测方法报道甚少。Lund等[9]报道了液相色谱-紫外检测器(liquid-chromatographyultraviolet,LC-UV)测定3%乙酸浸泡液中三聚氰胺方法;Wang Xiaoyu等[10]报道了毛细管电泳-质谱联用(capillary elecrot phoresis-mass spectrometry,CE-MS)测定体积分数3%乙酸浸泡液中三聚氰胺及三聚氰酸的方法。本实验建立了以亲水作用色谱串联质谱(hydrophilic interaction chromatography-mass spectrometry/mass spectrometry,HILIC-MS/MS)检测食品接触产品在水、体积分数4%乙酸溶液、体积分数10%乙醇溶液、异辛烷和橄榄油模拟物中三聚氰胺和三聚氰酸迁移量的方法。结果表明,该法简便、快速、准确可靠。
1 材料与方法
1.1 试剂与仪器
三聚氰胺(99.0%)和三聚氰酸(98.0%)标准品 德国Dr.Ehrenstorfer公司;橄榄油(化学纯) 国药集团化学试剂有限公司;乙腈(色谱纯) 德国默克公司;乙酸、乙醇、异辛烷均为国产分析纯,水为超纯水。
三聚氰胺和三聚氰酸混合溶液的制备:分别用水溶解三聚氰胺和三聚氰酸,定容在容量瓶中,质量浓度均为1000mg/L。以体积分数90%乙腈溶液为溶剂配制不同浓度的三聚氰胺和三聚氰酸混合标准工作溶液。
4000Q Trap液相色谱-串联质谱仪(配有电喷雾离子源) 美国Applied Biosystems公司;AB204-L分析天平德国赛多利斯仪器公司。
1.2 样品前处理[11-12]
待测样品用清洁剂洗净,自来水冲洗,晾干,加入一定体积的模拟物浸泡,密闭后置于恒温箱。
对于水基食品模拟物:用水、4%乙酸溶液、10%乙醇溶液,浸泡后,直接吸取所得浸泡液,进过0.45μm微孔滤膜后待测。
对于油基食品模拟物Ⅰ:取橄榄油模拟提取物5.0g于25mL具塞试管中,加入5mL异辛烷,充分混合,再加入5mL体积分数10%异丙醇溶液,70℃水浴振荡30min,离心3min,分层,取下层水层,过0.2μm微孔滤膜后待测。
对于油基食品模拟物Ⅱ:取异辛烷模拟提取物5.0mL于25mL具塞试管中,充分混合,再加入5mL 10%异丙醇溶液,70℃水浴超声30min,离心3min,分层,取下层水层,过0.2μm微孔滤膜后待测。
1.3 LC-MS/MS条件
1.3.1 色谱条件
色谱柱:ZIC-HILIC亲水相互作用色谱柱(150mm×2.1mm,5μm),流动相:10mmol/L乙酸铵溶液及乙腈,梯度洗脱条件见表1。流速:0.40mL/min;柱温:35℃,进样量:1 0μL。
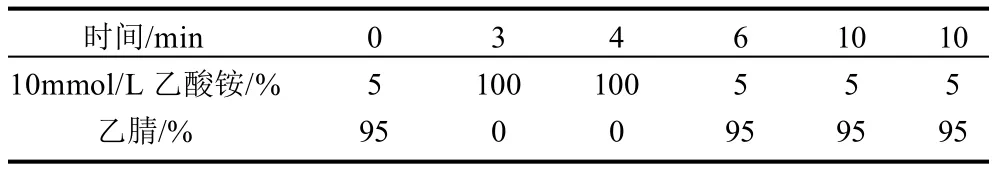
表1 三聚氰胺和三聚氰酸测定的梯度洗脱条件Table 1 Elution conditions for the separation of MEL and CYA
1.3.2 质谱条件
离子源:电喷雾离子源;扫描方式:MEL采用正离子模式,CYA采用负离子模式;多反应监测,电喷雾电压:5000V;气帘气(氮气)压力:0.172MPa;离子源温度:500℃;雾化气压力:0.379MPa;辅助气压力:0.379MPa;其他质谱参数见表2。
2 结果与分析
2.1 液相色谱条件的选择与优化
由于三聚氰胺和三聚氰酸都含有氨基,具有较强的极性和亲水性,因此在传统的C8和C18反相柱上不易保留,且易受样品中其他杂峰干扰。对于极性化合物,亲水作用色谱是一种理想的分离方法[13],在亲水色谱系统中,通过改变有机相和水相的配比实现保留时间的调整。本法以乙酸铵缓冲液作为水相、乙腈作为有机相在梯度洗脱模式下对待测组分进行分离优化。

表2 三聚氰胺和三聚氰酸的主要质谱参数Table 2 MS/MS parameters for MEL and CYA

图1 三聚氰胺(A)和三聚氰酸(B)分离色谱图Fig.1 HPLC profiles of melamine (A) and cyanuric acid (B)
优化色谱条件下在水模拟物中三聚氰胺和三聚氰酸分离色谱图见图1,可看出在优化条件下,三聚氰胺和三聚氰酸可实现基线分离。
2.2 质谱条件优化
用以流动注射方式将50mg/L三聚氰胺与三聚氰酸标准溶液注入电喷雾质谱,分别在正、负离子模式下进行母离子全扫描,得到三聚氰胺与三聚氰酸的一级质谱。三聚氰胺正离子模式的离子峰强度比负离子峰强度高3个数量级,而三聚氰酸负离子模式离子峰强度比正离子峰强度高。三聚氰酸的强吸电子基团使其在负离子模式下具有更好的灵敏度,因此选择正离子模式检测三聚氰胺,负离子模式检测三聚氰酸,三聚氰胺的准分子离子为m/z127.1,三聚氰酸为m/z128.0。
以m/z127.1为母离子作三聚氰胺二级质谱,以m/z128.0为母离子作三聚氰酸二级质谱,并进行质谱条件优化。分别对电喷雾电压2000~5500V,去簇电压30~100V,入口电压5~20V,碰撞池出口电压5~20V,碰撞气能量10~20V范围的各质谱参数进行优化,得到的优化质谱条件见表2。三聚氰胺与三聚氰酸的二级质谱图见图2。三聚氰胺主要碎片离子为m/z85.0和m/z68.0,其强度比为2:1,以二级质谱碎片离子m/z85.0和m/z68.0及其强度比作定性确证,提取m/z68.0、85.0、127.1三个离子质量色谱峰面积作三聚氰胺定量分析;三聚氰酸主要碎片离子为m/z42.0和m/z85.0,其强度比为3:2,以二级质谱碎片离子m/z42.0和m/z85.0及其强度比作定性确证,提取m/z42.0、85.0、128.0三个离子质量色谱峰面积作三聚氰酸定量分析。

图2 标准品三聚氰胺ESI+(A)和三聚氰酸ESI-(B)质谱图Fig.2 ESI+ MS mass spectrum of melamine
2.3 方法的线性范围及检出限
在本法确定的实验条件下,分别以浸泡液逐级稀释成标准系列质量浓度进行测定,以定量离子的响应峰面积(Y)对相应组分的质量浓度(X)/(ng/mL)作图,分别得到三聚氰胺和三聚氰酸检测限、线性范围、相关系数和线性方程见表3。结果表明三聚氰胺在1~100ng/mL、三聚氰酸在2~200ng/mL范围内定量离子的响应峰面积和样品质量浓度之间有很好的线性关系。
选择不含MEL和CYA的密胺碗,按照上述实验步骤进行测定,得到20个空白样品的质谱图,按照3倍信噪比计算对应目标组分的检测限,10倍信噪比计算对应目标组分的定量限,结果见表3。
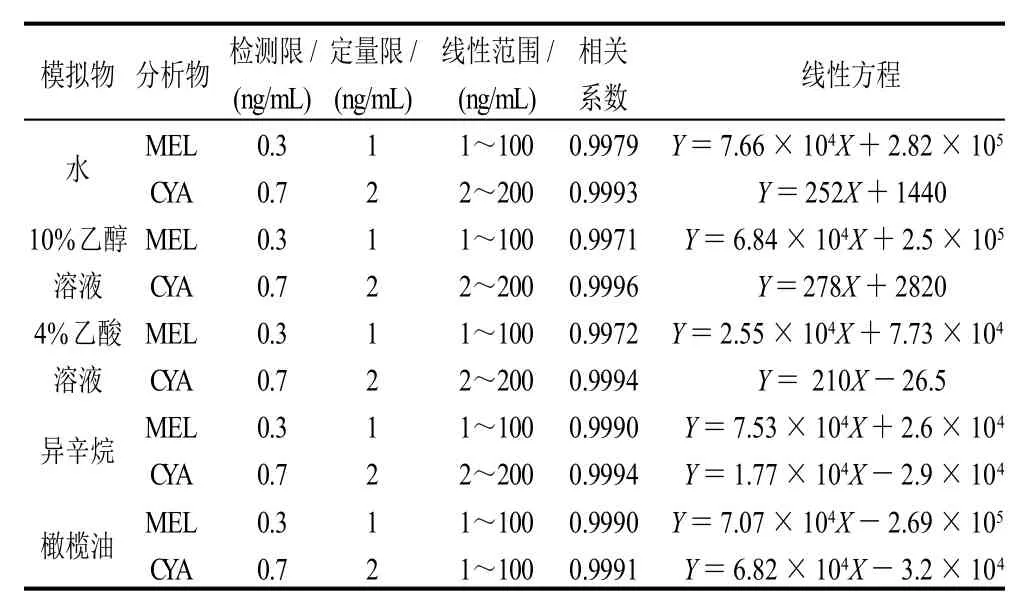
表3 不同模拟物中三聚氰胺和三聚氰酸检测限及线性方程Table 3 LOD, linear ranges, correlation coefficients and linear equations of melamine and cyanuric acid in different stimulant solutions
2.4 回收率和精密度
选取自制空白密胺碗,在水、4%乙酸溶液、10%乙醇溶液浸泡液中分别添加50ng/mL三聚氰胺和三聚氰酸标准溶液,平行测定6次考察方法的回收率。该方法中三聚氰胺和三聚氰酸的平均回收率分别为86.2%~134.0%和78.9%~156.0%,相对标准偏差分别为6.44%~17.93%和5.95%~11.78%,表明所建立的该方法重复性好。
在水、4%乙酸溶液、10%乙醇溶液、异辛烷和橄榄油浸泡自制密胺碗和密胺盘,浸泡液处理后,按建立的方法检测,平行测定6次考察方法的精密度,结果见表4。密胺餐具在5种模拟液测定结果都具有良好的重复性,相对标准偏差均在5.69%范围之内。

表4 不同模拟物中测定实际样品中的三聚氰胺和三聚氰酸单体迁移量Table 4 Migration amounts of melamine and cyanuric acid in different stimulant solutions determined by the HILC-MS/MS method
2.6 样品测定
市售密胺餐具50个,采用建立的浸泡和检测方法对密胺餐具中三聚氰胺和三聚氰酸迁移量进行检测,结果表明,其中有4个样品检出三聚氰胺,检出范围为0.27~2.07μg/mL,三聚氰酸均未检出。
3 结 论
本实验建立用亲水作用色谱串联质谱联用技术同时检测食品接触产品中三聚氰胺与三聚氰酸单体迁移量的方法,样品浸泡液无需前处理,使用高效液相色谱分离后串联质谱仪测定,方法有机溶剂用量少、操作简单、灵敏度高,检测限低,前处理简单,满足FDA、欧盟、国标等法规限量的检测需求,适用于食品接触产品中三聚氰胺与三聚氰酸的检测。有关食品接触产品中三聚氰胺及三聚氰酸的系统性风险评估将在后续工作中展开。
[1] CARBAS P, MELONI M, SPANEEDDA L. High-performance liquid chromatographic separation of cyromazine and its metabolite melamine[J]. Journal of Chromatography, 1990, 505(2): 413-416.
[2] LORI O L, SUSAN J S, KENNETH D S, et al. Disposition of cyromazine in plants under environmental conditions[J]. J Agric Food Chem, 1990,38(3): 860-864.
[3] KIRK O. Encyclopedia of chemical technology[M]. 4th. New York :John Wiley & Sons, 1993: 834-851.
[4] KOWALSKY L. Certified pool-SPA operator[M]. Taxas: National Swimming Pool Fundation, 1992: 46.
[5] World Health Organization (WHO). Expert meeting to review toxicological aspects of melamine and cyanuricacid [EB/OL]. (2008-11-01)h t t p://ww w.wh o.i n t/fo o d sa fe t y/f s_ma n a g e me n t/conclusions_recommendations.pdf
[6] JUTZIK, COOK A M, HUTTER R. The degradative pathway of the striazine melamine. The steps to ring cleavage[J]. Biochemistry Journal,1982, 208(3): 679-684.
[7] SHELTON D R, KARNS J S, MCCARTY G W, et al. Metabolism of melamine byKlebsiella terragena[J]. Applied Environmental Microbiology, 1997, 63(7): 2832-2835.
[8] 李锋格, 姚伟琴, 苏敏, 等. 气相色谱-质谱法快速测定牛奶中的三聚氰胺和三聚氰酸[J]. 色谱, 2009, 27(2): 233-236.
[9] LUND K H, PETERSEN J H. Migration of formaldehyde and melamine monomers from kitchen-and tableware made of melamine plastic[J].Food Additives and Contaminants, 2006, 23(9): 948-955.
[10] WANG Xiaoyu, CHEN Yi. Determination of aromatic amines in food products and composite food packaging bags by capillary electrophoresis coupled with transient isotachophoretic stacking[J]. Journal of Chromatography A, 2009, 1216(43): 7324-7328.
[11] 井伟, 唐熙, 吕水源, 等. LC-ESI MS/MS测定蜜胺餐具中三聚氰胺的迁移量[J]. 分析测试学报, 2011, 30(3): 269-273.
[12] 井伟, 陈旻实, 李小晶, 等. HPLC同时检测食品接触材料中三聚氰胺与三聚氰酸单体迁移量[J]. 分析试验室, 2011, 30(4): 34-38.
[13] ANDERSEN W C, TURNIPSEED S B, KARBIWNYK C M, et al.Determination and confirmation of melamine residues in catfish, trout,tilapia, salmon, and shrimp by liquid chromatography with tandem mass spectrometry[J]. J Agric Food Chem, 2008, 56(12): 4340-4347.
Simultaneous Determination of Melamine and Cyanuric Acid in Food Contact Packaging Materials by Hydrophilic Liquid Chromatography-Tandem Mass Spectrometry
An HILC-MS/MS method was developed to simultaneously determine melamine and cyanuric acid in food contact packaging materials. Samples were extracted with H2O, 4% acetic acid (V/V), 10% ethanol isooctane (V/V) and olive oil separately,kept in a 70 ℃ incubator for 2 h and then filtered through a 0.2 μm microporous membrane prior to injection into an HILC-MS/MS system. Melamine and cyanuric acid were separated, identified and quantified on HILC column by gradient mobile phase and monitored in a positive/negative electrospray ionization and multiple reaction monitor (MRM) mode. A good linear range was achieved over the concentration range of 1-100 ng/mL and 2-200 ng/mL for melamine and cyanuric acid in different stimulants, respectively. The limits of detection and limits of quantification were in the range of 0.4-0.8 ng/mL. The recovery rates of melamine and cyanuric acid were 134.0%-86.2% and 156.0%-78.9% with RSDs of 6.44%-17.93% and 5.95%-11.78%. This method was simple, rapid, and accurate, and suitable for the determination of melamine and cyacuric acid in food contact packaging materials.
HILC-MS/MS;food contact packaging materials;melamine;cyanuric acid;migration
O658
A
1002-6630(2012)16-0159-04
2011-06-01
福建省科技计划重点项目(2009Y0001);国家质量监督检验检疫总局2011年度科技计划项目;福建出入境检验检疫局科技计划项目(FK2010-22)
吕水源(1975—),男,高级工程师,学士,主要从事消费品安全研究。E-mail:lsy75@126.com
*通信作者:李小晶(1976—),女,高级工程师,博士,主要从事消费品安全研究。E-mail:lxjciq@hotmail.com

