碳纳米管CNT(5,5)内环氧乙烷的阴离子聚合机理
陈晋忠,明瑞豪,吴 静,王罗新
碳纳米管CNT(5,5)内环氧乙烷的阴离子聚合机理
陈晋忠,明瑞豪,吴 静,王罗新*
(武汉纺织大学 材料科学与工程学院,湖北 武汉 430073)
采用B3LYP/6-311++G**和ONIOM(B3LYP/6-311++G**:UFF)方法分别对环氧乙烷非受限状态以及在单壁碳纳米管CNT(5,5)内的阴离子聚合反应进行计算。结果表明,环氧乙烷与其亲核试剂(OH-)进攻产物形成的复合物进入CNT(5,5)碳纳米管内是一个放热过程,说明反应复合物进入CNT(5,5)形成包结物在能量上是有利的。由于碳纳米管的限制作用,环氧乙烷阴离子聚合的反应物、过渡态以及产物的结构与非受限状体下有所不同,在碳纳米管内的反应过程中分子构型会发生一定的扭转,以适应碳纳米管内的空间限制。与非受限状相比,环氧乙烷阴离子聚合反应的活化能垒增加了13.2 kcal/mol,表明碳纳米管CNT(5,5)对环氧乙烷阴离子聚合反应起到一定的抑制作用。
碳纳米管;环氧乙烷;受限作用;阴离子聚合
纳米管 (carbon nanotube, CNT) 是1991年被发现的一种具有准一维管状结构的纳米材料[1],其独特的物理和化学性质以及广泛的应用前景使其成为纳米科技领域的一个研究热点[2~5]。碳纳米管的空腔是真正意义上的微纳米反应器,可以改变处于其内部的分子性质和化学活性。理论计算表明[6,7],碳纳米管的空腔对SN2反应有重要影响,是抑制还是促进SN2反应与反应物种有关。我们的研究也发现,碳纳米管对一些分子的热解反应亦会产生显著影响,这种影响与碳纳米管的尺寸有关联[8,9]。
有关碳纳米管与高分子的相互作用研究较多,但研究碳纳米管内的聚合反应迄今较少报道。本文以环氧乙烷的阴离子开环聚合反应为模型,研究其在CNT(5,5)碳纳米管内的阴离子聚合反应机理。环氧化物的阴离子开环聚合可以用氢氧化物、醇盐、金属氧化物、金属有机化合物或其他阴离子活性物来引发。本文以-OH作为环氧乙烷的引发剂,研究环氧乙烷在CNT(5,5)碳纳米管内发生聚合的反应物、过渡态以及产物的结构与能量变化,讨论了碳纳米管CNT(5,5)对环氧乙烷阴离子开环聚合的影响。
1 计算方法
组合的量子化学ONIOM 方法广泛用于研究与碳纳米管相关的化学反应体系,该方法是将所研究的体系可以分为两层或三层,分别用不同的化学模型处理。分层ONIOM方法的优点是既保证了所研究化学问题的计算精度,同时也可以提高计算效率。本文中将环氧乙烷与碳纳米管形成的包结物分为两层来处理:内层为环氧乙烷,采用高水平的密度泛函理论B3LYP 方法进行计算;外层为碳纳米管, 采用分子力学 UFF(universal force field) 力场处理。密度泛函理论结合UFF分子力学方法在有关碳纳米管内的化学反应研究中已有许多成功的应用[10-12 ]。计算选取的CNT(5,5)碳纳米管两端的悬键用氢原子进行饱和。环氧乙烷的反应物与CNT(5,5)碳纳米管形成的包结物记为@CNT(5,5),其余体系的表示方法类似,所有计算采用 Gaussian 03软件包[13]完成。
2 结果与讨论
2.1 环氧乙烷阴离子聚合的分子结构分析
环氧乙烷在亲核试剂或亲电试剂的作用下发生均聚反应,这方面的理论研究已有报道。运用密度泛函方法,张治国等[4]计算了环氧乙烷的聚合反应过程, 他们认为环氧乙烷的基态分子不能发生均聚,只有当环氧乙烷基态分子被亲电试剂或亲核试剂进攻后,才能进一步引发环氧乙烷均聚。我们采用B3LYP/6- 311++G**方法,对环氧乙烷在羟基引发下发生均聚反应的反应物、产物以及过渡态分子结构进行了优化,其中环氧乙烷分子标记为EO,亲核试剂羟基进攻环氧乙烷的产物标记为EO-OH-,两者形成的复合物标记为R(EO-EO-OH-),聚合反应的过渡态标记为TS(EO-EO-OH-),产物标记为P(EO-EO-OH-),优化得到的分子结构参数如图1所示。从分子结构来看,图1给出的优化结构与文献结果非常一致[14],表明我们采用B3LYP/6-311++G**方法进行计算是合理的。

EO EO-OH-R(EO-EO-OH-)TS(EO-EO-OH-)P(EO-EO-OH-)
图2-图4分别给出了环氧乙烷在羟基引发下于CNT(5,5)内发生均聚反应的反应物、过渡态以及产物的分子结构,分别标记为R(EO-EO-OH-)@CNT(5,5)、TS(EO-EO-OH-)@CNT(5,5)和P(EO-EO-OH-)@CNT(5,5)。与图1所示的结构参数相比,可以看出碳纳米管对环氧乙烷聚合过程中的分子结构有一定影响。例如,与非受限状态相比,受限于碳纳米管内的反应复合物R(EO-EO-OH-)@CNT(5,5)的O4—C5键缩短了0.0105nm,C3O4C5键角压缩了39.3°,O4C5C6键角扩张了52.9°。另一个变化是二面角O4C5C6O7由121.5°变为-115.0°,表明受碳纳米管的影响,EO-OH-进攻环氧乙烷EO时,分子结构要做一定旋转调整,以适应CNT(5,5)的空间限制。就聚合反应的过渡态而言,碳纳米管的限制作用亦影响到分子结构。对比图3和图1中的TS(EO-EO-OH-)可以看出,尽管受限于碳纳米管内的过渡态TS(EO-EO-OH-)的O4—C5键变化不明显,但C3O4C5键角压缩了12.8°,另一个显著变化是二面角C2O4C5C6由-76.4°变为-173.1°,而C5—O7键长由0.1773nm增加到0.1814nm。 图4所示的P(EO-EO-OH-)@CNT(5,5)结构中,O4—C5键的键长为0.1468 nm,比非受限状态0.1457 nm有所增长。此外,非受限状态下,C3O4C5C6二面角为-71.9°,表明C3O4C5C6原子排列可以成为顺式结构,而在碳纳米管内,C3O4C5C6二面角为-179.9°,此时C3O4C5C6原子排列为反式结构。我们以不同初始结构出发均不能优化出C3O4C5C6原子排列为顺式结构的产物,表明受碳纳米管CNT(5,5)的影响,O4和C5原子连接成键时,通过分子键的旋转,最终聚合物分子结构会成为规整的反式结构。


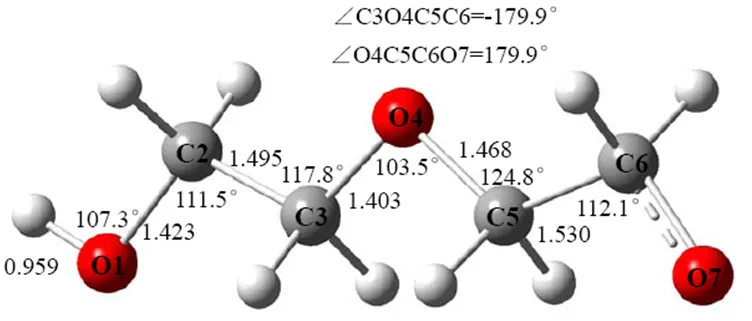
图4 受限于CNT(5,5)碳纳米管内环氧乙烷阴离子聚合反应的产物分子结构(键长:Ǻ;健角:度)
2.2 环氧乙烷阴离子聚合的能量分析
采用ONIOM(B3LYP/6-311++G**:UFF) 方法,计算环氧乙烷在碳纳米管内发生阴离子聚合反应的能量,表1给出了对应的反应物、过渡态、产物的能量值。作为比较,采用B3LYP/6-311++G**方法计算的环氧乙烷在非受限状态下的反应物种能量也列于表中。已有的研究结果表明,羟基进攻环氧乙烷生成阴离子产物EO-OH-为无能垒的放热过程,可自发进行[14]。当EO-OH-进攻环氧乙烷时,首先形成复合物R(EO-EO-OH-),进一步的反应要经历过渡态TS(EO-EO-OH-),此时所需克服的活化能垒为8.0 kcal/mol,这一计算结果与文献报道值非常一致。此外,计算的产物P(EO-EO-OH-)相对于R(EO-EO-OH-)的能量为-14.9 kcal/mol,表明反应为放热过程。
对于复合物R(EO-EO-OH-)在CNT(5.5)碳纳米管内的聚合反应,我们首先要考虑该复合物能否自由进入碳纳米管内。从表1中可以看出,EO-EO-OH-与CNT(5,5)的能量之和比R(EO-EO-OH-)@CNT(5,5)的能量高出69.5 kcal/mol,即环氧乙烷复合物进入碳纳米管是一个放热过程,这说明环氧乙烷复合物进入CNT(5,5)碳纳米管在能量上是有利的。相对于R(EO-EO-OH-)@CNT(5,5),聚合反应的过渡态能量为21.2 kcal/mol,与非受限状态相比升高了13.2 kcal/mol,表明碳纳米管CNT (5,5)抑制环氧乙烷阴离子聚合。
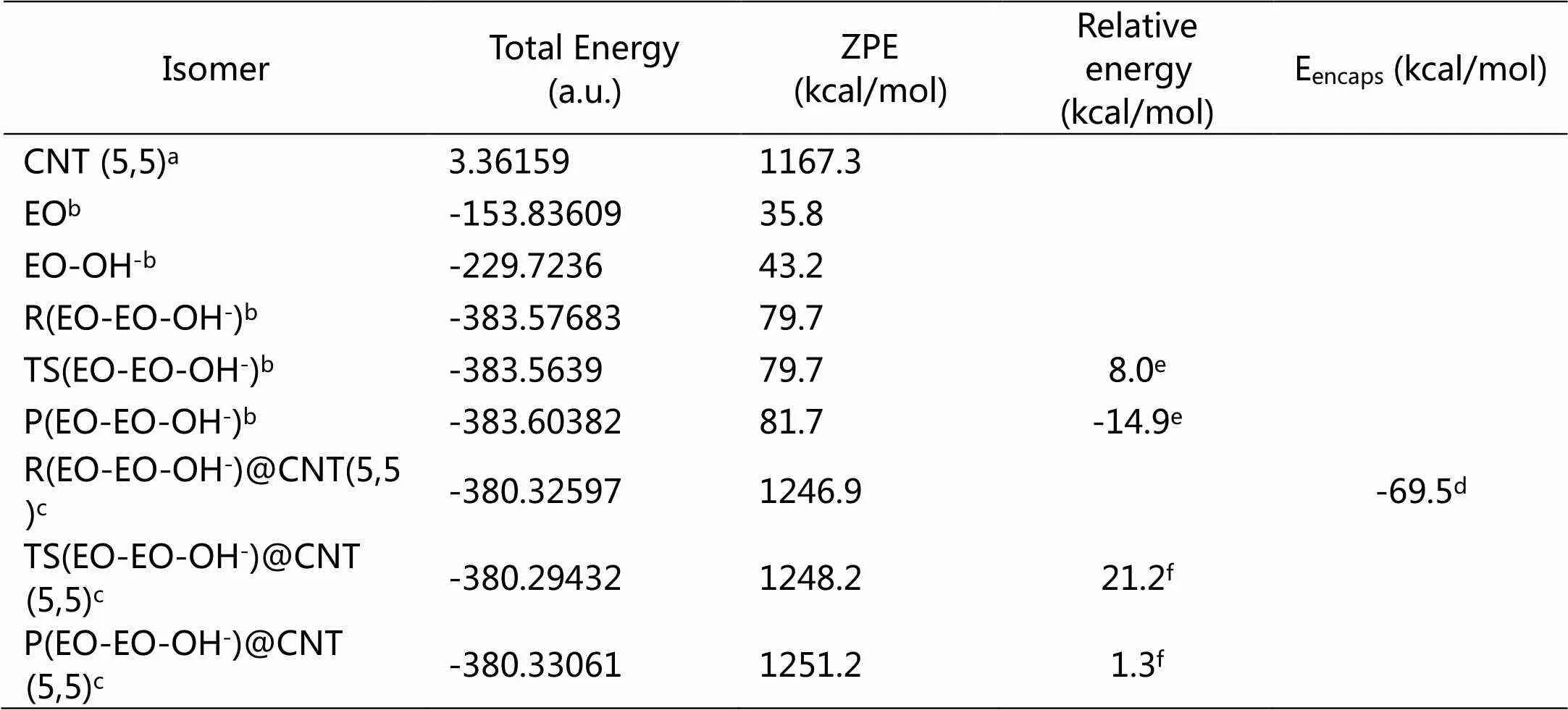
表1 环氧乙烷阴离子聚合反应物种的能量
注:a: calculated at the UFF force field. b: calculated at the B3LYP/6-311++G** level of theory.c: calculated at the ONIOM(B3LYP/6-311++G**:UFF) level of theory. d: Eencaps= ER(EO-EO-OH-)@CNT(5,5)+ ZPER(EO-EO-OH-)@CNT(5,5)- ER(EO-EO-OH-)- ZPER(EO-EO-OH-)- ECNT(5,5)- ZPECNT(5,5).e: relative to the energy of R(EO-EO-OH-) f: relative to the energy of R(EO-EO-OH-)@CNT(5,5)
结合前面的能量计算,受限于碳纳米管内与非受限下的环氧乙烷阴离子聚合的能量变化如图5所示。很明显,碳纳米管的限制作用对环氧乙烷的阴离子聚合反应有显著影响,尽管环氧乙烷的聚合反应物可以进入CNT (5,5)碳纳米管内,但碳纳米管在一定程度上抑制了聚合反应。此外,产物的能量也受到了碳纳米管的影响,非受限状态下,从反应物R(EO-EO-OH-)到产物P(EO-EO-OH-),反应放出14.9 kmol/mol的能量,而在碳纳米管内的该步反应要吸收1.3 kmol/mol的能量。

图5 环氧乙烷阴离子聚合反应的能量图
Halls 等对受限于碳纳米管内的Cl+H3CCl 反应进行了计算,也发现与非受限环境下相比,CNT(6,6)碳纳米管可以将该反应的活化能垒提高高6.6 kcal/mol[7],他们认为碳纳米管空腔内部存在一定的极性,可能对极性分子参与的反应产生影响,并据此提出了碳纳米管空腔可以看作一维“固体溶剂”的理论。这一理论可以解释CNT (5,5)碳纳米管对环氧乙烷阴离子聚合反应的影响。然而,应该看到,碳纳米管并不是导致所有的反应活化能垒上升,例如,CNT(8,0)和CNT(9,0)碳纳米管可以将H3N+H3CCl 反应的活化能垒分别降低13和12 kcal/mol[6]。因此,鉴于碳纳米管的独特性能,目前并不能排除碳纳米管的其它一些效应引起环氧乙烷阴离子聚合反应能量的变化,这还需要更深入的研究。
3 结论
理论计算表明, 环氧乙烷阴离子聚合反应复合物进入CNT(5,5)碳纳米管内是一个放热过程。与非受限状态相比,档EO-OH-进攻环氧乙烷EO时,碳纳米管内的环氧乙烷复合物构型发生一定扭转,以适应CNT(5,5)的空间限制,最终产物的构型为全反式结构。碳纳米管的限制效应导致环氧乙烷在管内聚合的过渡态能量增加了13.2 kcal/mol。此外,CNT(5,5)碳纳米管对环氧乙烷阴离子聚合产物的能量亦产生一定影响。
[1] Iijima S. Synthesis of carbon nanotubes [J]. Nature, 1991, 345: 56-58.
[2] Qi Li, Lijie Dong, Jingfei Fang, and Chuanxi Xiong. Property-Structure Relationship of Nanoscale Ionic Materials Based on Multiwalled Carbon Nanotubes[J]. ACS Nano, 2010, 4 (10): 5797-5806.
[3] Lei Y, Xiong C, Dong L, et al. Ionic Liquid of Ultra-long Carbon Nanotubes[J]. Small, 2007, 3(11): 1889-1893.
[4] Lei Y, Xiong C*, Guo H, et al. Controlled Viscoelastic Carbon Nanotube Fluids[J]. J Am. Chem. Soc., 2008, 130: 3256-3257.
[5] Charlier J C, Limbin P H. Electronic structure of carbon nanotubes with chiral symmetry [J]. Phys Rev B, 1998, 57(24): 15037-15039.
[6] Halls M D, Bernhare S H. Chemical inside carbon nanotubes: The menshutkin SN2 reaction [J]. J Phys Chem B, 2002, 106(37): 1921-1925.
[7] Halls M D, Raghavachari K. Carbon nanotube inner phase chemistry: The Cl− exchange SN2 reaction [J]. Nano Lett, 2005, 5(10): 1861-1866.
[8] 王罗新,许杰,邹汉涛,等.手性和尺寸对受限于单壁碳纳米管内的硝基甲烷热解反应的影响[J].物理化学学报, 2010,26(03):721-726.
[9] Luoxin Wang, Changhai Yi, Hantao Zou, et al. On the isomerization and dissociation of nitramide encapsulated inside an armchair (5,5) single-walled carbon nanotube[J]. Materials Chemistry and Physics, 2011, 127: 232-237.
[10]Luoxin Wang, Changhai Yi, Hantao Zou, Houlei Gan, Jie Xu, Weilin Xu, Adsorption of insensitive explosive TATB on single-walled carbon nanotubes[J]. Molecular Physics, 2011, 109: 1841-1849.
[11]Liu, L. V.; Tian, W. Q.; Wang, Y. A. J. Adsorption of Small Gas Molecules onto Pt-Doped Single-Walled Carbon Nanotubes [J]. J. Phys. Chem. B, 2006, 110:1999.
[12]Basiuk, V. A. J. Side‐Wall Opening of Single‐Walled Carbon Nanotubes (SWCNTs) by Chemical Modification: A Critical Theoretical Study [J]. J. Phys. Chem. B, 2003, 107: 8890
[13]Frisch, M. J.; Trucks, G. W.; Schlegel, H. B.; et al. Gaussian 03.Revision E.01[M]. Wallingford, CT: Gaussian Inc., 2005.
[14]张治国, 尹 红, 陈志荣.环氧乙烷均聚反应机理的理论研究[J].化学学报, 2004, 62(20): 1988-1992.
Anionic Polymerization Mechanism of Ethylene Oxide within CNT(5,5)
CHEN Jin-Zhong, MING Rui-hao, WU Jing, WANG Luo-Xin
(School of Materials Science and Engineering, Wuhan Textile University, Wuhan Hubei 430073, China)
Anionic polymerization mechanism of ethylene oxide (EO) confined inside a single-walled carbon nanotube, CNT(5,5), was calculated at the ONIOM(B3LYP/6-311++G**:UFF) level of theory. Meanwhile, the polymerization of EO in the isolated state was also calculated at the B3LYP/6-311++G** method. We found that the encapsulation process was exothermic and favored in energy when the complex, which was formed by the EO and the EO/nucleophile (OH-) adduct, was entranced into CNT(5,5). Due to the confinement of CNT(5,5), the geometric parameters of reactant, transition state and product within nanotube were different from the corresponding parameters in the isolated state. During the reaction process of EO complex inside nanotube, rotation of the molecular configuration occurred for the EO complex in order to adapt to the inner space of nanotube. The energy calculation showed that the activation energy of the anionic polymerization within nanotube was 13.2 kcal/mol higher than the value in the case of the isolated state, which suggested that that the anionic polymerization of ethylene oxide was inhibited by the confinement in CNT(5,5).
Carbon Nanotube; Ethylene Oxide; Confinement Effect; Anionic Polymerization
O641.12+1
A
1009-5160(2012)03-0030-04
湖北省教育厅科学研究计划项目资助(Z20101601).
*通讯作者:王罗新(1971-),副教授,研究方向:纺织新材料、功能高分子.

