离子液体的非常规制备技术研究进展
李 臻,陈 静,夏春谷
(中国科学院兰州化学物理研究所羰基合成与选择氧化国家重点实验室,甘肃 兰州 730000)
特约评述
离子液体的非常规制备技术研究进展
李 臻,陈 静,夏春谷
(中国科学院兰州化学物理研究所羰基合成与选择氧化国家重点实验室,甘肃 兰州 730000)
离子液体的大规模应用有赖于其制备技术的不断进步。然而,常规制备方法反应时间长、产品纯化繁琐、不宜规模化等问题,制约着离子液体的工业化应用进程。针对离子液体制备过程的关键环节,综述了目前离子液体非常规制备技术的研究进展,重点介绍了微波、超声波、微波-超声、微反应和STT过程强化制备离子液体的技术研究现状,指出现阶段虽然非常规制备技术取得了重要进展,但是仍然需要通过深入细致的研究,建立完善的理论指导体系,同时还要加快功能化离子液体和绿色化制备技术开发。
离子液体;非常规技术;微波辅助;超声波;微反应工艺
1914年,在文献[1]中描述了在12 ℃熔融的乙基硝酸铵,这是有关离子液体的最初报道。20世纪40年代,Frank Hurley和Tom Wier在寻找一种温和条件电解Al2O3时,将N-烷基吡啶加入AlCl3中,加热试管后,发现两固体的混合物自发地形成清澈透明的液体,这就是今天所说的室温离子液体[2-5]。虽然这一现象在当时并没有引起人们的注意,但是此后的研究表明,在这样一个偶然的条件下发现的室温离子液体不仅给化学研究提供了一个全新的领域,而且有望对面临污染、安全等重要问题的现代工业带来突破性进展。参阅已有的文献,可以将室温离子液体(room temperature ionic liquid, RTIL,简称为离子液体)定义为在室温或接近常温时呈液态的,完全由有机阳离子与无机或有机阴离子组成的盐。离子液体拥有液态温度范围广、蒸气压极低、溶解性好、电化学窗口宽、热稳定性和抗氧化性高等优点,并且离子液体的组成和性质具有较大的可调控性[6-7]。这些其它液体无法比拟的性质给大部分传统化学化工过程提供了新的思路和改造的空间,使其在当今化学工程的绿色化进程中显示了巨大的潜力和应用前景,也成为推动离子液体研究不断向前发展的动力之一[8-10]。
离子液体种类繁多,通过调变阳离子或阴离子的结构,以及改变阳离子、阴离子的不同组合,可以设计并合成出不同的离子液体。迄今为止,已合成的离子液体达到数百种,在很多领域的研究和应用受到了广泛关注。离子液体的制备技术是离子液体研究的重要方向之一,是将离子液体推向实际应用的关键环节。鉴于此,多种非常规制备技术已经被用于离子液体的规模化制备。本文将重点介绍近年来在离子液体非常规制备技术方面取得的进展。
1 常规制备方法存在的问题
结构简单的离子液体的典型制备过程包括直接合成法和两步合成法。如图1中步骤1所示,直接合成法主要通过酸碱中和反应或季铵化反应一步合成离子液体。如乙基硝酸铵[1]、氯化(或溴化)1-丁基-3-甲基咪唑[11-12]和氯化(或溴化)N-丁基吡啶[13-15]的合成均采用此方法。两步合成法即是首先通过步骤1的季铵化反应制备出含目标阳离子的卤盐,然后在步骤2中用目标阴离子置换卤素阴离子,或加入Lew is 酸来得到目标离子液体[16-19]。通过两步合成法可以获得更为多样的离子液体,然而此方法制备的离子液体必须确保阴离子置换完全,否则即使残留少量的卤素阴离子也会对最终产品的物理化学性质和应用产生极大的影响。在步骤 2中,利用离子交换树脂通过阴离子交换是获得高纯度离子液体的有效方法。
多数离子液体的合成是强放热反应,而离子液体通常黏度较大,为及时散热和增强传质,可采取使用有机溶剂、卤代烃过量等措施,不仅合成反应周期长,而且产物提纯难,产率也不高。最近,Deetlefs和 Seddon在新书《Green Solvents》中就离子液体制备过程的绿色化作了详细的评述[20]。他们认为传统加热回流的方式制备离子液体并非环境友好的绿色过程,并且不可避免地带来离子液体纯化过程的非绿色化。通过对离子液体制备和纯化过程的SWOT分析,可以发现离子液体制备方法存在进一步改善的空间(图2)[21]。
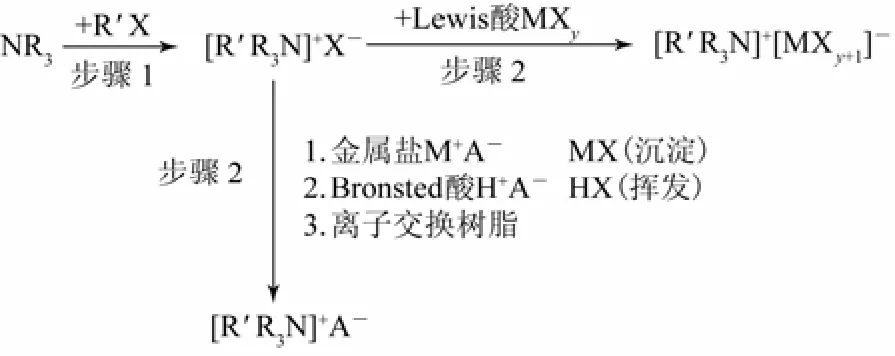
图1 直接法和两步法合成离子液体
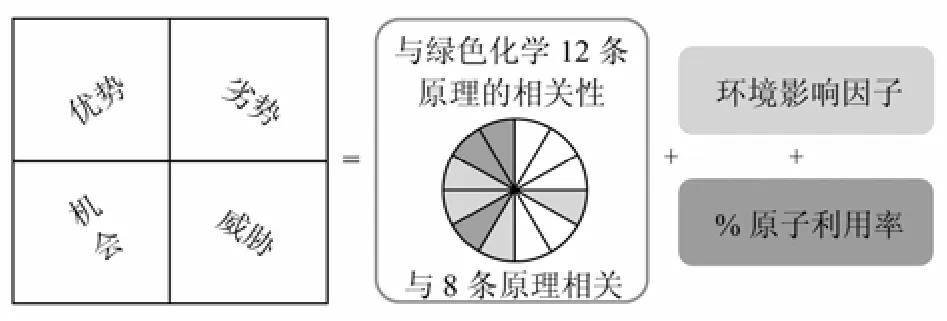
图2 离子液体制备过程的绿色化评估[21]
2 非常规制备技术
微波[22]和超声波[23]辅助的有机合成方法产生于20世纪80年代,目前这两种非常规技术在实验室以及工业界被广为应用。离子液体完全由离子组成,能够有效地吸收微波能量,离子液体作为非常规介质在微波/超声辅助的化学反应中获得了成功应用。因此,“非常规技术”与“非常规介质”的协同作用为寻求更为高效经济且环境友好的离子液体制备技术提供了可能[24]。
2.1 微波辅助制备离子液体
微波是一种强电磁波,在微波照射下能产生热力学方法得不到的高能态原子、分子和离子,可以迅速增加反应体系中自由基或碳阳离子的浓度。从能量角度分析,只要能瞬间提高反应物分子的能量,使体系中活化分子增加,就有可能增加反应速率,缩短反应时间,最大限度地提高原料利用率。由于这些优点契合绿色化学的基本思想,微波辅助的有机合成近年来逐渐引起人们的关注并得到广泛发展。
Varma等[25-26]最先报道了在家用微波炉中卤化1,3-二烷基咪唑类离子液体的无溶剂合成,不但极大地缩短了合成反应的时间,而且避免了使用过量的底物和有机溶剂。家用微波炉的微波能量分布不均,温度和压力均不可控,致使合成反应的结果重现性很差。在无溶剂条件下,即使是合成极少量的离子液体(1~2 mmol)也容易因为过热使反应失控,甚至引起微波系统的损坏,操作安全性不能保障。Chan等[27]利用水的比热容较大、可以有效转移过多热量的特点,采用水浴的方式控制反应温度,可以在较为温和的条件下实现无溶剂体系卤素阴离子离子液体的合成,制备量达到 0.3~2.0 mol,这是微波辅助制备较大量离子液体的初次尝试。通过改进的方法虽然提高了反应的安全性与稳定性,但是操作较为复杂,而且敞开体系并不适合大批量离子液体的一次性制备。
为适应大批量离子液体制备的需要,多种适合实验室应用的微波合成装置相继问世。例如CEM、M ilestone、Biotage 等公司都生产专用的微波合成系统。图3所示的这些微波设备具有温度、压力可调的特性,不仅增强了操作的安全性,还保证了批次合成结果的重现性[28]。Seddon等[29]研究了使用CEM公司专业的微波合成设备制备卤化烷基咪唑类和烷基吡啶类离子液体的过程,微波功率可根据原料卤代烷烃的反应活性进行设定,制备量达到0.15~0.3 mol。表 1 列出了微波合成离子液体的条件和产率,可以看出咪唑类离子液体的合成速率较吡啶类的快,对于卤代烃而言,其快慢顺序为碘代>溴代>氯代。Khadilkar等[30]使用相同的微波合成设备开展了含卤素阴离子的离子液体合成研究,对于 [C4mim]Cl,在相同的条件下两个研究组的收率分别为 96% 和 91%(表1,序号1和序号2)。对于[C4Py]Cl,在不同的条件下收率分别为 90%和66%,显然 200 ℃左右的高温不利于 [C4Py]Cl的合成(表1,序号5和序号6)。随着微波技术的快速发展,微波合成的规模也从批次制备发展到可以连续化制备。2008年,Erdmenger等[31]采用微波辅助连续流动法制备[Bm im]Cl离子液体,通过优化反应条件,制备量达到了约460 g/h。

图3 专用微波合成设备
阴离子交换是获得不同阴离子离子液体的重要步骤,2002年,Varma和Namboodiri首次报道了微波辅助合成阴离子为四氟硼酸根的1,3-二烷基咪唑离子液体,通过优化合成反应条件,可以获得 91%的收率(表2,序号1)[32]。2005年,Singh等[33]报道了另一例非卤素阴离子离子液体[C4m im][HSO4]的微波辅助制备过程(表2,序号2),并将制备的离子液体成功用于催化香豆素的合成。微波辅助的离子交换反应不但速率快,而且交换完全,离子液体收率高。该方法也被成功用于Lew is酸性离子液体的制备,如表2中所列的[C4m im][A lCl4][34]、[C4mim][InCl4][35]和[C4mim][GaCl4][36]。
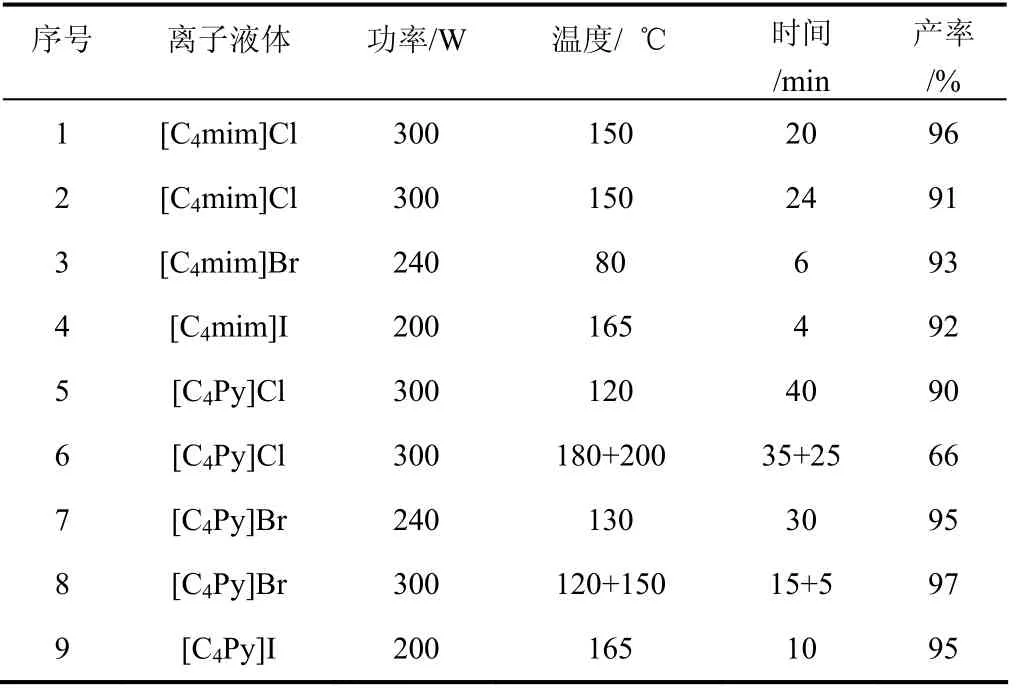
表1 微波合成卤素阴离子离子液体的条件及产物收率

表2 微波辅助合成非卤素阴离子离子液体和Lewis酸性离子液体
2006年,Pal和Kumar借助微波技术制备了常规方法难于合成的离子型化合物,如图4所示。这些新颖的咪唑基离子液体液晶化合物在较宽的温度范围内具有介晶态[37],此研究为多种结构新颖、功能独特的离子液体合成提供了新思路。
离子液体的纯度是评价其性质和应用的重要指标,Kärkkäinen等[38]的研究表明,即使采用专用的微波合成仪,为了获得高纯度的离子液体,必须对温度和反应时间进行严格控制。对于[C4mim]Cl,最佳的合成温度为 130 ℃,[C4m im]PF6和[C4mim] DCA则为 80 ℃。此外,Kärkkäinen指出,ESI-MS(电喷雾质谱)技术和NMR表征技术的结合,可以实现对离子液体纯度的监控。
从廉价易得、环境友好的原料出发制备离子液体是离子液体绿色化研究的重要内容,目前以氨基酸、糖类、生物碱等为原料的制备方法已有大量报道。氨基酸与强酸的酸碱中和反应可以合成氨基酸阳离子型离子液体,该过程对环境几乎没有污染,同时也使氨基酸分子的手性中心被自然地引入离子液体产品中。L-谷氨酸和氟硼酸、硝酸、硫酸、盐酸在微波作用下发生中和反应,一步即可获得系列新型氨基酸离子液体。这些离子液体常温下多为低熔点的固体,熔点范围为 69~193 ℃[39]。李巍等[40]以苏氨酸(Thr)和对甲苯磺酸(p-TsOH)为原料, 用一步法在微波反应仪中合成了苏氨酸对甲苯磺酸盐离子液体(Thr-TsOH),并采用对甲苯磺酸法一步制得苏氨酸对甲苯磺酸盐的甲酯和乙酯两种离子液体。Thanh等[41]在无溶剂的条件下,采用微波辅助法制备了手性麻黄素类离子液体。在严格控制反应时间和温度一致的情况下与传统加热方式进行比较,发现微波活化方式在产率上要远远高于传统加热。当R为丁基时,在 93 ℃ 反应 10 m in,对应于不同的阴离子,离子液体产率在 72%~85% 之间,制备过程如图5所示。Bica等[42]则以樟脑磺酸和莰烯为手性源,利用微波法制备了基于咪唑阳离子的手性离子液体,并用作丙烯酸和环戊二烯Diels-Alder反应的溶剂。
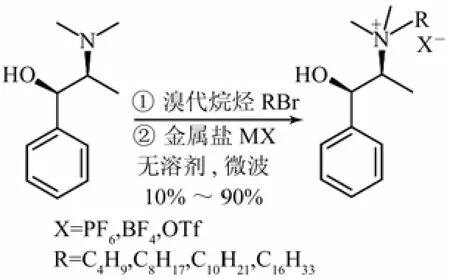
图5 无溶剂微波辅助制备手性麻黄素类离子液体[41]
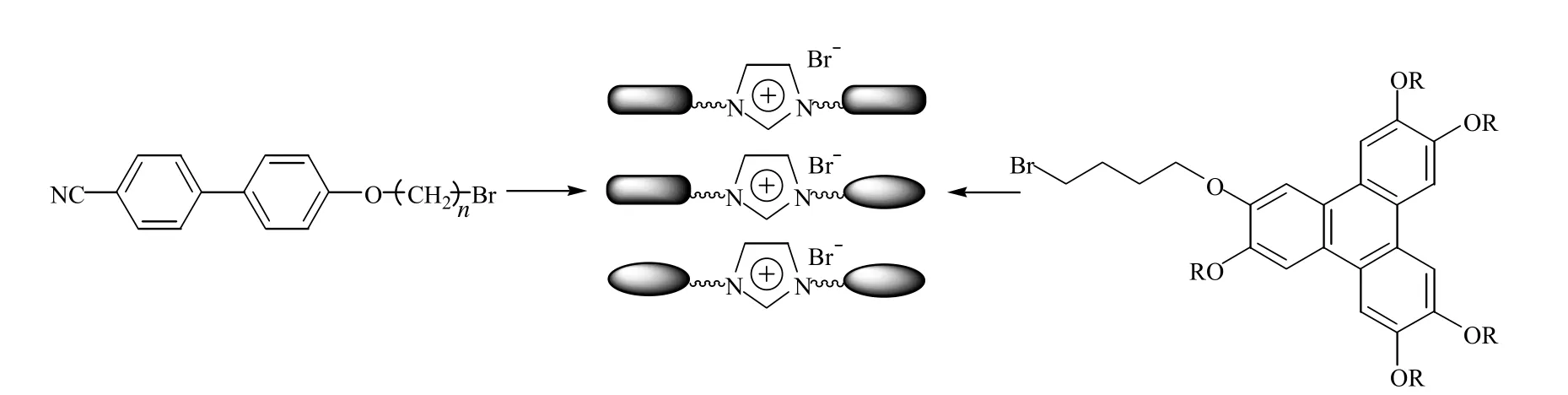
图4 微波辅助制备离子液体液晶化合物[37]
三组分一步法可以直接合成非卤素阴离子的离子液体。2003年,Xu等[43]采用传统加热回流的方式直接一步法合成基于咪唑阳离子的离子液体,对于溴代烷烃和氯代烷烃,通常需要 15 h 和 35 h 才能得到高于 87% 的离子液体收率。图6是微波辅助一步法制备非卤素阴离子型离子液体的示意图,这是一种更为高效的离子液体制备方法,此类报道目前还不多见。2008年,有两个研究组相继报道了离子液体的微波一步合成方法。Cravotto等[44]采用微波一步法合成阴离子为、、OTf-和的离子液体,在密闭体系中获得中等以上的收率,见图 7。与传统的合成方式比较,微波辅助一步法不需要溶剂和过量的卤代烷烃,副产物仅为无毒无害的无机盐,因此更为环境友好。Horikoshi等[45]则针对[Bm im]BF4的微波一步无溶剂法制备过程中,微波频率、时间和温度的影响作了详细考察,在5.8 GHz的微波频率下反应30 m in,产物收率达到了87%。
2.2 超声波法制备离子液体
超声波的波长远大于分子尺寸,因而不能对分子直接起作用,而是通过周围环境的物理作用来影
响分子。利用超声空化作用能减小液体中悬浮粒子的尺寸,提高异相反应速率,已广泛应用于各种材料的制备。Namboodiri 等[46]采用超声波作为能量源,在密闭体系无溶剂条件下合成了系列烷基咪唑类室温离子液体。溴代和碘代烷烃与烷基咪唑的反应在室温下 0.5~2 h 即可完成,收率均高于90%,而氯代烷烃的反应则相对较慢。Lévêque等[47]使用[Bm im]Cl和铵盐为原料,研究了超声波辅助合成[Bm im]BF4、[Bm im]PF6、[Bmim]CF3SO3和 [Bmim] BPh4的反应。在超声波作用下反应的时间只需要1 h,与常规磁力搅拌所需的5~8 h相比大幅度减少,从而提高了合成效率。随后,该研究组又详细研究了超声波频率、声波功率和探头直径对合成[Bm im]BF4的影响,证实超声波对反应的促进是物理效应而非化学作用(图 8)[48]。Lévêque研究组持续致力于超声波辅助的离子液体制备方法绿色化研究,并实现了超声波辅助一步法制备离子液体[49]。
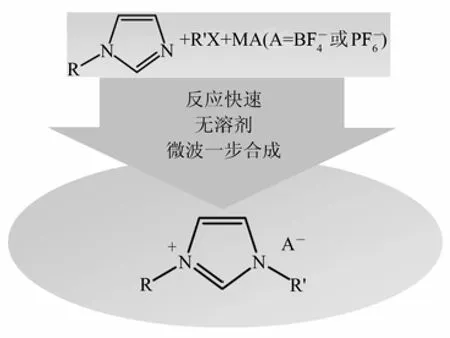
图6 微波一步法制备离子液体示意图

图7 微波辅助一步法合成阴离子为、、OTf-和的离子液体[44]
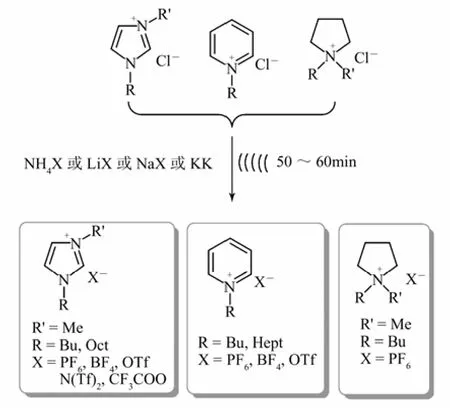
图8 超声波辅助法合成离子液体[48]
超声波辅助法也被用来研究功能化离子液体的制备,Zhao等[50]利用超声波辅助的方法一步合成了一系列阳离子含有 3-氯-2-羟丙基功能团的吡啶基离子液体,与常规搅拌反应方式相比,不但时间大幅度缩短,产品收率和纯度均大为改观。
最近,陈勇等[51]采用超声波辅助法一步制备带—SO3H官能团的吡啶磺酸类Brönsted酸性离子液体,与传统方法相比,合成反应时间由原来的72 h缩短到120 min。在超声功率为200 W和超声温度为30 ℃条件下,离子液体收率可达到 92%。
2.3 微波-超声组合法制备离子液体
微波和超声都属于简单易行又非常有效的过程强化手段,在降低能耗的同时,这些环境友好技术的应用不仅加快反应速度,还使化学反应在获得高产率的同时提高了选择性。将两种强化技术组合能否进一步提升过程的经济性,为离子液体的绿色化制备开辟新途径,是人们迫切想知道的。Cravotto等在微波-超声组合强化技术以及微波-超声序列强化技术领域开展了卓有成效的研究工作[24,52]。使用微波和超声技术的组合能有效提高一步法制备离子液体的效率,微波-超声组合法制备离子液体化学反应、反应条件及分离收率见图9和表3。从表 3数据看出,大多数离子液体在3~25 min这样极短的时间里分离收率达到80%以上。即使是惰性的底物,如氯代烷烃和 LiN(Tf)2,在优化的条件下仍然能获得令人满意的结果[53]。

图9 微波-超声组合法制备离子液体的化学反应
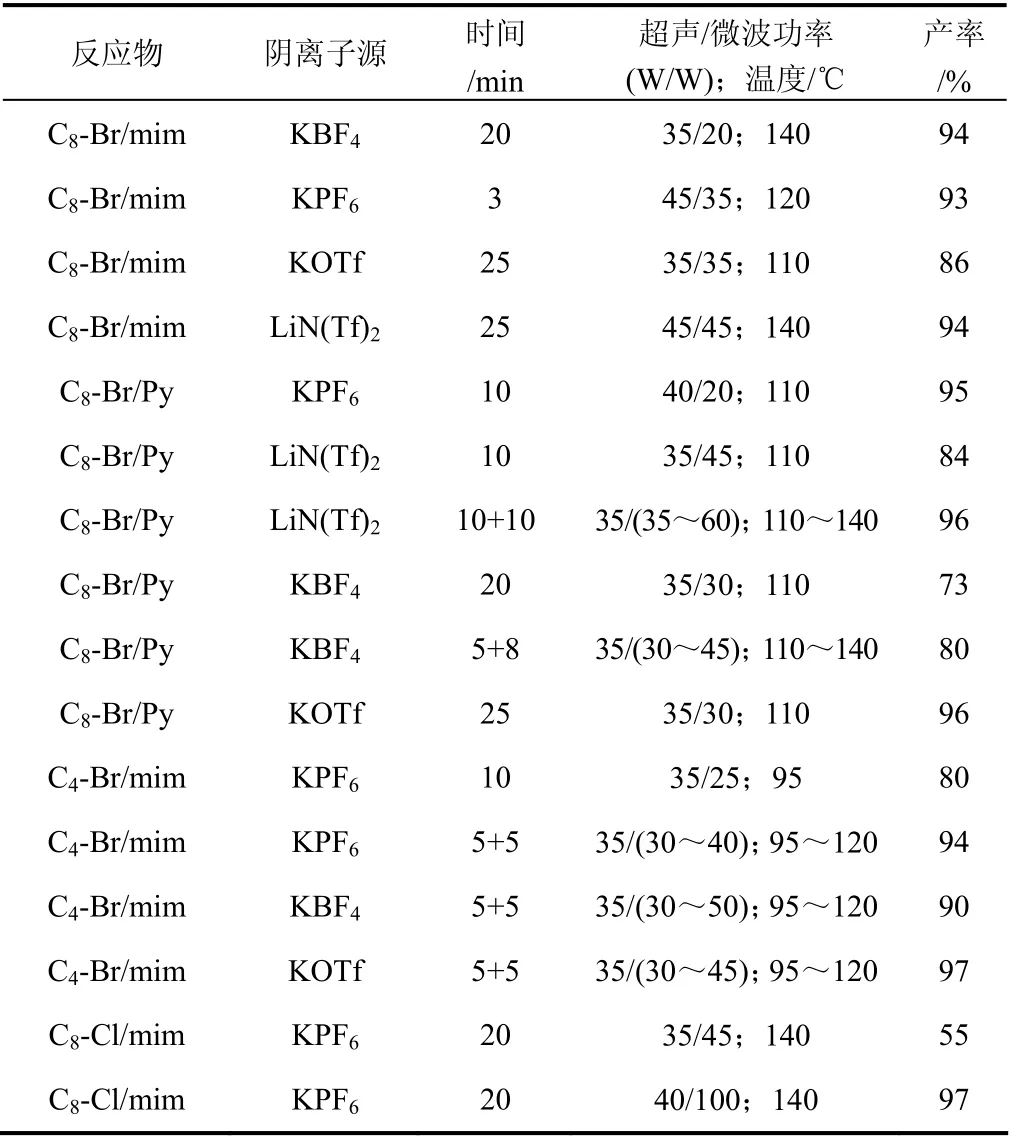
表3 微波-超声组合法制备离子液体反应条件及分离收率
2.4 微反应工艺制备离子液体
微化工系统是一种带有微反应器或微分离单元的新型化工系统,是实现化工过程绿色、安全、高效的重要方法。微反应器(micro-reactor)作为微化工系统的重要核心之一,起源于20世纪90年代,是利用特征尺度为微米级的微通道来强化化工传质过程的一种新技术。近年来,与微反应器相关的流动、混合、反应等方向的研究工作发展十分迅速,已经成为科学研究的热点之一[54-57]。一般来说,微反应器常用在连续流动体系,其优点集中体现在以下几个方面:传质、传热效率高,返混概率小以及能更好地控制反应温度和停留时间,使化学反应向着有利于所需产品的方向进行;由于能够改变化学反应的激烈程度,因此在高温、高压和难实现过程体系的应用过程中,微结构反应器要强于传统常规的批次反应器;基于数量叠加的放大原理,避免了传统化工工艺的放大效应,在单个微通道中实现的化学反应能通过简单的微通道数量放大达到工业生产规模[58]。
如前所述,离子液体的制备过程通常伴随着强烈的放热效应,加之大多数离子液体的高黏度及与原料的不相溶性,制备过程中随着离子液体的生成,会形成液/液两相,搅拌反应的方式既不利于散热,也不利于相间传质。加入有机溶剂或某一原料过量加入虽然在一定程度上能加强传热、传质,但是如果反应条件控制不当,温度仍然难以控制。因此传统方法合成的离子液体产品通常呈现较深的颜色,产品的纯度很难保证。这些弊病如果不一一消除,那么在规模化生产中会增加运行成本和造成环境污染。采用传质、传热效率高的连续流动微反应装置则可以有效避免上述离子液体制备中的问题,实现无溶剂条件下离子液体的大批量生产[59]。
德国不莱梅大学环境研究与技术中心的 Waterkamp等[60-61]开展了微反应器连续制备[Bm im]Br的过程强化研究。与传统制备过程相比,微反应过程无需使用有机溶剂,并且由于微反应器良好的传热性能,可以有效控制反应的强烈放热效应,使反应几乎能够在恒温条件下进行。从图 10可见微反应器在反应温度控制方面具有优势。在优化的合成反应条件下,[Bm im]Br的时空收率达到1.27 kg/(L·h),是4 L规模批次反应器的24倍。连续法制备规模达到 9.3 kg/d,并且产品的纯度高于99%。Waterkamp研究组还详细研究了微反应制备过程中反应温度和流速对 [Bm im]Br产品色泽的影响。他们发现升高温度或降低流速都会使产品带有颜色,而通过采用毛细管段塞流来增强传质,在微反应器中,无溶剂条件下可以在145 ℃高温下通过提高流速实现高纯度[Bm im]Br的连续化制备,时空收率高达1240 kg/(L·d)[62]。

图10 微反应器和批次反应器制备过程温度随时间变化趋势比较[61]
Renken和 Hessel等[63-64]为进一步优化微反应器的性能,设计了微反应器与两段毛细管式反应器的组合,与单一毛细管反应器相比,空时从4 h骤减为4.6 min,装置的反应性能提高了50倍。采用此组合型反应器合成了离子液体[Em im]EtSO4,时空收率达到15.84 kg/(L·h)。M inrath等[65]首次将微波辅助加热引入到微反应器中,考察了溴化1-甲基-3-己基-咪唑盐离子液体的制备过程。实验证明使用≤ 50 W的微波功率,约10 min的停留时间即可获得优异的转化率和选择性。当微波功率为200 W时,停留时间可以减少到小于2 m in。
Thoeming[66]在配有涡轮式微混器的单级和多级管式微反应装置上研究了反应物摩尔比对离子液体产品质量的影响。采用多级装置在低温下可以获得无色的[Bmim]Br,反应物1-甲基咪唑的转化率达到99%。2009年,Löwe等[67]将热管换热技术与微
反应器技术集成,大大改善了装置的热交换性能,并选择1-甲基咪唑与三氟甲磺酸甲酯经烷基化制备1,3-二甲基咪唑三氟甲磺酸根离子液体为探针反应来研究装置的性能。对于这样一个快速且强烈放热的二级动力学过程,利用如图11所示的热管与微反应器的组合,在反应温度为333~353 K,停留时间为4 s时,转化率达到100%,装置的生产能力达到0.74 kg/h。同年,Wilms等[68]报道了一种简单、高效制备多种高纯离子液体的方法。他们利用HPLC泵、微混合器和毛细管组合成连续流动微反应器,由于具有高的比表面/体积比和优异的传质传热性能,通过操作条件的调变,该反应器系统可实现如图 12所示的阳离子含有取代芳基和乙烯基的咪唑类离子液体的制备。

图11 装有热管系统的微反应器[67]

图12 基于咪唑阳离子的各类离子液体[68]
Hu等[69]的工作表明,利用微通道反应器还可以进行离子液体合成反应动力学研究。他们通过测定反应的停留时间分布(residence time distribution, RTD),认为微通道系统可以看作活塞流反应
器(plug flow reactor, PFR),适合开展强烈放热或高黏度体系快速反应的动力学研究。例如,1-甲基咪唑与溴代正丁烷制备[Bmim]Br的反应,测得的反应活化能为78.4 kJ/mol,反应速率为
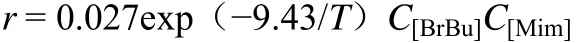
最近,Zimmermann等[70]报道了一种新颖的低成本离子液体制备方法。他们采用简单易得、价格低廉的烷基伯胺、乙二醛、甲醛、无机酸或有机酸为反应原料,利用如图13所示的微反应装置,实现了两种阳离子结构对称的水溶性离子液体[C4C4im]OAc和[C4C4im]Cl的连续化制备,产率达到70%~90%,纯度大于 95%。

图13 多用途微反应装置(X型混合器由Little Things Factory公司制造)[70]
2.5 STT(spinning tube-in-tube)过程强化技术制备离子液体
美国环境保护署(EPA) Gonzalez教授及其合作者遵循绿色化学的理念,潜心开发化学品的清洁合成技术,发明了适用于固液、气液和气固液等混合相反应体系,以及高黏性液体反应体系的 STT®(spinning tube-in-tube)反应器。STT技术来源于电子封装中的微铣削工艺,其作用原理如图 14所示。STT®反应器高速的剪切力能使反应物达到分子水平的混合,其突出优势在于拥有极高的传质、传热效率和极高的相间作用力,因此获得极高的反应速率和产率,并且没有废弃物产生。STT®反应器已经成功用于有机化学品、生物柴油、生物医药、电子材料和离子液体等的制备。2009年,Gonzalez和Ciszewski报道了使用STT®反应器在无溶剂条件下连续化制备一系列基于烷基咪唑的离子液体的研究工作。与传统批次制备方法相比,该制备过程仅需要3~4 h,原料的转化率超过99%,离子液体的产量可以达到每天十几千克[71]。制备过程如图 15所示。
STT®反应器的优点包括:可实现连续操作、易于小型化、没有放大效应、日常维护简单、完全封闭无有害物释放、组建和操作成本低等,因此极有可能在某些离子液体商业化生产中获得应用。
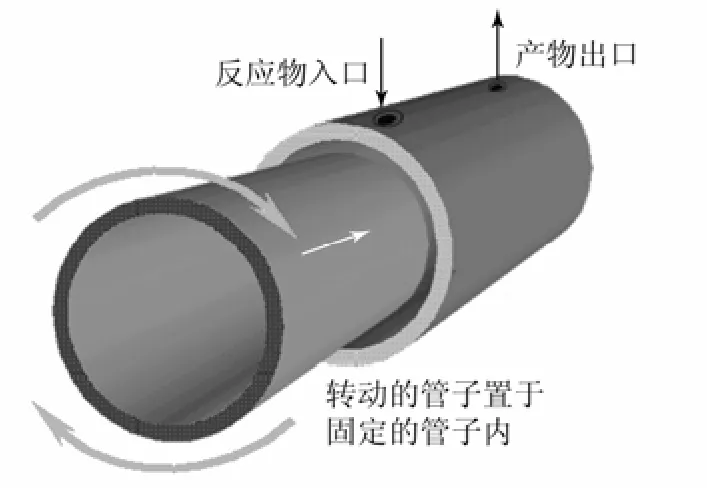
图14 STT技术 tube-in-tube 原理

图15 Innovator 200 STT®反应器制备离子液体示意图[71]
3 结 语
人类社会的发展离不开化学工业,而人类社会的可持续发展更依赖于绿色化学化工技术的研究与开发。离子液体的出现为绿色化学带来了新希望。大量的研究表明,离子液体的应用为很多重污染、高能耗传统化工过程开辟了新途径。然而离子液体工业应用的前提是实现低成本、绿色化的大规模制备。利用各种过程强化技术开发新型高效的制备工艺,大幅度减少过程的能耗、物耗和废弃物排放,必将推动和促进离子液体的产业化应用进程。
如上所述,近年来非常规制备技术在离子液体大量制备方面取得了重要进展,但是有些问题仍然不可忽略。
(1)针对特殊功能的离子液体的制备技术研究尚显不足。例如,用于酸、碱催化过程的酸或碱功能化离子液体的非常规制备方法未见报道。
(2)虽然微波、超声波等技术已经成功用于有机合成、日用品、食品、水处理等方面,但是离子液体的特殊物理化学性质使得这些技术的应用变得相对复杂。只有进一步认识过程的本质规律,才能形成完善的理论体系指导开发适合于离子液体制备的过程强化技术。
(3)必须重视离子液体制备过程以及其本身对环境的影响,开发原料绿色、过程绿色、产品绿色的离子液体制备新技术。
相信随着研究的不断深入和相关技术的发展,在业界人士的共同努力下,必将克服重重困难,使离子液体的制备技术获得重大突破。
[1] Walden P. Molecular weights and electrical conductivity of several fused salts[J].Bull. Acad. Imper. Sci. (St Petersburg),1914,1800:405-422.
[2] Hurley F H. Electrodeposition of alum inum:US,2446331[P]. 1948-08-03.
[3] W ier T P,Hurley F H. Electrodeposition of alum inum:US,2446349[P]. 1948-08-03.
[4] W ier T P. Electrodeposition of alum inum:US,2446350[P]. 1948-08-03.
[5] Hurley F H,Wier T P. The electrodeposition of alum inium from non-aqueous solutions at room temperature[J].J. Electrochem. Soc.,1951,98(5):207-212.
[6] Olivier-Bourbigou H,Magna L,Morvan D. Ionic liquids and catalysis∶ Recent progress from know ledge to applications[J].Appl. Catal. A∶General,2010,373:1-56.
[7] Kirchner B. Ionic Liquids:Topics In Current Chem istry [M]. Clare B,Sirwardana A,MacFarlane D R. Germany:Springer-Verlag Berlin and Heidelberg GmbH & Co. K,2009:1-40.
[8] 杨雅立,王晓化,寇元,等. 不断壮大的离子液体家族[J]. 化学进展,2010,22 (7):1499-1508.
[9] 李雪辉,赵东滨,费兆福,等. 离子液体的功能化及其应用[J]. 中国科学B辑:化学,2006,36 (3):181-196.
[10] 张晓春,张锁江,左勇赵,等. 离子液体的制备及应用[J]. 化学进展,2010,22 (7):1499-1508.
[11] Huddleston J G,Visser A E,Reichert W M. Characterization and comparison of hydrophilic and hydrophobic room temperature ionic liquids incorporating the im idazolium cation[J].Green Chem.,2001,156-164.
[12] Ropel L,Belveze L S,Aki S N V K,et al. Octanol-water partition coefficients of im idazolium-based ionic liquids[J].Green Chem.,2005,7:83-90.
[13] Behar D,Neta P. Reaction kinetics in ionic liquids as studied by pulse radiolysis∶ Redox reactions in the solvents methyltributylammonium bis( trifluoromethylsulfonyl) im ide andN-butylpyridinium tetrafluoroborate[J].J.Phys. Chem. A,2002,106: 3139-3147.
[14] Hurley F H,W ier T P. Electrodeposition of metals from fused quaternary ammonium salts[J].J. Electrochem. Soc.,1951,98 (2):203-208.
[15] Kochv R,M illeer L L,Osteryaung R A. Electroinitiated Friedel-crafts transalkylations in a room-temperature molten salt medium[J].J. Am. Chem. Soc.,1976,98 (17):5277-5284.
[16] Wilkes J S,Levisky J A,Wilson R A,et al. A lkyl im idazolium chloroalum inate melts∶ A new class of room temperature ionic liquids for electrochem istry spectroscopy and systhesis[J].Inorg. Chem.,1982,21:1263-1268.
[17] Christopher J A,Martyn J G,Seddon K R. Friedel-crafts reactions in room temperature ionic liquids[J].Chem. Common.,1998,19:2097-2098.
[18] Wilkes J S, Zaworotko M J. Air and water stable 1-ethyl-3-methylim idazolium based lonic liquids[J].Chem. Commun.,1992,16:965-967.
[19] Fuller J,Carlin R T. Structure of 1-ethyl-3-methylim idazolium hexafluorophosphate∶ Model for room temperature molten salts[J].Chem. Commun.,1994,299-300.
[20] Deetlefs M,Seddon K R. The Green Synthesis of Ionic Liquids:in Handbook of Green Chem istry[M]. Wasserscheid P,StarkMaggel A. Germany:Wiley,2010,6:3-38.
[21] Deetlefs M,Seddon K R. Assessing the greenness of some typical laboratory ionic liquid preparations[J].Green Chem.,2010,12:17-30.
[22] Loupy A. Microwaves in Organic Synthesis[M]. Germany:Wiley-VCH Weinheim,2006.
[23] Cravotto G,Cintas P. Power ultrasound in organic synthesis∶ Moving cavitational chem istry from academ ia to innovative and large-scale applications[J].Chem. Soc. Rev.,2006,35(2):180-196.
[24] Lévêque J M,Estager J,Draye M,et al. Synthesis of ionic liquids using non conventional activation methods∶ An overview[J].Monatshefte für Chemie,2007,138:1103-1113.
[25] Varma R S,Namboodiri V V. An expeditious solvent-free route to ionic liquids using microwaves[J].Chem.Commun.,2001,643-644.
[26] Varma R S,Namboodiri V V. Solvent-free preparation of ionic liquids using a household m icrowave oven[J].PureAppl.Chem.,2001,73:1309-1313.
[27] Law M C,Wong K Y,Chan T K. Solvent-free route to ionic liquid precursors using a water-moderated m icrowave process[J].Green Chem.,2002,4:328-330.
[28] Roberts B A,Strauss C R. Toward rapid, green, predictable microwave-assisted synthesis[J].Accounts of Chemical Research,2005,38:653-661.
[29] Deetlefs M,Seddon K R. Impoved preparations of ionic liquids using microwave irradiation[J].Green Chem.,2003,5:181-186.
[30] Khadilkar B M,Rebeiro G L. M icrowave-assisted synthesis of room-temperature ionic liquid precursor in closed vessel[J].Org. Proc. Res. & Devel.,2002,6:826-828.
[31] Erdmenger T,Paulus R M,Hoogenboom R,et al. Scaling-up the synthesis of 1-butyl-3-methylimidazolium chloride under microwave irradiation[J].Aust. J. Chem.,2008,61:197-203.
[32] Namboodiri V V,Varma R S. An improved preparation of 1,3-dialkylim idazolium tetrafluoroborate ionic liquids using m icrowaves[J].Tetrahedron Lett.,2002,43:5381-5383.
[33] Singh V,Kaur S,Sapehiyia V,et al. M icrowave accelerated preparation of [bm im][HSO4] ionic liquid∶ An acid catalyst for improved synthesis of coumarins[J].Catal. Comm.,2005,6:57-60.
[34] Varma R S,Namboodiri V V. M icrowave-assisted preparation of dialkylim idazolium tetrachloroalum inates and their use as catalysts in the solvent-free tetrahydropyranylation of alcohols and phenols[J].Chem. Comm.,2002,342-343.
[35] Kim Y J,Varma R S. M icrowave-assisted preparation of imidazolium-based tetrachloroindate(III) and their application in the tetrahydropyranylation of alcohols[J].Tetrahedron Lett.,2005,46:1467-1569.
[36] Kim Y J,Varma R S. M icrowave-assisted preparation of 1-butyl-3-methylim idazolium tetrachlorogallate and its catalytic use in acetal formation under m ild conditions[J].Tetrahedron Lett.,2005,46:7447-7449.
[37] Pal S K,Kumar S. M icrowave-assisted synthesis of novel im idazolium-based ionic liquid crystalline dimmers[J].Tetrahedron Lett.,2006,47(50):8993-8997.
[38] Kärkkäinen J,Asikkala J,Laitinen R S,et al. Effect of temperature on the purity of product in the preparation of 1-butyl-3-methylimidazolium-based ionic liquids[J].Z. Naturforsch,2004,59b:763-770.
[39] Rong H,Li W,Chen Z Y,et al. Glutamic acid cation based ionic liquids∶ M icrowave synthesis, characterization, and theoretical study[J].J. Phys. Chem. B,2008,112:1451-1455.
[40] 李巍,荣华,吴新民,等. 苏氨酸对甲苯磺酸盐及其酯化物的微波合成、表征及量化计算[J]. 物理化学学报,2008,24(5):868-872.
[41] Thanh G V,Pegot B,Loupy A. Solvent-free m icrowave-assisted preparation of chiral ionic liquids from (-)-N-methylephedrine[J].Eur. J. Org. Chem.,2004,5:1112-1116.
[42] Bica K,Gmeiner G,Reichel C,et al. M icrowave-assisted synthesis of camphor-derived chiral im idazolium ionic liquids and their application in diastereoselective diels-alder reaction[J].Synthesis,2007,9:1333-1338.
[43] Xu D Q,Liu B Y,Luo S P,et al. A novel and eco-friendly method for the preparation of ionic liquids[J].Synthesis,2003,17:2626-2629.
[44] Cravotto G,Gaudino E C,Boffa L,et al. Preparation of second generation ionic liquids by efficient solvent-free alkylation ofN-heterocycles w ith chloroalkanes[J].Molecules,2008,13:149-156.
[45] Horikoshi S,Hamamura T,Kajitani M,et al. Green chem istry w ith a novel 5.8-ghz m icrowave apparatus. Prompt one-pot solvent-free synthesis of a major ionic liquid∶ The 1-butyl-3-methylimidazolium tetrafluoroborate system[J].Org. Process Res. Dev.,2008,12:1089-1093.
[46] Namboodiri V V,Varma R S. Solvent-free sonochem ical preparation of ionic liquids[J].Org. Lett.,2002,4(18):3161-3163.
[47] Lévêque J M,Luche J L,Pétrier C,et al. An improved preparation of ionic liquids by ultrasound[J].Green Chem.,2002,4:357-360.
[48] Lévêque J M,Desset S,Suptil J,et al. A general ultrasound-assisted access to room-temperature ionic liquids[J].Ultrasonics Sonochemistry,2006,13:189-193.
[49] Estager J,Lévêque J M,Cravotto G,et al. One-pot and solventles synthesis of ionic liquids under ultrasonic irradiation[J].SYNLETT,2007,13:2065-2068.
[50] Zhao S H,Zhao E L,Shen P,et al. An atom-efficient and practical synthesis of new pyridinium ionic liquids and application in Morita–Baylis–Hillman reaction[J].Ultrasonics Sonochemistry,2008,15:955-959.
[51] 陈勇,赵文军,高林. 超声波辅助法一步合成B酸离子液体[J]. 工业催化,2009,17(6):27-29.
[52] Cravotto G,Cintas P. The combined use of m icrowaves and ultrasound∶ improved tools in process chem istry and organic synthesis[J].Chem. Eur. J.,2007,13:1902-1909.
[53] Cravotto G,Boffa L,Lévêque J M,et al. A speedy one-pot synthesis of second-generation ionic liquids under ultrasound and/or m icrowave irradiation[J].Aust. J. Chem.,2007,60:946-950.
[54] Hessel V, Hardt S, Löwe H. Chem ical M icro Process Engineering-Fundamentals, Modelling and Reactions[M]. Germany:Wiley-VCH Weinheim,2004.
[55] Hessel V,Löb P,Krtschil U,et al. M icrostructured reactors for development and production in pharmaceutical and fine chem istry[J].Ernst Schering Foundation Symposium Proceedings,2007,3:205-240.
[56] 陈光文. 微化工技术研究进展[J]. 现代化工,2007,27(10):8-13.
[57] 赵玉潮,张好翠,沈佳妮,等. 微化工技术在化学反应中的应用进展[J]. 中国科技论文在线,2008,3(3):157-169.
[58] Koch M V,VandenBussche K M,Chrisman R W. M icro Instrumentation for High Throughput Experimentation and Process Intensification:M icroreactor Concepts and Processing[M]. Hessel V,Löb P,Löwe H,et al. Weinheim,Germany:W iley-VCH,2006∶85-130.
[59] Kashid M N,Renken A,Kiw i-M insker L. M icrostructured reactors and supports forionic liquids[J].Chemical Engineering Science,2011,66:1480-1489.
[60] Waterkamp D A,Thöming J,Heiland M,et al. Process intensification in strongly exotherm ic alkylation reactions by m icroreaction technology as illustrated by the synthesis of ionic liquids[J].Chem.Ing.Tech.,2007,79:1482-1483.
[61] Waterkamp D A,Heiland M,Schluter M,et al. Synthesis of ionic liquids in micro-reactors—a process intensification study[J].Green Chem.,2007,9:1084-1090.
[62] Waterkamp D A,Engelbert M,Thöming J,et al. On the effect of enhanced mass transfer on side reactions in capillary m icroreactors during high-temperature synthesis of an ionic liquid[J].Chem. Eng. Technol.,2009,32(11):1717-1723.
[63] Renken A,Hessel V,Löb P,et al. Ionic liquid synthesis in a microstructured reactor for process intensification[J].Chem. Eng. Process,2007,46:840-845.
[64] Hessel V,Loeb P,M iszcuk R,et al. European Process Intensification Conference - 1[C]//Copenhagen,Denmark,2007.
[65] Minrath I,Beck M,Pitton D,et al. 10th International Conference on M icroreaction Technology (IMRET 10)[C]//New Orleans,LU,2008.
[66] Thoem ing J. 1st Sino-German Symposium on Ionic Liquids[C]// Dalian,China,2008.
[67] Löwe H,Axinte R D,Breuch D,et al. Heat pipe controlled syntheses of ionic liquids in m icrostructured reactors[J].Chem. Eng. J.,2009,155:548-550.
[68] Wilms D,Klos J,Kilbinger A F M,et al. Ionic liquids on demand in continuous flow[J].Org. Proc. Res. Dev.,2009,13:961-964.
[69] Hu S Z,Wang A J,Löwe H,et al. Kinetic study of ionic liquid synthesis in a microchannel reactor[J].Chem. Eng. J.,2010,162:350-354.
[70] Zimmermann J,Ondruschka B,Stark A. Efficient synthesis of 1,3-dialkylim idazolium-based ionic liquids∶ the modified continuous radziszewski reaction in a m icroreactor setup[J].Org. Proc. Res. Dev.,2010,14:1102-1109.
[71] Gonzalez M A,Ciszewski J T. High conversion, solvent free, continuous synthesis of imidazolium ionic liquids in spinning tube-in-tube reactors[J].Org. Process Res. Dev.,2009,13(1):64-66.
Advances in non-conventional preparation technology of ionic liquids
LI Zhen,CHEN Jing,XIA Chungu
(State Key Laboratory for Oxo Synthesis and Selective Oxidation, Lanzhou Institute of Chem ical Physics, Chinese Academy of Sciences, Lanzhou 730000, Gansu, China)
Large-scale application of ionic liquids depends on the continuous advancement of preparation technology. However, the classic procedure for ionic liquids synthesis is excessively time-consum ing and unsuitable for mass production, which restricts industrial application of ionic liquids. Aim ing at the key process in ionic liquids preparation, the research progress of the non-conventional techniques for preparation of ionic liquids is summarized. The current ionic liquids preparation technologies, such as m icrowave, ultrasound, microwave-ultrasound, m icroreactor and Spinning Tube-in-Tube (STT) process intensification are reviewed. A lthough important progress has been made in non-conventional preparation technique at this stage, intensive research work is still required in order to establish theoretical guidance, and the development of task-functionalized ionic liquids and green preparation technique should be accelerated.
ionic liquid;non-conventional techniques;m icrowave assistant;ultrasound;m icroreactor process
O 645.4
A
1000–6613(2012)09–1861–10
2012-06-01;修改稿日期:2012-06-13。
国家自然科学基金重点项目(21133011),国家重点基础研究发展计划(国家973计划,2011CB201404)及“十二五”国家科技支撑重点项目(2011BAE17B00)。
李臻(1973—),女,博士,副研究员,主要从事清洁催化和功能化离子液体研究。E-mail zhenli@licp.cas.cn。联系人:夏春谷,研究员,博士生导师,主要从事均相催化和清洁化工技术。E-mail cgxia@licp.cas.cn。

