紫叶矮樱组培快繁技术的研究
杨 燕,杨亚平
(1.晋中职业技术学院,山西 晋中 030600;2.山西潞安矿业集团公司林业处,山西 长治 046204)
紫叶矮樱组培快繁技术的研究
杨 燕1,杨亚平2
(1.晋中职业技术学院,山西 晋中 030600;2.山西潞安矿业集团公司林业处,山西 长治 046204)
以紫叶矮樱的带芽茎段为外植体进行研究,结果表明,外植体消毒采用5%NaClO处理20min,效果最好,3月下旬到4月中旬为最适取材季节,启动培养以1/2MS+6-BA1.5mg/L+NAA0.05mg/L为最佳组合培养基配方,生根培养最佳培养基为1/2MS+IBA1.0mg/L+IAA1.0mg/L,其次为1/2MS+NAA1.5mg/L.
紫叶矮樱;组织培养;离体快繁
紫叶矮樱(Prunus×cistena‘Pissardii')系紫叶李和矮樱杂交种,蔷薇科(Rosaceae),李属(Prunus),是世界著名的观赏树种,在园林绿化中占有重要位置.进行紫叶矮樱的组织培养,选择适宜的培养条件和培养方法,为紫叶矮樱的大批量快速繁殖提供理论依据,指导生产具有重要意义.
1 试验材料与方法
1.1 材料及条件
供试材料为山西太谷龙岗庄园经济林基地的二年生紫叶矮樱嫁接苗(山桃为砧木),取紫叶矮樱带芽茎段为外植体,以MS、1/2MS、B5、WPM为基本培养基.该实验在山西农大林学院实验苗圃组培室进行.
1.2 试验步骤及方法
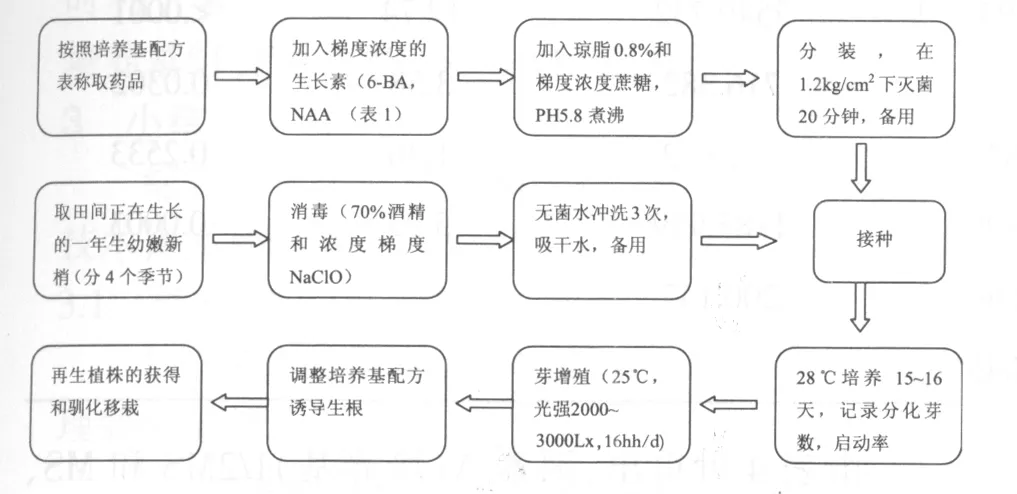
1.3 试验数据统计分析
采用SAS for windows统计分析软件包对实验观测数据进行方差分析,LSD检验.
2 试验结果与分析
2.1 不同消毒方法对外植体启动的影响
试验中对NaClO灭菌设计了 3%、5%、7%、10%四个浓度梯度,4种消毒处理方法对外植体的启动结果有较大差异.5%NaClO(有效CL%≥0.5%)消毒液处理后的污染率为6.67%,死亡率为0,启动率为93.33%,整体表现为消毒效果最好.这与Found[1]等(1995)的研究结果一致.
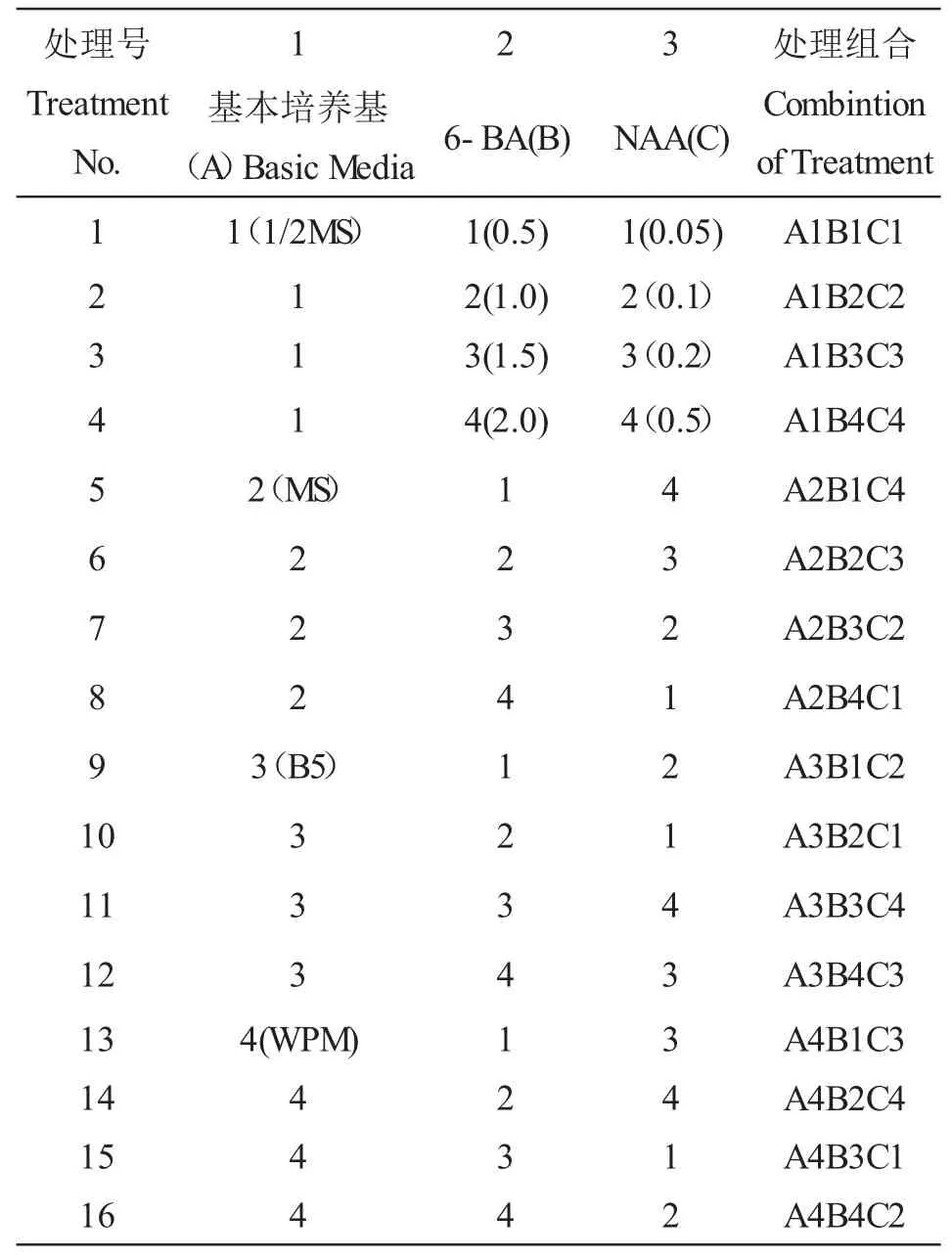
表1 启动培养正交试验设计方案
2.2 不同取材季节对外植体启动的影响
本试验分别在2006年3月下旬、4月中旬、5月下旬、7月上旬、9月中旬取材,进行重复试验,3月下旬到4月中旬所取材料的污染率在5-8%,死亡率在10%左右,启动率在81-85%,整体优于其它几个时间段.F.Enjalric等(1988)在对三叶胶初级培养污染的研究中发现高温、多雨的环境更有利于污染的发生,而且随着植物材料年龄的增长,植物材料的健康状况不断恶化,组培污染也会更加严重[2].由此可见,3月下旬到4月中旬为紫叶矮樱外植体最适取材季节.
2.3 不同培养基对紫叶矮樱分化芽及启动率的影响
外植体接入培养基后,生长情况各异,试验中,变化最明显的是1/2MS培养基添加不同激素配比的组合,于7月14号下午接种,18号观察芽长和茎高已经见长,具体结果见表2.
对表2中启动率的结果进行方差分析,结果见表3.
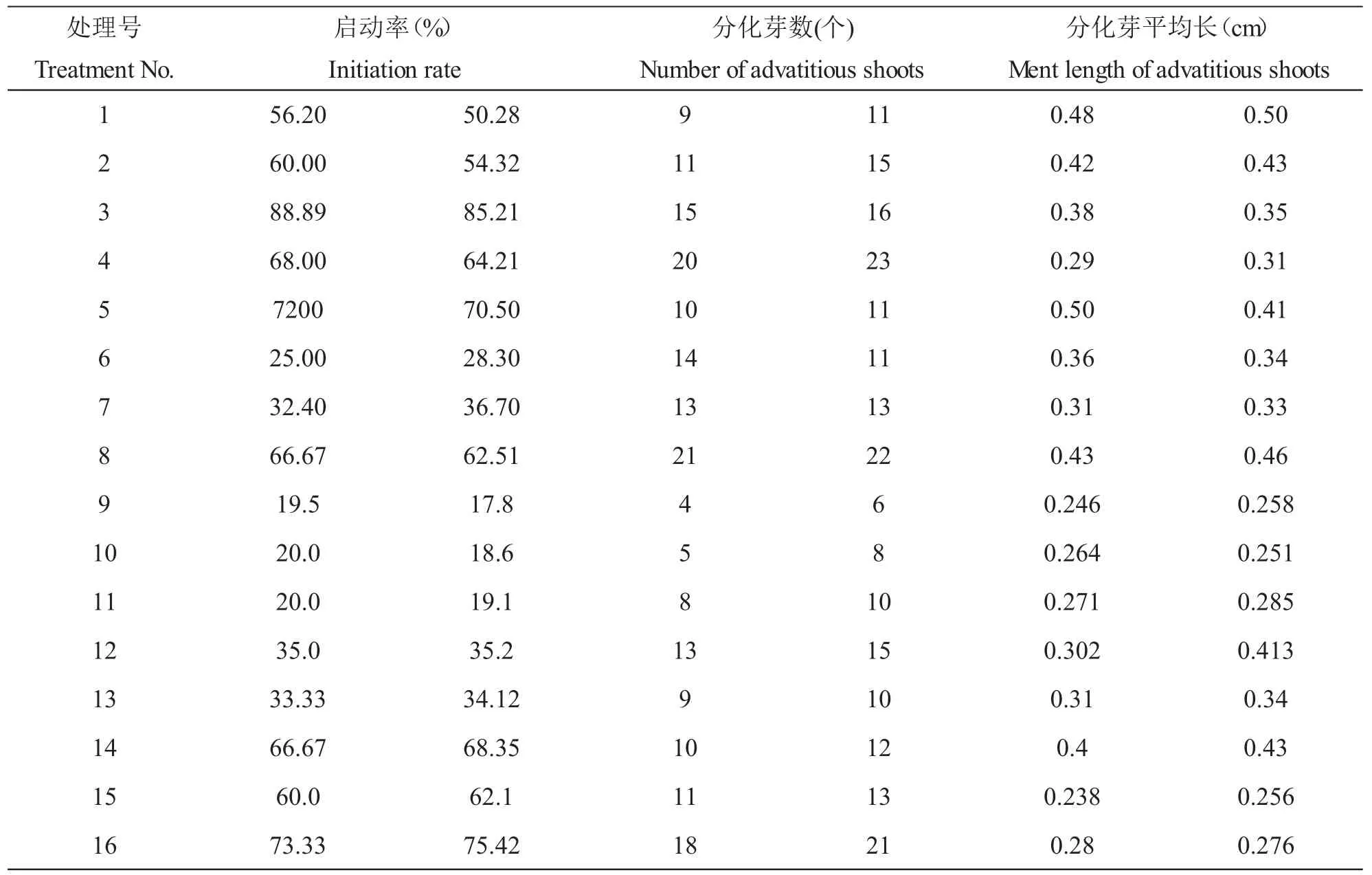
表2 启动培养结果

表3 启动率的方差分析
由表3知,因素A(培养基)对启动率的影响极显著,因素B(6-BA)对启动率的影响显著,分别对其进行多重比较,采用LSD检验,结果见表4.
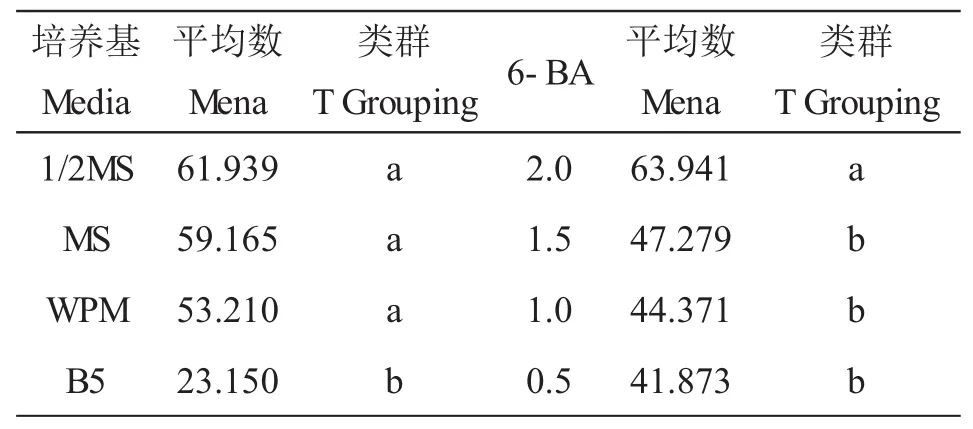
表4 培养基和6-BA 4水平显著性检验(0.05)
由表4可得出,因素A(培养基)1/2MS和MS、WPM差异不显著,MS、WPM可以替换1/2MS,根据均值大小,选取1水平,即培养基为1/2MS时,对启动率的作用效果最好.这三者均和B5差异显著.因素 B(6-BA)4 水平和 3、2、1 水平间差异显著,3、2、1三水平间差异不显著,即6-BA2.0mg/L为最适合的6-BA浓度.
本试验方差分析表明,最优处理组合应为A1B4,因素C(NAA)F检测不显著,其水平可任取.
对表2中分化芽平均长的结果进行方差分析,因素A(培养基)、因素B(6-BA)对分化芽长的影响作用极显著,因素C(NAA)的影响作用显著,分别对其进行多重比较,可得出,因素A(培养基)1、2、3水平间差异不显著,和4水平差异显著,从均值来分析,1/2MS培养基为最好的基本培养基.因素B(6-BA)3水平和4水平、1水平差异显著,从均值来分析,3水平效果最好,即6-BA1.5mg/L.浓度过高过低都不利于芽子生长.因素C(NAA)4水平间差异显著,1水平和3、4水平及显著,和2水平差异显著,2水平和3、4水平差异极显著.从均值来分析,1水平效果最好,即NAA0.05mg/L.
本试验方差分析表明,最优组合为A1B3C1,即最优组合为 1/2MS,6-BA1.5mg/L,NAA0.05mg/L.
综合以上分析,在紫叶矮樱启功培养中,最适合的培养基配方为1/2MS+6-BA1.5mg/L+NAA0.05mg/L.
2.2 生根培养基的筛选
将高、壮的紫叶矮樱无根苗接种于生根培养基上,一周后开始出现乳白色根芽,20d时观察生根情况,统计平均生根数,计算生根率,其结果见表5.

表5 不同培养基生根结果
对表5的每组数据进行方差分析和LSD检验,综合平均生根数、生根率、根生长情况三方面因素,认为1/2MS+IBA1.0mg/L+IAA1.0mg/L最适于紫叶矮樱生根,IBA具有很好的诱发根原基形成的能力,IBA和IAA又具有不同的生理活性,二者配合使用,可以达到很好的生根效果,但浓度过高过低均对根的形成、生长不利,浓度范围在1.0~1.5mg/L时利于紫叶矮樱生根.其次,利于紫叶矮樱生根的培养基组合为1/2MS+NAA1.5mg/L.
3 小结
综合上述试验结果和分析,紫叶矮樱快速繁殖技术体系要点如下:
3.1 外植体启动情况
1.外植体的消毒以5%的NaClO消毒20min处理效果最佳.
2.外植体取材以3月下旬到4月中旬效果最佳.此时外植体积累了较丰富的内源激素,抵抗病菌的能力强或有些病菌还没有活跃起来,污染率低,启动率高.
3.以 1/2MS+6-BA1.5mg/L+NAA0.05mg/L为最优启动培养基组合.
3.2 生根培养
最佳生根培养基为1/2MS+IBA1.0mg/L+IAA1.0mg/L,其次为 1/2MS+NAA1.5mg/L.一周后 1/2MS+IBA1.0mg/L+IAA1.0mg/L中有根长出,20d后平均生根数为2~5.4条,生根率为48.6~94.7%.
〔1〕Found M M,Gomaa A H,El Zaher M H A,et al.Factors influencing in vitro establishentand multiplications stages of peach[J].Acta Horticulture,1995,(409):191-196.
〔2〕Enjalric,F,Carron,M.P.&.Lardet,L.Contamination of primary cultures in tropical areas:The case of Hevea brasiliensis.Acta Horticulturae,1988,225:57-65.
〔3〕陈振光.园艺植物离体培养学[M].北京:中国农业出版社,1996.
S687
A
1673-260X(2012)02-0047-03

