连续柱状晶组织Cu-12%Al合金在3.5%NaCl和10%HCl溶液中的腐蚀行为
黄海友,聂铭君,栾燕燕,谢建新
(北京科技大学 新材料技术研究院 材料先进制备技术教育部重点实验室,北京 100083)
连续柱状晶组织Cu-12%Al合金在3.5%NaCl和10%HCl溶液中的腐蚀行为
黄海友,聂铭君,栾燕燕,谢建新
(北京科技大学 新材料技术研究院 材料先进制备技术教育部重点实验室,北京 100083)
采用静态浸泡腐蚀实验、电化学分析方法等研究连续定向凝固方法制备的具有连续柱状晶组织的Cu-12%Al(质量分数,下同)合金在3.5%NaCl(质量分数)溶液和10%HCl(体积分数)溶液中的耐腐蚀性能及腐蚀机理。结果表明:Cu-12%Al合金在3.5%NaCl溶液中的耐腐蚀性能可达到耐蚀级。虽然在40 ℃以下的10%HCl溶液中该合金的耐腐蚀性能可达到耐蚀级,但在40 ℃以上的10%HCl溶液中的耐腐蚀性能欠佳。连续柱状晶组织Cu-12%Al合金的耐腐蚀性能优于Al含量为5%~11%的传统铝青铜和QBe2合金的耐腐蚀性能,但劣于QBe2.15合金的耐腐蚀性能。在3.5% NaCl溶液和10%HCl中连续柱状晶组织Cu-12%Al合金的自腐蚀电位分别为−271 mV(vs SCE)和−333 mV (vs SCE)。腐蚀发生后试样表面的Al元素含量明显下降,腐蚀机制为脱铝腐蚀。
Cu-12%Al合金;连续柱状晶组织;耐腐蚀性能;脱铝腐蚀
铝青铜由于具有优良的力学性能、耐腐蚀性能和耐磨性能,被广泛应用于机械制造、交通运输、船舶海洋和电力电器等众多领域,是现代工业中应用极其广泛的铜合金[1−2]。随着铝含量的升高,铝青铜的强度、弹性性能和形状记忆性能都得到大幅度提高,但塑性急剧变差。例如,使用传统铸造方法制备的多晶82.7Cu-13Al-4.3Fe高铝青铜合金的室温拉伸伸长率仅为1%[3],极大地制约了该合金的应用。季灯平等[4]和刘景平等[5]采用连续定向凝固方法制备了具有连续柱状晶组织的Cu-12%Al高铝青铜合金(铝含量高于9%的铝青铜,一般称为高铝青铜),发现该合金具有优良的物理和力学性能:室温拉伸伸长率达到20%,是普通铸造高铝青铜合金QAl11-6-6的2.5倍;弹性模量达到168 GPa,比典型的铍青铜QBe2(约120 GPa)提高了40%以上;电导率达到22.2%IACS,远高于QAl9-4、QAl10-3-1.5、QAl10-4-4等合金的电导率[6]。该合金有望发展成为一种新型易加工的高弹高导材料,例如,在导电弹性元件领域作为铍青铜的替代材料具有潜在的应用前景。
由于铝青铜表现出较好的耐腐蚀性能,在船舶、海洋工业和化工领域中具有广泛应用。同时,在腐蚀环境中的应用又推动了铝青铜腐蚀行为和腐蚀机理的研究。到目前为止,铝青铜耐腐蚀性能与腐蚀机理的研究主要集中在铝含量低于9.4%的低铝青铜[7−9],而对高铝青铜合金耐腐蚀性能的研究还远远不足[10−12]。普通铸造方法制备的高铝青铜合金可能由多相组成,不同相之间由于腐蚀电位的不同,会造成选择性腐蚀[11]。而且,不同组织铝青铜合金的腐蚀机理也不相同,例如单相α-铝青铜合金基本不发生脱铝腐蚀,而多相铝青铜则有脱铝腐蚀倾向[13−14]。连续定向凝固技术制备的Cu-12%Al高铝青铜合金具有不同于普通铸造合金的组织形貌(连续柱状晶组织)和相组成,这些特殊的组织特征有效改善了高铝青铜合金的物理和力学性能[4−5,15],但具有连续柱状晶组织的高铝青铜的耐腐蚀性能和腐蚀机理都有待研究。为此,本文作者研究具有连续柱状晶组织的Cu-12%Al合金在20~80 ℃温度范围内,人造海水环境(3.5%NaCl溶液,质量分数)和酸性环境(10%HCl溶液,体积分数)中的耐腐蚀性能和腐蚀机理。
1 实验
1.1 实验材料
实验采用99.9%的纯Cu和纯Al作为原料,采用真空熔炼和氩气保护下拉式连续定向凝固技术制备Cu-12%Al合金线材,具体设备和制备流程见文献[4]。坯料的制备工艺参数如下:熔体温度1 100 ℃,拉坯速度45 mm/min,结晶器长度59 mm,冷却距离8 mm,冷却水温20 ℃,冷却水流量400 L/h。制备出的线材直径为6 mm。采用比色法对坯料化学成分进行分析,Al含量为11.99%(质量分数),其余为Cu。
1.2 静态腐蚀实验
从坯料上截取d6.0 mm×30 mm的圆柱试样进行静态腐蚀实验,实验前采用水磨砂纸将试样工作面打磨至光亮,用乙醇和去离子水经超声清洗,干燥后逐一编号。使用螺旋测微仪对每个试样的直径和高度进行测量,并计算工作面面积;使用精度为0.1 mg的电子天平称量试样初始质量。腐蚀介质为3.5%NaCl溶液和10%HCl溶液,分别采用去离子水、分析纯NaCl和分析纯浓HCl溶液配制。将试样悬挂,放入腐蚀介质中浸泡(腐蚀溶液体积与试样面积的比不小于20 mL/cm2),实验温度分别为20、40、60和80 ℃,实验持续时间为168 h。腐蚀后的试样先用去离子水冲洗,然后用软毛刷去除表面腐蚀产物,再用19%HCl(体积分数)溶液超声波清洗1 min,干燥后称量。按式(1)计算腐蚀速率[16]

其中:D为按深度计的腐蚀速率(mm/a);v=(w0−w1)/(St)为按质量计的腐蚀速率(g/(m2·h)),w0试样的初始质量(g),w1为清除腐蚀产物后试样的质量(g);S为试样的工作面面积(m2);t为腐蚀时间(h);ρ为金属的密度(g/cm3)。
去除表面腐蚀产物后的试样表面形貌观察、横截面观察和成分分析使用带EDAX9100能谱分析仪的S2520扫描电子显微镜(SEM)。将腐蚀后的试样用环氧树脂封装后,使用砂纸打磨掉1 mm左右,抛光后进行横截面观察。
1.3 电化学分析
将坯料加工成尺寸为5 mm×20 mm×4 mm的试样进行电化学分析。实验前用水磨砂纸将试样工作面打磨至光亮,再用蒸馏水及丙酮清洗,干燥后将试样及与仪器连接的导线用704胶封装,有效工作表面积约为1 cm2,封装后再次用蒸馏水及丙酮清洗工作表面,干燥后采用PS−168B型电化学测试系统测定极化曲线,电解池为三电极系统,试样作为工作电极,参比电极为饱和甘汞电极(SCE),辅助电极为铂电极。扫描速率为0.5 mV/s,扫描范围为−700~1 500 mV(相对自腐蚀电位,从负到正)。实验温度为室温 (18 ℃)。所用腐蚀介质与静态腐蚀实验的相同。
2 实验
2.1 定向凝固Cu-12%Al合金的组织
铸态Cu-12%Al合金的组织形貌如图1所示。由图1可知,在本工艺条件下制备的Cu-12%Al合金具有连续柱状晶组织,晶界与凝固方向基本平行,不含横向(与凝固方向垂直)晶界,平均晶粒直径为1 mm左右。对铸态Cu-12%Al合金样品的横截面进行XRD分析表明,合金组织为单一的1β′马氏体相,如图2所示。

图1 定向凝固制备的Cu-12%Al合金的金相组织(SD表示合金铸坯凝固方向,白色箭头为纵向(与凝固方向平行)晶界)Fig. 1 Micrographs of Cu-12%Al alloy fabricated by continuous unidirectional solidification (SD denotes solidification direction, and white arrows point to longitudinal grain boundaries): (a) Cross section; (b) Longitudinal section
2.2 静态腐蚀
连续定向凝固制备的Cu-12%Al合金腐蚀前和在3.5%NaCl和10%HCl溶液中于不同温度下浸泡168 h去除表面腐蚀产物后的表面腐蚀形貌分别如图3和4所示。由图3和4可以看出,随着温度的升高,合金的腐蚀程度不断增加。在10%HCl溶液中试样的腐蚀程度明显比相同温度下3.5%NaCl溶液中的高。
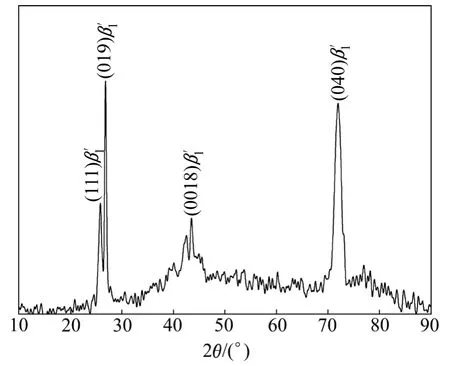
图2 定向凝固Cu-12%Al合金的XRD谱Fig. 2 XRD pattern of Cu-12%Al alloy fabricated by continuous unidirectional solidification

图3 腐蚀前Cu-12%Al合金的表面形貌Fig. 3 Surface morphology of Cu-12%Al alloy before corrosion
对腐蚀后的合金试样采用SEM能谱对其表面成分进行分析,不同腐蚀条件下试样表面Al元素的含量列于表1。由表1可知,腐蚀后,合金组织中的A1元素含量明显降低。随着腐蚀程度的加深,Al元素含量降低。
为了进一步研究合金的脱铝腐蚀行为,对腐蚀后样品的横截面形貌进行观察,发现在两种腐蚀溶液中,当腐蚀发生后,样品表面会形成一层贫铝富铜的表面层,称之为脱铝层,如图5所示。在3.5%NaCl溶液中,不同温度下的脱铝层平均厚度基本相同,约为100 μm,如图5(a)所示。这说明,在中性溶液中,脱铝腐蚀速率随温度变化不明显。在10%HCl溶液中,随温度升高,脱铝层厚度减小,如图5(b)和(c)所示。这说明,在酸性溶液中,随着温度的升高,Cu元素的腐蚀速率明显加快,造成脱铝层变薄。

图4 不同腐蚀条件下Cu-12%Al合金的表面形貌Fig. 4 Surface morphologies of Cu-12%Al alloy under different corrosion conditions: (a) 20 ℃, 3.5%NaCl; (b) 20 ℃, 10%HCl; (c) 40 ℃, 3.5%NaCl; (d) 40 ℃, 10% HCl; (e) 60℃, 3.5%NaCl; (f) 60 ℃, 10%HCl; (g) 80 ℃, 3.5%NaCl; (h) 80 ℃, 10%HCl

表1 不同温度下腐蚀后合金组织中Al元素的含量Table 1 Al contents on alloy surface after corrosion

图5 经腐蚀后Cu-12%Al合金的横截面形貌Fig. 5 Cross-section micrographs of Cu-12%Al alloy after corrosion (Three pictures in right hand of (a) illustrate results of local composition analysis, red and green colors denote Cu and Al, respectively): (a) 60℃, 3.5%NaCl; (b) 20 ℃, 10%HCl; (c) 60 ℃, 10%HCl
将实验数据代入式(1)后可以计算出合金在不同温度下的腐蚀速率,结果如图6所示。由图6可知,当温度由20 ℃上升到80 ℃时,高铝青铜合金的腐蚀速率也随之加快,分别由0.056 mm/a增加到0.12 mm/a (3.5%NaCl)和0.086 mm/a增加到3.20 mm/a (10% HCl)。在3.5% NaCl溶液中,腐蚀速率随温度的上升基本呈线性缓慢上升;而在10%HCl溶液中,当温度低于40 ℃时,腐蚀速率变化较缓,而当温度高于40 ℃,腐蚀速率迅速加快。
2.3 电化学分析
采用PS−168B型电化学测试系统测得Cu-12%Al高铝青铜合金在3.5%NaCl和10%HCl溶液中的极化曲线,结果分别如图7(a)和(b)所示。
由极化曲线可得,Cu-12%Al合金在腐蚀介质中的稳定电位ER(自然腐蚀电位)为−271 mV (vs SCE) (3.5%NaCl)和−333 mV (vs SCE) (10%HCl)。在阴极极化区,从阴极极化曲线可以看出,在不同介质中发生了不同的去极化还原反应。在3.5%NaCl溶液中为溶解氧的去极化还原;而在10%HCl溶液中发生的是H+的去极化还原。在阳极极化区,在实验扫描电位范围内,两种溶液中合金的电化学行为均以阳极溶解过程为主,并存在活化−钝化转换区(图7中曲线AB段,28~78 mV(vs SCE) (3.5%NaCl)、−63~−45 mV(vs SCE) (10%HCl))。在阳极极化区,随着电位的升高,试样表面先发生溶解,生成的腐蚀产物附着在试样表面,对腐蚀的进行有一定的阻碍作用,故电流密度出现先增大后减小趋势;但是腐蚀产物不十分致密,不足以阻挡腐蚀的继续进行,随着电位的升高(B点后),电流密度继续增大。

图6 Cu-12%Al合金腐蚀速率随温度的变化Fig. 6 Variation of corrosion rate of Cu-12%Al alloy with temperature
3 讨论
3.1 连续柱状晶组织Cu-12%Al合金的耐腐蚀性能
由图6中的数据可知,连续定向凝固制备的连续柱状晶组织Cu-12%Al合金在3.5%NaCl溶液中达到腐蚀4级标准中的耐蚀级(0.05~0.5 mm/a)[16],具有较好的耐腐蚀性能。Cu-12%Al合金在40℃以下的10% HCl溶液中的耐腐蚀性能也可以达到耐蚀级,但在40℃以上的10%HCl溶液中的耐腐蚀性能欠佳。

图7 Cu-12%Al合金的极化曲线Fig. 7 Polarization curves of Cu-12%Al alloy in different solutions: (a) 3.5% NaCl; (b) 10% HCl

表2 不同Al含量铝青铜与铍青铜在10%HCl溶液中的耐腐蚀性能比较Table 2 Comparison of corrosion resistance of Al bronze and Be bronze with different Al contents in 10%HCl solution
表2所列为Cu-12%Al合金在10%HCl溶液中耐腐蚀性能与其他牌号的铝青铜合金和铍青铜耐腐蚀性能的比较。可以看出,使用定向凝固方法制备的Cu-12%Al合金比铝含量更低的其他牌号铝青铜和QBe2具有更好的耐腐蚀性能。这主要有如下两个原因:1)连续定向凝固方法能够有效降低铸造组织中的气孔和缩孔等严重影响材料耐腐蚀性能的铸造缺陷,从而改善材料的耐腐蚀性能;2)使用普通铸造方法制备的铝青铜一般由(α+γ2)共析相、β1′相和α相等多种合金相组成。有研究表明,(α+γ2)共析相为优先腐蚀相,而β1′相的耐腐蚀性能较优[10,18],定向凝固方法制备的高铝青铜Cu-12%Al合金组织为单一的β1′相,合金内部无不同合金相引起的电位差,避免了多相组织中选择性腐蚀的发生,从而使合金具有更高的电化学稳定性和更优的耐腐蚀性能。
3.2 连续柱状晶组织Cu-12%Al合金的腐蚀机理
实验过程中发现经3.5%NaCl溶液腐蚀后的试样表面有白色絮状物生成,部分腐蚀产物从表面脱落,形成白色沉淀物,腐蚀后溶液仍为无色。对白色腐蚀产物进行定性分析的结果表明,腐蚀产物为Al(OH)3。用19%HCl溶液去除腐蚀产物后,试样表面呈现纯铜的颜色。这些现象表明:在NaCl溶液中Cu-12%Al合金的Al元素发生了选择性腐蚀,即氧的去极化腐蚀,反应式如下:

由图5(a)可以更清楚地看出,当脱铝腐蚀发生后,合金表面形成了一层贫铝富铜的脱铝层,随着腐蚀的进行,脱铝层不断增厚。富铜的脱铝层在3.5%NaCl中性溶液中具有较好的稳定性,不发生溶解。因此,腐蚀后溶液为无色,较厚的脱铝层能够起到降低腐蚀速率、保护基体的作用。因此,Cu-12%Al合金在NaCl溶液中具有较好的耐腐蚀性能。
经10%HCl溶液浸泡腐蚀后,试样表面呈红色,没有产生腐蚀产物沉淀,溶液呈绿色,试样表面有气泡产生,腐蚀后溶液中含有Al3+和Cu2+。这些现象表明:Cu-12%Al合金在10%HCl溶液中不仅发生了Al元素选择性腐蚀,而且Cu元素也参与了腐蚀反应。与3.5%NaCl溶液中发生的氧去极化腐蚀不同,合金在HCl溶液中发生的是如下氢的去极化腐蚀:

与在3.5%NaCl溶液中一样,由于脱铝反应的发生,合金表面也形成了一层脱铝层(见图5(b)和(c))。但是,富铜脱铝层能够被10%HCl溶液溶解,而且随着温度的升高,溶解速度加快。脱铝层的不断溶解使其对基体的保护作用减弱,腐蚀反应能够不断进行,因此,在10%HCl溶液中,Cu-12%Al合金的耐腐蚀性能较差。
4 结论
1) 高铝青铜Cu-12%Al合金在20~80 ℃的3.5% NaCl溶液中具有较好的耐腐蚀性能,达到耐蚀级。在40 ℃以下的10%HCl溶液中也可达到耐蚀级,但在40℃以上的10%HCl溶液中其耐腐蚀性能欠佳。
2) 高铝青铜Cu-12%Al合金的腐蚀速率随温度的升高而增大,当温度由20 ℃上升到80 ℃时,其腐蚀速率由0.056 mm/a增加到0.12 mm/a (3.5%NaCl)和由0.086 mm/a增加到3.20 mm/a (10%HCl)。
3) 腐蚀发生后,合金组织中的Al含量明显下降,高铝青铜Cu-12%Al合金在3.5%NaCl和10%HCl溶液中均发生脱铝腐蚀。
4) 高铝青铜Cu-12%Al合金在3.5%NaCl和10%HCl溶液中的自腐蚀电位分别为−271 mV (vs SCE)和−333 mV (vs SCE)。
REFERENCES
[1]钟卫佳. 铜加工技术实用手册[M]. 北京: 冶金工业出版社, 2007: 165−180. ZHONG Wei-jia. Utility handbook of copper processing techniques [M]. Beijing: Metallurgical Industry Press, 2007: 165−180.
[2]刘 平, 任凤章, 贾淑果, 等. 铜合金及其应用[M]. 北京: 化学工业出版社, 2007: 84−91. LIU Ping, REN Feng-zhang, JIA Su-guo, et al. Copper alloy and its application [M]. Beijing: Chemical Industry Press, 2007: 84−91.
[3]DAVIS J R. Copper and copper alloys [M]. Ohio: ASM International, 2001: 557.
[4]季灯平, 刘雪峰, 谢建新, 余均武, 李卫河, 荣鸣雷. Cu-12%Al铝青铜线材的连续定向凝固制备[J]. 金属学报, 2006, 42(12): 336−341. JI Deng-ping, LIU Xue-feng, XIE Jian-xin, YU Jun-wu, LI Wei-he, RONG Ming-lei. Preparation of Cu-12%Al Al bronze wires by continuous unidirectional solidification [J]. Acta Metallurgica Sinica, 2006, 42(12): 336−341.
[5]刘锦平, 刘雪峰, 黄海友, 谢建新. 工艺参数对连续定向凝固Cu-12%Al线材表面质量、组织和性能的影响[J]. 北京科技大学学报, 2011, 33(5): 593−599. LIU Jin-ping, LIU Xue-feng, HUANG Hai-you, XIE Jian-xin. Effects of process parameters on the surface quality, microstructure and mechanical properties of Cu-12%Al wires fabricated by continuous unidirectional solidification [J]. Journal of University of Science and Technology Beijing, 2011, 33(5): 593−599.
[6]黄伯云, 李成功, 石力开. 有色金属材料手册[M]. 北京: 化学工业出版社, 2009: 351−370. HUANG Bu-yun, LI Cheng-gong, SHI Li-kuai. Nonferrous metals handbook [M]. Beijing: Chemical Industry Press, 2009: 351−370.
[7]ATEYA B G, ASHOUR E A, SAYED S M. Stress corrosion behavior ofα-aluminum bronze in saline water [J]. Corrosion, 1994, 50(1): 20−25.
[8]STUPNISEK-LISAC E, GALI’C N, GASPARAC R. Corrosion inhibition of copper in hydrochloric acid under flow conditions [J]. Corrosion, 2000, 56(11): 1105−1111.
[9]AL-HASHEM A, CACERES P G, RIAD W T, SHALABY H M. Cavitation corrosion behavior of cast nickel-aluminum bronze in seawater [J]. Corrosion, 1995, 51(5): 331−342.
[10]路 阳, 袁利华, 李文生, 金玉花. 高铝青铜Cu-14%Al-X合金在3.5%NaCl溶液中的腐蚀性能[J]. 机械工程学报, 2005, 14(9): 42−45. LU Yang, YUAN Li-hua, LI Wen-sheng, JIN Yu-hua. Corrosion resistance of Cu-14%Al-X Al-bronze alloy in 3.5%NaCl solution [J]. Chinese Journal of Mechanical Engineering, 2005, 14(9): 42−45.
[11]李文生, 王智平, 路 阳, 袁利华, 徐建林, 魏迪生, 高铝青铜Cu-14Al-X 合金在3.5%NaCl 溶液中的腐蚀行为[J]. 中国有色金属学报, 2006, 16(3): 511−517. LI Wen-sheng, WANG Zhi-ping, LU Yang, YUAN Li-hua, XU Jian-lin, WEI Di-sheng. Corrosion behavior of Cu-14Al-X bronze alloy in 3.5%NaCl solution [J]. The Chinese Journal of Nonferrous Metals, 2006, 16(3): 511−517.
[12]LI Wen-sheng, WANG Zhi-ping, LU Yang, YUAN Li-hua, XIAO Rong-zhen, ZHAO Xu-dong. Corrosion and wear behaviors of Al-bronzes in 5.0%H2SO4solution [J]. Transactions of Nonferrous Metals Society of China, 2009, 19(2): 311−318.
[13]韩 忠, 赵 晖, 林海潮. QAl9-2合金脱铝腐蚀的TEM研究[J]. 中国有色金属学报, 2001, 11(3): 428−432. HAN Zhong, ZHAO Hui, LIN Hai-chao. TEM observation on dealuminification corrosion of QAl9-2 alloy in marine environment [J]. Chinese Journal of Nonferrous Metals, 2001, 11(3): 428−432.
[14]韩 忠, 何毓璠, 林海潮, 赵 晖. QAl-9-2合金在3.5%NaCl溶液中脱合金腐蚀研究[J], 金属学报, 2000, 36(5): 521−524. HAN Zhong, HE Yu-fan, LIN Hai-chao, ZHAO Hui. Study on dealloying corrosion of QAl-9-2 alloy in 3.5%NaCl solution [J]. Acta Metallurgica Sinica, 2000, 36(5): 521−524.
[15]WANG Y, HUANG H Y, XIE J X. Enhanced room-temperature tensile ductility of columnar-grained polycrystalline Cu-12%Al alloy through texture control by Ohno continuous casting process [J]. Materials Letters, 2011, 65(7): 1123−1126.
[16]天华化工机械及自动化研究设计院. 腐蚀与防护手册: 第1卷. 腐蚀理论、试验及监测[M]. 第2版. 北京: 化学工业出版社, 2009: 264. Tianhua Institute of Chemical Machinery & Automation. Handbook for corrosion and protection: Vol.1. Corrosion theory, testing and monitoring [M]. 2nd ed. Beijing: Chemical Industry Press, 2009: 264.
[17]《重有色金属材料加工手册》编写组. 重有色金属材料加工手册(第一分册)[M]. 北京: 冶金工业出版社, 1979: 188−189. Writing Group of Heavy Nonferrous Materials Processing Manual. Heavy nonferrous materials processing manual (Vol.1) [M]. Beijing: Metallurgical Industry Press, 1979: 188−189.
[18]于 辉, 董飒英, 黄国胜, 孙明先, 王廷勇. 铝青铜在3.5%NaCI溶液中的脱成分腐蚀行为[J]. 中国腐蚀与防护学报, 2003, 23(6): 345−349. YU Hui, DONG Sa-ying, HUANG Guo-sheng, SUN Ming-xian, WANG Ting-yong. Corrosion behavior of Al-bronze in 3.5% NaCl solution [J]. Journal of Chinese Society for Corrosion and Protection, 2003, 23(6): 345−349.
(编辑 陈卫萍)
Corrosion behavior of continuous columnar-grained Cu-12%Al alloy in 3.5%NaCl and 10%HCl solutions
HUANG Hai-you, NIE Ming-jun, LUAN Yan-yan, XIE Jian-xin
(Key Laboratory for Advanced Materials Processing, Ministry of Education, Institute of Advanced Materials and Technology, University of Science and Technology Beijing, Beijing 100083, China)
The corrosion resistances and corrosion mechanism of a Cu-12%Al (mass fraction) alloy with continuous columnar-grained (CCG) microstructure fabricated by unidirectional solidification casting were investigated by static immersing tests and electrochemistry analysis in 3.5%NaCl (mass fraction) and 10%HCl (volume fraction) solutions. The results show that the corrosion resistances of the CCG Cu-12%Al alloy in 3.5%NaCl solution can achieve corrosionresistant level. The corrosion resistances in 10%HCl solution at a temperature below 40 ℃ can achieve corrosion-resistant level, however, if the temperature is above 40 ℃, the alloy has poor corrosion resistance in 10%HCl solution. In 10%HCl solution, the corrosion resistance of the CCG Cu-12%Al alloy is superior to that of the conventional Al bronzes with Al content of 5%~11% and QBe2 alloy, but inferior to that of QBe2.15 alloy. The corrosion potentials of the CCG Cu-12%Al alloy are −271 mV (vs SCE) in 3.5%NaCl and −333 mV (vs SCE) in 10%HCl. The content of Al in the surface layer of the alloy significantly decreases after corrosion, which proves that the Cu-12%Al alloy suffers dealuminization corrosion in 3.5%NaCl and 10%HCl solutions.
Cu-12%Al alloy; continuous columnar-grained microstructure; corrosion resistance; dealuminization corrosion
TG142.41
A
国家重点基础研究发展计划资助项目(2011CB606300);国家自然科学基金资助项目(51104015);国家“十二五”科技支撑计划资助项目(2011BAE23B00);中央高校基本科研业务费资助项目(FRF-TP-10-002B)
2011-10-20;
2012-05-25
谢建新,教授,博士;电话:010-62332254;E-mail: jxxie@mater.ustb.edu.cn
1004-0609(2012)09-2469-08

