沙棘籽渣水提物对正常和糖尿病小鼠血糖的影响
王捷思,张 雯,王洁琼,赵 頔,瞿伟菁
华东师范大学生命科学学院,上海 200062
沙棘籽渣水提物对正常和糖尿病小鼠血糖的影响
王捷思,张 雯*,王洁琼,赵 頔,瞿伟菁*
华东师范大学生命科学学院,上海 200062
本文研究了沙棘籽渣水提物(Aqueous extract of seabuckthorn seed residues,ASSR)对正常及糖尿病小鼠血糖、血脂代谢的影响。首先采用ASSR灌胃昆明种小鼠的急性毒性试验评价了ASSR的安全性;继而以250 mg/kg和500 mg/kg剂量的ASSR连续灌胃正常小鼠3周;以250、500和800 mg/kg剂量的ASSR连续灌胃Alloxan诱导的糖尿病小鼠3周,监测血糖,测定体重、血清胰岛素、总胆固醇和甘油三酯水平。结果显示:ASSR的LD50大于9.8 g/kg体重;连续给药3周,ASSR对正常小鼠的血糖和血脂代谢没有明显影响,但能明显降低糖尿病小鼠的血清葡萄糖和甘油三酯水平。上述结果表明:ASSR的LD50大于5 g/kg体重,按WHO急性毒性分级标准属于实际无毒级,其在实验性1型糖尿病小鼠模型上具有降血糖和降甘油三酯活性。
沙棘籽渣水提物(ASSR);急性毒性试验;1型糖尿病小鼠;降血糖作用
沙棘(seabuckthorn)为胡颓子科(Elaeagnaceae)沙棘属的灌木或小乔木。在我国,沙棘林广泛分布在“三北”及西南地区,具有良好的改良土壤和水土保持功能,是西部生态治理的优选植物,同时,沙棘也具有很高的药用价值。
沙棘的主要食用及药用部位沙棘果不仅营养成分丰富,而且是传统藏医及蒙医的习用药材,《中药大辞典》和《中华人民共和国药典》均有收载[1,2]。目前,国内外对沙棘果的生物活性进行了大量研究,研究表明沙棘全果和果肉提取物,果汁,果油和籽油具有增强免疫力,抗氧化,抗菌,抗炎症,抑制肿瘤,治疗高脂血症以及预防肝损伤作用[3]。作为果实的一部分,沙棘籽多被用于榨取重要的药用成分沙棘籽油,籽油榨取后,残渣成为制油工业的弃物,尽管其中仍含有多种活性成分,但未被充分利用。
本课题组前期对沙棘籽渣富含黄酮的醇提部位进行了系列研究,结果表明,沙棘籽渣黄酮在抗氧化、降血糖、调节血脂和降低血压等方面有明显作用[4]。此外,籽渣黄酮还可诱导人肝癌细胞凋亡[5]。沙棘作为传统的藏药和蒙药,其服用方式多为水煎煮入药[2],说明其水提部位为有效部位,具有明显功能。因此,为全面挖掘沙棘籽渣的活性部位和功效,本文研究了沙棘籽渣水提部位对正常及糖尿病动物血糖、血脂代谢的影响。
1 材料
1.1 材料与仪器
1.1.1 沙棘籽渣
沙棘籽渣(seabuckthorn seed residues)由内蒙古宇航人有限公司提供,相应的沙棘籽产于内蒙赤峰,采摘季节为每年11月份。所用沙棘的生药学鉴定由华东师范大学生物学系李宏庆副教授进行,存证标本号为:No.Wang S.Y.2006001,存放于华东师范大学生命科学学院植物标本馆(HSNU)。
1.1.2 沙棘籽渣水提物的制备
沙棘籽渣和蒸馏水按料液比1∶10混合,置于不锈钢容器内,先用武火煮沸,再用文火慢煮40 min,抽滤获取滤液;于滤渣中再加入5倍体积的蒸馏水,煮沸后文火慢煮30 min,抽滤,合并两次滤液,旋转蒸发仪浓缩,冷冻干燥,即得棕色固体物质—沙棘籽渣水提取物干粉(Aqueous extract of seabuckthorn seed residues,ASSR)。按生药比计算,每克沙棘籽渣水提取物干粉相当于10.64 g沙棘籽渣。
1.1.3 试验动物
昆明种远交群小鼠(KM小鼠),体重18~22 g,雌雄各半,由复旦大学医学院实验动物中心提供,合格证号:医动字02-22-1号。动物饲养于学院动物房,处于空气流通,室温23~25℃的环境中。小鼠给予标准实验动物饲料,自由饮水饮食,饲料具体成分为:9.2%水分,22.1%粗蛋白,5.28%粗脂肪,5.20%灰分,4.12%粗纤维,1.24%钙,0.92%磷,0.72%甲硫氨酸和亮氨酸混合物,1.34%赖氨酸和52.0%无氮浸出物。
1.1.4 药品与试剂
四氧嘧啶(Alloxan,Sigma公司产品),盐酸二甲双胍片(Metformin,上海信谊制药厂),格列苯脲(glibenclamide,上海信谊制药厂),酶法血清葡萄糖(serum glucose,Glu)、甘油三酯(triglyceride,TG)、总胆固醇(total cholesterol,TC)测定试剂盒购于上海科欣生物技术研究所;胰岛素(serum insulin,Ins)放免试剂盒购于华西医科大学糖尿病研究所,其余常规试剂为市售分析纯。
1.1.5 仪器
BS210S电子天平(Sartorius),DK-S24恒温水浴锅(上海精宏实验设备有限公司),DHG-9246A烘箱(上海精宏实验设备有限公司),XW-80A旋涡混合器(上海医科大学仪器厂),R1002B型旋转蒸发仪(上海申生科技有限公司),SHB-Ⅲ循环水式真空泵(上海申胜生物技术有限公司),TL-16R台式高速冷冻离心机(上海离心机械研究所),超低温冰箱(Thermo),FD20099D000冷冻干燥机(美国FTS)。
1.2 方法
1.2.1 LD50的测定
按Bliss法进行LD50的测试[6],取健康KM小鼠50只,设4个剂量组,每组10只小鼠,雌雄各半,随机分组。相邻组间给药剂量按1∶0.7等比级数递减,禁食12 h后,1、2、3、4组分别灌胃给予(intragastric,ig)ASSR 6.86 g/kg body weight(B.W.),9.8 g/ kg B.W.,14 g/kg B.W.,20 g/kg B.W.,5组为对照组ig给予等体积蒸馏水。给药后,动物皆在同一条件下喂养,自由饮水饮食,观察7 d。
1.2.2 最大耐受量(Maximum Tolerated Dose,MTD)的测定[6]
取健康KM小鼠20只,雌雄各半,以ASSR最大浓度0.5 g/mL,按小鼠最大给药容积0.5 mL/10g B.W.的药量灌胃,1 d 3次(每次间隔4 h),总给药量9.8 g/kg B.W.(104.27 g生药/kg B.W.)。另取6只KM小鼠,雌雄各半,ig水进行对照。给药后,与上述LD50测定相同条件下,观察7 d,记录动物反应情况。
1.2.3 正常小鼠分组与给药
正常雄性小鼠,随机分为对照组(给予蒸馏水)、Metformin给药组(150 mg/kg B.W.)、ASSR低剂量组和高剂量组,分别给予250,500 mg/kg B.W.剂量的ASSR,每组12只。给药组每天灌胃(ig)给予相应剂量Met和ASSR,对照组ig等体积蒸馏水,每天1次,连续20 d。每5 d监测体重和血糖,20 d时,尾静脉采血,分离血清,测定血清葡萄糖、总胆固醇和甘油三酯的含量。
1.2.4 Alloxan诱导的1型糖尿病模型小鼠制备
正常雄性小鼠适应性饲养3 d,禁食10 h后,随机选取10只为正常对照组(Normal control),其余小鼠根据预试验结果选用170 mg/kg B.W.剂量腹腔注射(ip)灭菌的柠檬酸缓冲液(0.1 mol/L,pH 4.6)配制的4%Allxoan溶液,现配现用。注射Allxoan将引起胰岛素应激性的大量分泌,引发致命的低血糖效应,故而注射后24 h,需向小鼠补充3%的葡萄糖水溶液。5 d后,小鼠禁食6 h,尾静脉采血,分离血清,测定空腹血清葡萄糖含量,血糖值大于15.0 mmol/L的小鼠为成型糖尿病鼠,选择血糖值15.0~25.0 mmol/L的小鼠进行实验。
1.2.5 糖尿病小鼠分组与给药
成型小鼠按血糖值分为5组,每组10只。糖尿病对照组(diabetic control),ig给予蒸馏水;格列苯脲组(glibenclamide),ig给予25 mg/kg B.W.剂量; ASSR低、中、高剂量组,分别灌胃给予250,500和800 mg/kg B.W.剂量的ASSR。4组间血糖平均值差异小于1.0 mmol/L;同时设有正常对照组(Normal control),ig蒸馏水。各组按剂量每天一次性灌胃,正常对照和模型对照组灌胃等体积的蒸馏水,连续3周,每周监测血糖和体重,3周后,各组小鼠禁食10 h,眼窦脉采血并处死,进行血液生化指标分析。
1.2.6 血清生化指标测定
血清中Glu、TC、TG含量按试剂盒说明书方法测定。Ins含量采用放射免疫法测定。
1.3 统计学分析
2 结果
2.1 ASSR的急性毒性试验
按Bliss法预试,观察ASSR小鼠1次灌胃(ig)后所产生的毒性反应和死亡情况。

表1 沙棘籽渣水提物小鼠经口染毒死亡情况Table 1 The mortality rate of mice after ig ASSR in acute toxicity test
由表1可知,除第1组无死亡外,其余组皆有小鼠死亡,但死亡率均低于50%。由于受到ASSR最大浓度和体积限制的缘故,在受试剂量范围内,未能测得Bliss法所要求的小鼠半数组的死亡率P>0.5和另半数组的死亡率P<0.5时的剂量范围,故未能测得ASSR小鼠灌胃的LD50。
鉴于以上情况,我们转而对ASSR的最大耐受量进行了试验,选取9.8 g/kg B.W.作为染毒剂量,结果见表2。

表2 沙棘籽渣水提物小鼠经口染毒最大耐受量情况Table 2 The MTD of ASSR by ig in mice
给予ASSR后,第1 d小鼠自由活动减少,食量下降,出现含ASSR粪便、肛门部位皮毛多污染。第2~3 d后动物的活动、食量、排粪便等皆逐渐恢复正常,与对照组比较,无明显差异。20只受试小鼠中有3只在第1、2 d死亡,解剖发现有2只系其食管及胃受伤(操作造成)所至,另1只死因不明,其余小鼠均未出现明显异常反应,第8 d结束试验,解剖存活小鼠胸、腹腔,肉眼观察其心、肝、脾、肺、肾、肠等脏器,与对照组比较,皆未发现明显病变和差异。根据最大耐受量试验要求,在观察期内,若有个别动物死亡,则可认为该受试物的LD50大于受试物剂量值[6],由此可以推断认为,ASSR的LD50应大于9.8 g/kg B.W.。
2.2 ASSR对正常小鼠血糖的影响
连续灌胃ASSR 20 d的受试小鼠的血糖变化见表3,结果显示各组血糖值无显著差异。
表3 ASSR对正常小鼠空腹血糖的影响(±s,n=12)Table 3 Effect of ASSR on fasting serum glucose level in normal mice(±s,n=12)

表3 ASSR对正常小鼠空腹血糖的影响(±s,n=12)Table 3 Effect of ASSR on fasting serum glucose level in normal mice(±s,n=12)
组别Group 空腹血清葡萄糖Serum glucose(mmol/L) 5 d 10 d 15 d 20 d Control 7.69±2.63 6.04±1.59 7.08±1.49 6.22±1.32 Met(150 mg/kg) 7.77±1.59 7.86±3.43 7.50±1.63 6.73±1.45 ASSR(250 mg/kg) 7.72±1.91 6.45±1.39 6.79±1.87 5.57±1.87 ASSR(500 mg/kg)7.56±0.73 6.85±1.42 7.04±1.25 6.34±1.45
2.3 ASSR对正常小鼠血脂和体重的影响
血清胆固醇和甘油三酯是反映脂代谢的常用综合性生化指标。各组小鼠的体重、血清胆固醇和甘油三酯含量见表4,从结果可见:各组小鼠间血清胆固醇和甘油三酯含量无显著差异。
表4 ASSR对正常小鼠体重和血清甘油三酯和总胆固醇的影响(±s,n=12)Table 4 Effect of ASSR on body weight,serum triglyceride and total cholesterol levels in normal mice(±s,n=12)
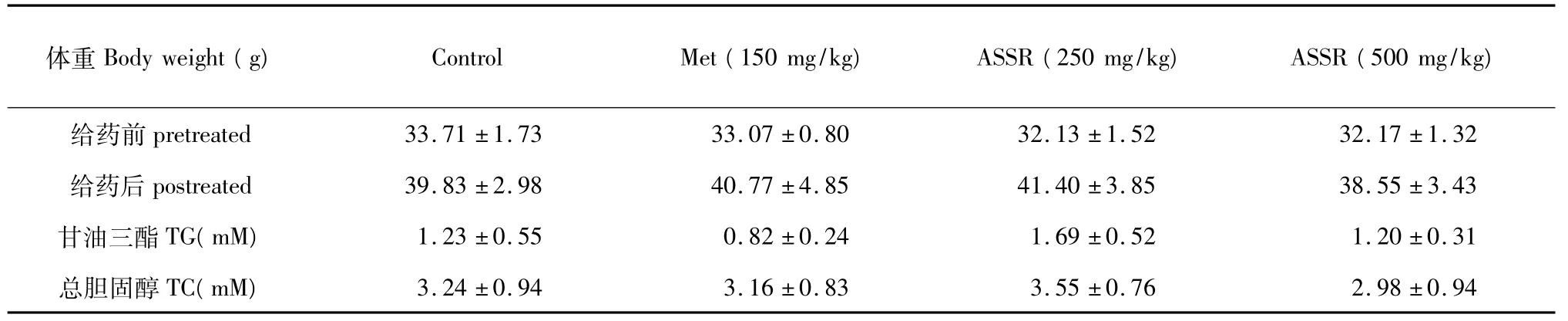
表4 ASSR对正常小鼠体重和血清甘油三酯和总胆固醇的影响(±s,n=12)Table 4 Effect of ASSR on body weight,serum triglyceride and total cholesterol levels in normal mice(±s,n=12)
Control Met(150 mg/kg) ASSR(250 mg/kg) ASSR(500 mg/kg)体重Body weight(g)给药前pretreated 33.71±1.73 33.07±0.80 32.13±1.5232.17±1.32给药后postreated 39.83±2.98 40.77±4.85 41.40±3.85 38.55±3.43甘油三酯TG(mM) 1.23±0.55 0.82±0.24 1.69±0.52 1.20±0.31总胆固醇TC(mM)3.24±0.94 3.16±0.83 3.55±0.76 2.98±0.94
2.4 ASSR对Alloxan诱导的糖尿病小鼠血糖的影响
表5中数据为各实验组小鼠给药前后的空腹血糖水平。由表可见,注射Alloxan后,模型小鼠的血糖水平极显著高于正常小鼠(P<0.01),并在整个实验过程中呈现持续增高的状态,以250,500,800 mg/kg剂量的ASSR连续灌胃2 w后,500 mg/ kg剂量使糖尿病小鼠的血糖显著降低,连续灌胃给药3 w后,3个剂量的ASSR均可显著降低糖尿病小鼠的血糖水平,ASSR高,中,低剂量组的降糖率分别为28.5%,28.5%和20.1%。格列苯脲治疗组在2 w,3 w时血糖值也明显低于模型对照组,降糖率分别为36.0%和18.86%。
表5 ASSR对Alloxan诱导的糖尿病小鼠血糖的影响(±s,n=10)Table 5 Effect of ASSR on fasting serum glucose level in alloxan-induced diabetic mice(±s,n=10)

表5 ASSR对Alloxan诱导的糖尿病小鼠血糖的影响(±s,n=10)Table 5 Effect of ASSR on fasting serum glucose level in alloxan-induced diabetic mice(±s,n=10)
注:与正常对照组相比,aP<0.05,aaP<0.01;与糖尿病模型组相比,bP<0.05,bbP<0.01;下同。Note:Compared with normal control,aP<0.05,aaP<0.01;compared with diabetic control,bP<0.05,bbP<0.01;The same below.
组别Group血清葡萄糖Serum glucose(mmol/L) 0 d 7 d 14 d 21 d Normal control 7.55±1.36bb7.96±1.36bb8.00±1.08bb7.51±1.30bbDiabetic control 18.28±3.25aa23.63±3.37aa26.72±2.42aa29.69±2.69aaDiabetic+Glib 18.37±2.77aa20.54±6.50aa17.10±9.78aab24.09±2.20aabDiabetic+ASSR(250 mg/kg) 18.36±2.70aa19.15±7.07aa22.00±8.14aa23.74±4.33aabDiabetic+ASSR(500 mg/kg) 18.37±2.74aa22.52±3.58aa16.14±9.52aab21.30±6.01aabbDiabetic+ASSR(800 mg/kg) 18.38±2.71aa22.37±5.15aa19.63±9.09aa21.23±6.89aabb
2.5 ASSR对Alloxan诱导的糖尿病小鼠血脂水平和体重的影响
与正常小鼠比较,Allxan诱导的1型糖尿病小鼠的血清甘油三酯水平极显著升高,同时小鼠体重和血清胰岛素水平极显著下降(P<0.01),结果如表6所示,灌胃500和800 mg/kg剂量的ASSR 3 w可显著降低糖尿病小鼠的血清甘油三酯水平(P<0.05,P<0.01)而对体重,血清胆固醇和胰岛素含量无明显影响。灌胃格列苯脲可明显降低(P<0.05)糖尿病小鼠的血清甘油三酯水平并能显著升高小鼠的血清胰岛素含量(P<0.01)。

表6 ASSR对Alloxan诱导的糖尿病小鼠体重、甘油三酯、总胆固醇和胰岛素水平的影响Table 6 Effect of ASSR on body weight,serum TG,TC and insulin levels in alloxan-induced diabetic mice
3 讨论
沙棘作为传统的藏药和蒙药,传统的服用方式多为水煎煮入药[2],说明其水提部位为有效部位,具有明显功能。实验室前期测定发现沙棘籽渣中仍含有多种营养成分,如蛋白,脂肪,维生素C,黄酮,糖和氨基酸等,可见籽渣中含有多种水溶性有效成分,提示水提部位应具有生物活性。在活性评价前,本文首先进行了沙棘籽渣水提部位的安全性评价,按照药物的急性毒性试验方法(Bliss法),未能找出小鼠半数组的死亡率P>0.5和另半数组的死亡率P<0.5时的剂量,故无法用Bliss法测出ASSR小鼠灌胃的LD50。按最大耐受量测定方法,以ASSR最大浓度0.5 g/mL,最大体积0.4 mL/10 g B.W.,1日灌胃3次,总给药量9.8 g/kg B.W.(104.27 g生药/kg B.W.),连续观察7 d,得知ASSR的LD50大于9.8 g/kg B.W.。根据WHO急性毒性分级标准[7],可知沙棘籽渣水提物ASSR毒性甚小,应属于实际无毒级。
本研究结果显示,ASSR对正常小鼠的血糖、血清胆固醇和甘油三酯水平无明显影响,说明ASSR不影响正常生理状态下的血糖和血脂代谢。
四氧嘧啶(Alloxan)是胰岛β细胞毒剂,通过产生超氧自由基破坏β细胞,使之合成前胰岛素减少,分泌减少;并同时破坏或减少胰岛素受体,使胰岛素功能降低,导致糖尿病的发生,产生高血糖、胰岛素缺乏的症状;由于胰岛素缺乏,脂解作用上升,有时甘油三酯和总胆固醇也会出现升高[8]。故而,Alloxan诱导的动物高血糖模型与人类的1型即胰岛素依赖性糖尿病类似,是评价降血糖药物疗效的常用模型[9]。采用这一模型,本研究评价了ASSR对糖尿病小鼠血糖和血脂的影响,结果表明:通过口服途径,ASSR可有效降低Alloxan诱导的1型糖尿病小鼠血清葡萄糖水平,降糖幅度在20% ~29%范围内,具有明显的降血糖活性。高血糖是糖尿病的核心症状[10],目前,对糖尿病治疗的最主要方向还是有效控制血糖水平,ASSR能明显控制糖尿病小鼠的高血糖水平,提示其可能对糖尿病的发展有一定的控制作用。此外,ASSR对糖尿病小鼠的血清胰岛素水平没有明显的影响,表明ASSR不能刺激小鼠胰岛素分泌,因此,ASSR的降血糖作用并非通过刺激胰岛素分泌这一途径来实现,推测可能是通过胰外途径来实现。
糖尿病是代谢相关疾病,尤其和脂代谢的关联最为紧密,对血脂和脂蛋白都有着显著的影响[11]。糖尿病引发的脂质代谢异常是导致动脉粥样硬化和冠心病、脑血管病慢性病变的重要危险因素之一[12,13]。通过饮食和药物治疗来控制血脂水平也是治疗糖尿病及其并发症的一个主要途径[12]。本研究结果表明:ASSR除能有效降低糖尿病小鼠的血糖外,还可明显降低血清甘油三酯水平,具有明显的降血脂功能,可在一定程度上改善糖尿病小鼠的脂代谢紊乱。鉴于糖尿病中脂代谢紊乱与并发症发生发展的密切关联,ASSR改善脂代谢紊乱的功能可能对糖尿病并发症有一定的预防作用。综合上述结果,ASSR具有降血糖的作用,并能改善糖尿病状况下的脂代谢紊乱,其降血糖作用和降血糖机理还需进一步评价和探索。
1 Chinese Pharmacopoeia Committee(国家药典委员会编).Chinese Pharmacopoeia 2000 Ed(Part 1)(中华人民共和国药典:2000年版一部).Beijing:Chemical Industry Press,2000.145.
2 Jiangsu New Medical College(江苏新医学院编).The Dictionary of Traditional Chinese Medicine(Part 2)(中药大辞典(下卷)).Shanghai:Shanghai Science and Technology Press,1986.2602.
3 Deng XJ(邓小娟),Si CS(司传颂),Liu Z(刘忠),et al.Progress of pharmacological research on Hippophae rhamnoides L.Chin Pharm(中国药业),2009,18:63-64.
4 Pang XF,Zhao JJ,Zhang W,et al.Antihypertensive effect of total flavones extracted from seed residues of Hippophae rhamnoides L.in sucrose-fed rats.J Ethnopharmacol,2008,117:325-331.
5 Sun B(孙斌),Zhang P(章平),Qu WJ(瞿伟菁),et al. Study on effect of flavonoids from oil-removed seeds of Hippophae rhamnoides on inducing apoptosis of human hepatoma cell.J Chin Med Mater(中药材).2003,26:875-877.
6 Sun JF(孙敬方).Animal Experimental Methodology(动物实验方法学).Beijing:People’s Medical Publishing House,2002.356-364.
7 Zhang Q(张桥).Basic Toxicology(毒理学基础).Beijing: People’s Medical Publishing House,2003.111-112.
8 Wang DJ(王多佳).Alloxan-induced diabetes and free radical reaction.Inter J Endocrinol Metab(国外医学内分泌分册),1994,14:144-146.
9 Zhang JT(张均田).Modern Pharmacological Experimental Methods(Part 1)(现代药理实验方法(上册)).Beijing: Peking Union Medical College-Beijing Medical University Joint Press,1998.1007-1008.
10 Bell GI.Molecular defects in diabetes mellitus.Diabetes,1991,40:413-417.
11 Pushparaj PN,Low HK,Manikandan J,et al.Anti-diabetic effects of Cichorium intybus in streptozotocin-induced diabetic rats.J Ethnopharmacol,2007,111:430-434.
12 Brown GB,Xue QZ,Sacco DE,et al.Lipid lowering and plaque regression.New insights into prevention of plaque disruption and clinical events in coronary disease.Circulation,1993,87:1781-1791.
13 Jiang GY(蒋国彦).Practical Diabetes(实用糖尿病学).Beijing:People’s Medical Publishing House,1997.5-8.
Effects of Aqueous Extract of Seabuckthorn Seed Residues on Blood Glucose in Normal and Alloxan-induced Diabetic Mice
WANG Jie-si,ZHANG Wen,WANG Jie-qiong,ZHAO Di ,QU Wei-jing*
School of Life Science,East China Normal University,Shanghai 200062,China
In present study,the effects of aqueous extract of seabuckthorn(Hippophae rhamnoides L.)seed residues (ASSR)on serum glucose and lipid profiles in normal and alloxan-induced diabetic mice were investigated.To evaluate the safety of ASSR,we observed the acute toxic reaction of mice after intragastric administration of ASSR.Then,ASSR were orally administered to normal(250 and 500 mg/kg)and diabetic mice(250,500 and 800 mg/kg)once a day lasting for 3 weeks,and the change of serum glucose,insulin,total cholesterol,triglyceride and body weight were observed to examine the effects of ASSR on serum glucose and lipid profiles.Results showed that the LD50of ASSR was higher than 9.8 g/kg body weight(B.W.).Oral administration of the extract once a day for 3 weeks significantly lowered fasting serum glucose and triglyceride levels in diabetic mice,and no effect was seen in normal mice both in serum glucose and lipids levels.These results indicated ASSR has no obvious acute toxicity and possessed significant hypoglycemic and hypotriglyceridemic effects in alloxan-induced diabetic mice.
aqueous extract of seabuckthorn(ASSR);acute toxic reaction;type 1 diabetic mice;hypoglycemic effect
Q949.329;R587.1
A
1001-6880(2012)05-0599-06
2011-04-07 接受日期:2011-06-22
*通讯作者 Tel:86-21-54341011;E-mail:wzhang@bio.ecnu.edu.cn

