高效液相色谱法测定一次性使用输液器中DEHP溶出量
刘曦 于晶晶 王红 刘嘉馨 中国医学科学院 北京协和医学院 输血研究所 (成都 610052)
高效液相色谱法测定一次性使用输液器中DEHP溶出量
刘曦 于晶晶 王红 刘嘉馨
中国医学科学院 北京协和医学院 输血研究所 (成都 610052)
以乙醇水溶液作为浸提液,模拟临床使用条件,建立高效液相法(HPLC)测定一次性使用输液器中邻苯二甲酸二(2-乙基)己基酯(DEHP)溶出量的方法,为制定聚氯乙烯(PVC)医疗器械产品中增塑剂DEHP溶出量检测标准提供实验依据。
一次性使用输液器 HPLC 增塑剂 DEHP
1. 前言
邻苯二甲酸二(2-乙基)己基酯(DEHP)是聚氯乙烯(PVC)类一次性使用输液器中最具代表性的增塑剂,被广泛使用。DEHP与PVC分子之间仅以范德华力和氢键相连,在临床使用过程中,DEHP会从PVC输液器中迁移出来,伴随药物输注进入人体。近年相关研究表明,DEHP具有慢性毒性[10~11],人体内的长期累积会影响肌肉骨骼系统和中枢神经系统[1]、肝脏组织[2],特别是男性生殖健康[3]。因此,美国FDA在其发表的关于DEHP增塑PVC医疗器械安全性评价的研究报告[4]中,提出要重视和监控医疗器具中DEHP的释放。鉴于此,本文建立了测定一次性PVC输液器中DEHP溶出量的高效液相色谱法(HPLC)。
2. 材料与方法
2.1 试剂与仪器
95%乙醇(成都科隆化学试剂公司,AR),甲醇(国药化学试剂公司,色谱纯),DEHP标准品(山东宏信化工股份有限公司,纯度≥99.5%),纯水/超纯水系统(美国Pall,Cascada),旋转蒸发仪(德国IKA,RV10),紫外/可见光分光光度计(美国Beckman,DU800),高压液相色谱(美国Waters,e2695-2489),国产一次性使用输液器(批号:20110511 09)。
2.2 浸提液的制备
按照GB14232.1-2004中醇溶出物测定要求,用95%乙醇和超纯水,通过液体比重天平测定并配制2000m L密度为(0.9373~0.9378)g/m l的乙醇水混合液作为浸提液。
2.3 色谱条件
检测器:紫外/可见光检测器,检测波长n=272nm;色谱柱:Sunfire C18,5.0 μm,4.6mm×150mm;柱温:室温;流动相:甲醇(色谱纯);流量:1.0m l/m in;进样量:5μl。
2.4 方法学研究
2.4.1 DEHP 特征吸收波长的选择
精密称取DEHP标准品 2.0010 g,用甲醇稀释至100m l,得到浓度为20.01 m g/m l的标准储备液。取标准储备液,用甲醇稀释 200倍,得到0.10mg/m L的标准工作溶液,用紫外/可见分光光度计在190nm~1100nm范围内进行扫描,根据吸收光谱曲线确定HPLC检测波长(n)。
2.4.2 DEHP保留时间的确定
取DEHP标准储备液,用甲醇稀释得到一定浓度的标准工作溶液,在2.3色谱条件下进样测量,得到DEHP的出峰保留时间。
2.4.3 标准曲线的绘制
取DEHP标准储备液用甲醇逐级稀释,得到2001ug/m l~5ug/m l浓度的标准溶液,按照2.3中色谱条件进样测定,得到各浓度的峰面积值。 以峰面积值(Y)为纵坐标,DEHP浓度(X)为横坐标,绘制DEHP标准曲线并得到线性回归方程。
2.4.4 灵敏度试验
取DEHP标准储备液用甲醇逐级稀释,得到一系列浓度的标准工作溶液,按照2.3 色谱条件进样测定,将信噪比≥100的最小DEHP浓度定为定量检测限。
2.4.5 精密度试验
取DEHP标准储备液用甲醇逐级稀释,得到浓度为 1500 µg/m l~5 µg/m l的标准工作溶液,按照2.3色谱条件进样测定,每种浓度样品连续进样测定5次,得到其峰面积,计算变异系数(RSD),进行测量值的精确度表征,考察结果重复性。
2.4.6 加标回收率
准确吸取3份浸提液各1m l,与浓度分别为2000ug/m l、1000ug/m l、500ug/m l 各1m l DEHP标准工作液均匀混合,得到高、中、低三种浓度的加标回收样品溶液,用旋转蒸发仪蒸干,冷却至室温,残余物用4m L甲醇涡旋溶解后得到样品检验液,静置数分钟后吸取上清,按2.3色谱条件对每个加标回收样品检验液测定3次,计算回收率(%)和变异系数(RSD)。
2.5 供试液的制备及测定
将配制好的乙醇水浸提液用胶塞玻璃瓶分装(500m l/瓶,共4瓶,),悬挂于输液架上,取出输液器样品,模拟临床操作和条件,调节流速在2.5~3.0m l/m in范围内(流速上限),收集全部流出液作为供试液1;重复上述操作,调节流速在0.5~1.0m l/m in范围内(流速下限),依次对每瓶浸提液进行输注,收集全部流出液作为供试液2。
将上述供试液分别用旋转蒸发仪蒸干,冷却至室温,残余物用4m L甲醇涡旋溶解后得到样品检验液,静置数分钟后吸取上清,按2.3色谱条件进样测定得到峰面积值,将其代入相应线性回归方程即得DEHP浓度(C,ug/m l),按下式换算每套输液器的DEHP溶出量(M,mg/套):
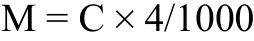
3.结果与讨论
3.1 DEHP 特征吸收波长的确定
如图1所示,DEHP在190nm处有饱和键(C-C)吸收峰、202~238nm处有不饱和键(C=C、C=O)和杂原子饱和键(C-O-C)的吸收峰,在272nm处有苯环特征吸收峰。因此,以272nm作为HPLC的检测波长。
3.2 DEHP 出峰保留时间
见图2。
3.3 供试液制备方法的选择
已有不少研究[2~3],[5~8]对供试液的制备采用的是截取产品某一部分,对其进行浸泡和萃取的方式。这种方法在产品的质量控制评价方面是可行的[5~8],但通过这种方法测得的DEHP溶出量却难以反映产品临床实际使用时的风险[2~3],因为产品使用时与浸提液的接触是动态过程,而浸泡方法是静态过程,这两种浸提过程对DEHP的浸提能力会有较大区别。另外,产品使用时与浸提液的接触是整个内腔而不是局部,所以局部浸提的结果不能反映产品使用的真实情况。因此本研究采用模拟临床使用条件的供试液制备方法。
再者,输液药物分为晶体液类(生理盐水、葡萄糖等)和脂类药物。已有安全性评价结果显示[12],DEHP在与晶体液接触时溶出极少,其进入人体的含量对人体几乎没有危害。而DEHP与脂类药物接触时却容易溶出。所以我们只针对一次性使用输液器输注脂类药物时DEHP溶出量进行研究。乙醇水溶液是脂类溶剂,可替代脂类药物作为本研究的溶出检测液。
同时针对一次性使用输液器的使用要求,流速一般为0.5m l/m in~3m l/m in,本研究分别选择了0.5~1.0m l/m in和2.5~3.0m l/m in两种流速,全面考察此产品的DEHP溶出量。
3.4 DEHP标准曲线的测定
由图3可知,线性回归方程1:Y = 828.32X +22000,相关系数r=0.9986,结果显示DEHP浓度在2001ug/m l~5ug/m l范围内与其峰面积值线性关系良好。
由于2001ug/m l~5ug/m l的线性相关范围较宽,在确定一次性输液器中DEHP溶出量时会存在较大误差,因此把整个浓度范围划分为高、低2个浓度等级,即2001ug/m l~100ug/m l和250ug/m l~5ug/m l,分别在各自范围内得到标准曲线和线性回归方程,如下:

图1 . DEHP吸收光谱(190nm~400nm)

图2 . DEHP 的HPLC 保留时间
图4、图5显示,线性回归方程2:Y = 804.71X+53814,相关系数r = 0.9982;线性回归方程3:Y = 924.42X + 5588.6,相关系数r = 0.9991。结果显示DEHP浓度在2001ug/m l~100ug/m l和250ug/m l~5ug/m l范围内与其峰面积值线性关系良好。
3.5 方法灵敏度
由表2可知,本方法的DEHP定量检测限为0.5ug/m l。
3.6 方法精密度
见表3,RSD均<5%,表明此方法在较宽的线性范围内具有良好的精密度。
3.7 加标回收率结果

图3 . DEHP标准曲线1(浓度范围:2001ug/m l~5ug/m l)
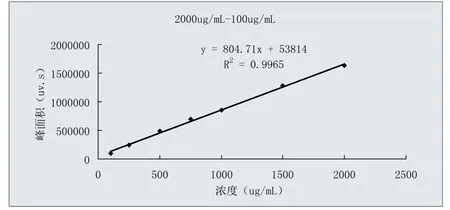
图4 . DEHP标准曲线2(浓度范围:2001ug/m l~100ug/m l)
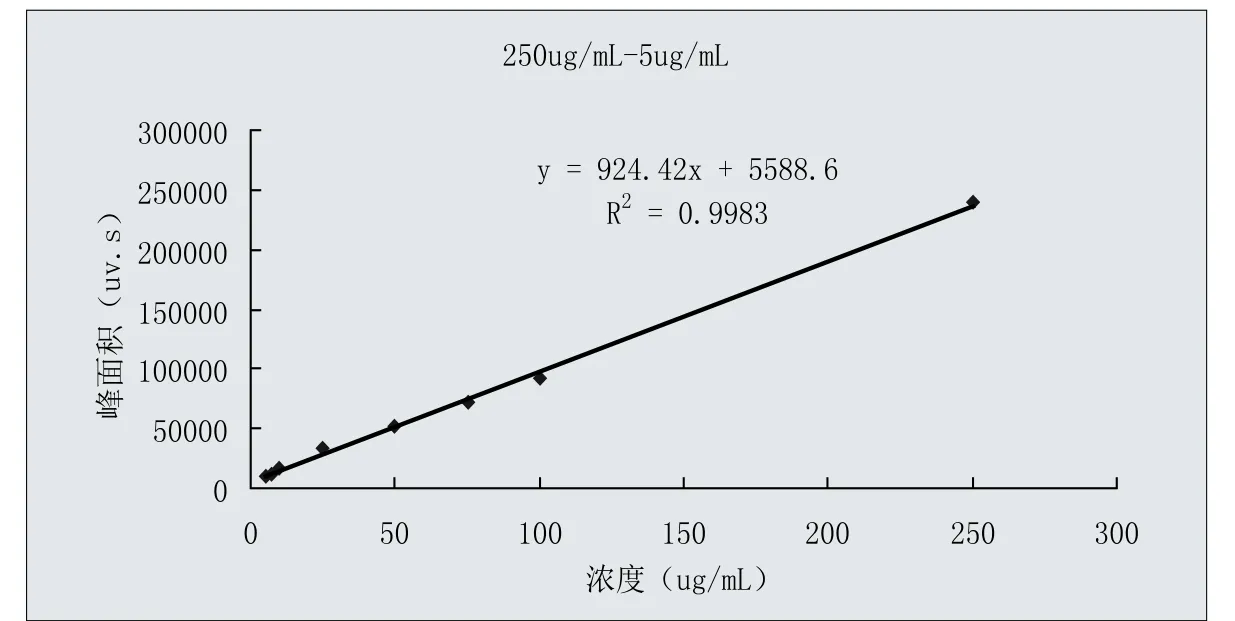
图5 . DEHP标准曲线3(浓度范围:250ug/m l—5ug/m l)
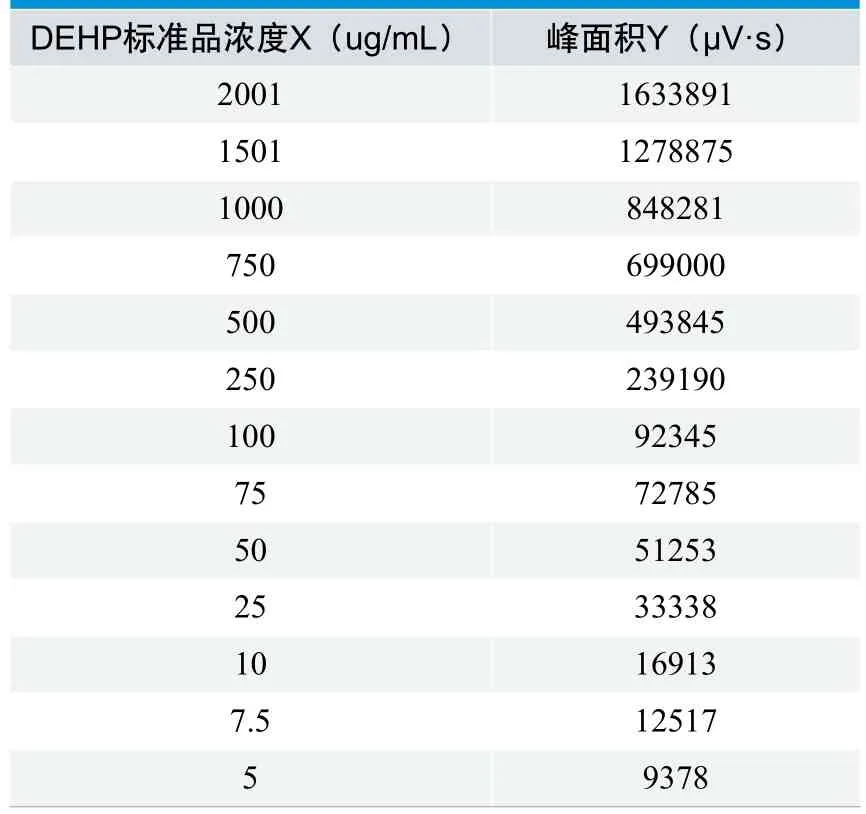
表1 . DEHP标准溶液浓度对应峰面积值
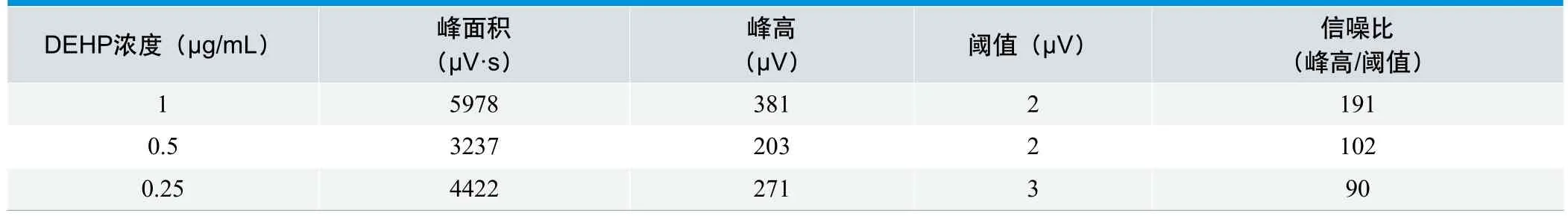
表2 . 信噪比临界100的DEHP标准工作液浓度
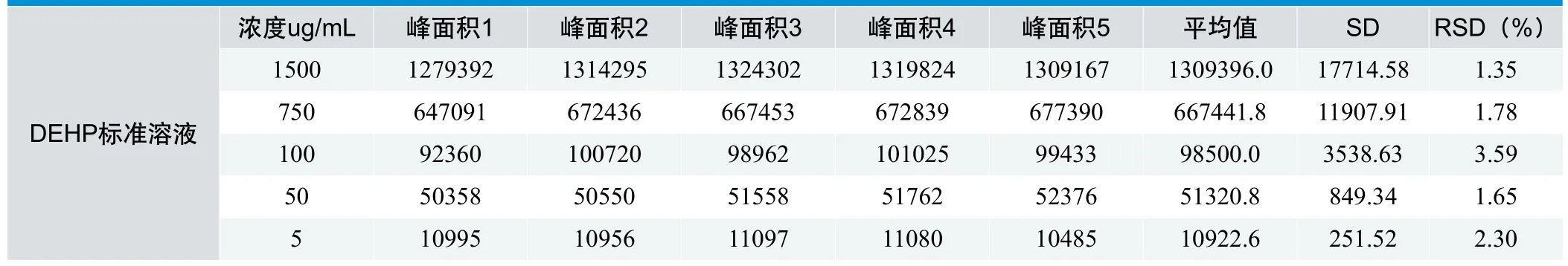
表3 . 精密度试验结果
加标回收率测定考察的是供试液制备和处理以及仪器测试过程中待测目标物的前处理情况,以此来衡量测试方法的可行性。回收率一般在90%~110%之间比较合适[9]。结果见表4,本方法回收率均在98%~103%之间,RSD均<5%,说明采用的测量方法准确度高,精确度好。
3.8 一次性使用输液器样品DEHP溶出量测定
见图6、图7,由样品检验液1和2的 DEHP色谱图及其峰面积,对比DEHP标准曲线,认为较适用的是2001ug/m l~100ug/m l范围内的线性回归方程2,据此计算出样品检验液1和2中的DEHP浓度(n=3),见表5。
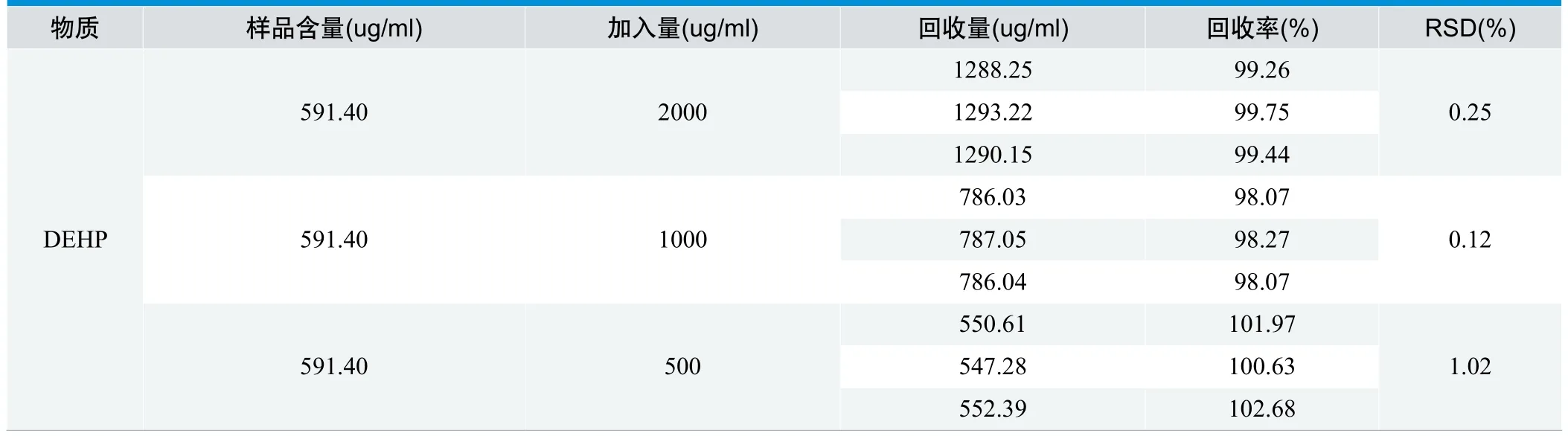
表4 . DEHP 加标回收率和精密度
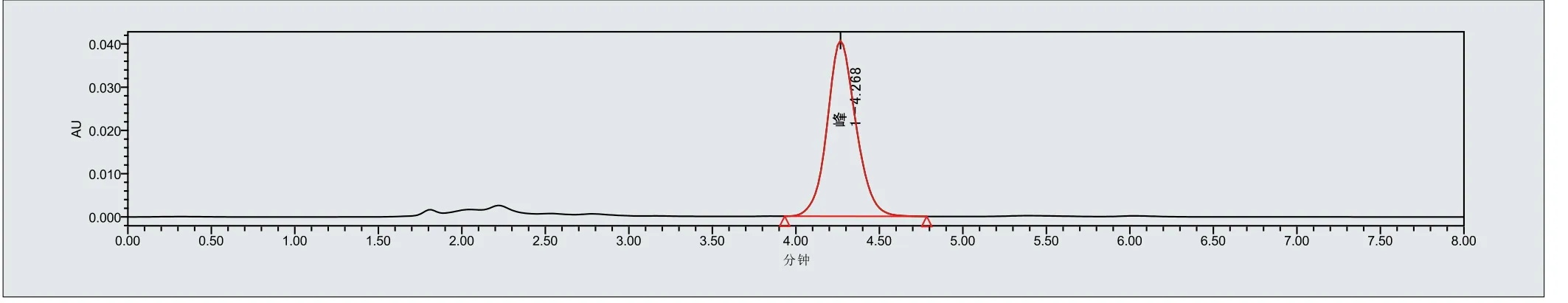
图6 . 样品检验液1 中DEHP色谱图例
图7 . 样品检验液2 中DEHP色谱图例
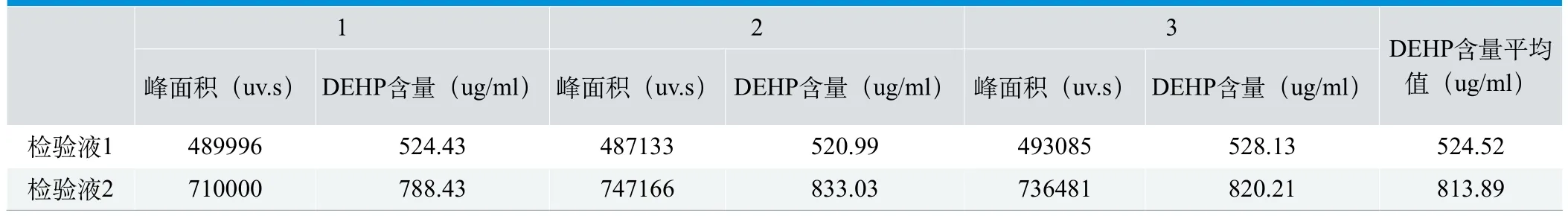
表5 . 样品检验液中DEHP含量测定结果
以2.5~3.0m l/m in的流速用此一次性使用输液器进行输注,在本试验条件下每套产品DEHP溶出量(mg)为:524.52×4/1000=2.10
以0.5~1.0m l/m in的流速用此一次性使用输液器进行输注,在本试验条件下每套产品DEHP溶出量(mg)为:813.89×4/1000=3.26
DEHP的溶出量与浸提液的接触时间成正比。2.10mg的溶出量是在临床输注流速上限的情况下测得,浸提液与输液器的接触时间较短,可视为最小溶出量;而3.26g的溶出量是在临床输注流速下限的情况,浸提液与输液器的接触时间较长,属于极限浸提,可视为最大溶出量。所以,此一次性使用输液器在临床使用输注脂类药物时的DEHP溶出量应在2.10mg~3.26mg之间。这个数值范围可作为本类产品DEHP风险分析的参考数据。
4.结论
本试验证明,高效液相色谱法(HPLC)在2000ug/m l~5ug/m l的较宽DEHP浓度范围保持良好的线性关系。不同规格、不同厂家的一次性使用输液器以及不同类型的PVC医疗器械产品,在临床使用过程中DEHP溶出量可能相差较大,HPLC标准曲线的较宽线性范围则能很好地适应产品特点,有利于确保检测的可靠性。同时精密度和回收率试验也表明此方法准确度高、精确度好且操作简单、分析快速,易于推广。
在我国的医疗器械分类监管中,其相关的国家和行业标准中并没有针对临床实际使用条件下PVC医疗器械产品中的DEHP溶出指标的限量要求和统一方法。因此,为更好地保护患者的身体健康,应尽可能地在相关产品标准上体现这一点。
[1] 胡晓宇,张克荣,孙俊红等. 中国环境中邻苯二甲酸酯类化合物污染的研究. 中国卫生检验杂志, 2003, 13 (1) : 9.
[2] 郑涤新,耿媛媛,王婕等. 导管类医疗器械DEHP检测方法辨析.化学工程与装备, 2010,6:175-176.
[3] 唐云华, 麦伟忠, 曾戎等. 体外循环管道PVC增塑剂浸出量的测定及对比. 广州化工, 2011, 39(8):92-93.
[4] US FDA(2002): Safety assessment of di(2-ethylhexyl)phthalate(DEHP) released from PVC medical devices[R].
[5] 印晖,金念祖。 紫外分光光度法测定一次性使用体外循环管道中DEHP溶出量. 药物鉴定, 2006,15(14):9—10.
[6] 葛海生,刘元瑞,汪 杰. 气相色谱法测定PVC输液袋中DEHP的含量. 武警医学, 2006,17: 97-98.
[7] 周志明,毛明英,周 冕. PVC制品中增塑剂DEHP含量的测定. 塑料科技, 2008,36(11):82-85.
[8] 朱九群, 兰婉玲, 张罗红. HPLC测定PVC输液袋中的邻苯二甲酸二(2 - 乙基己基)酯. 华西药学杂志, 2009,24(3):318-319.
[9] KUMAR N, VERMA N, SONGH O, et al. Estimation of A tenolol by Reverse Phase High Performance Liquid Chromatography. Journal of Chemistry. 2010, 7(3): 962- 966.
[10] H. M. Koch, R. Preuss, J. Angerer. Di(2-ethylhexyl)phthalate (DEHP): human metabolism and internal exposure – an update and latest results. International Journal of Andrology. 2006, 29(1): 155-165.
[11] Holger M Koch, Bernd Rossbach, Hans Drexler, et al. Internal exposure of the general population to DEHP and other phthalates—determination of secondary and primary phthalate monoester metabolites in urine. Environmental Research. 2003, 93(2):177-185.
[12] 奚廷斐 王春仁. 邻苯二甲酸二异辛酯增塑聚氯乙烯医疗器械的安全性评价. 《中国医疗器械信息》2005, 11(2): 27-30.
参考文献
[1] GB 9706.1-2007 《医用电气设备 第1部分:安全通用要求》
[2] YY 0649-2008 《高电位治疗设备》
Determ ination of DEHP Released from Transfusion Instrum en t for Single Use by HPLC
LIU Xi YU Jing-jing WANG Hong LIU Jia-xin
Institute of Blood Transfusion, Chinese Academy of Medical Sciences (Chengdu 610052)
We used ethyl alcohol-water as leaching medium, simulating clinical operation, to develop the HPLC for determination of DEHP released from transfusion instrument for single use, in order to give the experimental foundation for establishing the test standard of the plasticizer DEHP release of PVC medical instrument. Key words: transfusion instrument for single use, HPLC, plasticizer, DEHP
1006-6586(2012)05-0029-06
R197.39
A
2011-12-02
刘曦,实习研究员;王红,通讯作者,助理研究员