纳米磁性膨润土复合材料表征及降解甲基橙研究
李文兵,张玉佳,张 秀,王 娟,姜 露,朱亦男,王光华
(1.武汉科技大学煤转化与新型炭材料湖北省重点实验室,湖北武汉,430081;2.武汉科技大学化学工程与技术学院,湖北武汉,430081)
纳米磁性膨润土复合材料表征及降解甲基橙研究
李文兵1,2,张玉佳2,张 秀2,王 娟2,姜 露2,朱亦男2,王光华1,2
(1.武汉科技大学煤转化与新型炭材料湖北省重点实验室,湖北武汉,430081;2.武汉科技大学化学工程与技术学院,湖北武汉,430081)
以纯化膨润土为原料,通过铁盐与膨润土浆液反应制备非均相纳米磁改性Fe3O4/膨润土复合材料,研究其对甲基橙的降解性能。结果表明,纳米磁性颗粒以Fe3O4附载于膨润土上形成磁性集合体,其对甲基橙废水等温吸附符合Langmuir等温吸附模型。在p H为7、温度为25℃、纳米磁性膨润土投加量为1 g/L、H2O2投加量为2.5 mmol/L、降解时间为120 min条件下,对模拟甲基橙废水降解率达96%,CODCr去除率为94.7%,色度去除率为88.8%。
纳米磁性膨润土;降解;Fe3O4;废水回用
工业废水中由芳烃类有机物引起的COD和色度用常规物理和化学方法处理效果较差[1-3],处理该类有机物的一种高级氧化技术是用活性自由基将其降解为二氧化碳和水[4]。有关均相Fenton反应高级氧化技术处理有毒害污染物的报道较多[5-7],但其存在p H适用范围窄、催化剂回收困难造成二次污染、活性低、成本较高等缺点[8]。因此,高活性、低成本、环境友好、非均相类Fenton催化剂技术成为当前最具应用潜力的高级氧化技术。
近年来,磁性纳米技术在环境修复领域受到广泛关注,磁性纳米颗粒不仅能吸附和催化降解污染物,还可在外加磁场作用下分离回收利用。纳米磁催化剂主要用于针铁矿(α-FeOOH)[9]和磁赤铁矿(γ-Fe2O3)[10],而用于磁铁矿(Fe3O4)的较少[11]。研究发现,纳米磁铁矿的催化性能在铁氧类催化剂中最好[9-12],具有类过氧化氢酶作用。膨润土具有良好的离子交换性、吸附性和高比表面积,铁盐改性后的膨润土可用于芳烃类有机废水处理[13-15],但存在液固分离困难和二次污染问题。而膨润土负载纳米Fe3O4用于处理难降解芳烃的报道很少。为此,本文以廉价的纯化膨润土为载体,通过铁盐与膨润土浆液反应制备非均相纳米磁改性Fe3O4/膨润土复合材料,并对纳米催化材料进行表征;以甲基橙为目标污染物,通过模拟试验,研究纳米磁性膨润土对甲基橙模拟废水的降解效果。
1 试验
1.1 原料
膨润土取自河南信阳,采用沉淀法进行纯化处理,筛选粒径小于10μm的纯化膨润土;三氯化铁(FeCl3·6H2O)、硫酸亚铁(FeSO4·7H2O)和氢氧化钠均为分析纯;模拟甲基橙废水溶液(200 mg/L)。
1.2 纳米磁性膨润土制备
将2 g膨润土溶解于100 m L蒸馏水,加入十六烷基三甲基溴化铵(CTAB)阳离子表面活性剂溶液(0.5 g,50 m L),混合后在70℃温度下高速搅拌,反应1 h;按n(FeSO4·7 H2O)∶n(FeCl3·6H2O)=2∶3的比例,将硫酸亚铁和三氯化铁溶于100 m L蒸馏水中,再加至CTAB-膨润土混合溶液中,在氮气保护下,于70℃高速搅拌10 min,搅拌时逐滴加入1 mol/L的NaOH溶液,沉淀物的颜色由棕色逐渐变为黑色,混合溶液p H为11时停止滴加。再将混合液于70℃搅拌1.5h,停止搅拌后在50℃水浴中晶化1 h。在外加磁场作用下,沉淀物与溶液分离,将上层清液移除,将所得到固体分别用蒸馏水和无水乙醇清洗4次,然后在80℃下干燥12 h,研磨,过200目筛,即制得纳米磁性膨润土复合材料(NMB)。
1.3 纳米磁性膨润土表征
用理学Rigaku D/MAX-RB转靶型X射线衍射仪进行粉体物相分析,扫描半径为3°~70°,Cu靶,Kα(λ=0.154 056 nm,U=40 k V,I=50 m A)。用FEI Nava 400 Nano扫描电镜进行SEM分析。用BRUKER VERTEX70型傅里叶变换红外光谱仪进行FT-IR分析,溴化钾压片,扫描范围4 000~500 cm-1。
1.4 等温吸附
取0.05 g纳米磁改性膨润土和不同浓度的废水溶液,配制50 m L混合液,在25℃恒温下,以150 r/min搅拌1.5 h,吸附平衡后,再在25℃以3 000 r/min离心20 min;准确移取上清液5 m L进行分析,以下式计算吸附量:

式中:Q为吸附量,mg/g;V为溶液体积,L;C0和Ce分别为吸附前和吸附平衡时的浓度,mg/L;m为纳米磁改性膨润土质量,g。
1.5 降解处理
向浓度为200 mg/L的废水中加入纳米磁性膨润土,在25℃温度下,以150 r/min搅拌1.5 h,吸附平衡后加入H2O2,搅拌均匀后调至一定的p H值,此时降解反应开始进行并计时,反应至残留的H2O2消失,将反应液以5 000 r/min离心30 min,取 上清液进 行底物[16]、色 度[17]和CODCr
[18]测定。膨润土对甲基橙的降解率为(1-Ct/C0)×100%,其中Ct为吸附t时刻的浓度。
2 结果与讨论
2.1 两类膨润土晶相分析
膨润土和纳米磁性膨润土XRD图谱如图1所示。由图1可知,与JCPDS标准Fe3O4卡相比较,纳米磁性膨润土为尖晶石结构Fe3O4矿物。经谱峰拟合,结合Scherrer公式,得出纳米磁性膨润土中Fe3O4的平均晶体粒径为1 6 nm。图1(b)中2θ角为35.62°处的特征峰较图1(a)中相应峰尖锐,这是由于膨润土表面结合Fe3O4的特征峰叠加所致,图1(b)中,2θ=43.26°、53.56°、5 7.12°处均出现了Fe3O4特征峰,且未见Fe2O3特征峰,表明与膨润土结合的铁是以Fe3O4形态存在,这正是改性膨润土具有磁性的原因所在[19]。
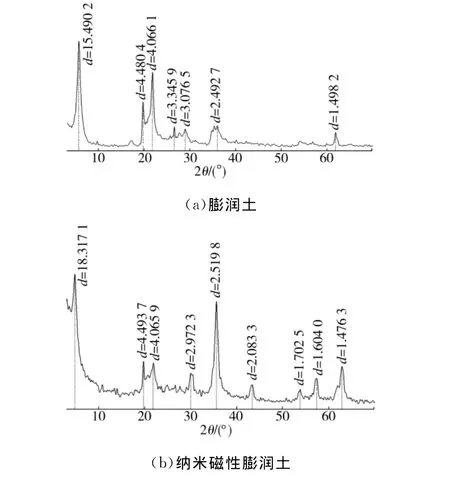
图1 膨润土和纳米磁性膨润土XRD图谱Fig.1 XRD patterns of the refined bentonite and nanomagnetic-bentonite
2.2 两类膨润土显微组织
膨润土和纳米磁性膨润土的SEM照片如图
2所示。从图2中可看出,膨润土颗粒结构紧密,

图2 膨润土和纳米磁性膨润土SEM照片Fig.2 SEM images of refined bentonite and nano-magneticbentonite
表面平整,几乎看不到孔隙;而纳米磁改性膨润土颗粒疏松,表面有明显的刻蚀痕迹,经磁改性后的纳米磁性膨润土表面凹凸不平,并分布有许多颗粒,其原因是合成的Fe3O4粒子附于膨润土矿物表面所致。
2.3 两类膨润土的FT-IR分析
膨润土和纳米磁性膨润土红外光谱如图3所示。从图3中可看出,膨润土和纳米磁性膨润土的红外光谱均出现典型的膨润土吸收峰,表明改性过程中膨润土基本骨架无明显变化。在3 410~3 430 cm-1附近出现的较宽吸收峰属于蒙脱石层间吸附水的羟基伸缩振动吸收峰;1 6 3 0~1 640 cm-1附近吸收带为层间吸附水的羟基弯曲振动吸收峰;1 038 cm-1附近出现的宽而长的吸收峰归属于蒙脱石晶格中八面体Si—O—Si的伸缩振动吸收峰;520 cm-1处为Si—O—Al的弯曲振动吸收峰;470 cm-1处吸收带为Si—O—Si弯曲振动吸收峰;图3(b)中未出现新的吸收峰,表明在制备纳米磁性膨润土过程中,Fe3O4颗粒未与膨润土中的矿物形成新的化学键。由于纳米微粒具有较高的表面能及膨润土中主要矿物存在固有电荷[20],使得纳米Fe3O4通过静电引力负载于膨润土矿物颗粒表面,从而形成纳米磁性膨润土。
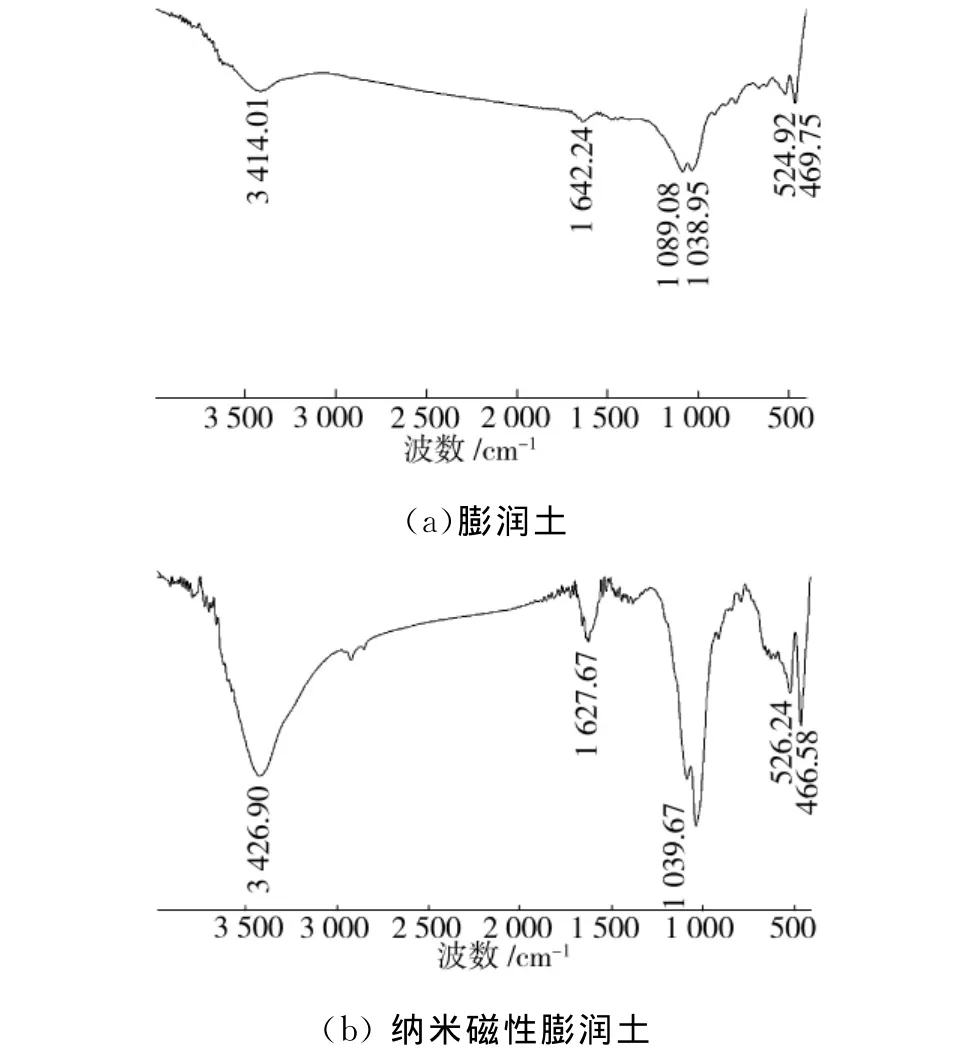
图3 膨润土和纳米磁性膨润土FT-IR光谱Fig.3 FT-IR spectra of refined bentonite and nano-magnetic-bentonite
2.4 纳米磁性膨润土对甲基橙的等温吸附
纳米磁性膨润土对模拟废水甲基橙等温吸附(25℃暗室)曲线如图4所示。从图4中可看出,纳米磁性膨润土对甲基橙平衡吸附量随甲基橙浓度增大而增加,根据Giles分类法[21],该等温吸附曲线符合L型等温吸附模型,表明纳米磁性膨润对甲基橙表现出较好的吸附能力。采用Langmuir和Freundlich等温吸附模型拟合,得如下等温吸附方程:

式中:qe为平衡吸附量,mg/g。
改性使膨润土表面引入了金属离子(如铁离子),从而增加了改性膨润土对带异种电荷分子的吸引力[22];此外,膨润土中还引入表面外含有较多Fe—OH基团的纳米Fe3O4颗粒,因而增加了改性复合材料的比表面积,同时也提高了其对极性分子的吸引力[23]。因此,经过纳米磁改性所制复合材料具有有效吸附模拟废水甲基橙的能力。上述模型结果显示,Freundlich拟合方程中R2值小于Langmuir拟合方程中R2值,表明纳米磁性膨润吸附甲基橙用Langmuir方程拟合较为合适。
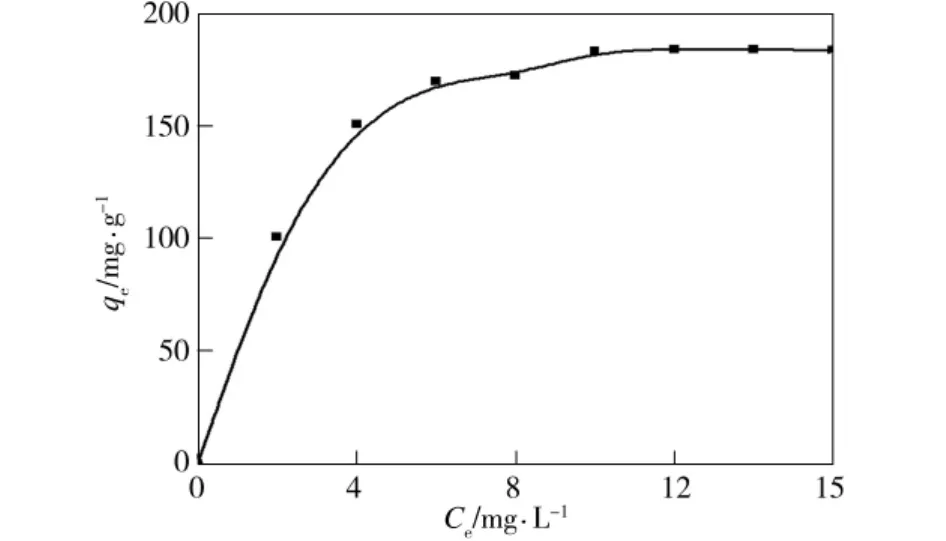
图4 纳米磁性膨润土对甲基橙等温吸附曲线Fig.4 Adsorption isotherms of methyl orange by nanomagnetic-bentonite
2.5 纳米磁性膨润土降解甲基橙效果
在p H为7、温度为25℃、纳米磁性膨润土投加量为1 g/L条件下,对模拟废水甲基橙进行降解,纳米磁性膨润土对甲基橙降解曲线如图5所示。从图5中可看出,在一定浓度范围内,纳米磁性膨润土对甲基橙降解率随反应液中H2O2投加量增加而增大;反应液中H2O2投加量为2.5 mmol/L时降解效率最佳,降解120 min后其降解率高达96%并趋于稳定。
在纳米磁性膨润土中,纳米Fe3O4颗粒尖晶石结构表面活性位点存在如下两个反应[24]:
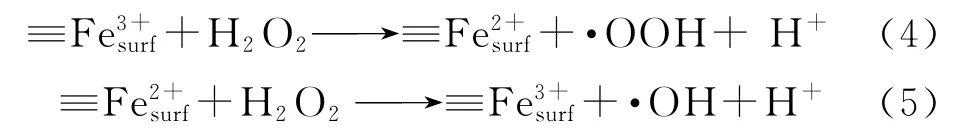
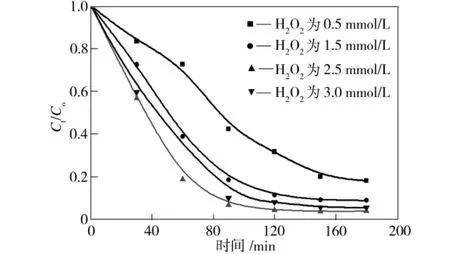
图5 纳米磁性膨润土对甲基橙降解曲线Fig.5 Degradation curve of methyl orange by nano-magnetic-bentonite
增加H2O2投加量可以增大·OH的浓度,加快降解反应速率[16],但H2O2投加量过大又抑制了·OH产生量,导致降解效率降低,故本研究确定H2O2最佳投加量为2.5 mmol/L。
p H为7、温度为25℃、纳米磁性膨润土投加量为1 g/L、H2O2投加量为2.5 mmol/L时,降解时间对废水色度和CODCr去除率的影响如图6所示。从图6中可以看出,纳米磁性膨润土对模拟废水CODCr和色度均有较好的去除效果,120 min时CODCr去除率达94.7%、色度去除率达88.8%,此时模拟废水处理后的CODCr低于60 mg/L,色度不大于30倍,达到国家工业回用水水质标准。
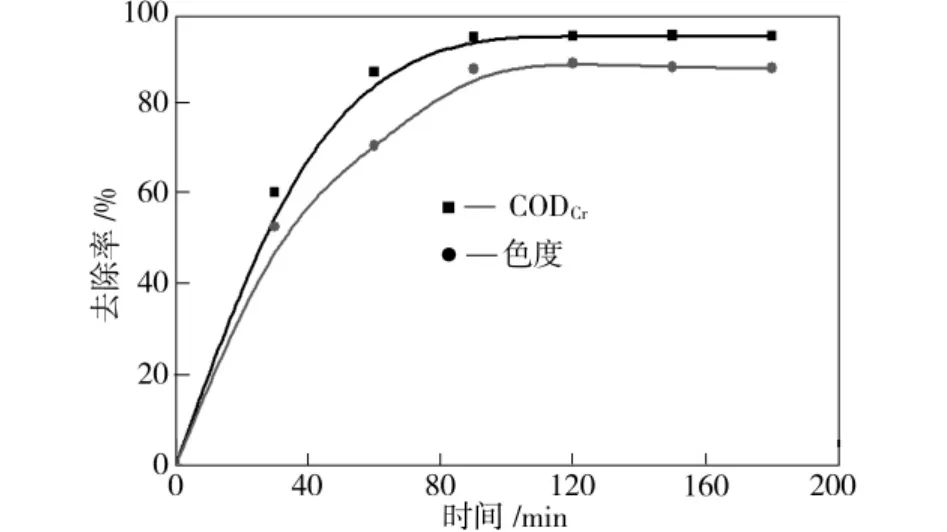
图6 降解时间对废水色度和CODCr去除率的影响Fig.6 Effect of degradation time on the removal rate of CODCrand discoloration of wastewater by nano-mgneticbentonite
3 结论
(1)纳米磁性膨润土中纳米磁性颗粒以Fe3O4附载于膨润土上形成磁性集合体。
(2)纳米磁性能润土对甲基橙模拟废水的等温吸附符合Langmuir等温吸附模型。
(3)在p H为7、温度为25℃、纳米磁性膨润上投加量为1 g/L、H2O2投加量为2.5 mmol/L、降解时间为120 min条件下,纳米磁性膨润土对甲基橙度水的降解率达96%、CODCr去除率为94.7%,色度去除率为88.8%。
[1] Ghose M K.Complete physico-chemical treatment for coke plant effluents[J].Water Research,2002,36(5):1 127-1 134.
[2] Czaplicka M.Qualitative and quantitative determination of halogenated derivatives in wastewater from coking plant[J].J Separ Sci,2003,26:1 067-1 071.
[3] 何苗,张晓健,瞿福平,等.焦化废水中芳香族有机物及杂环化合物在活性污泥法处理中的去除特性[J].中国给水排水,1997,13(1):14-17.
[4] Wang N,Zhu L,Wang M,et al.Sono-enhanced degradation of dye pollutants with the use of H2O2activated by Fe3O4magnetic nanoparticles as peroxidase mimetic[J].Ultrason Sonochem,2010,17:78-83.
[5] Goi A,Trapido M.Hydrogen peroxide photolysis,Fenton reagent and photo-Fenton for the degradation of nitrophenols:a comparative study[J].Chemosphere,2002,46:913-922.
[6] Spadaro J T,Lorne I,Renganathan V.Hydroxyl radical mediated degradation of azo dyes:evidence for benzene generation[J].Environ Sci Technol,1994,28:1 389-1 393.
[7] Chen F,Ma W,He J,et al.Fenton degradation of malachite green catalyzed by aromatic additives[J].J Phys Chem A,2002,106:9 485-9 490.
[8] 权真真,尹平河.铁柱撑膨润土/UV/Fenton催化降解五氯苯酚研究[J].工业水处理,2011,31:32-35.
[9] Chun C L,Penn R L,Arnold W A.Kinetic and microscopic studies of reductive transformations of organic contaminants on goethite[J].Environ Sci Technol,2006,40:3 299-3 304.
[10]Elsner M,Schwarzenbach R P,Haderlein S B.Reactivity of Fe(II)-bearing minerals toward reductive transformation of organic contaminants[J].Environ Sci Technol,2004,38:799-807.
[11]Chun C L,Penn R L,Arnold W A.Degradation of drinking water disinfection by products by synthetic goethite and magnetite[J].Environ Sci Technol,2005,39:8 525-8 532.
[12]Wang W,Yao J.Synthesis of magnetically separable Sn doped magnetite/silica core-shell structure and photocatalytic property[J].Mater Res Bull,2010,45:710-716.
[13]Rodriguez J M,Lopez A J,Bruque S.Interaction of phenamiphos with montmorillonite[J].Clays ClayMiner,1988,36:284-288.
[14]Danis T G,Albanis T A,Petrakis D,et al.Removal of chlorinated phenols aqueous and mesoporous aluminum phosphates[J].Water Research,1998,32:295-302.
[15]Konstantinou I K,Albanis T A,Petrakis D,et al.Removal of herbicides from aqueous solution by adsorption on Al-pillared lays[J].Water research,2000,34:3 123-3 136.
[16]温丽华,李益民,刘颖,等.含铁的柱撑膨润土光催化降解甲基橙[J].化学学报,2005,63:55-59.
[17]奚旦立,张裕生,刘秀英.环境监测[M].北京:高等教育出版社,1995:389-392.
[18]Catrinescu C,Teodosiu C,Macoveanu M,et al.Catalytic wet peroxide oxidation of phenol over Feexchanged pillared beidellite[J].Water Research,2003,37:1 154-1 160.
[19]曹吉林,陈学青,刘秀伍,等.磁性膨润土净水剂制备及其应用[J].天津大学学报,2007,40:454-460.
[20]王维清,冯启明,董发勤,等.磁性膨润土的制备及其性能[J].硅酸盐学报,2010,38:684-688.
[21]Giles C H,MacEwan T H,Nakhwa M,et al.Studies on adsorption XI:a system of classification of solution adsorption isotherms and its use in diagnosis of adsorption mechanisms and in measurement of specific surface areas of solids[J].J Chem Soc London,1960,56:3 973-3 993.
[22]Catrinescu C,Arsene D,Teodosiu C.Catalytic wet hydrogen peroxide oxidation of para-chlorophenol over Al/Fe pillared clays(AlFePILCs)prepared from different host clays[J].Applied Catalysis B:Envirnmental,2011,101:451-460.
[23]Liang X,Zhu S,Zhong Y,et al.The remarkable effect of vanadium doping on the adsorption and catalytic activity of magnetite in the decolorization of methylene blue[J].Applied Catalysis B:Envirnmental,2010,97:151-159.
[24]Song W,Cheng M,Ma J,et al.Decomposition of hydrogen peroxide driven by photochemical cycling of iron species in clay[J].Environ Sci Technol,2006,40:4 782-4 787.
Nano-magnetic modified bentonite:preparation and its degradation of methyl orange
Li Wenbing1,2,Zhang Yujia2,Zhang Xiu2,Wang Juan2,Jiang Lu2,Zhu Yinan2,Wang Guanghua1,2
(1.Hubei Coal Conversion and New Carbon Materials Key Laboratory,Wuhan University of Science and Technology,Wuhan 430081,China;2.College of Chemical Engineering and Technology,Wuhan University of Science and Technology,Wuhan 430081,China)
Nano-magnetic modified bentonite(NMB)was prepared through a reaction between the iron salt solution and the dispersion solution of refined bentonite,and its degradation capability for methyl orange was investigated.The results show that Fe3O4nanoparticles occur on the surface of bentonite particles and form magnetic aggregation,whose isothermal adsorption of methyl orange wastewater can be well fit to Langmuir model.Under the conditions of p H=7.0,T=25℃,ρ(NMB)=1.0 g/L,andρ(H2O2)=2.5 mmol/L,the degradation rate of methyl orange reaches 96%at 120 min,and the removal rates of CODCrand discoloration are 94.7%and 88.8%,respectively.
nano-magnetic bentonite;degradation;Fe3O4;wastewater reuse
TD985;TQ424.2
A
1674-3644(2012)03-0202-05
[责任编辑 彭金旺]
2011-12-05
高等学校博士学科点专项科研基金联合资助项目(20114219110002);武汉科技大学煤转化与新型炭材料湖北省重点实验室开放基金资助项目(WKDM201107);武汉科技大学绿色制造与节能减排科技研究中心开放基金资助项目(A1201,B1209).
李文兵(1973-),男,武汉科技大学副教授,博士.E-mail:liwenbing@126.com
王光华(1953-),男,武汉科技大学教授,博士生导师.E-mail:wghuah@21cn.com

