消癌平注射液治疗中晚期肿瘤临床研究meta分析
王中奇,王妙新*
上海中医药大学附属龙华医院,上海 200126
通关藤又名通光藤、乌骨藤、乃浆藤、通关散和白暗消等,始载于《滇南本草》,曾经收载于《云南省药品标准》(1974 版)和《中国药典》(1977 版)。现代药理研究表明,通关藤含多种苷及苷元等成分,具有明显的抗肿瘤活性。中药通关藤为萝藦科牛奶菜属植物通关藤Marsdenia tenacissima的干燥茎。
消癌平注射液主要成分为通关藤精提取物,单味多组份,具清热解毒、化痰软坚的功效,用于治疗食管癌、胃癌、肺癌、肝癌,并可配合放疗、化疗进行辅助治疗。消癌平注射液单药及辅助放、化疗用于治疗肿瘤有数十年的历史,其临床研究报道非常多,用法用量多样,疗程长短各异,试验样本量均较小。本文通过采用meta分析方法,对以往的临床研究进行综合分析,考察消癌平注射液治疗中、晚期肿瘤的有效性和安全性。
1 资料方法
1.1 文献资料来源
收集2003年至2011年9月在中国知网CNKI、维普期刊资源整合服务平台、万方数据知识服务平台和中国生物医学文献服务系统公开发表的论文,以“消癌平注射液”、“治疗”、“肺癌”、“肝癌”、“食管癌”、“胃癌”为关键词进行检索。同时收集了药企试验报告、学术会议汇编、学位论文等资料。
1.2 文献纳入标准
(1)南京圣和药业生产的消癌平注射液(2002年开始生产、销售消癌平注射液)相关资料。(2)给药途径为静脉滴注。(3)单药或联合放、化疗治疗肿瘤。(4)疗效评定按照国际公认标准执行的文献。
1.3 文献剔除标准
(1)使用方式为肌注的临床研究文献。(2)无消癌平注射液具体用法用量的临床研究文献。(3)以消癌平注射液为基本治疗,联用其它药物的临床研究文献。(4)非对照临床研究文献。(5)抄袭或重复发表的临床研究文献。(6)未进行临床有效性评价的文献。(7)以回顾性资料作对照组的文献。
1.4 统计方法
采用Cochrane协作网提供的RevMan5.1.6软件。纳入研究的文献质量采用Jadad量表评分:1~3分视为低质量,4~7分视为高质量。计数资料采用合并的风险比(risk ratio,RR)值。各个文献研究间异质性检验结果 P>0.1,选用固定模型(fixed model),否则选用随机模型。对该研究合并效应的影响因素进行敏感性分析,利用RevMan 5.1.6软件绘制的漏斗图进行发表性偏倚分析。
2 结 果
2.1 文献质量
共检索到文献21篇。其中1篇是以消癌平注射液为基本治疗,联用其它药物的临床研究;5篇系2002年之前开展的试验研究;1篇以回顾性资料作对照组;1篇无消癌平注射液用法用量描述;2篇未设对照组。共计10篇,不予采用。最终有11篇文献符合要求,文献概况及其Jadad评分见表1。
2.2 有效性和安全性分析
2.2.1 消癌平注射液治疗中、晚期肿瘤的用法、用量分析 11篇文献中均以消癌平注射液联合化疗治疗肺癌、肝癌和食管癌,用药疗程:21~28天,众数为21天。每疗程用药时间:7~15天,中位数为10~15天。给药剂量:40~120 mL,中位数为60 mL。

表1 文献概况及其Jadad评分
2.2.2 消癌平注射液治疗中、晚期肺癌临床有效性的meta分析 9篇消癌平联合治疗肺癌的结果显示:消癌平注射液联合化疗治疗晚期非小细胞肺癌的临床有效率消癌平组和对照组分别为28.57%~66.67%和21.43%~51.72%。
总样本量:消癌平组265例,对照组267例。异质性检验Chi2=1.85,P=0.99,采用固定模型,合并效应值RR为1.27。消癌平联合化疗组与单纯化疗组治疗晚期非小细胞肺癌临床有效率分别为:50.19%和39.70%,消癌平联合化疗组优于单纯化疗组,两组间差异有统计学意义(P=0.01)。见表2。
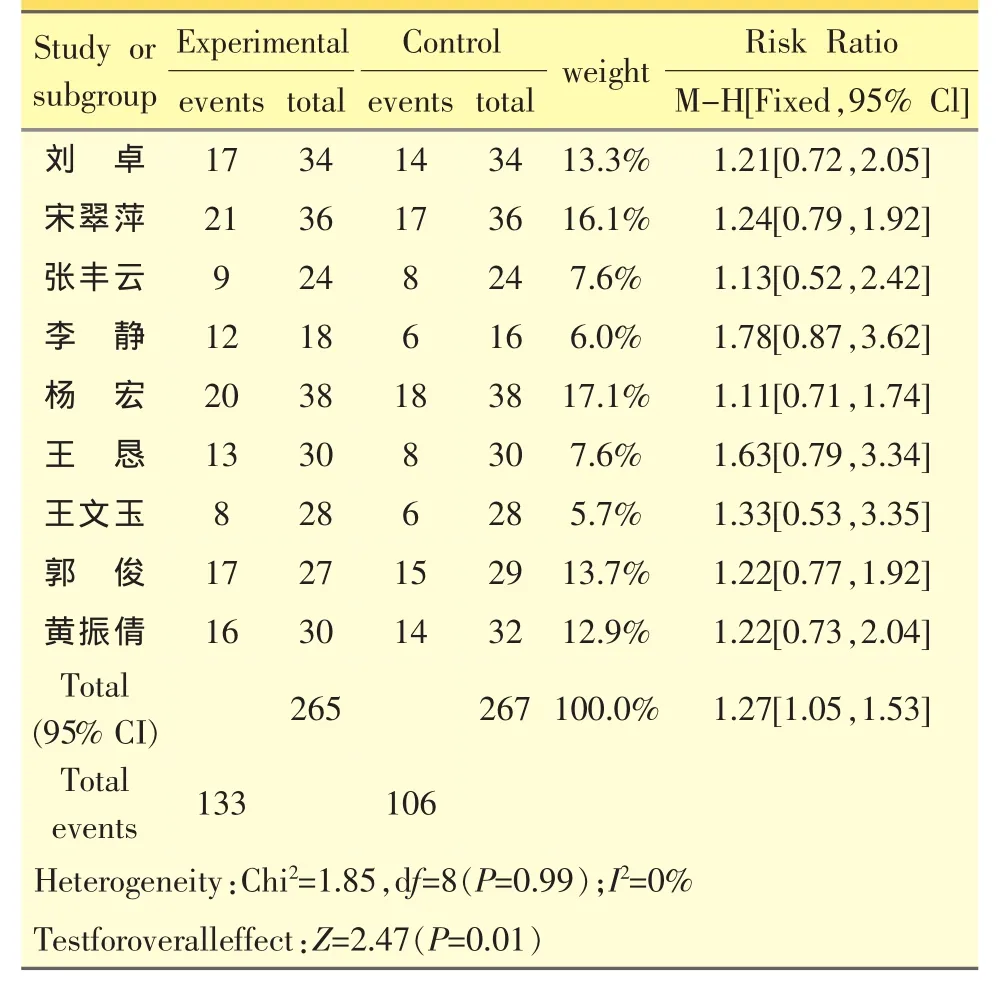
表2 消癌平注射液治疗中、晚期肺癌临床有效性的meta分析
偏倚分析:漏斗图显示各点呈对称分布,可认为发表性偏倚较小。
2.2.3 消癌平注射液治疗中、晚期肺癌临床控制率的meta分析 9篇消癌平联合治疗肺癌的结果显示:消癌平注射液联合化疗治疗晚期非小细胞肺癌的临床控制率消癌平组和对照组分别为62.5%~94.44%和56.67%~94.74%。
总样本量:消癌平组265例,对照组267例。异质性检验Chi2=9.81,P=0.28,采用固定模型,合并效应值RR为1.11。消癌平联合化疗组与单纯化疗组治疗晚期非小细胞肺癌临床控制率分别为:85.28%和76.77%,消癌平联合化疗组优于单纯化疗组,两组间差异有统计学意义(P=0.01)。见表3。
偏倚分析∶漏斗图显示各点呈对称分布,可认为发表性偏倚较小。

表3 消癌平注射液治疗中、晚期肺癌临床控制率的meta分析
李凯等[2]使用消癌平注射液联合治疗晚期食管癌的临床观察显示:消癌平联合化疗组与单纯化疗组的有效率分别为46.7%和40.0%;吞咽困难和胸痛的临床症状缓解率分别为54.5%和40.9%,差异无统计学意义(P>0.05);生活质量改善,消癌平组KPS评分比治疗前明显增加,差异有统计学意义,对照组治疗前后比较差异无统计学意义。
郭俊等[11]使用消癌平注射液辅助介入治疗原发性肝癌35例报道显示:与对照组相比,临床疾病控制率分别为80.0%和65.7%,差异无统计学意义(P>0.05);中位生存期分别为:25(8~68)月和 20(3~60)月,消癌平组延长了5个月,差异有统计学意义(P<0.05);生活质量改善比较,消癌平组KPS提高25例(71.4%),对照组17例(48.6%),消癌平组高于对照组,差异有统计学意义(P<0.05)。
2.3 消癌平注射治疗中、晚期肿瘤生活质量改善率的meta分析
纳入研究文献9篇,总样本量:消癌平组282例,对照组286例。异质性检验Chi2=11.03,P=0.20,采用固定模型,合并效应值RR为1.80。消癌平联合化疗组与单纯化疗组的生活质量改善率(KPS评分治疗后较治疗前增加≥10分)分别为:57.09%和31.82%,消癌平联合化疗组优于单纯化疗组,两组间差异有统计学意义(P<0.00001)。见表4.1。
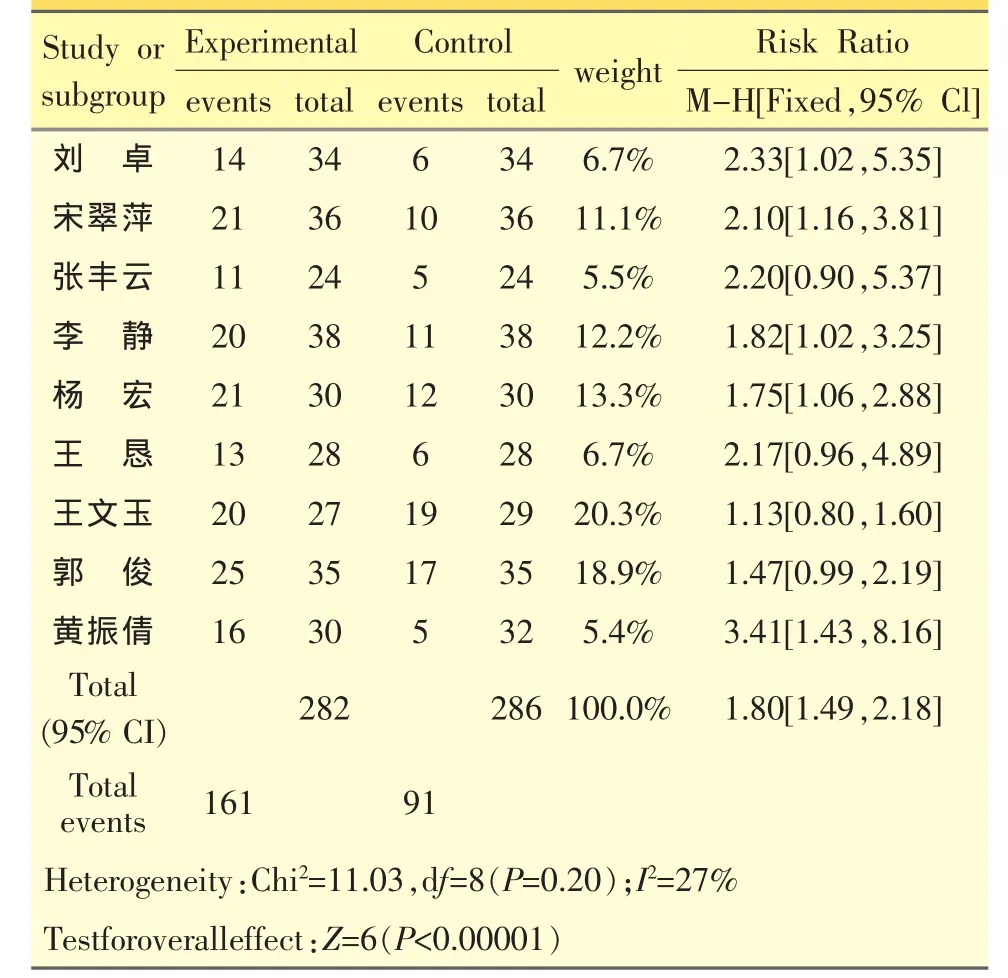
表4.1 消癌平注射治疗中晚期肿瘤生活质量改善的meta分析1
偏倚分析:漏斗图显示各点分布对称性欠佳,可能存在发表性偏倚,见图1。
不考虑分析结果中权重值为20.3%的最大值进行meta分析,见表4.2和图2。结果与前述分析结果一致,消癌平联合化疗组优于单纯化疗组,两组间差异有统计学意义(P<0.00001)。漏斗图显示各点呈对称分布,可认为发表性偏倚较小。

图1 9篇文献生活质量改善meta分析漏斗图
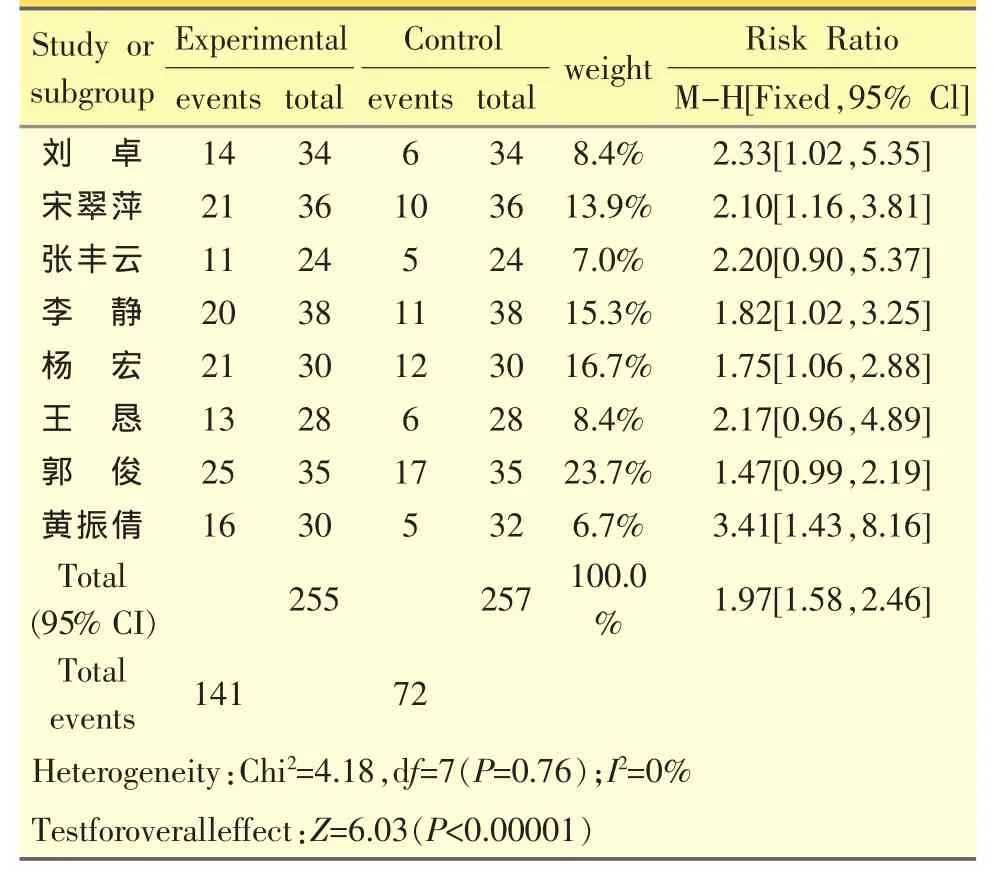
表4.2 消癌平注射治疗中晚期肿瘤生活质量改善的meta分析2
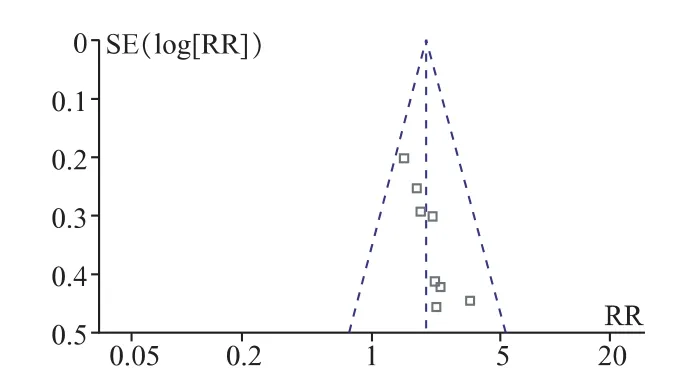
图2 8篇文献生活质量改善meta分析漏斗图
2.4 中、重度不良反应发生率meta分析
纳入研究文献7篇,不良反应总例次:消癌平组673例次,对照组681例次。异质性检验Chi2=5.72,P=0.46,采用固定模型,合并效应值RR为0.81。消癌平联合化疗组与单纯化疗组的中重度(Ⅲ~Ⅳ度)不良反应例次发生率分别为:11.59%和14.24%,两组间差异无统计学意义(P=0.13),提示,消癌平注射液降低化疗引起的中、重度不良反应例次发生率的效果不显著。见表5。偏倚分析:漏斗图显示各试验中各点呈对称分布,可认为发表性偏倚较小。
2.5 敏感度分析
将固定模型换成随机模型进行分析,结果基本一致,见表6。

表5 消癌平注射液联合治疗中晚期肿瘤不良反应比较meta分析
3 结论与讨论
3.1 资料等级
研究中收集的文献资料,在随机序列的产生和随机化隐藏的描述方面普遍交待不明确,难以判断其随机化的质量。其中3篇文献未提及试验分组设计、实施步骤,这可能与中医药专家在临床研究观察中对随机对照试验设计的重要性认识不足有关,从而导致研究中所有文献的Jadad评分低于4分,属低质量文献资料。
3.2 敏感性和发表性偏倚
对研究中收集的文献进行meta分析,漏斗图提示发表性偏倚均较小。按不同效应模型进行分析,得到的结果与基本分析结果一致,各个文献研究间异质性差异较小。
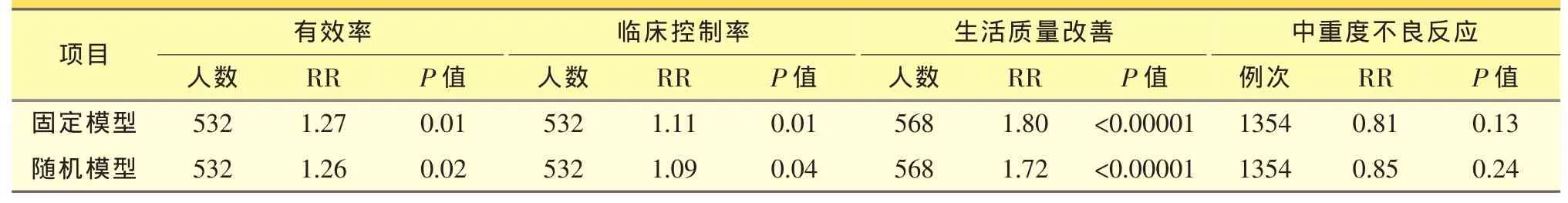
表6 敏感性分析
3.3 疗效评价
Meta分析结果提示:消癌平联合化疗与单纯化疗相比能明显提高患者的生活质量、临床有效率和临床控制率,两组间差异均有统计学意义(P<0.05)。消癌平注射液对降低化疗引起的中、重度不良反应发生率效果不明显。
中药用于抗肿瘤治疗,较西药具有一定的优势,不管是传统的细胞毒性药物,还是现在的单克隆抗体、小分子酪氨酶抑制剂,均具有毒性大的缺点。经过化疗后的患者,在体内癌细胞生长受到抑制的同时,正常细胞也受到不同程度的损伤,治疗过程中常发生中、重度不良反应。而中药抗肿瘤药物——消癌平注射液作用温和,具有显著改善和提高患者生活质量的功效,数十年临床应用证明其改善患者生活质量的功效是确切的,目前发表的临床试验报道均支持这一结论。对其治疗肿瘤的减毒、增效作用,由于历史原因,尚缺乏符合目前临床试验要求的随机、双盲、平行对照临床试验数据支持,尤其缺乏作为抗肿瘤药物有效性的终点指标——生存期(OS)的RCT试验数据。应在对该药进行安全性再评价工作的基础上,开展该药的临床验证试验工作,进一步评价消癌平注射液的临床试验疗效,补充符合目前国家要求的临床试验数据,为临床应用提供详实参考。
[1]黄振倩,谭 获,王春燕,等.消癌平注射液联合化疗治疗中晚期肺癌的临床研究[J].临床肿瘤学杂志,2007,12(2):97-9,102.
[2]李 凯,邹华伟.消癌平联合化疗治疗晚期食管癌的临床观察[J]. 中华肿瘤防治杂志,2007(16):1272-3.
[3]宋翠萍.消癌平注射液联合化疗治疗中晚期非小细胞肺癌 36 例[J].2008,49(6):494.
[4]刘 卓,徐 卓,徐丽莎.消癌平配合化疗治疗中晚期肺癌临床观察[J].现代中西医结合杂志,2008(30):4720-1.
[5]王 恳,郭志雄.消癌平注射液联合NP方案治疗晚期肺癌56例近期疗效观察[J].肿瘤基础与临床,2009(1):47-8.
[6]李 静,张 华.泽菲联合消癌平治疗晚期非小细胞肺癌38例临床观察[J].中国中医药科技,2009(3):206.
[7]张希华.消癌平注射液联合NP方案化疗治疗中晚期非小细胞肺癌疗效观察[J]. 社区医学杂志,2009,7(13):81.
[8]王文玉,周 云,张晓菊,等.消癌平注射液联合化疗治疗晚期非小细胞肺癌的临床观察 [J].临床肿瘤学杂志,2009(10):936-8.
[9]张丰云,李秋文,管静芝,等.消癌平注射液联合GP方案治疗晚期非小细胞肺癌疗效观察 [J].肿瘤基础与临床,2011(5):415-7.
[10]杨 宏,吕 爽,王 珏,等.消癌平注射液联合NP方案治疗晚期NSCLC的临床观察[J].中国医药导报,2011(8):64-5.
[11]郭 俊,邬雨春,王海江,等.消癌平注射液辅助介入治疗原发性肝癌疗效观察 [J].包头医学院学报,2011(3):61-2.

