糖尿病肾病患者抗糖尿病药物的选择
安徽省立医院内分泌科 叶山东
糖尿病肾脏病变是糖尿病患者的重要并发症之一, 其最典型特征是糖尿病肾小球硬化症——即所谓的糖尿病肾病(Diabetes Nephropathy,DN),是糖尿病患者最重要的微血管慢性并发症之一。此外,糖尿病患者尤其是2型糖尿病患者,常可合并其他各种肾脏病变如高血压肾病、尿酸性肾病、慢性肾炎和泌尿系感染等,而导致肾脏受损或肾功能不全,可广义地称为糖尿病慢性肾脏病变。1999年美国肾脏病基金会(NKF)公布的《指南》提出了新的慢性肾脏病(chronic kidney disease,CKD)定义[1],《指南》将CKD的确定基于肾损伤的证据和肾小球滤过率(GFR),与病因无关。慢性肾脏病变的肾脏损伤定义为:肾脏结构或功能异常≥3个月,可以有或无GFR下降,可表现为下面任何一条:①病理学检查异常。②肾损伤的指标:包括血、尿成分异常或影像学检查异常;有或无肾脏损伤证据。蛋白尿(微量或大量蛋白尿)是CKD重要的临床表现之一。《K/DOQI指南》及ADA建议使用CG、MDRD等公式评估GFR。糖尿病肾病或糖尿病慢性肾脏病变临床非常常见,糖尿病肾病患者如何合理使用抗糖尿病药物是临床经常遇到的问题,目前临床广泛应用的抗糖尿病药物包括胰岛素促泌剂(磺酰脲类药物和格列奈类药物)、双胍类药物、α-葡萄糖苷酶抑制剂(GI)、噻唑烷二酮类药物(TZDs)、DPP-4抑制剂、GLP-1受体激动剂和胰岛素等几乎均不同程度经肾脏排泄或降解,故临床在使用或选择抗糖尿病药物时,应了解其是否存在糖尿病肾脏病变及其肾功能情况合理选择。糖尿病肾病的诊断和慢性肾脏疾病的分期
临床典型的糖尿病肾病结合临床表现、尿白蛋白排泄、肾功能及其病理改变可分为5期[2](见表1)。白蛋白尿(见表2)是临床诊断糖尿病肾脏病变的常规指标,但鉴于尿白蛋白排泄有较大的变异性,建议在为期6个月期间收集三次尿标本,其中两次结果在上述范围,可诊断为持续性白蛋白尿,提示慢性肾脏损害。糖尿病肾病患者Ⅰ-Ⅲ期肾小球滤过率(GFR)多正常,甚至高于正常,对抗糖尿病药物的临床应用无特别影响,Ⅳ期患者肾功能可正常或降低,临床应结合慢性肾脏疾病分期(见表3)合理选择药物和调整剂量。糖尿病肾病时不同抗糖尿病药物的应用
1.磺脲类药物
磺脲类药物是临床应用最广泛的降血糖药物之等;第三代主要有格列美脲。所有磺脲类药物药物口服经胃肠道吸收入血循环,绝大部分(95%~98%)与血浆蛋白结合,然后经肝脏或肾脏清除,一些被肝脏转变活性或无活性的代谢中间产物,肝脏灭活是药物清除的主要途径,肾脏亦是排泄活性或无活性代谢产物的主要器官[3-6]。该类药物一般在CKD3期及以上(即GFR小于60ml/min)时应避免使用,其中格列喹酮因其95%由胆道排泄,仅5%从肾脏排泄,CKD3期及以上患者可以考虑使用,但应注意监测血糖,调整剂量,避免低血糖。格列美脲可低剂量使用(其经肝脏氧化代谢后60%经肾脏排泄,其余经大便排泄),但透析或尿毒症患者避免使用。常用磺脲类药物的药理特点(见表4)。
2.格列奈类药物
此类药物主要包括瑞格列奈和那格列奈,它们也是与胰岛B细胞上磺酰脲类药物受体的亚单位结合,口服刺激胰岛素分泌快而短暂。具有快速降低餐后高血糖的作用,并减少空腹或餐前低血糖的发生风险[3-6]。瑞一,因其降血糖作用确切且价格相对低廉,仍是目前各大指南推荐的抗糖尿病药物之一。磺脲类药物临床常分为第一代、第二代和第三代。第一代有氯磺丙脲、甲磺丁脲(D860)、 氯磺丙脲及乙酰磺环己脲,但目前国内临床常应用的仅有甲苯磺丁脲(D860);第二代有格列本脲、格列齐特、格列吡嗪及格列喹酮格列奈口服吸收后90%的代谢产物经胆汁排泄进入粪便,8%的代谢产物经肾脏排泄进入尿液,因此CKD3期及以上和透析糖尿病患者可以考虑使用。那格列奈主要在肝脏被氧化修饰,代谢产物85%左右从尿中排泄,16%原形从肾脏排泄,CKD3期及以上患者可低剂量应用。

表1 糖尿病肾病诊断和分期

表2 尿白蛋白排泄异常的标准
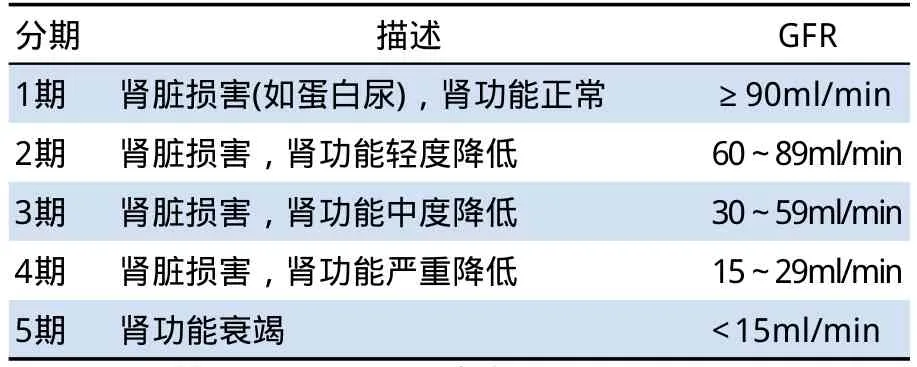
表3 慢性肾脏疾病分期
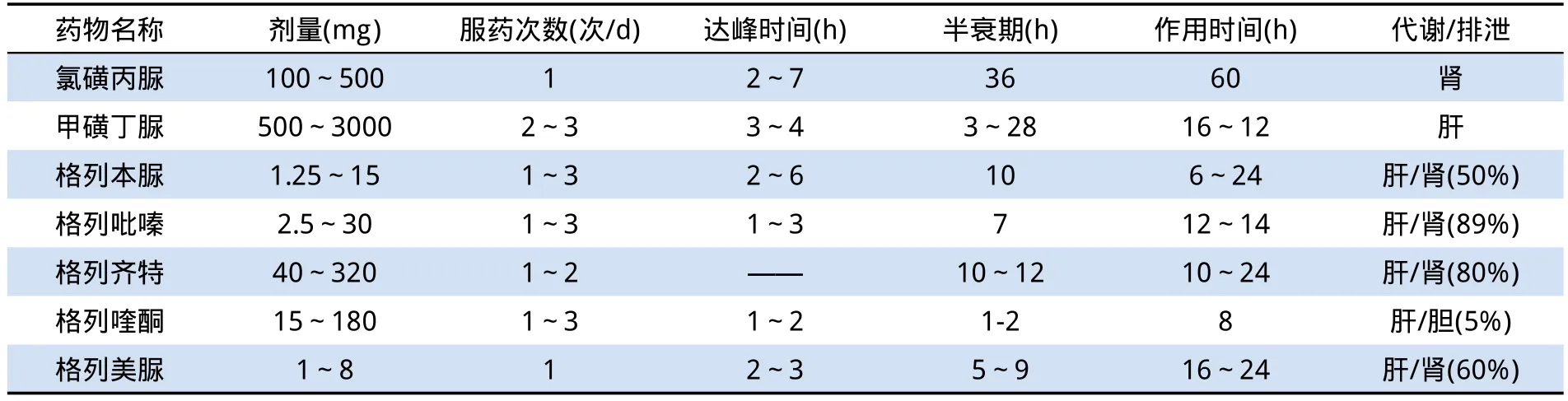
表4 国内常用磺脲类药物的药理特点
3.双胍类药物
双胍类药物于1957年用于临床治疗糖尿病,至今已达60余年。临床曾用的双胍类药物有正丁双胍(buformin)、苯乙双胍(phenformin)和二甲双胍(metformin)。苯乙双胍亦因其常致乳酸酸中毒的危险性增加而渐被淘汰,但在一些发展中国家如中国仍被小心地使用,因其价格低且效果肯定,只要严格注意掌握适应证,仍是一种可选择的药物。二甲双胍因其不良反应少,近年来在国内外受到广泛使用,现已被各国糖尿病指南(如ADA、EASD、IDF和CDS等)推荐为2型糖尿病的首选抗糖尿病药物,并认为二甲双胍在没有禁忌证的情况下,应一直保留在其治疗方案中[3,6-12]。二甲双胍口服生物利用度为50%~60%,吸收后不被肝脏代谢,80%从肾小管排泄,原型从尿中排出,20%从粪便中排出。肝肾功能正常时,二甲双胍不增加血中乳酸浓度。目前认为二甲双胍在治疗剂量引起的乳酸酸中毒非常罕见,有研究报告表明,2型糖尿病患者服用二甲双胍为酸中毒原因的发病率不比服用其他降糖药引起酸中毒的发病率高,提示二甲双胍正常量服用时,乳酸酸中毒的发生更多取决于基础疾病的严重性,而非药物本身。现行推荐使用二甲双胍的肌酐临界值为130~150 mol/L(对应eGFR30~59ml·(min·1.73m2)-1,即3期CKD患者应权衡其他危险因素决定是否用药,而CKD4~5期(eGFR<30ml·(min·1.73m2)-1为二甲双胍使用的绝对禁忌。最新公布的国际血糖控制指导方针(National Evidence Based Guidelines for Blood Glucose Control),推荐eGFR<30ml·(min·1.73m2)-1为禁忌,eGFR30~45ml·(min·1.73m2)-1则慎重使用,eGFR>60ml·(min·1.73m2)-1可以安全地使用。对于轻、中度肾功能损害的患者使用二甲双胍其益处大于弊处[12]。
4.α-葡萄糖苷酶抑制剂(GI)
α-葡萄糖苷酶抑制剂是国内从95年初始用于临床,主要有阿卡波糖(acarbose)和伏格列波糖(voglibose),其共同的核心结构为苯环化合物与氨基右旋糖苷键,其中以阿卡波糖应用较广泛[3-6]。该类药物因其主要在消化道直接发挥作用,并在肠中由微生物分解代谢。全身性不良反应少,主要表现为消化道症状,单独使用不出现低血糖,肾功能不全时(CKD3~5期)可以比较安全地使用。但鉴于该类药物有1%~2%被吸收,且有报道GI导致肝功能损害的病例,因此,糖尿病合并慢性肾脏疾病选择GI类药物(尤其在剂量较大时)时,早期应注意检测肝功能,一旦出现肝功能损害应及时减量或停药。
5.噻唑烷二酮类药物(TZDs)
TZDs是一类较新型口服抗糖尿病药物,主要包括罗格列酮和吡格列酮,其主要通过直接改善胰岛素抵抗而发挥抗高血糖的作用,同时对胰岛B细胞有一定的保护作用,其降血糖作用肯定且比较持久和稳定[3,4,13-16]。该类口服吸收后主要在经N-去甲基作用和羟基化后与硫酸盐和葡萄糖醛酸结合,代谢产物无明显的生物活性,主要经胆道和肾脏排出体外,部分从粪便排泄。TZDs在CKD患者中无禁忌证,且有不少研究提示TZDs对防治肾小球硬化有益并不依赖于血糖的降低,但TZDs存在出现液体潴留的问题,尤其在糖尿病合并CKD时,心功能不全慎用或禁用。
6.DPP-4抑制剂
胰高糖素肽-1(glucagon-like peptide-1,GLP-1),在摄食后回肠黏膜上皮L细胞可分泌GLP-1(肠促胰岛素)。GLP-1可葡萄糖依赖性地促使胰岛素分泌和抑制胰高糖素分泌,改善2型糖尿病患者的葡萄糖代谢。但在体内分泌的GLP-1很快被二肽基肽酶-4(DPP-4)降解而起不到有效的降血糖效果。现已开发多种DPP-4抑制剂如西格列汀、沙格列汀和维格列汀等,它们有效提高血GLP-1浓度和活性,而发挥明显的降血糖作用,且低血糖少,不增加体重等,现已被广泛推荐为2型糖尿病可选择的降糖药物之一[3,13,14]。该类药物主要通过肾脏直接排出(79%),其余的经代谢后排出。对于肾脏功能不全的患者,应适当减少其用量。有研究报告轻度肾功能损害(内生肌酐清除率为30~60ml/min)患者,DPP-4抑制剂只需用药量的1/2,对于重度肾功能损害(内生肌酐清除率<30ml/min)患者,药量可减为常用剂量的1/4。
7.GLP-1受体激动剂
已知体内分泌的GLP-1可为DPP-4所迅速降解并由肾脏清除,其半衰期仅为1~2分钟,不能用于糖尿病的治疗。现已人工合成GLP-1受体激动剂——艾塞那肽(exenatide,53%的氨基酸顺序与天然GLP-1一致)和GLP-1类似物——利拉鲁肽(在天然的GLP-1的分子结构上更换一个氨基酸,同时增加一个16碳棕榈酰脂肪酸侧链),可抵抗DPP-4的降解,从而延长半衰期,发挥降糖效果[3,4,13-17]。临床研究已证实GLP-1受体激动剂有良好的降血糖效果,且低血糖少见并一定程度降低体重。鉴于GLP-1受体激动剂-艾塞那肽通过肾脏清除,2012年欧洲糖尿病协会(EASD)和美国糖尿病学会(ADA)2型糖尿病高血糖治疗共识不建议CKD4~5期糖尿病患者(GFR<30ml/min)使用,利拉鲁肽的使用也不是很安全[4]。
8.胰岛素
自1922年胰岛素应用于临床以来,已历时90年,它挽救了无数糖尿病患者的生命。糖尿病合并肾脏病变的患者是胰岛素使用的适应证,不论是动物胰岛素、人胰岛素还是胰岛素类似物(包括短效胰岛素、速效胰岛素、中效、长效胰岛素、预混胰岛素和超长效胰岛素——甘精胰岛素和地特胰岛素),但应注意剂量的调整[3,4,16-18]。糖尿病合并肾脏病变,尤其是尿毒症时,患者常有胃肠道症状,食欲差,进食少;肾脏灭活胰岛素下降,胰岛素半衰期延长;患者常有胃植物神经病变,致胃排空延缓,食物消化吸收发生改变;肾脏的糖异生和糖原储存减少;最后一些患者可能尚存在不同程度的脑垂体前叶功能减退,使胰岛素拮抗激素水平降低等,上述多种因素的存在常使患者胰岛素用量明显减少,如不注意随时调整胰岛素剂量,很易发生低血糖症。极少数2型糖尿病患者在合并严重肾脏病变时,胰岛素需要量显著减少,甚至停用而血糖不高。
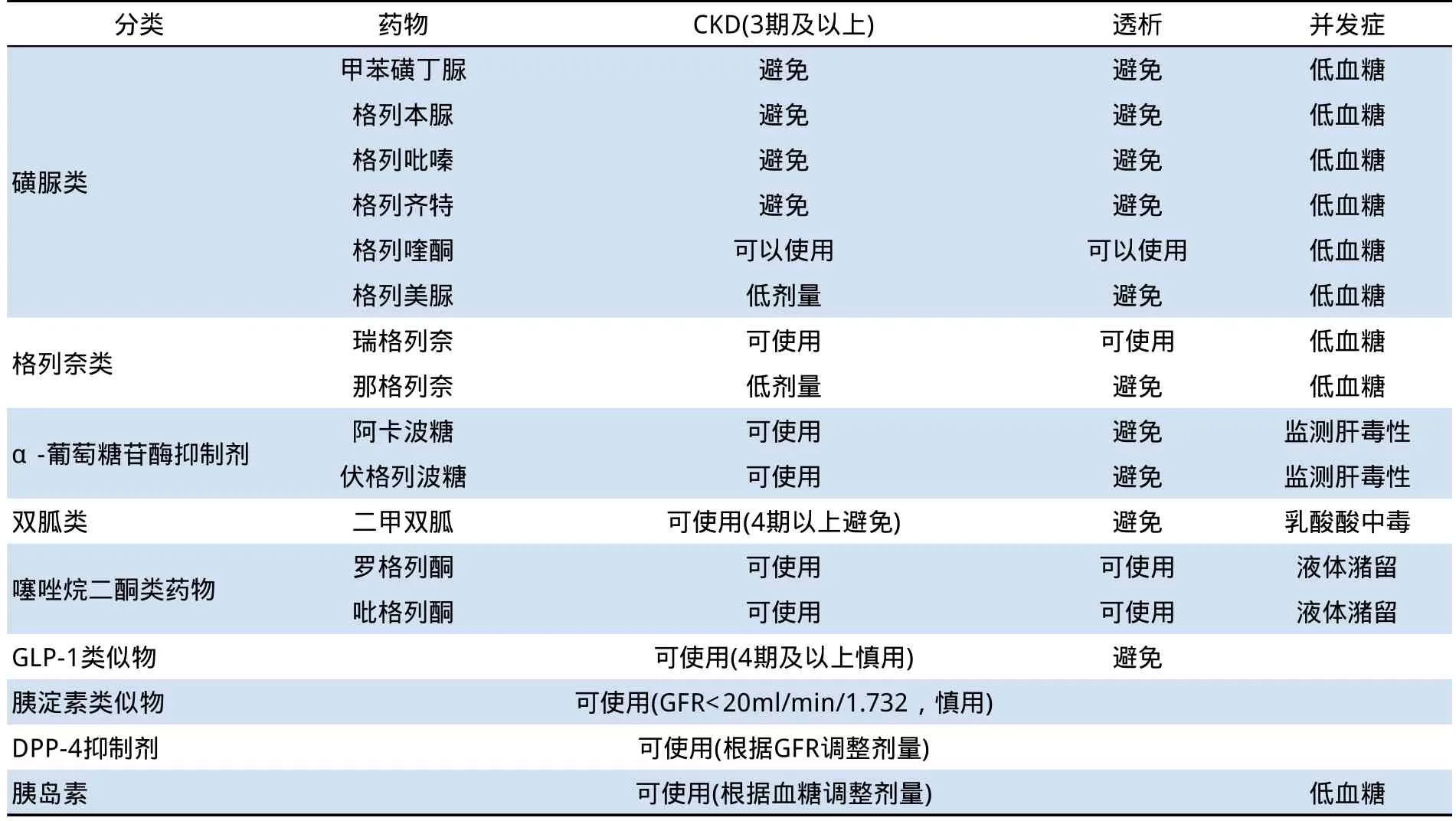
表5 糖尿病合并慢性肾脏疾病和抗糖尿病药物的选择
9.其他
钠糖共同转运子-2(SGLT2)是一种低亲和力的转运系统,其在肾脏中特异性的表达并且在近曲小管的肾脏血糖重吸收中发挥非常重要的作用。SGLT2抑制剂特异性作用于肾近曲小管SGLT2蛋白,抑制肾小管葡萄糖的吸收,即通过增加尿糖的排出而降低血糖,目前正在进行其临床试验以评价其有效性和安全性[3,4,13]。胰淀素类似物如pramlintide(延缓胃排空,抑制胰高糖素分泌,增加饱腹感而协助降低血糖)在GFR>20ml·(min·1.73m2)-1可以使用。
总之,目前临床使用的几乎所有抗糖尿病药物本身对糖尿病肾脏均无明确的不良影响,甚至一些药物还存在降糖之外的肾脏保护作用,但一旦糖尿病合并肾脏损害,则可能影响所用抗糖尿病药物的体内代谢和降血糖效果,故临床在选择药物时应根据其不同的特点合理应用(见表5)。
[1]叶山东,朱禧星主编.临床糖尿病学(第二版)[M].合肥:安徽科技出版社, 2009.
[2]Levey AS, Stevens LA, Coresh J.Conceptual model of CKD:applications and implications[J].Am J Kidney Dis, 2009, 53(Suppl 3):S4-S16.
[3]Abe M, Okada K, Soma M.Antidiabetic agents in patients with chronic kidney disease and end-stage renal disease on dialysis:metabolism and clinical practice[J].Curr Drug Metab, 2011, 12(1):57-69.
[4]Inzucchi SE, Bergenstal RM, Buse JB, et al.Management of hyperglycemia in type 2 diabetes: a patient-centered approach:position statement of the American Diabetes Association (ADA)and the European Association for the Study of Diabetes (EASD)[J].Diabetes Care, 2012, 35(6): 1364-1379.
[5]Danne T, Bolinder J.New insulins and insulin therapy[J].Int J Clin Pract , 2011, 170(Suppl): 26-30.
[6]Kruger DF, Boucher JL, Banerji MA.Utilizing current diagnostic criteria and treatment algorithms for managing type 2 diabetes mellitus[J].Postgrad Med, 2011, 123(4): 54-62.
[7]Hung AM, Roumie CL, Greevy RA, et al.Comparative effectiveness of incident oral antidiabetic drugs on kidney function[J].Kidney Int,2012, 81(7): 698-706.
[8]Lachin JM, Viberti G, Zinman B, et al.Renal function in type 2 diabetes with rosiglitazone, metformin, and glyburide monotherapy[J].Clin J Am Soc Nephrol, 2011, 6(5): 1032-1040.
[9]Reilly JB, Berns JS.Selection and dosing of medications for management of diabetes in patients with advanced kidney disease[J].Semin Dial, 2010, 23(2): 163-168.
[10]Lubowsky ND, Siegel R, Pittas AG.Management of glycemia in patients with diabetes mellitus and CKD[J].Am J Kidney Dis, 2007,50(5): 865-879.
[11]van Berlo-van de Laar IR, Vermeij CG, Doorenbos CJ.Metformin associated lactic acidosis: incidence and clinical correlation with metformin serum concentration measurements[J].J Clin Pharm Ther,2011, 36(3): 376-382.
[12]Banerji MA, Purkayastha D, Francis BH.Safety and tolerability of vildagliptin vs.thiazolidinedione as add-on to metformin in type 2 diabetic patients with and without mild renal impairment: a retrospective analysis of the GALIANT study[J].Diabetes Res Clin Pract, 2010, 90(2): 182-190.
[13]Pilmore HL.Review: metformin: potential bene fi ts and use in chronic kidney disease[J].Nephrology (Carlton), 2010, 15(4): 412-418.
[14]Colagiuri S, Dickenson S, Girgis S, et al.National Evidence Based Guideline for Blood Glucose Control in Type 2 Diabetes[J].Canberra:Diabetes Australia and the NHMRC, 2009.
[15]Fang V, Wazny LD, Raymond CB.Hypoglycemics for the treatment of type 2 diabetes in patients with chronic kidney disease: a focus on new agents[J].CANNT J, 2012, 22(1): 30-36.
[16]Linnebjerg H, Kothare PA, Park S, et al.Effect of renal impairment on the pharmacokinetics of exenatide[J].Br J Clin Pharmacol, 2007,64(3): 317-327.
[17]中华医学会糖尿病学分会.2010年版中国2型糖尿病防治指南[M].北京:北京大学医学出版社, 2011.
[18]Chen SY, Siu K, Kovacs B, et al.Clinical and economic outcomes associated with National Kidney Foundation guideline-concordant oral antidiabetic drug treatment among type 2 diabetes patients with chronic kidney disease[J].Curr Med Res Opin, 2012, 28(4): 493-501.
