全程IMRT在宫颈癌根治性放疗中的临床研究
翟红岩
山东省泰安市肿瘤防治院,山东泰安 271000
宫颈癌体外放射治疗传统多采用体外2野或4野全盆照射(whole pelvic radiotherapy,WPRT),其中挡铅野的设定模式固定为盆腔正中挡铅4 cm宽。此种照射方式对于肿瘤居中的患者较为合理,但对于局部大块或一侧宫旁受侵致使宫颈宫体明显侧偏移位的患者,将会导致瘤体周边及宫旁剂量偏低,从而使肿瘤的局控率下降。如何使肿瘤放疗定位更为准确有效,近年来调强放射治疗(intensity modulated radiation therapy,IMRT)已在临床其他肿瘤的放疗中取得了显著的成果,但在宫颈癌根治性放疗中,因为腔内放疗地位的不可替代性,IMRT是否能代替传统挡铅野对膀胱、直肠的保护,如何与腔内放疗配合等在临床上研究较少。本研究通过对比IMRT与WPRT的疗效、并发症等,验证了IMRT在宫颈癌根治性放疗中的优势。
1 资料与方法
1.1 一般资料
选择本院FIGO分期为ⅡB~ⅢB初治宫颈癌患者共70例,其中,2007年1月~2009年6月的35例患者为IMRT组,2004年1月~2006年12月的35例行传统放疗的患者为对照组。研究组与对照组一般情况比较,差异均无统计学意义(P>0.05),具有可比性。 见表 1。
1.2 方法
治疗仪器:瑞典医科达PRECISE全数字化直线加速器。TPS(放疗计划系统)使用瑞典医科达PRECISE-plan。研究组给予盆腔IMRT治疗+腔内放疗+周化疗。对照组给予盆腔WPRT治疗+腔内放疗+周化疗。
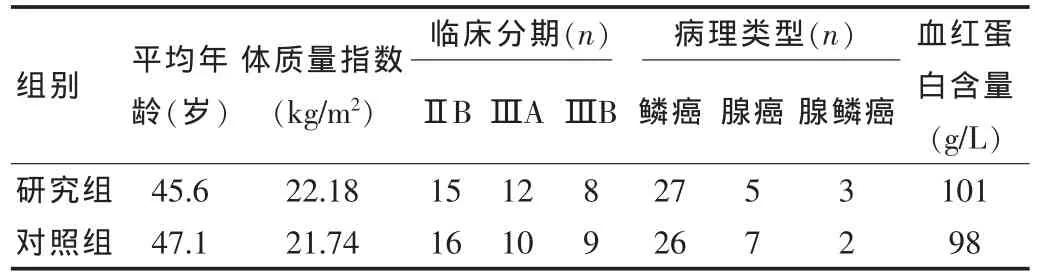
表1 两组患者一般情况对比
IMRT治疗:在CT下扫描,勾画出 CTV(主动脉旁淋巴结、髂总、髂内、髂外淋巴结区域和子宫)及周围危险器官(小肠、直肠、膀胱),CTV外放 0.5 cm形成 PTV,作IMRT计划,危及器官限量:小肠V30<50%;直肠V35<50%;膀胱V35<50%。设7个非共面照射野,8MV-X线,给予 PTV 45 Gy,97%的等剂量曲线包括PTV。
WPRT治疗:在X-ray下全盆定位,上界达腰5椎体下缘,下界达闭孔下缘,两侧界达真骨盆外侧缘外放2 cm,8MV-X线2野同照,DT180 cgy/d,5次/周;中平面 DT30Gy后,改为中央挡铅4 cm四野照射,继续完成DT15Gy。
腔内后装放疗:采用Ir-192腔内高剂量率远距离后装机。放疗前2周,每周1次阴道双管(源旁2 cm 20 Gy/2f),第3周始行宫腔管及阴道双管三管放疗,完成A点42 Gy/6f。
周化疗:每例患者均从第1周放疗开始,DDP 40 mg/周,共完成6次。
1.3 评价指标
(1)肿瘤消退情况:治疗结束后1个月根据CT检查和妇科检查情况,评价肿瘤消退情况。按照WHO疗效判断标准分为完全缓解(CR)、部分缓解(PR)、病情无变化(SD)和病情进展(PD)。 (2)放射损伤:按北美放射肿瘤学组(RTOG)标准评价。(3)复发率:两组患者均随访2年以上,评价1、2年复发率。
1.4 统计学方法
采用SPSS 13.0软件进行统计学处理,采用χ2检验,以P<0.05为差异有统计学意义。
2 结果
2.1 肿瘤消退情况
IMRT组CR率为77.78%,有效率(CR+PR)为100%;WPRT组CR率为51.43%,有效率为87.11%。IMRT组的肿瘤消退情况明显优于对照组,两组比较差异有统计学意义(P<0.05)。见表2。
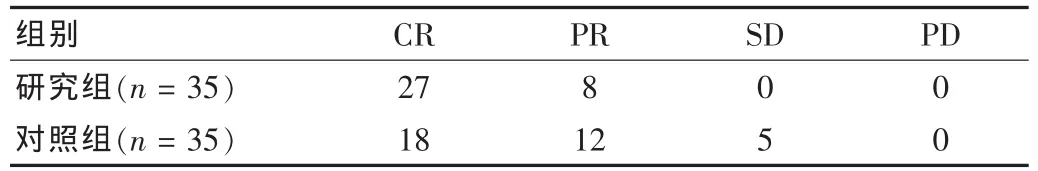
表2 两组肿瘤消退情况对比(n)
2.2 两组放射反应比较
对比两组放射反应情况,研究组胃肠道反应Ⅰ、Ⅱ度发生率为37.1%,对照组为65.7%;研究组膀胱反应Ⅰ、Ⅱ度发生率为20%,对照组为40%;研究组均明显受益(P<0.05)。但在骨髓抑制方面IMRT组较WPRT组无明显优势。详见表3。
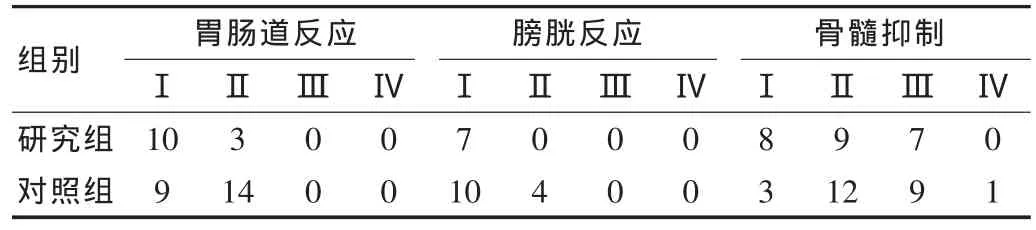
表3 两组放射反应比较(n)
2.3 复发率
两组均随访2年以上,其中IMRT组半年0复发(0%),1年共 2例复发(6.00%),2年共 5例复发(14.29%);WPRT组半年4例复发(11.43%),1年共9例复发(25.71%),2年共17例复发(48.57%)。IMRT的复发率明显低于WPRT组,两组比较差异有统计学意义(P<0.05)。
3 讨论
宫颈癌的根治性放疗多年来一直沿用2野或4野体外照射与腔内放疗配合的传统方式,其效果在临床上是得到公认的,但模式的统一也使肿瘤局控率和危及器官并发症的防治等方面多年来得不到更大的提高,对宫颈癌患者的生存率没有有效的改善。尤其对于局部大块或一侧宫旁受侵致使宫颈宫体明显偏移的患者,传统的盆腔正中挡铅4 cm的模式虽然有效的降低了直肠、膀胱等危及器官的受量,但同时也造成受侵对侧宫旁(尤其是A点到中线旁2 cm的部分)总剂量偏低,从而导致局控率低、局部复发率高,预后差。如何在保护危及器官的同时更好地提高肿瘤靶区受照射的准确性,如何使IMRT和腔内后装更好地结合起来,成为现今提高宫颈癌放疗疗效的主要问题。
近年肿瘤的放射治疗进入了精确放射治疗时代,是迄今为止采用当代技术实现放疗原则的必然趋势,调强技术在降低周围危及器官受到高剂量照射体积的同时,可以提高靶区的照射剂量,并且可以在一次照射中给予不同的靶区以不同的照射剂量,其在头颈部肿瘤、前列腺癌放疗中的应用已经得到肯定[1-3]。自2000年Roeske JC等[4]报道IMRT在妇科肿瘤中的应用以来,也已经有多篇有关宫颈癌调强放疗物理剂量分布的优势及临床结果报道[5-7],但大多为对宫颈癌术后放疗和以IMRT取代腔内放疗的研究。IMRT与腔内放疗配合在宫颈癌根治性放疗中的应用在国内鲜有报道。因为IMRT使肿瘤周围组织遭到的剂量达到最小,比传统的放疗更安全、副作用更小,在放射剂量不增加的前提下IMRT也有减少治疗副作用的优势。目前临床研究中,调强技术在宫颈癌根治性放疗中的应用已经初步显示出技术优势[8]。
在此研究中,充分利用了IMRT剂量分布的优势,在给予不规则野的CTV较高适形度的同时,严格限制危及器官受量,达到了提高肿瘤控制率、减少并发症的目的。证明了在同等处方剂量的情况下,IMRT较WPRT能更好的提高肿瘤受量,更好的保护危及器官,减少其受照体积及受量。与对照组相比,IMRT不仅更好地保证了膀胱、直肠等危及器官的总受量在安全范围内,减轻了危及器官的放射反应,还有效地提高了肿瘤局控率,降低了复发率,使患者远期生存率有了明显的受益,并对于下一步提高根治性放疗剂量的研究提供了可行空间。
[1]Tham IW,Lin S,Pan J,et al.Intensity modulated radiation therapy without concurrent chemotherapy for stageⅡB nasopharyngeal cancer[J].Am JClin Oncol,2010,33(3):294-299.
[2]Pawlowski JM,Yang ES,Malcolm AW,et al.Reduction of dose delivered to organs at risk in prostate cancer patients via image guided radiation therapy[J].Int JRadiat Oncol Biol Phys,2010,76(3):924-934.
[3]张学成,石梅,肖锋,等.鼻咽癌调强放疗腮腺功能恢复与剂量体积关系的探讨[J].中华肿瘤防治杂志,2009,16(6):447-450.
[4]Roeske JC,Lujan A,Rotmensch J,et al.Intensity modulated who e pelvic radiation therapy inpatients with gynecologic malignancies[J].Int J Radiat Oncol Biol Phys,2000,48(5):1613-1621.
[5]黄曼妮,李明辉,吴令英,等.宫颈癌调强适形放射治疗与三维适形放射治疗的剂量学比较[J].癌症进展,2009,7(4):436-441.
[6]Georg D,Kirisits C,Hillbrand M,et al.Image guided radiotherapy for cervix cancer:high-tech external beam therapy versus high tech brachytherapy[J].Int JRadiat Oncol Biol Phys,2008,71(4):1272-1278.
[7]黄曼妮,徐英杰,吴令英,等.宫颈癌调强放射治疗靶区设计的临床研究[J].癌症进展,2008,6(5):523-527.
[8]魏丽春,石梅.宫颈癌根治性放疗中三维适型调强放疗技术的应用[J].中华肿瘤防治杂志,2010,17(17):1387-1390.

