被“设计”出的妹妹
王臣

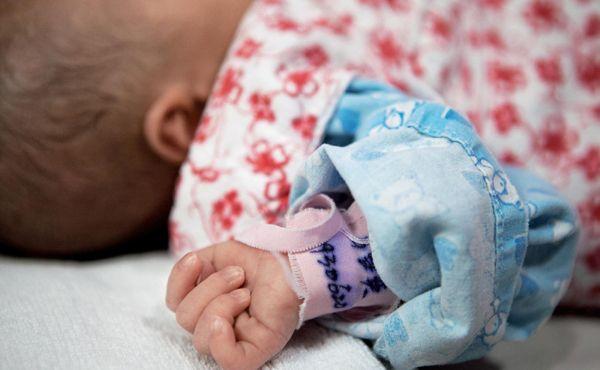
这是一个被寄予了太多希望的生命。
为了这一天,她的父母经过了长达14年的挣扎和等待,而将她送到这个世界上的,正是中山大学附属第一医院(以下简称中山一院)的PGD小组。
6月29日晚上8点40分,她在中山一院降生,作为一场被精密设计的医学计划的首例成果,同时,也是身患重病的姐姐的拯救者。
父母给她取名:柏希——希望的使者。
“我们不是在医院,就是在去医院的路上”
大约两年前,中山一院生殖中心接待了一对夫妇。
这不是一对普通的夫妻,他们双双是遗传性β-地中海贫血(以下简称β-地贫)基因携带者,更加遗憾的是,他们并不知道这件事,直到他们的女儿婷婷在6个月大时患上了贫血,他们带她去医院检查,才得知这性命攸关的消息。
这是一种中国长江以南各省目前发病率最高、影响最大的遗传病之一,尤以两广地区为甚,平均每1万个广东人里,就有183至336个人携带此基因,广西的统计数据则是广东的一倍还多。按照遗传规律,父母双方都是β-地贫基因携带者,下一代有75%的概率也是地贫患儿,其中25%的可能是重症地贫患儿。
婷婷没能逃出概率的魔爪。携带者、轻度地贫都是不需要治疗的,惟有重症地贫,必须依靠医疗手段才能生存,即使如此,仍然有些孩子没能活到他们的5岁生日。
从确诊开始,时间已经过去了14年,那个看不见、摸不到、却切切实实存在于婷婷身上的致病基因,一直折磨和考验着这不幸的一家人。
“这些年我们不是在医院,就是在去医院的路上。”婷婷妈妈这样描述他们的生活。
由于自身缺乏造血机能,从1岁开始,婷婷就依靠高量输血维持生命,随着年龄的增长,输血频率越来越高,到14岁时,她已达到每个月要进行两次高量输血的程度。
长期、大量输入血制品,虽能缓解自身无法造血的危机,然而由于血制品中含铁量较高,长期输入,其代谢产物含铁血黄素在人体内大量增加,加重对心脏、肝脏及内分沁系统的负担,在胰腺、甲状腺等脏器沉积,继而引发其他疾病。
重度β-地贫会引起骨骼变化,患儿因此都有一副一眼便能识别的面孔,婷婷也不例外:头颅很大、额部隆起、眼距很宽、鼻梁塌陷、面色苍白……贫血之外,她患上了继发性糖尿病,除了输血,又多了项注射胰岛素的工作。
婷婷每月治疗费约为六七千元。这并不是最关键的。父母宁可赔上身家性命,只想要一个结果:女儿能够恢复健康。
能长期有效治疗这种病的方法只有一个:通过移植造血干细胞,使婷婷恢复自身的造血机能。
他们当然尝试过了各种渠道,包括申请中华骨髓库的帮助。但根据医学统计,骨髓配型成功的概率极低,除直系亲属配型外,没有血缘关系的配对成功率仅为十万分之1.7。
婷婷一家痴痴等了五年,没有等来配型成功的消息。
被选择的生命
在婷婷出生8年前,1990年,世界上诞生了第一例PGD技术婴儿。这种全名为“植入前遗传学诊断”的技术,通过在体外受精-胚胎移植技术的基础上选择没有遗传缺陷的胚胎,再植入母亲子宫后正常妊娠,从而为携带致病基因的父母创造了生下健康婴儿的可能。
这种技术在中国获得首例成功时,婷婷已经两岁了。这例PGD婴儿也是在中山一院生殖中心的帮助下诞生的。如今回想,周灿权认为那时中国的PGD技术还处于初期,首例PGD婴儿的母亲是血友病基因携带者,遗传给男孩的概率很高,因此当时只是进行简单的性别筛选,阻断遗传病发的可能性。
也就是在同一年,在美国诞生了一个“被设计出生”的婴儿。她6岁的姐姐患有先天性免疫系统疾病,却迟迟找不到能够配型的骨髓,她的父母于是接受医学专家的建议,在医学筛选干预下生下了第二个女儿——她还是胚胎时就被科学家从若干胚胎中选出,因为她的基因健康,而骨髓也与姐姐相配,她出生的首要目的是为了给姐姐提供造血干细胞,帮她冶病,而不是为了证明父母的爱情。
“设计婴儿”一词因此产生。
然而生命能否被“设计”产生?操控一个生命的降生,使其为另一个生命服务,这是否有违伦理和道德?究竟是一个生命的健康更重要,还是另一个生命的尊严更重要?那些“设计”过程中被“牺牲”掉的生命,又该如何看待?从“设计婴儿”诞生之日起,此类讨论在西方国家就没有停止过。
哲学层面的讨论,无法解决父母们现实面临的问题——眼睁睁地看着自己的孩子因无法医治而死去,却什么也不做吗?
骨髓配型的结果迟迟不成功后,婷婷的父母做出了再生一个孩子来解救婷婷的决定。
那时,中国尚无“设计婴儿”成功的例子,中山一院生殖中心在成功辅助诞生了中国第一例PGD婴儿后,用了四年时间巩固和稳定PGD技术,直到2004年,才准备向“设计”方向进军。
因此,婷婷父母首先尝试的是自然怀孕,虽然父母双方均为β-地贫基因携带者,但仍有25%的可能性,生下一个正常健康的孩子。
婷婷妈妈成功怀孕了,却在孕期检测时,被诊断出胚胎患有重度β-地贫。引产。
几个月后,第二次怀孕,再做孕检,还是重度β-地贫。再次引产。
好运似乎始终不愿眷顾这个家庭。婷婷的父母一共尝试了三次自然怀孕,怀上的全部都是和婷婷一样患有重度β-地贫的胎儿。
这样努力了两三年之后,婷婷的父母在2010年4月走进了中山一院周灿权医生的办公室。
他们选择中山一院,因为这里是广东唯一拥有卫生部颁发的实施辅助生殖技术(PGD技术是其中一种)资质许可的医院。
中国虽然没有全社会地讨论“设计婴儿”背后的医学伦理问题,但卫生部2001年颁布的《人类辅助生殖技术管理办法》以及2003年《人类辅助生殖技术规范》中,并未作完全禁止的规定,前提是,只有具备法定资质的医疗机构方能实施此项技术,并需要经过医院内的伦理委员会批准。
2001年以后,全国共有5家医院先后取得该资质,分别在北京、广州、郑州、湖南和浙江。
在婷婷父母来到周灿权办公室时,对于结果将会如何,双方都不确定。
事实上,周灿权的PGD小组从2004年开始将研究方向转到“设计婴儿”上,进展并不顺利。
2004年,研究小组帮助一对β-地贫基因携带夫妻采用“设计婴儿”技术,筛选出两个无患病基因胚胎,其中一个配型与他们的第一个孩子相符,然而,将两个胚胎植入母体后,配型相符的胚胎却没有妊娠。
在本来只有1/16的低概率事件中,研究小组尽可能地扩大命中的可能性。前提条件有很多:试管婴儿技术的成熟、PGD技术的稳定、胚胎检测技术的成熟,以及细胞的成活率等等。
7年来,受各种各样因素的影响,“成功”始终没有到来。
因此,婷婷父母最初只要求周灿权医生用比较成熟的PGD技术帮助他们生下一个健康的孩子,但遗憾的是,虽然中山一院已有数百例PGD婴儿的成功案例,在婷婷父母这里,两次尝试都没能成功妊娠。
能尝试的都尝试了,还没有走过的,只有“设计婴儿”这条路。婷婷的父母决定做最后的努力。
“那咱们就试试吧!”周灿权这样告诉婷婷父母。
关键的48小时
2011年6月27日,广州,中山医院第一附属医院生殖医学中心。这一天在这里发生的事情,将有可能改变婷婷一家14年来的命运。
两个月前,36岁的妈妈打了促排卵针,从体内取出29个卵子,进行人工受精、早期胚胎发育等过程。这是普通的试管婴儿技术,唯一的不同,是29个卵子几乎是正常取卵值的两倍,因为“设计婴儿”胚胎的合格率远没有试管婴儿那么高,必须要用增加胚胎数量来提高成功的可能性。这29个卵子最终形成了12个优质胚胎。
早上8时,工作人员开始对这12个胚胎进行诊断前的准备工作,包括备液、调针、活检等。简单来说,就是从12个胚胎中各抽取一枚细胞,用以作为后续诊断哪个胚胎基因表型正常、配型相符的原材料。
这个过程要求既不能伤害胚胎,所取细胞又要完整可用,必须细致而谨慎。这些准备工作一直持续了4个小时。
肉眼当然无法看到这些被抽取出来的胚胎细胞,一切都是在高度电子显微镜下进行的。它们被放置在手指大小的试管里,送往下一站:前聚合酶链式反应(PCR)区。
这是一间不足8平方米的房间,两三台医疗仪器和电脑几乎占满了整个空间,为了防止外源性DNA污染,房间开着紫外线灯,“设计婴儿”最关键的一环就在这里展开。
为了使抽取出的胚胎细胞能够满足基因检测的样本量,要对这12个细胞进行“全基因组扩增”——在如实反应基因组原貌的基础上,大幅度增加其DNA的含量。
过程当然是复杂而无法轻易描述的,唯一可以证明其复杂程度的,是时间——整整8个小时,和成果——千万倍的扩增。
晚上8点,研究员换上特殊的外套,戴上一次性口罩、手套和帽子进入前PCR区。8小时的全基因组扩增后,每个胚胎细胞的扩增成果都被分装在13个试管里,准备进行不同基因位点的检测。
在过去的7年中,“成功”往往在以上阶段就“夭折”了。试管婴儿技术不够稳定;活检技术差以致用来检测的细胞成活率低,无法进行下一步的诊断;在2009年“全基因组扩增”技术应用之前,每个细胞只能进行一个位点的诊断,一旦出现基因重组,便意味着以前的工作全部白费……
12个胚胎细胞样本,共156个试管,在深夜10点被送入到检测基因图谱的仪器上,以形成此前所有工作的成果,也检测婷婷一家的噩运是否会到此终止。
24小时后,12个胚胎的基因图谱全部出现了。
12个胚胎中,有两个胚胎符合条件:既不携带β-地中海贫血基因,亦与婷婷基因相配,能够进行日后的骨髓移植手术。
然而这时还不能庆祝成功。
根据以往的经验,筛选出的胚胎移植到母体内后,仍有可能无法妊娠。2010年12月,就曾有两个“设计婴儿”胚胎被成功筛选出,但最终还是在妊娠阶段失败了。
婷婷的妈妈已是36岁的高龄产妇,此前有过多次引产和妊娠失败的经历,两个月前,还一次性取出了过多的卵子,为了不对她的子宫和卵巢形成刺激,这两个最终被选中的胚胎被存入了冷冻室,直至医生认为婷婷的妈妈身体允许再次妊娠后,再进行植入手术。
3个月后,两枚作为“姐姐的拯救者”的小胚胎终于进入了妈妈的子宫,其中一枚在妊娠过程中自然退化了,幸好,另一枚熬过了漫长的孕期,在9个多月后,通过剖腹产来到了这个世界。
婷婷一家的幸运背后,还有无数家庭等待通过这一技术拯救子女或家庭的命运。
据周灿权医生介绍,在中国遗传性疾病流行病学研究中,大约20%~50%人口面临遗传性疾病风险,目前已发现的遗传病超过3000种,常见的如血友病、蚕豆病、帕金森氏病、进行性脊肌缩症等,估计每100个新生儿中约有3~10个患有各种程度不同的遗传病。
而基因治疗是一种最根本、最有希望的治疗方法。通过“植入前遗传学诊断”(PGD)可以使有带病基因的父母生出健康的孩子,而通过在PGD基础上的基因筛选技术,这个健康的婴儿还可以为另一个患病的孩子提供治疗帮助。
据不完全统计,中山一院的PGD小组仅去年一年就做了200次PGD,今年3月至6月期间来就诊的同为β-地中海贫血基因携带者的夫妻就有三四十对,就在婷婷的父母接受“设计婴儿”的同一时期,共有5对β-地贫基因携带夫妇在这里接受了同样的辅助手段。
“成功”终于来了。共有两个家庭如愿,其中就包括婷婷一家,这也开创了国内医学界的首例。
但周灿权并不认同“设计婴儿”的叫法,“并不是‘设计而仅仅是‘筛选,这只是个挑选胚胎的过程,这样致病基因在人群中发病率会慢慢降低,对于提高人口素质,减少普通人群中的遗传疾病是非常有效的。我们做的就是这个工作。”
现在,新诞生的“希望使者”的脐带血已采集好,随时准备为姐姐进行造血干细胞移植,以完成“救世主”的使命。
“移植成功,这个故事才算完美,我们迈出的仅仅是最困难的第一步。”周灿权说。
当然,他们的父母不会提起孕育他们的目的和过程。他们最初是被“设计”亦或“筛选”出来的,但他们仍然拥有父母和家人的爱,甚至比别的孩子拥有的更多。

