早期肠内与肠外营养对中国人群胃癌患者术后血清蛋白水平影响的荟萃分析
渠宁 余铭 徐栋

[摘要] 目的 评价胃癌术后对患者进行肠内/肠外营养治疗的过程中患者的营养状况。 方法 检索国内外期刊全文数据库,筛选有关中国人群的随机对照临床试验。采用RevMan4.2进行Meta分析。 结果 纳入19篇研究。胃癌术后早期肠内营养与肠外营养相比,术后血清白蛋白的加权均数差(WMD)为1.72,95% CI[0.80,2.63],P = 0.0002;术后血清转铁蛋白的加权均数差(WMD)为0.13,95% CI[0.05,0.22],P = 0.002;术后血红蛋白加权均数差(WMD)为6.59,95% CI[5.56,7.61],P < 0.0001。 结论 胃癌术后患者早期接受肠内营养后血清营养蛋白水平及血红蛋白水平均优于肠外营养,提示肠内营养是胃癌术后一种有效的营养支持方式。
[关键词] 肠内营养;肠外营养;Meta分析;胃癌
[中图分类号] R735.2[文献标识码] B[文章编号] 1673-9701(2012)29-0111-04
胃癌患者术前及围手术期贫血及营养不良发生率高达70%~80%[1],传统术后早期营养以胃肠外营养(parenteral nutrition,PN)或全胃肠道营养(total parenteral nutrtion,TPN)为主要途径,但长期使用可能导致肠黏膜屏障损伤,而20世纪70年代出现的肠内营养(enteral nutrition,EN)通过口、鼻胃肠管及造瘘管提供营养物质至胃肠内,更加符合消化及吸收的正常生理状态,特别是术后早期肠内营养(early postopetative enteral nutrition,EEN)在临床营养中的应用逐渐广泛。国内邱家学等[2]学者的一项荟萃分析指出,行胃癌手术后的患者采用早期肠内营养与肠外营养相比,术后胃肠功能恢复较快、住院天数较短。本研究的目的在于综合国内外发表的中国人群相关随机对照试验(prospective randomized study)进行荟萃分析,评价胃癌术后早期肠内营养的营养效果。
1 资料与方法
1.1 一般资料
已公开发表的国内外关于比较中国人群胃癌术后早期肠内与肠外营养对血清蛋白水平影响的随机对照试验。
1.2 资料检索
由于国内外在肠内、肠外营养制剂上的配置和使用上存在差别,本研究检索限于2011年6月前公开发表的中文及英文中有关中国人群的相关文献。检索以下电子数据库:①中文:万方数据资源系统、维普中文科技期刊数据库、中国知网CKNI;②英文:ISI Web of Knowledge、MD Consult、Ovid、PubMed及相关链接文献,Cochrane临床对照试验注册资料库(CCTR)。中文检索词包括:肠内营养、肠外营养、胃癌、外科、中国人群。英文检索词包括:Enteral nutrition、Parenteral nutrition、Gastric cancer、Chinese study。根据检索结果检索全文。纳入标准:①随机对照试验;②术前确诊胃癌并接受胃癌根治性手术的中国人群患者;③试验组术后早期(术后24 h开始)给予肠内营养支持;对照组术后采用传统的肠外营养支持;④初始状态(术前1 d)及术后稳定期(术后7、8、9 d)外周静脉血白蛋白(Albumin,ALB)、转铁蛋白(Transferrin,TRF)、血红蛋白(Hemoglobin,HB)。排除标准:①非随机对照试验或伪随机对照试验;②患者因患有胃良性疾病、胃良性肿瘤、其他类型胃恶性肿瘤(非胃癌)而需手术;③研究目的不是比较早期肠内与肠外营养对胃癌患者术后营养效果以及动物试验和细胞实验;④重复发表;⑤无文献发表;⑥未提供足够数据;⑦统计学分析违反处理意向原则(intention to treat,ITT)。
1.3 资料提取
按事先制定的资料摘录表内容提取临床效应数据作为观察指标。信息包括:①患者资料:性别、年龄;②营养支持方式:肠内营养的配置及使用方式,腸外营养的配置;③营养效果评估指标:试验组与对照组初始状态(术前1 d)及术后稳定期(术后7、8、9 d)外周静脉血白蛋白(Albumin,ALB)、转铁蛋白(Transferrin,TRF)、血红蛋白(Hemoglobin,HB)。
1.4 统计学分析
采用Cochrane协作网提供的RevMan 4.2软件进行统计学分析。连续变量资料计算加权均数差(weighted mean difference,WMD)为合并统计量。对于未提供均数和标准差的连续变量资料,以中位数代替。纳入研究进行异质性检验。研究间无异质性(P > 0.05,I2≤50%)用固定效应模型分析,若有异质性(P < 0.05,I2>50%)则分析产生原因进行亚组分析(研究设计、试验条件、试验所定义的暴露、结局及测量方法等是否不同,协变量的影响大小),若异质性源于低质量研究,则进行敏感性分析,若仍有异质性则使用随机效应模型。如亚组只有一项研究仍用RevMan软件分析统计量。结果用95%可信区间表示(CI),检验水准 P < 0.05。采用漏斗图判断发表偏倚。
2 结果
2.1 纳入文献
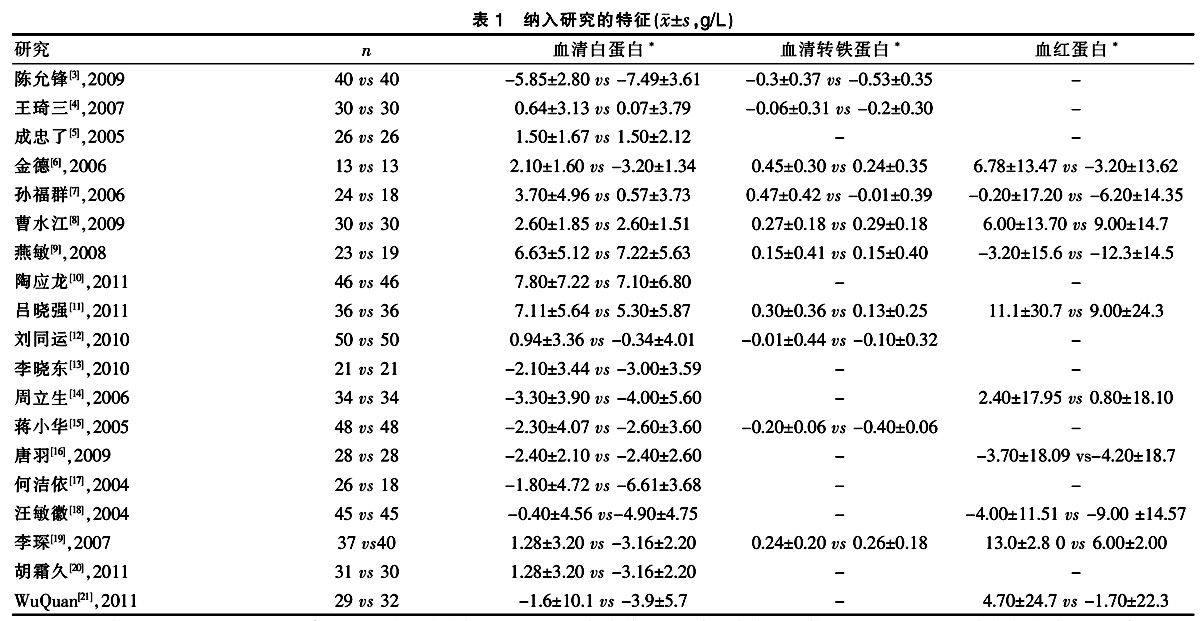
纳入18篇中文随机对照试验,1篇英文随机对照试验。总共包括1 221例中国胃癌术后接受营养支持的患者,其中617例术后早期采用肠内营养支持,604例术后早期采用肠外营养支持。肠内营养支持的来源主要集中于肠内营养混悬剂如能全力、百普力等,肠外营养支持的来源则多为医院自行配置。见表1。
2.2 术后血清白蛋白水平
所有19篇研究均对术后早期血清白蛋白进行描述,617例术后早期采用肠内营养支持,604例术后早期采用肠外营养支持。合并分析前进行异质性检验(P < 0.01,I2=83.8%),组内存统计学异质性,不适合采用固定效应模型进行合并分析。按不同设计方案、研究质量、参加人群特征、治疗时间的长短、肠内营养制剂类型等分成亚组,进行亚组分析仍无法消除组间差异。为消除异质性对结果的影响,采用随机效应模型进行合并分析。合并后的加权均数差(WMD)为1.72,95% CI[0.80,2.63], P = 0.0002。结果表明胃癌术后早期采用肠内营养治疗比肠外营养治疗可提高术后血清白蛋白水平。见表2。
2.3 术后血清转铁蛋白水平
10篇研究对术后早期血清转铁蛋白进行描述,331例术后早期采用肠内营养支持,324例术后早期采用肠外营养支持。合并分析前进行异质性检验(P < 0.01,I2=82.6%),组内存统计学异质性,不适合采用固定效应模型进行合并分析。按不同设计方案、研究质量、参加人群特征、治疗时间的长短、肠内营养制剂类型等分成亚组,进行亚组分析仍无法消除组间差异。为消除异质性对结果的影响,采用随机效应模型进行合并分析。合并后的加权均数差为0.13,95%CI[0.05,0.22],P = 0.002。结果表明胃癌术后患者早期采用肠内营养治疗比肠外营养治疗可提高术后血清转铁蛋白水平。见表2。
2.4 术后血红蛋白水平
10篇研究对术后早期血红蛋白进行描述,299例术后早期采用肠内营养支持,295例术后早期采用肠外营养支持。合并分析前进行异质性检验(P = 0.23,I2=23.2%),组内不存统计学异质性,采用固定效应模型进行合并分析。合并后的加权均数差(WMD)为6.59,95%CI[5.56,7.61],P < 0.0001。结果表明胃癌术后患者早期采用肠内营养治疗比肠外营养治疗可提高术后血红蛋白水平。见表2。
2.5 纳入文献的发表性偏倚
通过Meta分析的漏斗图分析显示,各试验中各点呈对称分布,大样本研究的效应值相对集中分布在图形的中部或顶部,小样本数据的效应值散在,宽广的分布在图形的底部。故可认为发表性偏倚较小(图1、图2、图3)。
3 讨论
胃癌患者术后给予充分的营养支持是必要的,对于术后营养支持的方式,国内外研究认为应在胃肠功能恢复后及时给予肠内营养[20,21]。胃癌手术因顾及吻合口而推迟进食时间及限制进食量,使得胃癌根治术后依赖静脉输液的时间为7~9 d。但20世纪70年代后的研究发现,术后消化道麻痹主要以胃和结肠明显,而术前功能正常的小肠大多在术后几小时便已恢复蠕动,约12 h便能吸收营养物质[22],目前多数学者把术后6~24 h内给予肠内营养定义为“早期”[9]。本研究纳入的16项研究中,肠内营养支持组均在术后第一个24 h内通过口、鼻胃肠管及造瘘管提供营养物质至胃肠内,营养支持时间较短的可选用鼻胃、鼻肠插管,时间长的以造瘘术为宜,患者均能耐受。合理的营养支持基于对患者正确的营养评价。目前,用于营养评价的常用临床生化指标包括血清白蛋白、前白蛋白、转铁蛋白。
血清白蛋白是由肝脏合成的体内重要营养物质,半衰期约15~19 d,常作为营养评价的一项指标。而血清转铁蛋白半衰期较短约为7 d,因而更加敏感,是反映患者营养状况的另一项指标[23]。曾有临床研究表明[24],早期肠内营养支持可以改善患者蛋白质代谢,促进蛋白质合成,从而改善患者机体的营养状况。本研究中纳入16项中文比较早期肠内与肠外营养对胃癌患者术后营养效果的随机对照试验,通过荟萃分析发现,胃癌术后患者接受早期肠内营养后7~9 d复查血清白蛋白、血清前白蛋白及血清转铁蛋白均较肠外营养患者有所升高,提示肠内营养效果优于传统肠外营养,可以提供患者术后恢复足够的血清蛋白源,这与如前所述的肠内营养诸多优势密切相关。值得注意的是,纳入16项研究数据合并分析前存异质性,按不同设计方案、研究质量、参加人群特征、治疗时间的长短、肠内营养制剂类型等分成亚组,进行亚组分析后仍无法消除组间差异,这可能与部分研究的样本量大小、研究方法质量高低等因素相关,由于合并前已严格执行文献的纳入和排除标准并对纳入文章的质量评分,故本研究采用随机效应模型进行合并分析以消除异质性影响。
胃癌患者常因消化道慢性失血及维生素B12吸收障碍等因素伴随贫血的发生,术后更因创伤打击从而加重贫血癥状,而血红蛋白的合成需珠蛋白及亚铁离子的参与,其中血清转铁蛋白是血浆中主要的含铁蛋白质,以转铁蛋白-铁离子复合物的形式进入骨髓参与造血,故血清转铁蛋白水平亦用于贫血的诊断和治疗的监测。本研究荟萃分析发现,胃癌术后患者接受早期肠内营养后7~9 d复查血红蛋白水平高于肠外营养患者,与血清转铁蛋白分析结果呈正相关一致性,故血红蛋白的比较结果也提示肠内营养效果优于传统肠外营养效果。
本研究表明,进行胃癌手术的患者术后早期采用肠内营养治疗效果理想,为患者术后的恢复提供有力的保障。由于本文纳入的均为中国人群相关研究,且部分研究样本量低,研究方法尚待提高,故本文结论尚需国内外大样本高质量随机对照研究结果的支持。
[参考文献]
[1]Correia MI,Aiaffa WT,Da Silva AL,et al. Risk factor of malnutrition in patients undergoing gastroenterological and hernia surgery:an analysis of 374 patients[J]. Nutr Hosp,2001,16(2):59-64.
[2]沈颖,许可敏,邱家学. 肠内与肠外营养对胃癌手术后患者的临床影响——中文文献Meta分析[J]. 药品评价,2010,7(8):28-33.
[3]陈允锋. 早期肠内营养对胃癌行全胃切除术后肝功能的营养[J]. 海南医学,2009,20(9):182-184.
[4]王琦三,王海江,陈鹏,等. 早期肠内营养对胃癌术后患者营养状况和肠功能的影响[J]. 新疆医科大学学报,2007,30(12):1387-1389.
[5]成忠了,牛彦锋,王国斌,等. 早期肠内营养对胃癌术后近期免疫和营养状况的影响[J]. 肠内与肠外营养,2005,12(4):207-212.
[6]金德,孙玉成,刘军贵,等. 老年人胃癌术后早期肠内营养支持的临床研究[J]. 吉林医学,2006,27(7):730-731.
[7]孙福群. 胃癌根治术中隧道式空肠置管术后早期肠内营养支持的应用研究[J]. 中国医师进修杂志,2006,29(6):12-14.
[8]曹水江,蒋清华,方子兴. 胃癌术后肠内营养和全胃肠外营养的疗效比较[J]. 中国现代普通外科进展,2009,12(10):907-908.
[9]燕敏,纪福,李琛,等. 胃癌患者术后早期肠内营养与全肠外营养的临床研究[J]. 外科理论与实践,2000,5(1):17-20.
[10]陶应龙,范旻,姚俊英. 胃癌术后不同营养支持方式对比分析[J]. 海南医学,2011,22(11):28-31.
[11]吕小强. 胃癌术后2种营养方式支持的比较研究[J]. 中外医疗,2010,29(18):10-11.
[12]刘同云,毛伟征,李杨,等. 胃癌术后早期肠内营养支持的研究[J]. 中国现代普通外科进展,2010,13(11):868-870.
[13]李晓东. 胃癌术后早期肠内营养对肝功能影响的临床研究[J]. 医学信息,2010,23(12):47-48.
[14]周立生,刘俊,江叟. 胃癌术后早期肠内营养的意义[J]. 上海医学,2006,29(8),544-546.
[15]蒋小华,李宁,朱维铭,等. 胃癌术后早期肠内免疫营养的作用[J]. 肠外与肠内营养,2005,12(2):102-105.
[16]唐翀. 胃癌术后营养支持的临床分析[J]. 中国现代药物应用,2009,3(21):54-55.
[17]何洁依,谢勇,李萍,等. 胃癌术后的早期肠内营养支持[J]. 中国临床医学,2004,11(3):374-376.
[18]汪敏徽,否维孝. 肠内营养在胃癌术后的临床应用[J]. 中华胃肠外科杂志,2004,7(4):330-333.
[19]李琛,燕敏,朱正纲,等. 胃癌患者全胃切除术后早期肠内营养与肠外营养疗效和费用比较[J]. 临床外科杂志,2007,2(15):141-142.
[20]胡霜久,马小庆. 胃癌根治术后早期肠内营养与肠外营养的疗效比较[J]. 中国医学创新,2011,3(8):36-38.
[21]Wu Q,Yu JC,Kang WM,et al. Short-term effects of supplementary feeding with enteral nutrition via jejunostomy catheter on post-gastrectomy gastric cancer patients[J]. Chin Med J,2011,124(20):3297-3301.
[20]陈川宁,綦晓龙,徐亮,等. 肠内生态营养对大鼠创伤后影响肠免疫功能的初步研究[J]. 四川医学,2010,31(4):22.
[21]Huhmann MB,August DA. Nutrition Support in Surgical Ontology[J].Nutr Clin Pract,2009,24(4):520-526.
[22]Nachlas MM,Younis MT,Roda CP,et al. Gastrointestinal motility studies as a guide to postoperative management[J]. Ann Surg,1972,175(4):510-522.
[23]洪铮,江志伟,黎介寿.胃肠道肿瘤患者营养支持[J]. 肠外与肠内营养,2002,10(4):238-240.
[24]黄东平,张顾颈,罗浩,等. 胃肠道术后早期不同途径肠内营养的应用[J]. 肠外营养,2002,9(2):65-67.
(收稿日期:2012-05-02)

