微波改性废酵母菌吸附废水中铜(Ⅱ)离子热力学动力学研究
时代
(沈阳职业技术学院,辽宁 沈阳110045)
1 引言
为了满足社会日益增长的需求,矿物质开采和加工业迅速发展,这导致世界各地重金属污染严重。水中的重金属离子对人类产生严重的毒害作用,去除水中的重金属离子是需要迫切解决的课题。铜离子是城市污水中常见的重金属离子,其主要来源于某些工业废水,如漂洗和电镀废水中都含有大量的铜。铜离子会通过生物吸附作用在人体内积累,对人体健康造成了严重的威胁[1]。铜离子会使动物蛋白变性而产生毒性。因此,重金属离子在水中的浓度须降低到国家环境安全规定水平之下。
目前,有多种技术方法可用于去除水溶液中的重金属[2,3]。这些方法有絮凝法、化学沉淀法、离子交换法和吸附再生法[4]。其中吸附再生法是活性污泥法的一种。这种方法可以充分提高活性污泥的浓度,降低有机营养物和微生物之比,简单经济有效,现被广泛采用。
发酵工业的生物残渣含有细菌、酵母菌等多种类微生物,如饮料工业中的酵母菌、制作柠檬酸的真菌、酶工业中的葡萄糖和脂酶等[7,12]。本研究是以一种微波改性的废酵母菌作为吸附剂对废水中的铜离子进行吸附,因为活的酵母菌虽然效果好,但是价格较高且难以保存[4,5],给实验增加了难度。而废酵母菌具有易固化、反复使用的优点,可用于制造特殊生物吸附剂[6]。用失活的废酵母菌吸附废水中的重金属离子,能够节约废水处理成本,还可对生物残渣进行废物利用,达到了真正的以废治废[9,10]。
本研究对废酵母菌吸附废水中重金属离子Cu2+的实验过程进行了热力学、动力学研究,评价了废酵母菌对废水中重金属离子Cu2+的吸附效率[14],并对实验结果的数据采用Langmuir等温式进行了拟合。
2 实验方法
实验材料选用蒸馏水溶解定量分析纯的硫酸铜,配制500 mg/L的Cu2+溶液。实验用废酵母菌为沈阳某制药厂的液体状废菌泥。对废菌泥进行处理,将其取200m L置于烧杯中,放入微波炉在中高温状态下加热15min,对其进行微波改性,取出后放于烘箱内在恒温115℃状态下烘干,研磨成粉备用。
在不同参数条件下,在含一定浓度的初始溶液中分别加入不等量的微波改性酵母菌,搅拌后进行离心分离,取上清液测定其中残留Cu2+离子的含量。
3 结果和讨论
3.1 溶液的p H值对Cu2+吸附效果的影响
在温度25℃时,用 HCl和 NaOH(质量分数为10%)调节200m L含铜废水(浓度为100 mg/L)的p H值,在其p H 值为4.0、5.0、6.0、7.0、8.0、9.0、10.0时,用0.6g的微波改性废酵母菌加入废水中,振荡速度180r/min,反应120min,沉淀10 min,测定含铜废水反应后铜离子的变化见图1。
由图1可知,Cu2+的吸附效果受到p H值较大的影响。实验在振荡吸附时间充足、吸附剂用量适宜的前提下进行,Cu2+的去除率随着溶液p H值的升高而逐渐增大。当p H=7时,溶液为中性,溶液中吸附剂对Cu2+的去除率达到最大。这说明微波改性酵母菌对溶液中Cu2+吸附实验进行的最佳p H为7。
Cu2+的去除效果与溶液p H有关,因为酸碱性的变化会影响官能团的离子电荷性。在p H<7(溶液为酸性)时,大量的H3O+与金属离子竞争吸附位点,导致废酵母菌对Cu2+的吸附能力下降;当p H>7(溶液为碱性)时,生物吸附活性点受到影响,水解生成的氢氧化物沉积在废酵母菌表面,影响废酵母菌对Cu2+的吸附能力。
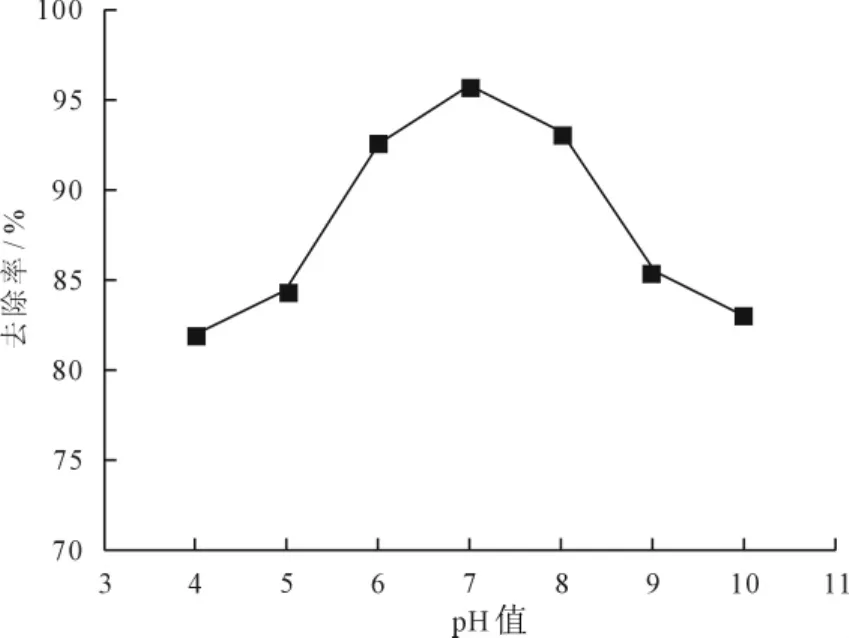
图1 溶液p H值对Cu2+吸附效果的影响
3.2 反应时间对Cu2+吸附效果的影响
在温度为25℃时,用 HCl和NaOH(质量分数为10%)调节200m L含铜废水(浓度为100 mg/L)的p H=7,取0.6g微波改性废酵母菌加入废水中,在振荡速度为180r/min时,将各组的反应时间分别取为30、60、90、120、150、180min,反应后沉淀10 min取其上清液测量浓度,所测定的铜离子去除率的变化趋势见图2。
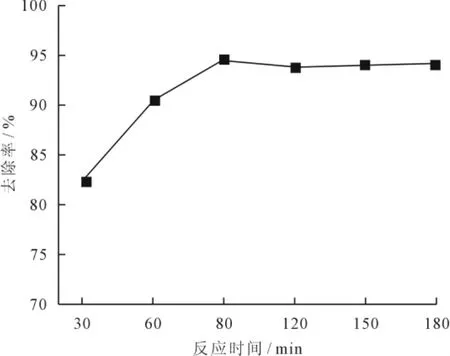
图2 反应时间对Cu2+吸附效果的影响
由图2可知,在初始的60min中,微波改性废酵母菌有大量的活性位点可与Cu2+反应,在这个过程中吸附反应速度非常快,溶液中Cu2+的去除率急剧上升,吸附效果非常好。溶液中可用于吸附Cu2+的生物活性吸附位点相对减少,Cu2+的去除率的上升趋势减缓,随着反应时间的增长,吸附剂与溶液充分接触反应,Cu2+的去除率逐渐增大。当吸附反应时间为90min时,去除率达到最大,为94.91%。
用准二级速率方程来拟合吸附过程,其吸附反应动力学分析见图3。由图可估算出qe=23.87mg/g,该值与 实 验 值 qe=23.68mg/g 接 近,相 关 系 数 R2=0.999 78。分析表明准二级动力学模型可以很好描述微波改性废酵母菌对废水中Cu2+的吸附过程。
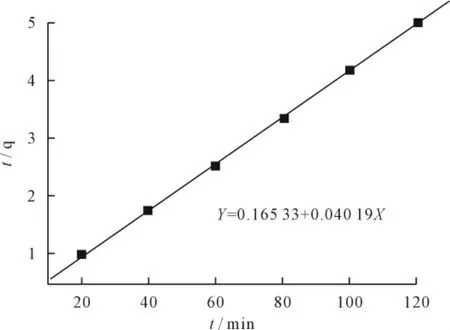
图3 准二级动力学方程拟合吸附剂对Cu2+的吸附
3.3 反应温度、溶液初始浓度及Cu2+浓度对吸附效果的影响
分别在反应温度为25、40、55、70℃时,将浓度分别为40、60、80、100、120、140 mg/L的含铜废水150m L用质量分数为10%HCl及NaOH调节p H值至7,废水中加入0.6g微波改性废酵母菌,在振荡速度为180r/min时反应90min后,沉淀10 min取上清液,测定其反应后Cu2+的变化,不同温度下吸附剂对Cu2+的吸附等温线见图4。
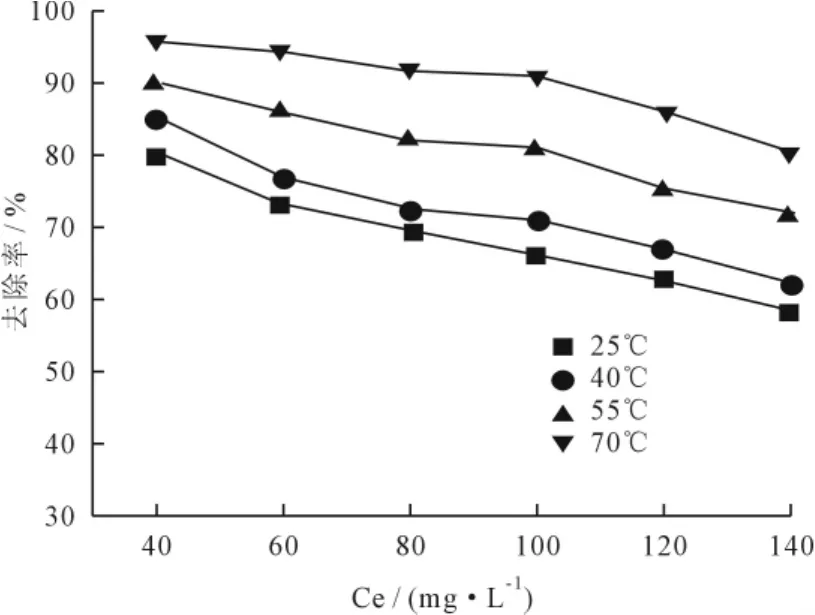
图4 不同温度下微波改性酵母菌对不同初始浓度的Cu2+吸附等温线
由图4可知,溶液中剩余铜离子的浓度也随着含铜废水初始浓度的增加而增加,吸附剂对Cu2+的去除率降低。当C0=40mg/L时铜的去除率最好,达到96.23%。
在吸附剂投加量不变的前提下,吸附位点的数量有限,当初始Cu2+浓度较低时,吸附剂能够提供充足的生物活性位点,此时Cu2+的去除率很高;而当初始Cu2+浓度升高时,其生物活性位点相对不足,吸附位点产生竞争,致使Cu2+无法完全被有限的废酵母菌吸附,导致对Cu2+的去除率下降。本次吸附反应过程采用Langmuir等温式对实验数据进行拟合(图5)。
图5中4条等温线的qm和KL数值通过线性回归实验数据得到。不同温度下Cu2+在微波改性酵母菌上的等温吸附常数见表1。表1显示吸附剂对Cu2+的吸附行为与Langmuir吸附等温线有较好相关性。
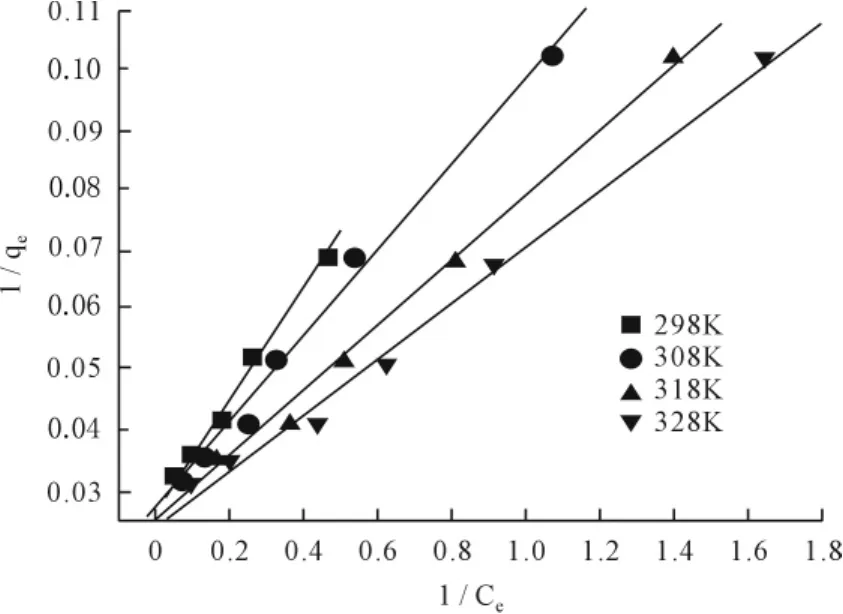
图5 微波改性酵母菌对Cu2+的Langmuir吸附等温线
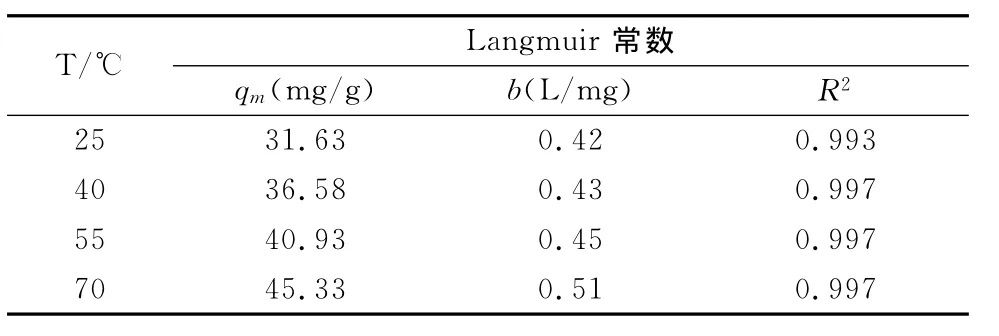
表1 不同温度下Cu2+在微波改性酵母菌上的等温吸附常数
由表1可知,随着反应温度不断升高,吸附剂对Cu2+的吸附量qe也随之增大。不同温度下吸附反应达到平衡,通过ln(qe/ce)对qe作图(图6)推出qe=0时的值。根据最小平方分析得到直线上的各点的热力学常数K0,数据见表2。
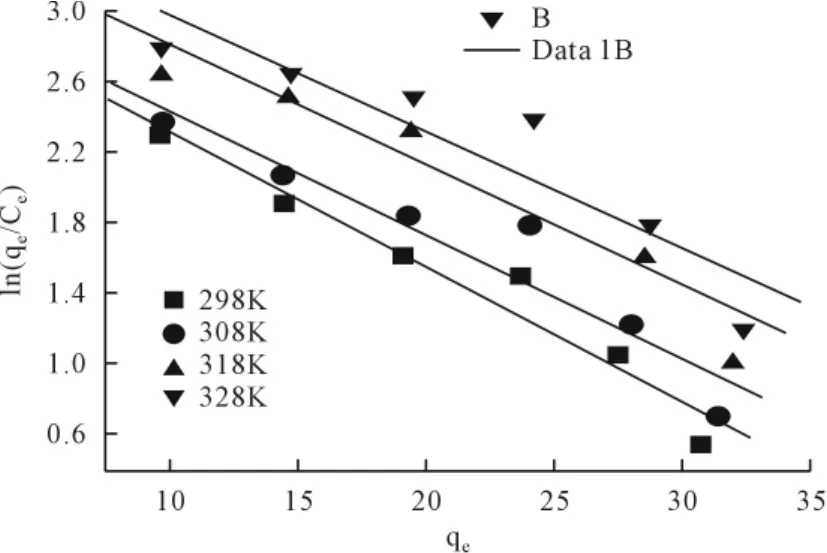
图6 不同温度下微波改性酵母菌对Cu2+的qe-ln(qe/ce)图

表2 不同温度下Cu2+在废酵母菌上的热力学常数K0
通过ln K对1/T作图,得到图7,计算出吸附反应的焓变△H和熵变△S。实验得到的标准焓变△H=3.169 09kJ/mol,这表明吸附剂对Cu2+的吸附过程是一个吸热反应。温度的升高有利于吸附的进行,在这4个温度下标准自由能变化△G0<0,并且随着温度的升高而变小,这说明了微波改性酵母菌对Cu2+的吸附过程是一个自发的过程,自发的程度随着温度的升高而增大。正的熵变△S=20.214 86J/Kmol可导致酵母菌表面官能团与被吸附溶液发生离子交换。△S0的正值也说明吸附质的自由度增加了。
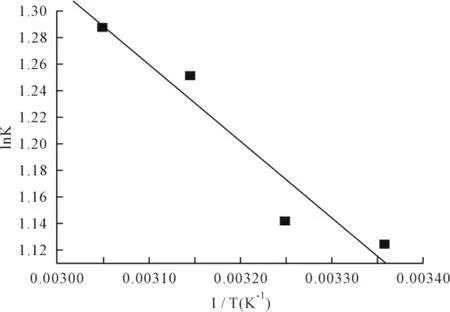
图7 Van'Hoff方程拟合微波改性酵母菌对Cu2+的吸附
4 结语
吸附剂微波改性废酵母菌对Cu2+的吸附过程表明,微波改性废酵母菌对Cu2+的吸附效果比较好,能够有效地去除废水中的Cu2+。
微波改性废酵母菌的最佳反应条件为:温度55℃、p H值7、吸附剂投加量4g/L、振荡速度180r/min、反应时间90min,废液中Cu2+的吸附效果达到最好。
由微波改性废酵母菌对Cu2+的吸附过程拟合,可知该吸附过程符合Langmuir吸附等式。微波改性酵母菌对Cu2+的吸附速率随着反应温度的升高而加快。正的标准焓变△H揭示废酵母菌对Cu2+的吸附过程是吸热反应。标准自由能变化△G0为负,说明该吸附反应是自发过程。吸附剂微波改性废酵母菌对Cu2+的吸附动力学模型能够较好地符合准二级动力学方程。
[1]邹家庆.工业废水处理技术[M].北京:化学工业出版社,2003.
[2]格鲁什科R M.工业污水中有毒金属及无机化合物[M].北京:科学出版社,1979.
[3]张剑波,王维敬,祝 乐.离子换树脂对有机废水中铜离子的吸附[J].水处理技术,2001,27(1):29~32.
[4]张景来,王剑波,常冠钦,等.冶金工业污水处理技术及工程实例[M].北京:化学工业出版社,2003.
[5]戴日成,张 统,郭 茜.印染废水水质特征及处理技术综述[J].给水排水,2000(10):211~213.
[6]Yao-Hui Huang,Chan-Li Hsueh,Hui-Pin Cheng,et al.Thermodynamics and kinetics of adsorption of Cu(II)onto waste iron oxide.Department of Chemical Engineering[M].Tainan:National Cheng Kung University,2006.
[7]张洪玲,吴海锁,王连军.生物吸附重金属的研究进展[J].污染防治技术,2003,16(4):53~56.
[8]Vethkar A V,Palnikar K M.Recovery of Gold form Solutiongs U-sing Cladasporium Biomass Beads[J].Journal of Bioteehnoloy,1998(63):121~136.
[9]Matis K A,Zouboulis A I,Grigoriadou A A,et al.Metalbiosorption-floation,application to cadmium removal[J].Appl Microbiol Biotechnol,1996(45):569~573.
[10]吴 涓,李清彪.重金属生物吸附的研究进展[J].离子交换与吸附,1998,14(2):180~18.
[11]李 霞.重金属对微生物的毒性作用[J].吉林师范学院学报,1995,20(3):64~65.
[12]甘一如.重金属的生物吸附[J].化学工业与工程,1999,16(1):19~25.
[13]夏 君,瞿建国,马锦民.含锌废水的微生物处理技术[J].化工环保,2005,25(3):191~194.
[14]Lawrence R Drake,Gray D Rayson.Plant-derived,materials for matel lon-seletive binding and preconcentration[J].Anal Chem,1996(68):22A~27A.
[15]Duncan J R,Brady D Rose,Peter D Miner.Bioprocess[J].Proc Eng Found Conf,1995(6):189~197.

