天可力氨糖胶囊中氨基葡萄糖硫酸钾测定方法比较
吴素玲,张卫明,孙晓明,张锋伦,许国宁
(南京野生植物综合利用研究院,江苏南京210042)
本实验参照GB/T 20365-2006采用液相色谱法[1]及应用 Fdson—Morgan反应原理采用比色法[2-6]对天可力氨糖胶囊中氨基葡萄糖硫酸钾含量进行测定比较,建立了天可力氨糖胶囊中氨基葡萄糖硫酸钾含量的测定方法。
1 液相法测定氨基葡萄糖含量
1.1 材 料
1.1.1 材料及试剂 氨基葡萄糖盐酸盐标准品:中国药品生物制品检定所;
天可力氨糖胶囊:自制,主要成分为:氨基葡萄硫酸钾∶中药A和中药B=55∶45(m/m);
氨基葡萄糖硫酸钾盐:由扬州日兴生物化工制品有限公司提供,为白色结晶粉,纯度≥99%;
植物提取物A和植物提取物B:由宣城伊康天然产物科技开发责任有限公司提供;
戊烷磺酸钠:江苏省疾控中心提供,分析纯;
HPLC分析用乙腈:色谱纯,美国TEDIA;
HPLC分析用水:为娃哈哈纯净水;
戊烷磺酸钠溶液:称取0.174 g戊烷磺酸钠,用纯净水溶解,移至100 mL容量瓶中,定容,溶液浓度为10 mmol/L。
1.1.2 主要仪器设备 电子天平EL-410s:美国Setra;KQ-600E型数控超声波清洗器:昆山市超声仪器有限公司;Agilent 1200高效液相色谱仪:安捷伦科技有限公司;色谱柱:Zorbax C18(5 μm,150 mm×4.6 mm),安捷伦科技有限公司。
1.2 实验方法
1.2.1 标准溶液的配制 称取氨基葡萄糖盐酸盐标准品13.8 mg,加入2.5 mL乙腈,振荡使其分散均匀,再加入纯净水,超声溶解,定容至25 mL,摇匀,备用。浓度为:0.552 mg/mL。
1.2.2 样品待测液的制备 (1)氨基葡萄糖硫酸钾盐溶液:称取样品35.0 mg,加入2.5 mL乙腈,振荡使其分散均匀,再加入水,超声溶解,定容至50 mL,摇匀,备用。HPLC测定前,用0.2 μm 滤膜过滤。(2)植物提取物A溶液:称取样品51.6 mg,后面操作同(1)。(3)植物提取物B溶液:称取样品49.9 mg,后面操作同(1)。(4)天可力氨糖胶囊溶液:称取胶囊内容物129.6 mg,加入5.0 mL乙腈,振荡使其分散均匀,再加入水,超声溶解,定容至100 mL,摇匀,备用。HPLC测定前,用0.2μm滤膜过滤。
1.2.3 HPLC的色谱条件 HPLC的色谱条件是:Agilent 1200,四元泵;Eclipse XDB - C18,分离柱(4.6 mm ×15 mm,5 μm);柱温25 ℃;DAD 检测器;流动相:乙腈:戊烷磺酸钠水溶液(10 mmol/L。0.87 g戊烷磺酸钠溶解于500 mL水中)=1∶9;流速:0.5 mL/min;进样量:10 uL。检测波长:192 nm。
1.2.4 HPLC的色谱测定 分别将标准液、各样品液注入液相色谱仪以上述色谱条件进行色谱测定,记录其峰面积,对照标准液浓度进行计算。
1.2.5 计 算 (1)样品氨基葡萄糖含量按照以下公式计算:
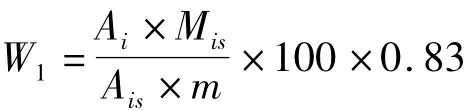
式中,W1:样品中氨基葡萄糖含量,%;Ai:样品溶液中被测物峰面积;Mis:标准溶液中被测物标准品的质量,mg;Ais:标准溶液被测物标准品的色谱峰面积;m:样品的质量,mg;0.83:氨基葡萄糖(179)与盐酸氨基葡萄糖(216.35)的相对分子质量比。
(2)样品氨基葡萄糖硫酸钾盐含量=样品中氨基葡萄糖含量÷0.6
式中0.6为:氨基葡萄糖(179)与氨基葡萄糖硫酸钾盐(297.32)的相对分子质量比。
1.3 结 果
通过HPLC测定,各图谱结果如下图1、图2、图3、图 4、图 5。记录其峰面积,对照标准液浓度按上述公式进行计算得结果为下表1。
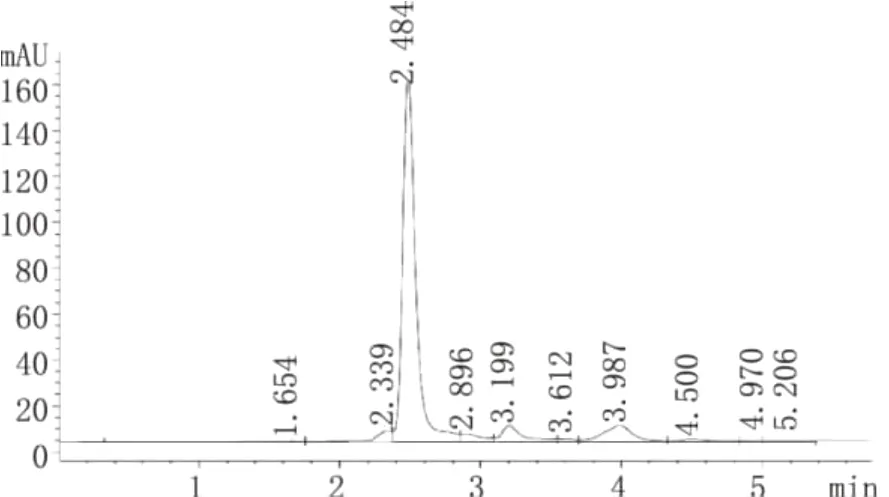
图1 氨基葡萄糖盐酸盐图谱
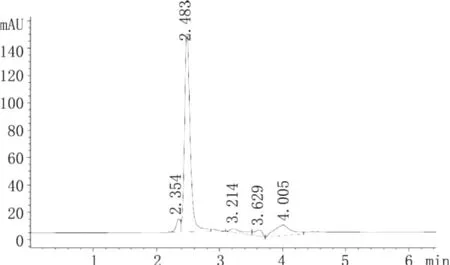
图2 氨基葡萄糖硫酸钾图谱
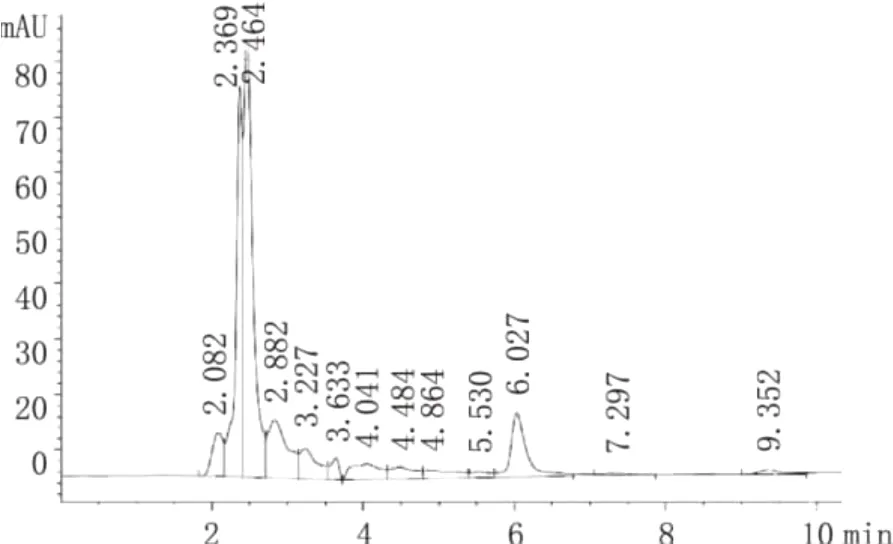
图3 植物提取物A图谱
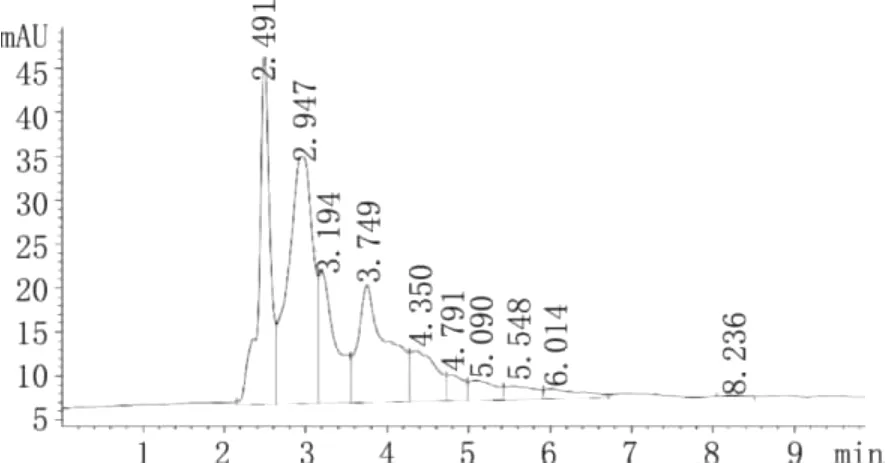
图4 植物提取物B图谱
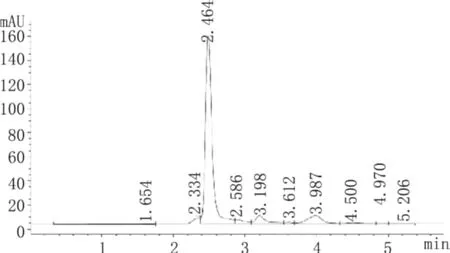
图5 天可力氨糖胶囊内容物图谱
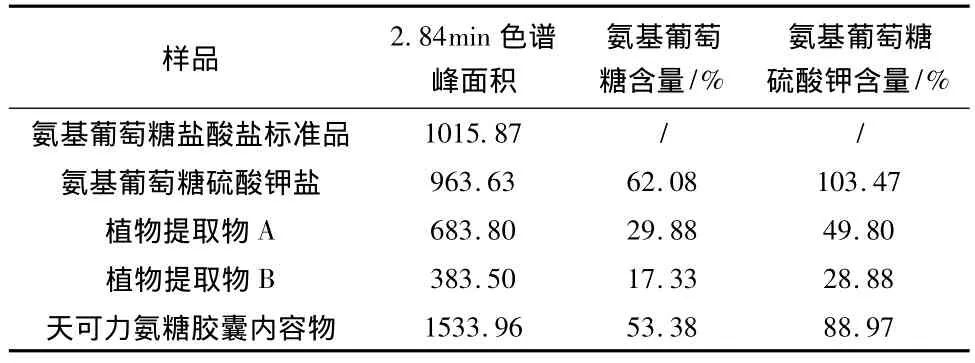
表1 含量分析结果
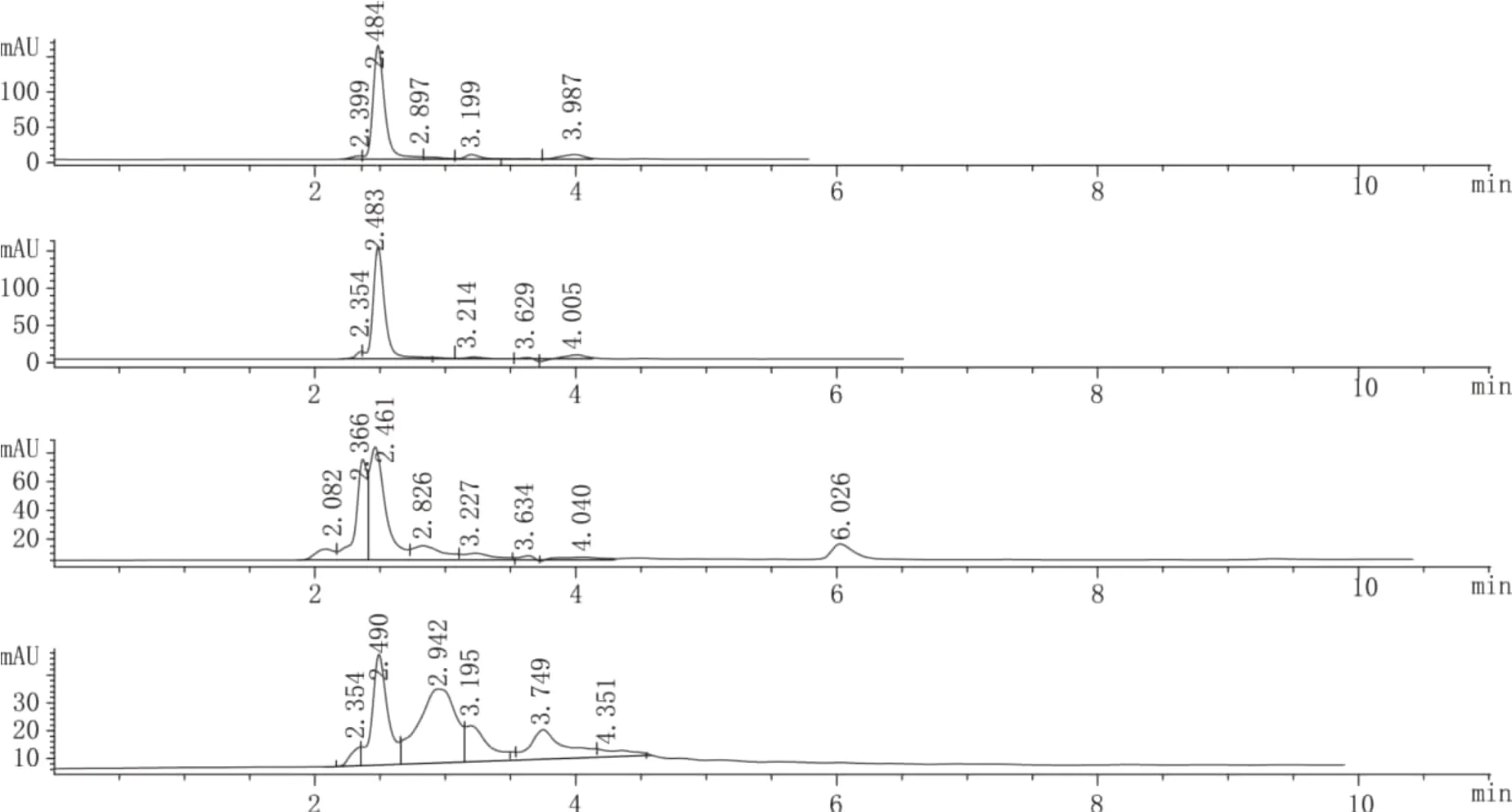
图6 对比图
1.4 结果分析
把图1、图2、图3、图4的图谱进行对比得到如下 图6。
从各HPLC图谱及上面的对比图都能清楚看出氨基葡萄糖盐酸盐、氨基葡萄糖硫酸钾盐、植物提取物A、植物提取物B在该色谱条件下,2.84 min均有明显的色谱峰,也就是说通过这个方法植物提取物A和植物提取物B中都能测得氨基葡萄糖含量。并且从结果数据看如果折成氨基葡萄糖硫酸钾则含量达到49.80%和28.88%,这对天可力氨糖胶囊中实际添加的氨基葡萄糖硫酸钾测定有相当大的干扰作用。
天可力氨糖胶囊配方中氨基葡萄糖硫酸钾含量为55%,但从表1中可见测得得到的含量值为88.97%,这个测得方法导致测得氨基葡萄糖硫酸钾含量为实际含量的162%。
这个方法对添加有植物提取物等成分比较复杂的混合物中的氨基葡萄糖的含量是很不可靠的。
2 比色法测定氨基葡萄糖含量
2.1 材 料
2.1.1 材料及试剂 氨基葡萄糖盐酸盐标准品、天可力氨糖胶囊、氨基葡萄糖硫酸钾盐、植物提取物A和植物提取物B:见1章;
盐酸、无水乙醇、碳酸钠、乙酰丙酮、对二甲氨基苯甲醛:市售,为分析纯;
Na2CO3试液:精确取其5.3 g碳酸钠,溶于蒸馏水中,定溶至100 mL.浓度为0.5 mol/L;
乙酰丙酮试液:取2 mL乙酰丙酮溶液,加碳酸钠溶液溶解,定溶至100 mL。(过夜后用)含量为2%;
对二甲氨基苯甲醛酸醇溶液:精确取其0.6 g,分别加入10mL无水乙醇和10 mL浓盐酸配制而成。含量为3%。
2.1.2 主要仪器设备 电子天平EL-410s、KQ-600E型数控超声波清洗器:见1节;TU-1800紫外可见分光光度计:北京普析通用仪器有限责任公司;旋转蒸发器RE-52AA:海亚荣生化仪器厂,做水浴锅用。
2.2 方法与结果
2.2.1 测定方法扫描验证 取样品和标准品用蒸馏水配制成浓度约100 μg/mL的溶液,各取2 mL加5 mL2%乙酰丙酮试液和3 mL蒸馏水摇匀,置沸水浴中加热20 min后流动冷却水冷却;再加2 mL3%对二甲氨基苯甲醛酸醇溶液和8 mL无水乙醇摇匀,置60℃水浴中加热60 min后流动冷却水冷却,在40 min内不同放置时间后进行400~700 nm波长范围扫描。
结果一:标准品盐酸氨基葡萄糖和样品氨基葡萄糖硫酸钾在254 nm附近都有明显的吸收峰,而植物提取物A和植物提取物B没有吸收峰。见图7、8、9、10。
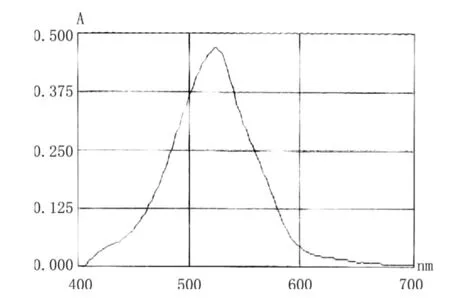
图7 盐酸氨基葡萄糖扫描图
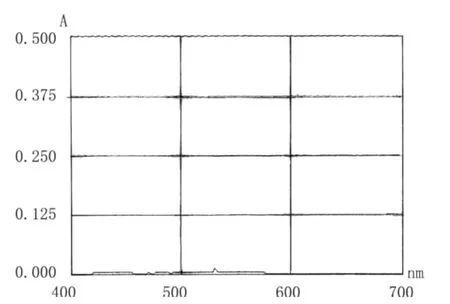
图8 植物提取物A扫描图
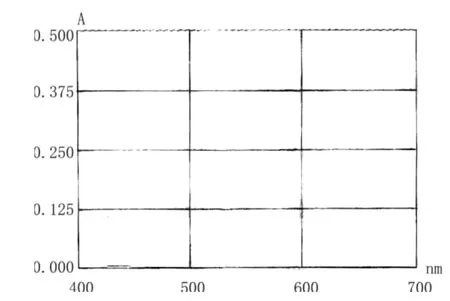
图9 植物提取物B扫描图
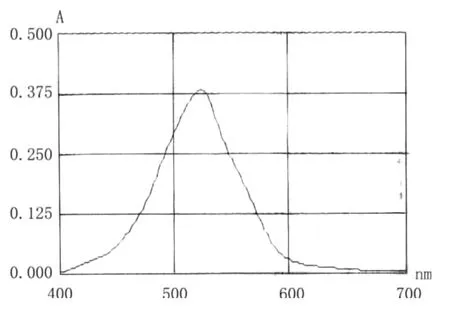
图10 氨基葡萄糖硫酸钾扫描图
结果二:标准品在40 min内不同放置时间进行扫描其吸收峰及吸收值略有变化,其吸收峰基本在524 nm处,吸收值5到10 min时有所上升,10 min后逐渐下降,但变化非常小。具体数据列于下表2。
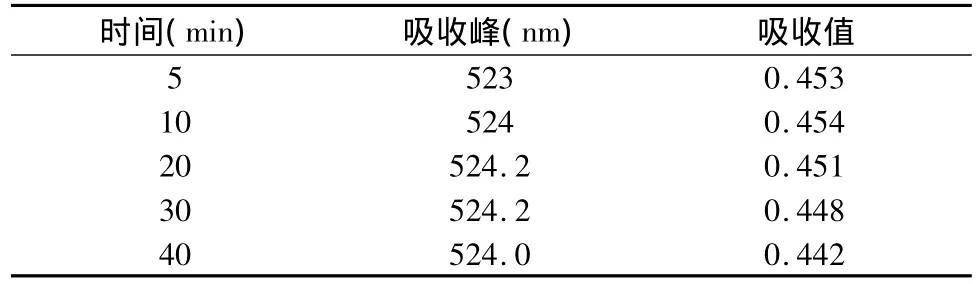
表2 不同放置时间其吸收峰及吸收值的变化
根据上述结果,我们决定测定时,时间为10 min后,测定波长为524 nm。
2.2.2 标准曲线的制备 称取氨基葡萄糖盐酸盐标准品50 mg,定溶于50 mL容量瓶中,浓度为1 mg/mL;然后分别取 0.25、0.50、0.75、1.00、1.25、1.50、1.75 mL定容至10 mL容量瓶,制成浓度为:25μg/mL、50μg/mL ......150μg/mL、175μg/mL 的标准液。分别按下表2顺序在各试管中加入各种试剂,流动水冷却置10 min左右后,以“0”管作空白对照,测定OD250值并填入表2中。以OD254值为纵坐标,标准溶液浓度为横坐标绘制标准曲线,得标准曲线为:Y(μg/mL)=0.196X-O.004,R=0.997(n=6)。结果表明实验中标准溶液浓度在175 μg/mL内与吸收值(λ=254 nm)有线性关系良好。

表2 试剂加量表
2.3 样品中氨基葡萄糖含量的测定
2.3.1 样品配制 精确称取1.000 g待测样溶于蒸馏水中,定容于100 mL容量瓶中,于30℃下超声波溶解30 min,再取1 mL定容于100 mL容量瓶中,待用。各样品浓度列入下表3。
2.3.2 样品的测定 分别取各样品液2 mL代替标准液,按标准曲线制备的方法,测定样品的OD250值,然后按照标准曲线回规方程计算氨基葡萄糖盐酸盐含量。然后折算成氨基葡萄糖含量及氨基葡萄糖硫酸钾含量。结果如下表3。
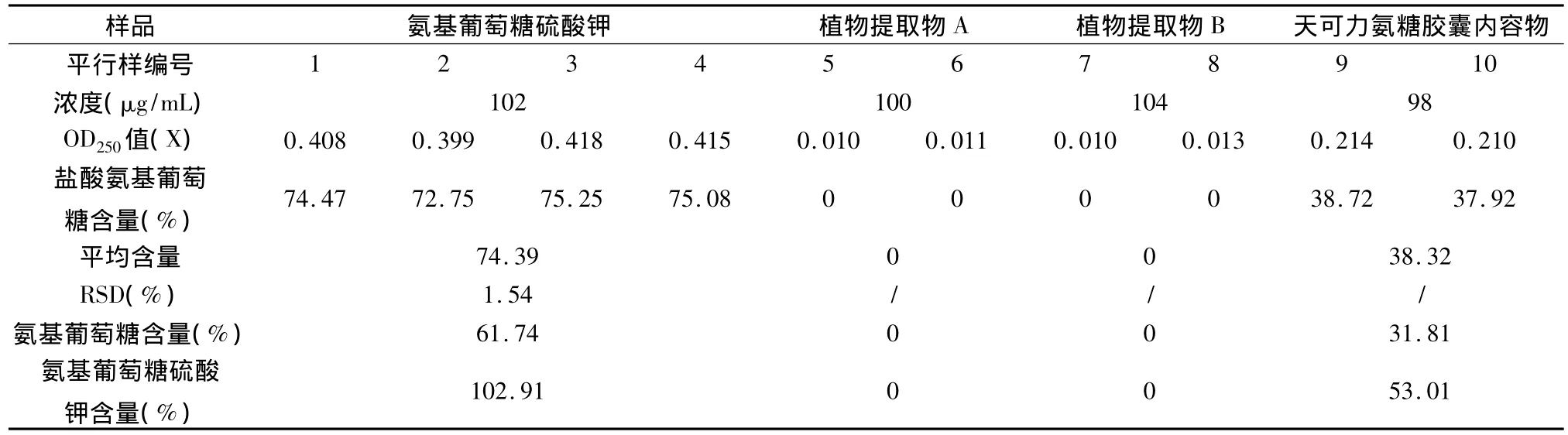
表3 样品中氨基葡萄糖含量
2.4 回收率的测定
精密称取30、50、70 mg氨基葡萄糖硫酸钾(纯度≥99%)各3份,各加约等量的已测定过氨基葡萄糖含量为零的植物提取物A,加蒸馏水溶解,移至9只100 mL容量瓶中,用蒸馏水定容至刻度;各取定容液10 mL置100 mL量瓶中,加水稀释至刻度,制成含盐酸氨基葡萄糖分别为30、50、70μg/mL试液各3份。按2.2标准曲线制备方法显色后,测定,计算回收率,结果见表4。
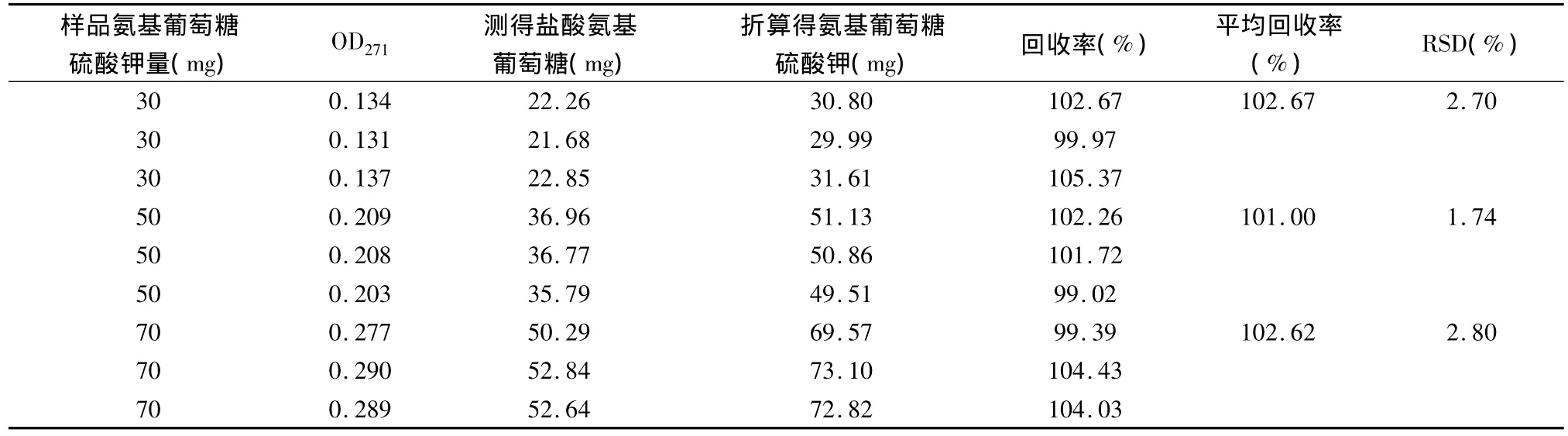
表4 回收率测定表
3 结果分析
本方法是利用氨基葡萄糖结构中2一甲基葡萄糖胺在碱性条件下与乙酰丙酮缩合形成生色吡咯,再与对二甲氨基苯甲醛在酸性条件下结合成红色缩合物,在524 nm波长处测定吸收值与标准品比较定量。测定时,氨基葡萄糖盐酸盐含量在170 μg/mL浓度范围内,呈良好线性关系,R=0.997,平均回收率102.09%。本实验方法经过方法学的考察,重复性良好,回收率高,结果数据准确可靠,方法灵敏、准确、简便,可供天可力氨糖胶囊中氨基葡萄糖硫酸钠含量测定。
[1] GB/T 20365-2006硫酸软骨素和盐酸氨基葡萄糖含量的测定液相色谱法[S].
[2] 中华人民共和国卫生部.药品标准 二部(第六册)[S].1998:108.
[3] 孙旭群,杨旭,王效山.N-甲基葡萄糖胺反应法测定盐酸氨基葡萄糖影响因素考察[J].中国医院药学杂志,2007,27(10):1478-1479.
[4] 冉兰,张榕,文霞,等.比色法测定盐酸氨基葡萄糖片的含量[J].华西药学杂志,2001,16(3):217 -2l8.
[5] 韩宝芹,刘万顺,崔丽华,等.昆羧甲基壳聚糖中氨基葡萄糖含量测定方法的研究[J].中国海洋大学学报,2004,34(5):811-815.
[6] 赵海珍,姚丽娜.中药保健品中D-氨基葡萄糖盐酸盐含量测定[J].黑龙江医药,2008,21(5):27-28.

