生物安全三级实验室核心区排风高效空气过滤器原位消毒的研究
韩文东,孙志平,丁悦娜,曹明波,瞿涤
1. 复旦大学上海医学院生物安全三级实验室,上海200032; 2. 上海申美空气洁净技术有限公司, 上海 200050
生物安全三级实验室(biosafety level 3 laboratory, BSL-3实验室)是高致病性病原微生物研究和检测的技术保障平台。在《人间传染的病原微生物名录》中归类为可引起人类或动物严重感染性疾病的第2类病原微生物(如高致病性禽流感病毒、结核分枝杆菌、朊病毒、粗球孢子菌等)的相关研究应在BSL-3实验室进行[1]。国务院424号令《病原微生物实验室生物安全管理条例》规定,BSL-3实验室在依法获得批准建设项目后,按照《实验室生物安全通用要求》(GB19489)的规范建设并通过中国合格评定国家认可委员会(China National Accreditation Service for Conformity Assessment,CNAS)的认可,所从事的实验活动需获得国务院卫生部或兽医主管部门的许可[2]。为适应我国生物安全实验室建设和管理的需要,新国家标准GB19489-2008自2009年7月1日起实施,要求已(在)建的BSL-3实验室须按照新国家标准进行认可转换评审。新国家标准中重点要求改进设施的内容:BSL-3实验室应在原位对排风高效空气(high efficiency particulate air,HEPA)过滤器进行消毒灭菌和检漏[3]。为适应此要求,本实验室对防护区内HEPA过滤器排风箱体进行改造,采用了可进行原位消毒和扫描检漏的设备 CamContain Ceil-X[4],通过连接粒子计数器等可在原位进行扫描检漏。该产品虽配置了配套的测试罩(universal test shroud),但无相应可实现原位消毒的配套设备,而BSL-3实验室更换排风HEPA过滤器时,需确保彻底消毒后方能拆卸以保证生物安全。根据本实验室的具体情况,设计消毒样机,通过甲醛熏蒸方法,利用生物指示剂对核心区排风HEPA过滤器原位消毒的效果进行了验证。
1 材料和方法
1.1 材料
1.1.1菌种嗜热脂肪芽胞杆菌菌片(SS1.K31)、枯草芽胞杆菌黑色变种(ATCC9372)购自北京鑫四环消毒技术开发有限公司,耻垢分枝杆菌(MC2155)由第四军医大学徐志凯教授惠赠,金黄色葡萄球菌(ATCC25923)由本实验室课题组保存。
1.1.2试剂胰蛋白胨、酵母提取物、胰蛋白胨大豆肉汤 (tryptone soya broth,TSB)购自英国Oxiod公司,溴甲酚紫(染料含量90%)、无水D-葡萄糖(纯度≥99.5%)购自Sigma公司,Difco Middlebrook 7H9 Broth培养基、Difco Middlebrook 7H10琼脂、 BBL Middlebrook ADC Enrichment培养基、BBL Middlebrook OADC Enrichment培养基购自美国BD公司。消毒剂为37%~40%甲醛溶液(分析纯,含10%~15%甲醇,国药集团化学试剂有限公司产品)。
1.1.3HEPA过滤器箱体特征BSL-3实验室核心区排风箱体CamContain Ceil-X wall mounted room-side exhaust containment(CX-S-28D38E-18D-F-F-12-F-BK-S-0-16D-0-0-2-S-1),美国Camfil Farr公司生产,HEPA过滤器对0.3 μm气溶胶粒子的过滤效率为99.99%~99.9995%。配套通用测试罩(UTS to perform pressure decay testing and decontamination)可通过连接测试车进行HEPA过滤器的原位扫描检漏。排风箱体后端连接排风管道处设有密封阀,且测试罩与箱体后端都配有消毒管道接口,从而可外接循环消毒风机实现对HEPA过滤器的原位消毒。
1.2 方法
1.2.1细菌菌片的制备嗜热脂肪芽胞杆菌菌片(SS1.K31),载菌量5×105~106CFU/片;枯草芽胞杆菌黑色变种(ATCC9372)菌片,载菌量5×105~106CFU/片;耻垢分枝杆菌(MC2155)菌片,取培养的菌液(OD450 nm为1.0)100 μl均匀涂布于0.5 cm×1.0 cm滤纸(滤纸购自Bio-Rad,Cat No. 1704085),取100 μl菌液倍比稀释后接种于Middlebrook 7H10琼脂(含10% OADC增菌液)平板培养,通过计数计算菌片的载菌量;金黄色葡萄球菌(ATCC25923)菌片,取培养的菌液(OD450 nm为1.0)100 μl均匀涂布于0.5 cm×1.0 cm滤纸,取100 μl菌液倍比稀释后接种于TSB琼脂平板培养,计算菌片的载菌量。
1.2.2消毒效果的微生物检测甲醛蒸汽熏蒸消毒程序结束后,将菌片取出,置于含5 ml培养液的培养管中,其中嗜热脂肪芽胞杆菌菌片90 ℃孵育60 min,培养基为溴甲酚紫葡萄糖蛋白胨培养基(胰蛋白胨10 g、葡萄糖5 g、1.6%溴甲酚紫乙醇溶液指示剂1 ml,加蒸馏水定容至1 000 ml,高压蒸汽灭菌121 ℃,15 min),56 ℃培养24 h后观察并记录;继续培养144 h,观察并记录细菌生长。枯草芽胞杆菌黑色变种菌片培养基为LB培养基(牛肉膏5 g、蛋白胨10 g、氯化钠5 g,加蒸馏水定容至1 000 ml,高压蒸汽灭菌121 ℃,15 min);耻垢分枝杆菌菌片培养基为Middlebrook 7H9培养基(含10% ADC增菌液);金黄色葡萄球菌菌片培养基为TSB培养基。以上3种菌片均置于37 ℃培养箱培养,24 h后观察并记录细菌生长情况。
1.2.3HEPA过滤器原位消毒菌片的放置将用于消毒检测的4种菌片置于24孔板,每种菌6个菌片/24孔板,共4块,分别放置于HEPA过滤器排风箱体内侧壁的正面、底面、顶面、侧面,待消毒。
1.2.4细菌菌片培养的结果判定金黄色葡萄球菌、耻垢分枝杆菌、枯草芽胞杆菌需在35~37 ℃培养24 h,肉眼无可见细菌菌落且培养液颜色无变化,则判定为无菌生长,即消毒有效;嗜热脂肪芽胞杆菌需在55~60 ℃培养168 h,肉眼无可见细菌菌落且培养液颜色无变化,则为消毒灭菌有效。
2 结果
2.1 用于HEPA过滤器原位消毒的循环消毒样机的设计与消毒程序的确定
2.1.1用于HEPA过滤器原位消毒的循环消毒样机的设计针对本实验室更换的Camfil Farr排风HEPA过滤箱体配套测试罩及其带有消毒剂灌注输出接口的结构特点[4],设计可用于该排风箱体消毒的循环消毒样机(图1)。样机尺寸为600 mm×300 mm×450 mm(长×宽×高),内部平均分为前后两室。在样机的前室内放置F50型甲醛熏蒸灭菌器(北京克力爱尔生物实验室工程有限公司)与AIRO-SWISS加湿器,以保证甲醛气体湿度;后室为循环风机,带动消毒气体沿排风方向定向循环穿透HEPA过滤器。
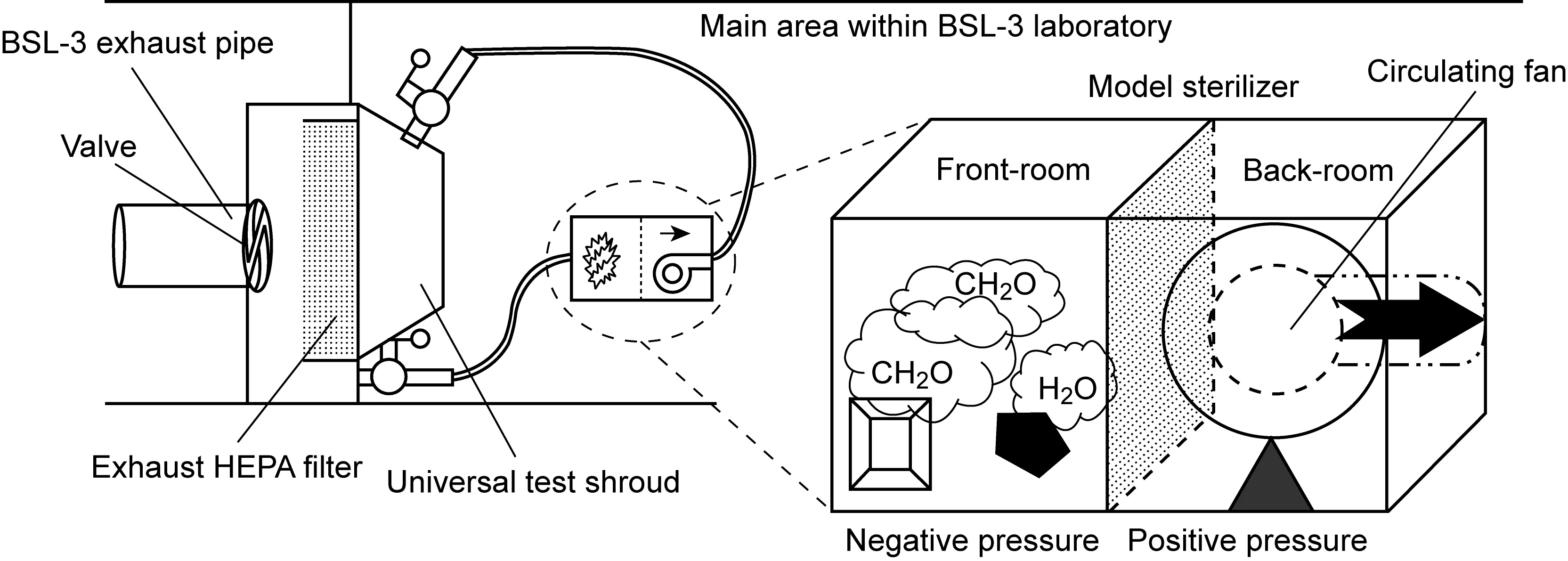
图1HEPA过滤器原位消毒的消毒样机设计图
Fig.1ModelsterilizerandprocessofsterilizationofHEPAfilterinsitu
1.2.5甲醛蒸汽循环消毒程序的确定甲醛蒸汽循环消毒程序分为3个阶段。① 甲醛气体发生:向F50型甲醛熏蒸灭菌器注入甲醛溶液(约37%),45 ml/m3(甲醛气体在消毒空间内比例约16 mg/L)[5],加热挥发甲醛完毕,同时加湿。② 循环穿透消毒过程:启动循环风机,甲醛消毒气体在风机带动下沿排风方向穿过HEPA过滤器。③ 排出消毒气体:打开CamContain箱体与排风管道连接处的密闭阀,开启外接风机15 min,将甲醛气体排出HEPA过滤器及消毒样机组成的循环系统。甲醛蒸汽消毒体系湿度约70%。为确定消毒的有效时间,将嗜热脂肪芽胞杆菌及金黄色葡萄球菌菌片(菌片置平皿中)放置于消毒样机管道的盲端,连接管道形成自循环(未连接HEPA过滤器排风箱体),分别熏蒸2 h和12 h,检测甲醛蒸汽熏蒸循环的消毒效果。结果显示,甲醛蒸汽循环消毒2 h,金黄色葡萄球菌菌片(107CFU/片)培养后培养液澄清透明,而嗜热脂肪芽胞杆菌菌片培养后培养液由紫色变成黄色并可见大量细菌生长(菌液浑浊)。甲醛蒸汽熏蒸消毒12 h后,嗜热脂肪芽胞杆菌菌片培养液为紫色透明状,未见细菌生长。
2.2 甲醛蒸汽循环消毒法对细菌消毒效果的评价
进一步采用嗜热脂肪芽胞杆菌、枯草芽胞杆菌黑色变种菌片及自制的耻垢分枝杆菌、金黄色葡萄球菌菌片(表1),通过消毒样机与CamContain排风箱体的消毒接口连接,对 HEPA过滤器原位甲醛蒸汽循环消毒法的消毒效果进行评估。首先将含有菌片的24孔板(每种菌片6个复孔)分别放置于待消毒HEPA过滤器排风箱体内侧壁的正面、底面、顶面、侧面。
经甲醛蒸汽循环消毒作用2 h后,取出菌片,培养24 h,金黄色葡萄球菌菌片和耻垢分枝杆菌菌片肉眼观察无菌生长;嗜热脂肪芽胞杆菌菌片的培养液由紫色澄清变黄色浑浊,枯草芽胞杆菌黑色变种菌片的培养液由浅黄色澄清变深黄色浑浊,均可见菌片附着大量细菌菌落,与未消毒对照组培养结果相似。经高压灭菌(121 ℃,15 min)的对照组培养后无菌生长(表2)。
表1用于评估HEPA过滤器原位消毒的细菌
Tab.1BiologicalindicatorsforsterilizationofHEPAfilterinsituwithformaldehydesterilization
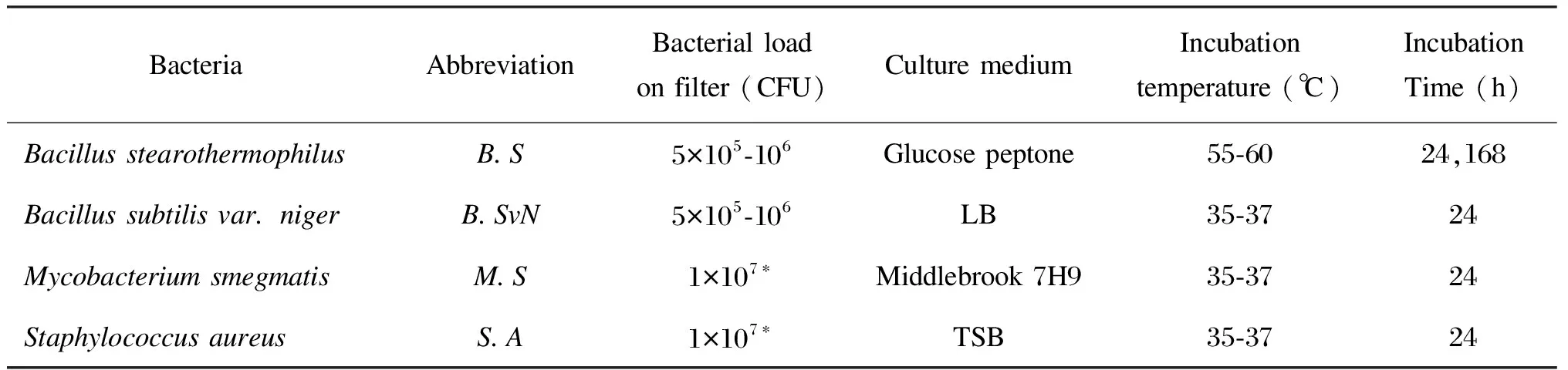
BacteriaAbbreviationBacterial load on filter (CFU)Culture mediumIncubation temperature (℃)Incubation Time (h)Bacillus stearothermophilusB.S5×105-106Glucose peptone55-6024,168Bacillus subtilis var. nigerB.SvN5×105-106LB35-3724Mycobacterium smegmatisM.S1×107∗Middlebrook 7H935-3724Staphylococcus aureusS.A1×107∗TSB35-3724
Pipet 100 μl bacterial suspension culture (OD450 nm=1.0) on rectangle filter paper (about 5 mm×10 mm, biological indicators ofMycobacteriumsmegmatis(MC2155),Staphylococcusaureus(ATCC25923) are achieved; and then inoculate 100 μl bacterial suspension culture (OD450 nm=1.0) diluted by 10 times on culture media plates, and bacterial load on filter was about 107CFU by counting the bacterial colonies on the plates.
表2室温甲醛蒸汽循环熏蒸消毒效果的评估
Tab.2Effectsofformaldehydesterilizationondifferentbiologicalindicators
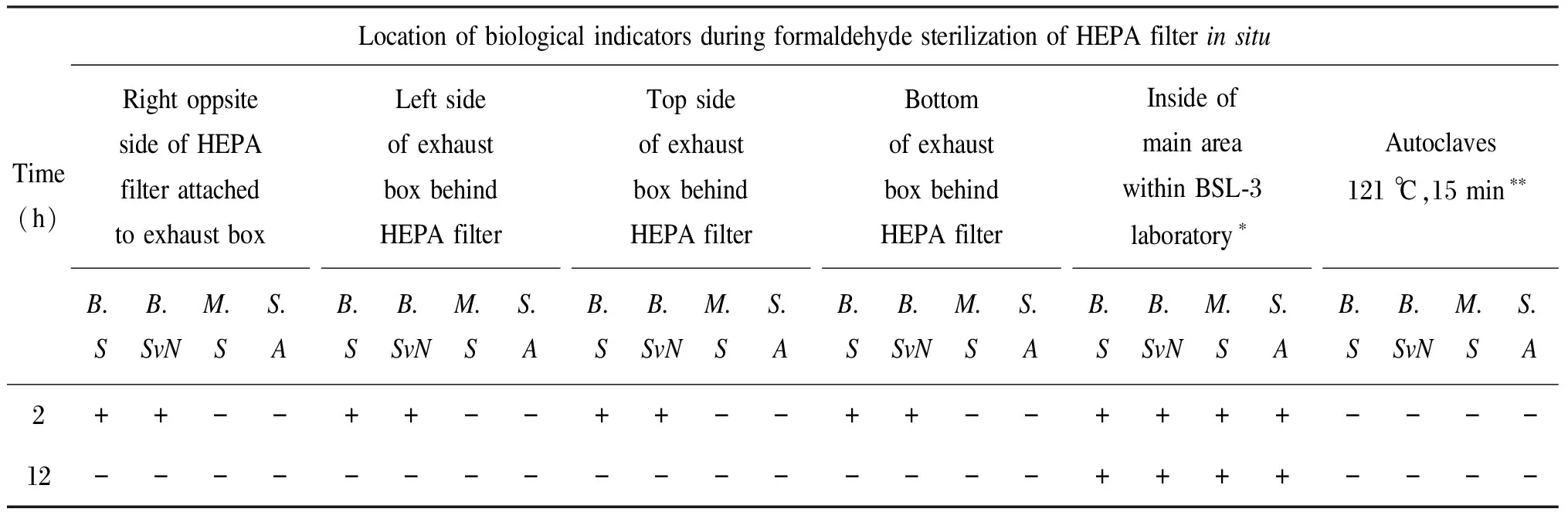
Time (h)Location of biological indicators during formaldehyde sterilization of HEPA filter in situRight oppsite side of HEPA filter attached to exhaust boxB.SB.SvNM.SS.ALeft side of exhaust box behind HEPA filterB.SB.SvNM.SS.ATop side of exhaust box behind HEPA filterB.SB.SvNM.SS.ABottom of exhaust box behind HEPA filterB.SB.SvNM.SS.AInside of main area within BSL-3 laboratory∗B.SB.SvNM.SS.AAutoclaves 121 ℃,15 min∗∗B.SB.SvNM.SS.A2++--++--++--++--++++----12----------------++++----
“+” indicates growth of bacteria after incubation; “-” indicates no growth of bacteria after incubation; *, negative control, no sterilization; **, positive control, autoclaved by 121 ℃, 15 min.
甲醛蒸汽循环消毒作用12 h后,取出用于检测HEPA过滤器原位消毒的菌片,培养24 h后,耻垢分枝杆菌与金黄色葡萄球菌的菌片均无细菌附着生长,培养液澄清透明;嗜热脂肪芽胞杆菌菌片培养液为紫色澄清,未见菌片有附着生长的细菌,继续培养144 h,未见培养液中细菌生长;枯草芽胞杆菌黑色变种菌片培养液为浅黄色澄清,未见菌片有附着生长的细菌,继续培养144 h,未见培养液中细菌生长(表2)。HEPA过滤器经甲醛蒸汽消毒灭菌后,对4个位置的菌片,每个位置每种菌片各取3个样本进行培养。结果显示,4个位置的培养结果一致,无明显生长差异(图2)。同时对放置于HEPA过滤器排风箱体内侧壁的正面、底面、顶面、侧面的菌片,进行平行培养,各组培养结果一致。
3 讨论
新国家标准《实验室生物安全管理要求》(GB19489-2008)指出,BSL-3实验室设计的送、排风系统必须确保实验室运行时气流由低风险区向高风险区流动,同时实验室的空气只能通过HEPA过滤器过滤后才能排出[3],因此实验室内操作的高致病性病原微生物随实验操作气溶胶(约0.3 μm颗粒)化后随定向气流流动,通过HEPA过滤器时被拦截于HEPA过滤器(对0.3 μm颗粒的过滤效率约99.99%)。在BSL-3实验室运行过程中,需定期更换HEPA过滤器。其一,可保证HEPA过滤器的前后阻力在可控制范围,保证送、排风系统联动机制的稳定,提高BSL-3实验室系统运行的稳定。《实验室生物安全管理要求》2008版较2004版在通风空调系统方面提出了更加严格的要求[3, 6],两者比较见表3。其二,BSL-3实验室核心区的排风HEPA过滤器存在被实验活动所操作的高致病性病原微生物污染的风险,因此更换HEPA过滤器前,必须在原位对HEPA过滤器进行彻底消毒,从而保证操作人员及BSL-3实验室内环境的生物安全。

图2室温甲醛蒸汽循环熏蒸12h后指示菌片培养
Fig.2CultureofbiologicalindicatorsforsterilizationofHEPAfilterinsituafter12-hourcontinuousformaldehydefumigationsterilizationatroomtemperature
表3不同气体消毒方法的对比
Tab.3Comparisonofdifferentgassterilizationsforsporicidalefficiency*

Types of sterilization Gas concentration (mg/L)TemperatureExposure time (min)Main disadvantagesLTSF8-1660-80>120Potential carcinogenEOG450-1 200 37-6360-360Hazards to skin and nervous system, carcinogen HPGP637-4452-75Low penetration capabilities
*, 106reduction of spores; LTSF, low-temperature steam formaldehyde; EOG, ethylene oxide gas; HPGP, hydrogen peroxide gas plasma.
目前,BSL-3实验室空间消毒的方法主要有低温甲醛蒸汽熏蒸消毒(low-temperature steam formaldehyde sterilization,LTSF)、环氧乙烷气体消毒(ethylene oxide gas sterilization,EOG)、过氧化氢气体消毒(hydrogen peroxide gas plasma sterilization,HPGP)。对比3种气体消毒方法(表3)可以看出,HPGP优于LTSF及EOG,但需专门的过氧化氢气化设备,价格昂贵而不能普及;而EOG对皮肤、神经系统的损伤及致癌能力较强。因此,本研究选择甲醛作为消毒剂。甲醛通过对蛋白质中的氨基、巯基基团及嘌呤碱环中的氮原子烷基化杀灭微生物[7]。在北欧、德国、英国及发展中国家,低温甲醛蒸汽熏蒸消毒广泛应用于不耐热医疗器械及其附件的消毒:向密闭容器中间断地注入水蒸气与甲醛[8],维持甲醛浓度在8~16mg/L、蒸汽温度处于70~75 ℃,以达到消毒效果。该方法操作简便、快速、价廉,可用于杀灭植物细菌、分枝杆菌及抵抗力更强的萎缩芽胞杆菌、嗜热脂肪芽胞杆菌等[9,10]。
目前仍无确切研究证实甲醛蒸汽在室温下消毒的效果[11]。BSL-3实验室核心区的排风HEPA过滤器消毒在室温下进行,消毒气体必须循环穿透HEPA过滤器才能达到彻底消毒的目的。本研究设计的甲醛蒸汽熏蒸消毒样机对HEPA过滤器原位消毒的结果显示,室温条件下,甲醛蒸汽浓度为16 mg/L,相对湿度70%,维持循环消毒时间12 h,可有效杀灭105~106嗜热脂肪芽胞杆菌及枯草芽胞杆菌,达到HEPA过滤器原位消毒的目的。
BSL-3实验室需监测采用的消毒程序对所操作的病原微生物(或模式菌)的灭菌效果,如实验室从事病毒、真菌或其他高致病性病原微生物,则应对相应微生物的灭菌效果进行监测(或采用灭菌抵抗性高于相应微生物的指示菌(biological indicator)。本实验室所操作的病原微生物是结核分枝杆菌,所以选择的细菌菌片指示剂既有耻垢分枝杆菌,又有抵抗性强的芽胞菌片,且常规灭菌效果监测都是通过对芽胞菌片的杀灭来直接反映消毒方法的有效性。枯草芽胞杆菌(106)是验证EOG效果的常用指示菌,嗜热脂肪芽胞杆菌 (105) 常用于高压蒸汽灭菌、过氧化氢气体及过氧乙酸溶液灭菌效果的验证。根据本实验室从事的病原微生物实验活动,选择嗜热脂肪芽胞杆菌、枯草芽胞杆菌、耻垢分枝杆菌、金黄色葡萄球菌作为消毒方法有效性验证的生物指示剂。结果显示,室温甲醛气体消毒2 h能有效杀灭耻垢分枝杆菌、金黄色葡萄球菌,但对嗜热脂肪芽胞杆菌及枯草芽胞杆菌无效。将甲醛气体消毒循环时间延长至12 h,可有效杀灭所有的测试细菌,包括嗜热脂肪芽胞杆菌及枯草芽胞杆菌。为了验证甲醛蒸汽循环消毒法对从事结核分枝杆菌的实验室排风HEPA过滤器的消毒效果,本研究选择耻垢分枝杆菌作为消毒效果的指示菌。结果显示,甲醛蒸汽循环2 h即可有效杀灭耻垢分枝杆菌,为BSL-3实验室消毒、清场方法的建立及风险评估提供了参考依据。本研究结果也提示:①不同BSL-3实验室应根据所操作的高致病性病原微生物及进行的相关实验活动,选择相应生物指示菌作为消毒效果的验证;②应根据BSL-3实验室排风HEPA过滤器的结构特点,设计消毒程序并进行有效性验证;③消毒程序的有效性验证实验设计应以简单、有效为原则,以保证有关工作的常态性,保障BSL-3实验室的生物安全。
[1] 中华人民共和国卫生部. 人间传染的病原微生物学名录[EB/OL]. 2006. http://www.moh.gov.cn/publicfiles/business/htmlfiles/mohbgt/pw10602/200804/20471.htm.
[2] 中华人民共和国国务院. 病原微生物实验室生物安全管理条例[EB/OL]. 2004. http://www.gov.cn/zwgk/2005-05/23/content_256.htm.
[3] 中华人民共和国国家质量监督检验防疫总局,中国国家标准化管理委员会. 实验室生物安全通用要求[S/OL]. 2008. http://ishare.iask.sina.com.cn/f/13579399.html?from=like.
[4] Farr C. CamContain Ceil ceiling mounted roomside exhaust containment module with auto-scan testing capability [EB/OL]. 2010. http://www.filterair.info/literature/Files/camcontain_ceil_product_sheet.pdf.
[5] Rutala WA, Weber DJ, the Heakthcare Infection Control Practices Advisory Committee. Guideline for Disinfection and Sterilization in Healthcare Facilities, 2008 [M/OL]. 2008. http://www.cdc.gov/hicpac/Disinfection_Sterilization/acknowledg.html.
[6] 中华人民共和国国家质量监督检验防疫总局,中国国家标准化管理委员会. 实验室生物安全通用要求[S/OL]. 2004. http://ishare.iask.sina.com.cn/f/12797767.html?from=like.
[7] Block SS. Disinfection, Sterilization, and Preservation [M]. 5th ed. Philadelphia: Lippincott Williams & Wilkins, 2001.
[8] Roncoroni AJ, Casewell MW, Phillips I. The disinfection of clinically contaminated Matburn suction pumps and baby incubators in an ‘Aseptor’ formalin cabinet [J]. J Hosp Infect,1980,1(3):251-259.
[9] Kanemitsu K, Kunishima H, Imasaka T, Ishikawa S, Harigae H, Yamato S, Hirayama Y, Kaku M. Evaluation of a low-temperature steam and formaldehyde sterilizer [J]. J Hosp Infect,2003,55(1):47-52.
[10] Kanemitsu K, Imasaka T, Ishikawa S, Kunishima H, Harigae H, Ueno K, Takemura H, Hirayama Y, Kaku M. A comparative study of ethylene oxide gas, hydrogen peroxide gas plasma, and low-temperature steam formaldehyde sterilization [J]. Infect Control Hosp Epidemiol,2005,26(5):486-489.
[11] Cumberland NS, Botting FG. Formaldehyde vapour cabinets [J]. J Hosp Infect,1991,19(1):67-70.

