重组结核分枝杆菌ESAT6-CFP10蛋白对不同分枝杆菌致敏豚鼠的皮试反应研究
蒲江 陶立峰 邓海清 王德海
据WHO统计,2010年,全球约有140万人死于肺结核,880万罹患结核病,结核病已成为当今世界第二大传染性疾病[1-2]。我国是全球22个结核病流行最严重的国家之一,同时也是全球27个耐多药结核病流行最严重的国家之一。据2010年全国第五次结核病流行病学调查的数据,全国15岁及以上人群活动性肺结核的患病率为459/10万[3],因此早期发现和诊断出高危人群,有效控制传染源,是结核病疫情控制的关键。
近几年,对早期分泌性抗原性靶蛋白(ESAT6)和早期培养滤液蛋白10(CFP10)抗原作为结核诊断的皮试试剂的研究较多,显示出很好的安全性及较好的诊断特异度和敏感度[4-11]。本研究以重组结核分枝杆菌ESAT6-CFP10蛋白作为抗原,对不同分枝杆菌菌种致敏的豚鼠进行皮试反应研究。
材料和方法
一、材料
1.动物:选取90只健康并未做过任何试验的SPF级(无特定病原体级)白色雌性豚鼠(Hartley品系),体质量300~400 g(一般体质量满足即可采用),周龄为15~20周。由中国食品药品检定研究院实验动物实验中心提供,实验动物使用许可证号:SYXK(京)2009-0017。
2.菌种:常见环境分枝杆菌组包括鸟分枝杆菌(CMCCB 95001)、胞内分枝杆菌(CMCCB 95002)、蟾蜍分枝杆菌(CMCCB 95003)、堪萨斯分枝杆菌(CMCCB 95013)、海分枝杆菌(CMCCB 95014)、瘰疠分枝杆菌(CMCCB 95017)、戈登分枝杆菌(CMCCB 95018)、苏加分枝杆菌(CMCCB 95019)、龟分枝杆菌脓肿亚种(CMCCB 95021)(简称“龟脓分枝杆菌”)、偶发分枝杆菌(CMCCB 95022)、草分枝杆菌(CMCCB 95024)、微黄分枝杆菌(CMCCB 95030);临床常见致病分枝杆菌组包括非洲分枝杆菌(CMCCB 95049)、牛分枝杆菌(CMCCB 95055)、结核分枝杆菌(CMCCB 95052,CMCCB 93020,CMCCB 93009);菌株由中国医学细菌保藏管理中心提供。卡介菌(疫苗株)由中国食品药品检定研究院提供。
3.主要试剂:结核菌素纯蛋白衍生物(purified protein derivative of tuberculin,TB-PPD),50 IU/ml,批号为20101105,液体制剂,由中国食品药品检定研究院提供;胞内分枝杆菌纯蛋白衍生物(PPD of Mycobacterium intracellulare,PPD-B),0.4 mg/支,由中国食品药品检定研究院提供;重组结核分枝杆菌ESAT6-CFP10蛋白,每支250μg/0.5 ml,液体制剂,批号为 M20101202,由安徽龙科马生物制药有限责任公司提供。
二、方法
1.菌液制备:取卡介菌冻干菌种(60 mg/支),以1 ml生理盐水溶解后制成浓度为60 mg/ml的菌液。将其余15种新鲜培养的分枝杆菌配制成10 mg/ml菌液(活菌含量约为1×108CFU/ml),临用前再以生理盐水进行10倍稀释。
2.动物筛选(皮试):将豚鼠左背侧局部去毛,皮内注射0.2 ml TB-PPD,于注射后24、48 h观察局部硬结的纵径与横径,根据48 h的反应结果进行判定,平均硬结反应直径(纵径与横径相加除以2)小于5 mm判为阴性[12]。90只豚鼠全部皮试阴性,留做实验。共分为18组实验,每组使用5只豚鼠。
3.致敏动物:于豚鼠腹股沟皮下注射制备的菌液[13],每种菌液致敏5只豚鼠(皮试48 h后,如果皮试阴性,即可开始致敏)。卡介菌(疫苗株)活菌致敏组豚鼠和结核分枝杆菌死菌致敏组豚鼠各注射0.2 ml/只,饲养于清洁级动物房;其他分枝杆菌活菌菌液致敏组豚鼠注射0.5 ml/只,饲养于负压动物房的负压动物笼具中。
4.重组结核分枝杆菌ESAT6-CFP10蛋白的制备:采用基因工程手段构建ESAT6-CFP10融合蛋白表达载体,筛选阳性菌落并测序正确,建立生产用种子批系统[14]。将工作种子通过复苏、传代后发酵,最终通过纯化获得重组结核杆菌ESAT6-CFP10目的蛋白。
5.致敏动物皮试:在致敏动物3~4周后,将豚鼠背部脊柱两侧去毛,以轮圈法[15]分别于豚鼠皮内注射1μg/ml和5μg/ml的ESAT6-CFP10蛋白、1μg/ml和5μg/ml的PPD-B、TB-PPD(50 IU/ml)各0.1 ml。于注射后24、48 h观察局部硬结的纵径与横径,根据48 h的反应结果进行判定,平均硬结反应直径≥5 mm判为阳性[16]。
结 果
一、临床常见致病分枝杆菌致敏豚鼠的皮试反应结果
皮试反应显示,TB-PPD、ESAT6-CFP10蛋白以及PPD-B对结核分枝杆菌、牛分枝杆菌、卡介菌(疫苗株)和非洲分枝杆菌活菌致敏豚鼠的皮试反应均呈阳性,而ESAT6-CFP10蛋白对卡介菌(疫苗株)、结核分枝杆菌死菌致敏豚鼠的皮试反应呈阴性(图1)。硬结直径统计及阳性比例见表1。
二、常见环境分枝杆菌组致敏豚鼠的皮试反应结果
PPD-B对鸟、胞内、蟾蜍、堪萨斯、海、瘰疠、戈登、苏加、龟脓、偶发、草、微黄分枝杆菌这12种常见环境分枝杆菌致敏豚鼠的皮试反应均呈阳性,而ESAT6-CFP10蛋白以及TB-PPD对上述分枝杆菌致敏豚鼠的皮试反应均呈阴性,48 h的皮试硬结直径与阳性比例结果见表2。
讨 论

图1 致敏豚鼠皮试硬结状况
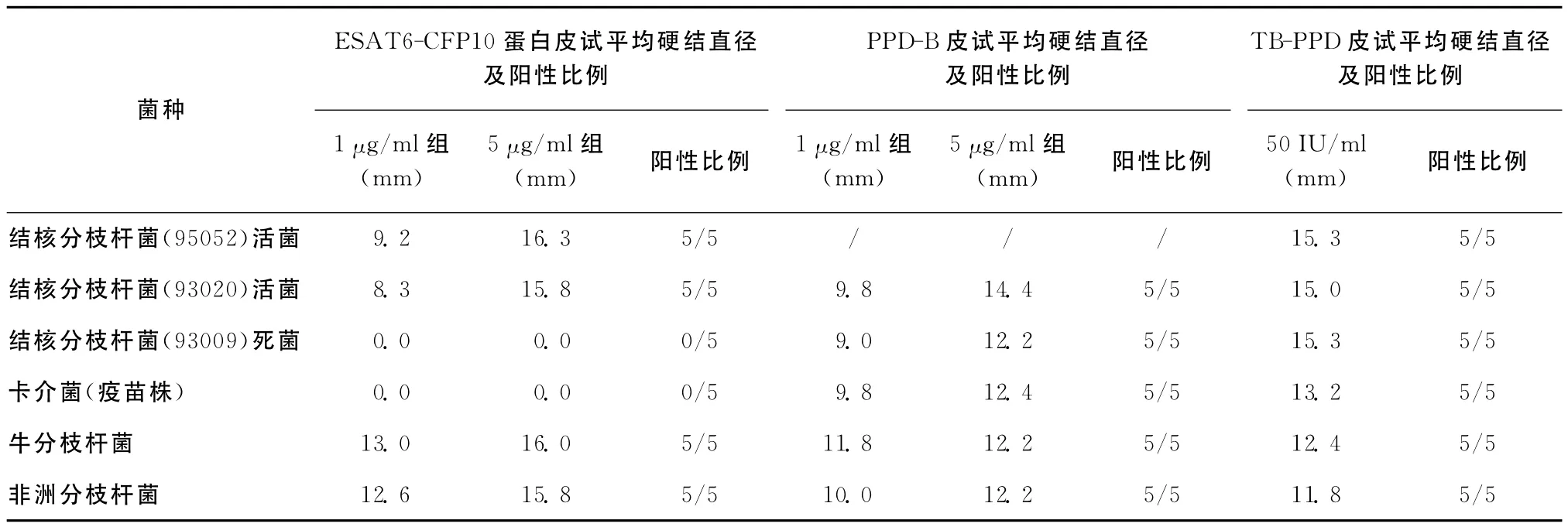
表1 临床常见致病分枝杆菌组致敏豚鼠致敏后48 h的皮试平均硬结直径及阳性比例

表2 常见环境分枝杆菌致敏组豚鼠48 h皮试平均硬结直径及阳性比例
多年来,结核菌素皮肤试验(tuberculin skin testing,TST)一直是筛选结核分枝杆菌潜伏感染和结核病辅助诊断的重要方法。但TST所用PPD所包含的抗原为常见致病性分枝杆菌(结核、牛和非洲分枝杆菌)、环境中的分枝杆菌(鸟、胞内、蟾蜍、堪萨斯、海、瘰疠、戈登、苏加、龟脓、偶发、草、微黄等分枝杆菌)及BCG所共有,诊断特异度较差,不能区分BCG接种、非致病性分枝杆菌感染和结核分枝杆菌感染,更不能鉴别结核分枝杆菌感染者体内有无存活的结核分枝杆菌;而卡介苗在世界范围内广泛接种会干扰TST的检测,减少其诊断效果。对于某些严重结核病、血行散播性肺结核或HIV感染者等免疫力低下者,TST诊断的敏感度也不理想。因此,寻找既能区别卡介苗接种还是结核分枝杆菌感染、结核分枝杆菌感染者体内有无活菌又敏感度高的诊断方法非常重要。
Maheiras等[17]确定了结核分枝杆菌基因的差别区(regions of difference,RD),其中最为重要的RD1区基因为结核分枝杆菌和牛分枝杆菌有毒株所特有,而BCG和大多数非结核分枝杆菌缺失。ESAT6是RD1区发现较早的重要分泌型蛋白,由Rv3875基因编码,全长285个碱基对,编码95个氨基酸。1998年Berthet等[18]在研究ESAT6基因表达调控机制时,发现了Lhp基因。Lhp基因即Rv3874基因,位于ESAT6基因上游34 bp处,和ESAT6基因处于同一操纵单元。此基因编码100个氨基酸,又由于其基因产物在早期培养滤液中出现,因此命名为培养滤液蛋白10(CFP 10)。ESAT6基因和CFP10基因处于同一操纵子中,一起进行协同转录。基因产物均为分泌性蛋白,存在于结核分枝杆菌的早期培养滤液中。
ESAT6蛋白和CFP10蛋白作为结核分枝杆菌的特异性抗原,两者具有大致相同的菌间分布特性。根据Swissprot和Genbank数据库资料分析,ESAT6基因和CFP10基因严格限制于结核分枝杆菌复合群和4种非典型分枝杆菌(堪萨斯、海、微黄和苏加分枝杆菌)中,BCG和大部分非结核分枝杆菌缺失[16,19-20]。虽然研究两基因菌间分布特性所用到的菌株不完全相同,但实验结果足以说明CFP10和ESAT6基因具有大致相同的菌间分布,即两基因严格限制于结核分枝杆菌复合群,BCG和大部分的非结核分枝杆菌缺失。
目前国内外研究较多的是将CFP10和ESAT6蛋白作为刺激原,应用体外酶联免疫吸附测定(enzyme linked immunosorbent assay,ELISA)或酶联免疫斑点法(enzyme linked immunospot assay,ELISPOT)技术诊断结核病。Ravn等[21]的一项研究结果显示:在39名无结核分枝杆菌暴露史的BCG接种健康人中,PPD-ELISA 的阳性率为100%,而CFP10-ESAT6-ELISA 阳性仅有1例,具有良好的诊断特异度。对痰菌阴性结核患者用ESAT6和CFP10抗原进行体外诊断,87%的患者能够被发现,敏感度较好。
近几年,以ESAT6为抗原作为结核诊断的皮试试剂研究也较多。国内张灵霞等[4]报道将ESAT6作为皮肤反应试剂用于结核病诊断,发现ESAT6皮试可以很好地区分结核分枝杆菌感染和BCG致敏的动物。国内徐苗等[5]对ESAT6基因进行改构得到重组11 k Da蛋白,在动物实验研究发现,重组结核分枝杆菌11 k Da蛋白对结核分枝杆菌活菌、牛分枝杆菌、非洲分枝杆菌和堪萨斯分枝杆菌致敏豚鼠的皮肤试验为阳性,而对灭活结核分枝杆菌、卡介菌和其他非结核分枝杆菌致敏豚鼠的皮肤试验均为阴性。Aggerbeck等[6]研究发现重组ESAT6蛋白在豚鼠、小鼠和狗等动物上均有较好的安全性,皮试浓度从1μg到1000μg仅有个别轻微不良反应出现。目前,ESAT6蛋白作为皮试试剂已经进入Ⅰ期临床,国外Arend等[7]随机双盲临床实验显示,ESAT6有很好的临床安全性和生物活性。国内 Wu等[8]报道在小部分志愿者中进行ESAT-6蛋白皮试,结果显示ESAT-6蛋白仅诱导结核患者阳性反应,BCG接种健康者为阴性反应。
目前以CFP-10蛋白作为皮试试剂,仅在动物实验见到相关报道,尚无临床试验数据。国外Van Pinxteren等[9]研究发现CFP10和ESAT6两种蛋白,均能很好的诱导结核分枝杆菌致敏豚鼠的皮试呈阳性反应。而在BCG和鸟分枝杆菌致敏豚鼠中,两种蛋白皮试结果阴性或仅有个别阳性,敏感度和特异度均好于PPD,但CFP10蛋白的特异度低于ESAT6蛋白。同时IFN-γ体外刺激试验结果显示两种蛋白联用的敏感度和特异度均高于单一蛋白[9]。Weldingh等[10]的实验结果也显示两种蛋白联用的敏感度与PPD相近,较单一抗原敏感度高。
本研究利用基因工程技术融合表达CFP10-ESAT6蛋白,该蛋白仅对活结核分枝杆菌、牛分枝杆菌和非洲分枝杆菌致敏动物呈阳性反应,对卡介菌接种或死结核分枝杆菌及常见环境分枝杆菌致敏动物均呈阴性反应,提示CFP10-ESAT6蛋白如果作为皮试试剂能够鉴别BCG接种和结核分枝杆菌感染,可为结核病的辅助诊断提供强有力的支持。如能应用于临床,将对结核病的诊断及传播控制有着非常重要的意义。但是由于本研究实验组数较多,工作量比较大,再加上课题时间的限制,每组实验只采用了5只豚鼠,统计学上可能存在一定的误差,这也是今后进一步深入研究所需要改进之处。
由于中国属于结核病高发地区,可为临床研究规模和内容提供良好空间,如果上述动物实验的数据能在人体得到验证,该结果将为临床上结核病的早期诊断和鉴别诊断提供重要的依据,为结核病的控制节省大量的资源。
[1] World Health Organization.WHO warns of consequences of underfunding TB.2011[2011-10-11].http://www.who.int/mediacentre/news/releases/2011/tb_20111011/en/index.html.
[2]World Health Organization.Global tuberculosis control 2011.Geneva:WHO,2011.
[3]全国第五次结核病流行病学抽样调查技术指导组,全国第五次结核病流行病学抽样调查办公室.2010年全国第五次结核病流行病学抽样调查报告.中国防痨杂志,2012,34(8):485-508.
[4]张灵霞,吴雪琼,史迎昌,等.几种结核分支杆菌重组蛋白诱发豚鼠迟发型超敏反应的研究.中国防痨杂志,2002,24(3):116-118.
[5]徐苗,罗永艾,黎有伦,等.重组结核分枝杆菌11000蛋白对结核分枝杆菌感染的鉴别作用.中华结核和呼吸杂志,2006,29(11):762-765.
[6]Aggerbeck H,Madsen SM.Safety of ESAT 6.Tuberculosis(Edinb),2006,86(5):363-373.
[7]Arend SM,Franken WP,Aggerbeck H,et al.Double-blind randomized Phase I study comparing rd ESAT-6 to tuberculin as skin test reagent in the diagnosis of tuberculosis infection.Tuberculosis(Edinb),2008,88(3):249-261.
[8]Wu X,Zhang L,Zhang J,et al.Recombinant early secreted antigen target 6 protein as a skin test antigen for the specific detection of Mycobacterium tuberculosis infection.Clin Exp Immunol,2008,152(1):81-87.
[9]Van Pinxteren LA,Ravn P,Agger EM,et al.Diagnosis of tuberculosis based on the two specific antigens ESAT-6 and CFP-10.Clin Diagn Lab Immunol,2000,7(2):155-160.
[10]Weldingh K,Andersen P.ESAT-6/CFP10 skin test predicts disease in M.tuberculosis-infected guinea pigs.PLoS One,2008,3(4):e1978.
[11]Huber CA,Ruf MT,Pluschke G,et al.Independent loss of immunogenic proteins in Mycobacterium ulcerans suggests immune evasion.Clin Vaccine Immunol,2008,15(4):598-606.
[12]卫生部疾病预防控制局,卫生部医政司,中国疾病预防控制中心.中国结核病防治规划实施工作指南(2008版).北京:中国协和医科大学出版社,2009.
[13]国家药典委员会.中华人民共和国药典三部.北京:化学工业出版社,2010.
[14]Sambrook J,Russell DW.分子克隆实验指南.3版.黄培堂,主译.北京:科学出版社,2002.
[15]中国生物制品标准化委员会.中国生物制品规程.北京:化学工业出版社,2000.
[16]Dillon DC,Alderson MR,Day CH,et al.Molecular and immunological characterization of Mycobacterium tuberculosis CFP-10,an immunodiagnostic antigen missing in Mycobacterium bovis BCG.Clin Microbiol,2000,38(9):3285-3290.
[17]Maheiras GG,Sabo PJ,Hickey MJ,et al.Molecular analysis of genetic differences between Mycobacterium bovis BCG and virulent M.bovis.Bacteriol,1996,178(5):1274-1282.
[18]Berthet FX,Rasmussen PB,Rosenkrands I,et al.A Mycobacterium tuberculosis operon encoding ESAT-6 and a novel lowmolecular-mass culture filtrate protein(CFP-10).Microbiology,1998,144(Pt11):3195-3203.
[19]Sorensen AL,Nagai S,Houen G,et al.Purification and characterization of a low molecular-mass T-cell antigen secreted by Mycobacterium tuberculosis.Infect Immun,1995,63(5):1710-1717.
[20]Harboe M,Oettinger T,Wiker HG,et al.Evidence for occurrence of the ESAT-6 protein in Mycobacterium tuberculosis and virolent Mycobacterium bovis and for its absence in Mycobacterium bovis BCG.Infect Immun,1996,64(1):16-22.
[21]Ravn P,Munk ME,Andersen AB,et al.Prospective evaluation of a whole-blood test using Mycobacterium tuberculosis-specific antigens ESAT-6 and CFP-10 for diagnosis of tuberculosis.Clin Diag Lab Immunol,2005,12(4):491-496.

