碳源对碳热法制备LiFePO4/C复合电极材料性能的影响
吴 浩 卢建树
(浙江工业大学材料化学实验室,浙江 杭州 310014)
0 引言
自从1997年具有橄榄石结构的磷酸铁锂被发现后就用在二次锂离子电池的正极材料中,其理论容量为170mAh/g,具有安全、环保、价格低廉、稳定性好等优点,被认为是动力型锂离子电池的首选正极材料[1-4]。但是由于LiFePO4材料极低的电子电导率和离子扩散速率的缺点,导致高倍率充放电性能较差。目前主要通过添加导电剂(碳、金属粉末等)和体相掺杂来提高材料的电子电导率[5-7];通过控制材料的粒径来提高离子扩散速率[8-9]。
通过国内外专家学者10多年的研究已经取得了相当大的进展,磷酸铁锂的制备工艺日益成熟。但是,LiFePO4要实现实用化生产,要解决许多问题,例如需要改善LiFePO4大电流下的充放电性能,需要提高材料的电子电导率和离子扩散速率;又如,目前的制备工艺还存在成本较高的问题,需要找到一种低成本、产业化生产的制备方法。
Barker等首次以廉价的Fe2O3为铁源,采用固相碳热还原法制备了LiFePO4,能降低成本,并且工艺简单,是一种重要的固相合成法[10-12]。为了提高磷酸铁锂材料的电化学性能和更好的实现其产业化,本研究以Fe2O3为铁源,采用不同的碳源,经过碳热还原法制备了LiFePO4/C复合材料,并深入研究了不同碳源对合成材料电化学性能的影响。
1 实验
1.1 样品制备
以分析纯试剂Fe2O3、(NH4)H2PO4、Li2CO3为原料按LiFePO4的化学计量比称量三份混合,然后按摩尔比n(Fe):n(C)=1:1各加入乙炔黑或葡萄糖或PEG6000,以无水乙醇为分散剂,置于400r/min的行星式球磨机中研磨8h。将研磨产物在60℃干燥箱中烘干后,将混合物放入瓷舟,置于高N2保护的管式炉中在350℃下保温3h预分解、造粒,然后升温到680℃煅烧8h,室温冷却研磨得LiFePO4/C复合物,分别标记为试样a、b、c。
1.2 材料表征
XRD测试所用的仪器为荷兰帕纳公司生产的X′Pert Pro仪器上进行,管压40kV,管电流300mA,扫描范围10°~75°,使用Cu靶Kα射线(λ=0.15406nm)。采用日本日立公司的扫描电子显微镜S-4700(II)观察粉末的微观形貌。
1.3 电池的组装和电化学性能测试
以制备的材料为正极活性物质,乙炔黑为导电剂,PVDF为粘结剂,按质量比75:15:10混合均匀,溶于NMP中搅成浆糊状,均匀的涂在铝片上,然后置于120℃真空干燥箱中干燥10h。以金属锂片为负极,聚丙烯为隔膜,LiPF6/EC+DMC(1:1)为电解液,在充满氩气的手套箱内组装成CR2032型电池,用LAND电池测试仪在0.1C、1C下进行恒流充放电循环测试,充放电范围为4.2~2.5V。
2 结果和讨论
2.1 XRD结果分析
图1是添加不同碳源制备而成的样品的XRD图谱。三种碳源制备的材料的峰形基本一致,说明合成得到了同样的物质。对照JCPDS数据,可知所合成样品与数据库中标号为81-1173的物质的2θ峰位及峰高序完全一致,该物质是橄榄石型磷酸铁锂(triphylite)。从图1中看出,三种样品XRD图谱的吸收峰位置相同,无杂峰存在,说明都合成得到了磷酸铁锂相。且纯度较高,峰形尖锐,背底平整,说明材料的结晶性能好。图谱中没有出现碳的衍射峰,说明碳源最后都以不定形碳的形式存在,不影响磷酸铁锂的晶体结构。

图1 样品的XRD图Fig.1 XRD patterns of the samples
2.2 SEM结果分析
图2是添加不同碳源制备而成的样品的SEM图。从图2中可以看出制备而成的样品成球形或类球形颗粒,样品a的颗粒较大,对照XRD图谱可知,样品a中乙炔黑经过高温烧结以后以不定形碳的形式残留,则球形颗粒间的不定型碳以小颗粒的形式分散在球形LiFePO4之间,表面未见包覆现象,这可能是乙炔黑在高温烧结过程中未迁移,没有均匀的包覆在LiFePO4表面;样品b以一次粒子和二次粒子的形式存在,且有明显的团聚现象,颗粒大小不均匀;样品c颗粒粒径分布比较均匀,以PEG6000为碳源制备而成的样品中,不定形碳以碳膜的形式分散在颗粒之间和表面,有包覆现象,能提高材料的电导率[13]。样品b、c的颗粒较a要小,主要是葡萄糖和PEG6000在预热阶段融化后均匀的分散在混合物中,经高温碳化后均匀的包覆在LiFePO4表面,能够阻碍晶粒的长大,起到细化晶粒的作用。由此可见不同碳源对材料的形貌和粒径有较大的影响,其中以PEG6000为碳源制备的样品的粒径均匀性和碳包覆效果较其他两组要好,且没有出现团聚现象,可以有更好的电化学性能。

图2 样品的SEM图Fig.2 SEM patterns of the samples
2.3 电化学性能
图3为添加不同碳源制备的样品在0.1C和1C下的首次充放电曲线,从图3中可以看出,添加不同的碳源对材料的电化学性能有很大的影响。以乙炔黑、葡萄糖、PEG6000为碳源制备的LiFePO4/C复合材料在0.1C下的放电比容量分别为116.7mAh/g、130.1mAh/g、144.7mAh/g,在1C下的放电比容量分别为99mAh/g、123.2mAh/g、132mAh/g。这是因为不同的碳源受热碳化后在终产物中的存在状态不同引起的。
在0.1C下不同碳源制备的材料均有较好的充放电平台,且以PEG6000为碳源制备的材料的放电平台为3.394V,接近理论值(3.4V),而在1C下以乙炔黑为碳源制备的材料出现明显的极化现象,充放电电压平台差为0.53V,相比理论值0.1V偏差较大,而以葡萄糖和PEG6000为碳源制备的材料充放电平台电压差分别为0.14V和0.18V,相对较小。这主要是因为以乙炔黑为碳源制备的材料中碳没有包覆效果,而葡萄糖和PEG6000有包覆效果,能提高材料的电导率。这说明以PEG6000为碳源制备的材料电化学性能较好。

图3 样品在0.1C下的首次充放电曲线(a)和在1C下的首次充放电曲线(b)Fig.3 First charge and discharge curves of the samples at 0.1 C(a)and(b)at 1 C
图4可见经过20次充放电循环后,a、b、c样品的放电比容量保持率分别为92.9%、97.0%、98.5%。样品a的放电比容量下降较明显,而b、c样品的放电比容量没有明显的下降趋势,说明循环性能较好。根据Anderson等人[14]提出的容量衰减的半径模型,样品在充放电过程中容量的衰减程度与样品的颗粒尺寸密切相关。根据SEM的分析结果可知,加入不同的碳源对产物的粒径和形貌有较大的影响,其中以PEG6000为碳源合成的材料颗粒较小且均匀,故循环性能较好。

图4 样品在0.1C下充放电20次的曲线Fig.4 cycling performance of the samples at 0.1 C for 20 times
图5为电池经过3次循环后的交流阻抗谱及拟合电路,由一个半圆弧和一段直线组成,经过分析可知曲线与坐标轴的交点反映的是溶液电阻,高频区的圆弧反映的是电解质电极界面的电荷转移引起的阻抗Rct,低频区的直线反应的是锂离子在电极材料中的扩散引起的Warbug阻抗。从图5可以看出三组样品的Re没有变化,但反应界面转移阻抗的Rct变化较大,以乙炔黑为碳源制备的试样的电荷转移阻抗为262Ω,较其他两组试样要大,这是因为以乙炔黑为碳源制备的材料中乙炔黑以小颗粒的形式分散在材料中,对LiFePO4的包覆效果差,而葡萄糖和PEG6000为碳源制备的材料中LiFePO4表面有包覆效果,故b、c试样的界面转移阻抗较小。界面转移阻抗小说明材料具有较好的电化学性能,有利于锂离子的嵌入和脱出。
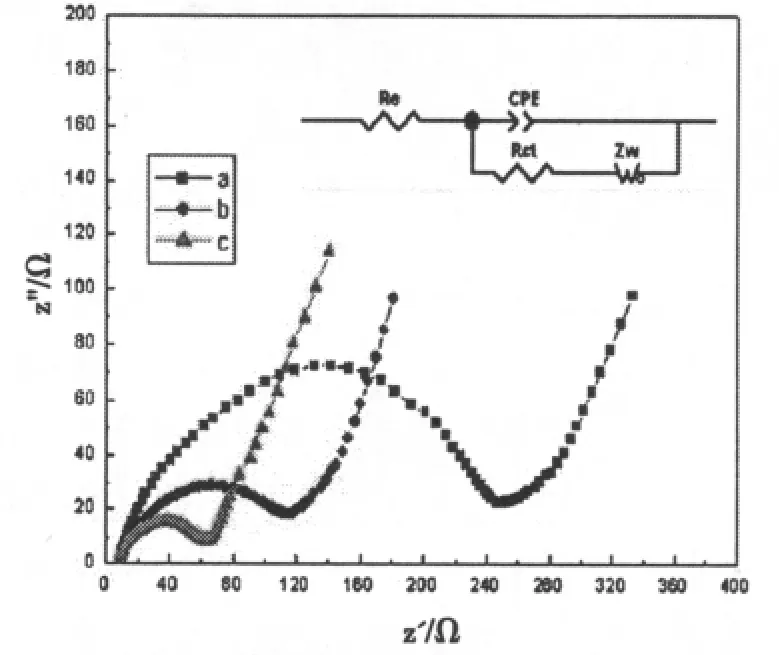
图5 样品的交流阻抗谱及拟合电路Fig.5 EIS analyses of the samples and equivalent circuit
3 结论
以廉价的Fe2O3为铁源,分别以乙炔黑、葡萄糖、PEG6000为还原剂和碳源,采用碳热还原法制备了橄榄石型的LiFePO4/C复合。结果表明不同的碳源对合成材料的电化学性能有很大的影响,这是因为加入不同的碳源对合成材料的形貌、颗粒大小有影响,且各种碳源的残留状态不同导致了对材料的包覆效果也不同。以PEG6000为碳源制备的材料颗粒均匀,没有团聚现象,且有较好的碳包覆效果,在0.1C、1C下首次放电比容量分别为144.7mAh/g、132mAh/g,0.1C下20次充放电循环后放电比容量损失仅为1.5%,表现出较优异的化学性能。
[1]Padhi A K,Nanjundaswamy K S,Goodenough J B.Phospho-olivines as positive-electrode materials for rechargeable lithium batteries[J].Journal of the Electrochemical Society,1997,144:1188-1193.
[2]Gao Fei,Tang Zhiyuan.Kinetic behavior of LiFePO4/C cathode material for lithium-ion batteries[J].Electrochimica Acta,2008,53:5071-5075.
[3]Myung S T,Komaba S,Hirosaki N H,et al.Emulsion drying synthesis ofolivine LiFePO4/C composite and its electrochemical proper ties as lithium intercalation material[J].Electrochim Acta,2004,49(24):4213-4222.
[4]赵新兵,谢健.新型锂离子电池正极材料LiFePO4的研究进展[J].机械工程学报,2007(01):69-76.
[5]Cho Y D,Feya G T K,Kao H M.The effect of carbon coating thickness on the capacity of LiFePO4/C composite cathodes[J].Journal of Power Sources,2009,189:256-262.
[6]Chung S Y,Bloking J T,Chiang Y M.Electronically conductive phospho-olivines as lithium storage electrodes[J].Nature Materials,2002,1:123-128.
[7]Andersson A S,Thomas J O.The source of first-cycle capacity loss in LiFePO4[J].Journal of Power Sources,2001,98:498-502.
[8]Yamada A,Chung S C,Hinokuma K.Optimized LiFePO4forlithium battery cathodes[J].Journalofthe Electrochemical Society,2001,148(3):A224-A229.
[9]Yang S F,Song Y N,Zavalij P Y.Performance of LiFePO4as lithium batterycathodeand comparison with manganese and vanadium oxides[J].Power Sources,2003,119:239-246.
[10]Barker J,Saidi M Y,Swoyer J L.Lithium iron(II)phosphor-olivines prepared by a novel carbothermal reduction method[J].Electrochem Solid-State Lett,2003,6(3):A53-A55.
[11]Liu Huiping,Wang Zhixing,et al.Synthesis and electrochemical properties of olivine LiFePO4prepared by a carbothermal reduction method[J].Journal of Power Sources,2008,184:469-472.
[12]Zhong M E,Zhou Z T.Preparation of high tapdensity LiFePO4/C composite cathode materials by carbothermal reduction method using two kinds of Fe3+precursors[J].Materials Chemistry and Physics,2010,119:428-431.
[13]Hee-Cheol Kang,Dae-Kyoo Jun,et al.Optimized solid-state synthesis of LiFePO4cathode materials using ballmilling.Journal of Power Sources,2008,179:340-346.
[14]Andersson A S,Beata K,Lennart H,et al.[J].Solid State Ionics,2000,130:41-52.

