CO32-和NH4+可以大量共存吗?——对2010 年江苏小高考试题第23 题的商榷
戴建良 王海富
(南京市金陵中学 江苏 南京 210005)
一、问题的提出
2010年江苏小高考试题第23题如下:
某溶液中可能含有下列6种离子中的某几种:Cl-、SO42-、CO32-、NH4+、Na+、K+。 为确认溶液组成进行如下实验:(1)200mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30g,向沉淀中加入过量的盐酸,有2.33g沉淀不溶。 (2)向(1)的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12L(已换算成标准状况,假定产生的气体全部逸出)。 由此可以得出关于原溶液组成的正确结论是
A.一定存在SO42-、CO32-、NH4+,可能存在Cl-、Na+、K+
B.一定存在SO42-、CO32-、NH4+、Cl-,一定不存在Na+、K+
C.c(CO32-)=0.01mol·L-1,c(NH4+)>c(SO42-)
D.如果上述6种离子都存在,则c(Cl-)>c(SO42-)
该题是一道关于离子检验的定量计算题,给出的答案是D。 判断过程如下:
4.30g沉淀中有2.33g是BaSO4,还有1.97g是BaCO3,所以200mL溶液中一定存在0.01mol SO42-和0.01mol CO32-。根据1.12L气体 (证明是NH3)可知溶液中一定存在0.05mol NH4+。 根据电荷守恒,0.05mol NH4+带0.05mol正电荷, 而0.01mol SO42-和0.01mol CO32-共带0.04mol负电荷,所以必定存在Cl-,且Cl-至少为0.01mol,Na+、K+可能存在,若存在,则Cl-大于0.01mol。
从考查学生的离子检验知识、电荷守恒原理、化学计算能力等方面来看,本题是一道好题。 但是命题者忽略了一个问题,那就是CO32-和NH4+能否大量共存。
二、实验及理论分析
1.实验
在试管中加入2mL 0.1mol/L NH4Cl溶液,再加入2mL 0.1mol/L Na2CO3溶液,微热,将湿润的红色石蕊试纸放在试管口,试纸变红,可见CO32-和NH4+能反应。
2.理论分析
CO32-和NH4+发生反应的离子方程式如下:
NH4++CO32-+H2O⇌NH3·H2O+HCO3-
首先根据电离常数计算此反应的平衡常数K
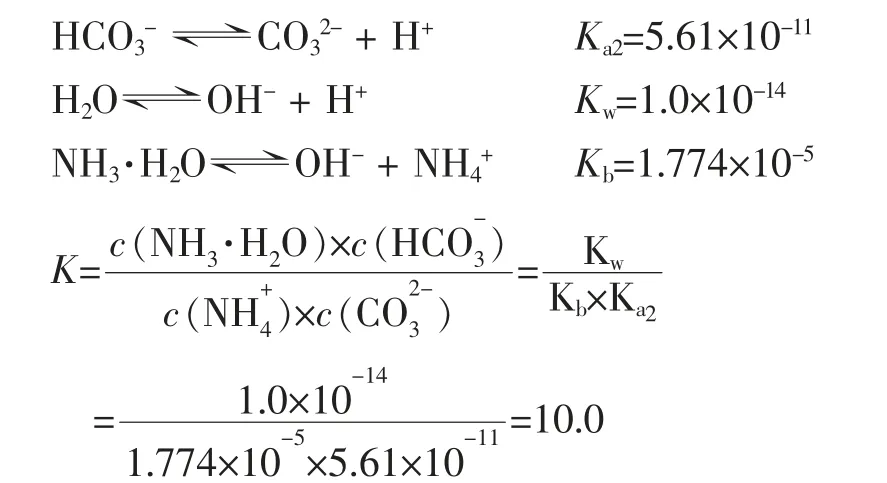
计算初始浓度为c(NH4+)=c(CO32-)=c0,平衡时反应物转化率x。

三、结论与讨论
1.结论
从上述计算结果可以看出等浓度的CO32-和NH4+会发生显著的反应,反应转化率达76%,所以CO32-和NH4+在溶液中不能大量共存, 会反应生成较多的NH3·H2O和HCO3-。
实际上CO32-和NH4+的反应在化学教材中早就出现过, 在老教材必修第一册的p21页有这样一个家庭小实验:
将30g研细的碳酸钠晶体装入小塑料袋底部, 压紧后,用细绳将塑料袋绑住,使碳酸钠晶体被封在塑料袋的下半部。 再将约20g研细的硝酸铵晶体装入塑料袋的上半部,用烧红的铁丝或锯条将塑料袋封口,即做成“冰袋”。 使用时,只要将细绳解下,用手使袋内两种粉末充分混合,便立即产生低温。在这个家庭小实验中,发生的反应即为:
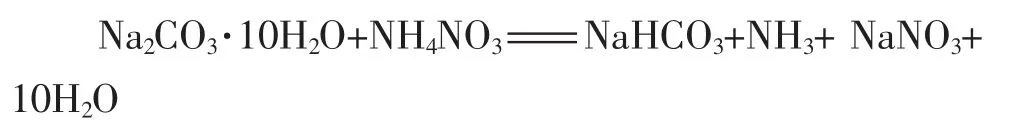
2.工业碳酸铵分析
既然CO32-和NH4+在溶液中不能大量共存,那么为什么工业上有碳酸铵产品呢? 工业碳酸铵是如何制备的?其稳定性如何? 笔者在《化工产品》和《无机化合物制备手册》中查到了碳酸铵制备和性质的相关信息。
工业碳酸铵:化学式为(NH4)2CO3·H2O,具有强烈的氨气味,一般得不到无水盐,工业品实际上是碳酸氢铵和氨基甲酸铵的复盐,在空气中不稳定,会逐渐变成碳酸氢铵(NH4HCO3)和氨基甲酸铵(H2NCOONH4)。
碳酸铵的工业制法如下:将CO2、氨及水蒸气直接合成碳酸铵,通入冷却室,用水直接冷却,再经精制即得。
碳酸铵精制法:将市售品研细放入密闭容器中,慢慢加氨水并振荡至完全溶解,在20~25℃下静置2天,再将其放在10~12℃的阴凉处,长时间静置后,即可析出结晶。迅速吸滤,干燥后移入完全密闭的容器中,往滤液中继续加入1/3的乙醇,结晶会进一步析出,这样得到的产品为一水合物。
由上可见,制备工业碳酸铵时,不是在水溶液中进行,而是用气体直接合成,目的就是为了防止在水溶液中碳酸铵发生双水解。 而在精制碳酸铵时,在氨水介质中进行的,抑制了碳酸铵的双水解。
[1] 北京师范大学无机化学教研室等编.无机化学(上册,第4版)[M].北京:高等教育出版社,2002.8:318
[2] 人民教育出版社化学室.全日制普通高级中学教科书(必修)化学1[M].2003.6:21
[3] 司徒杰生主编.化工产品手册:无机化工产品[M].北京:化学工业出版社,1999:117
[4] 朱文祥主编.无机化合物制备手册[M].北京:化学工业出版社,2006.4:479

