相转移催化合成羧甲基-羟乙基淀粉及工艺优化
张光旭 胡张雁 尤燕青 方 园
相转移催化合成羧甲基-羟乙基淀粉及工艺优化
张光旭 胡张雁 尤燕青 方 园
(武汉理工大学化学工程学院,武汉 430070)
羧甲基淀粉和羟乙基淀粉作为两种重要的变性淀粉,由于其合成条件苛刻和稳定性差等缺点限制了其应用。以甲醇为溶剂,筛选出四正丁基溴化铵(TBAB)作为相转移催化剂(PTC)对淀粉进行羟乙基化,合成了高取代度的羟乙基淀粉,并采用氯乙酸对其进行醚化,合成了羧甲基-羟乙基淀粉,既降低了传统合成方法的危险性,又克服了羧甲基淀粉的不稳定性。通过单因素分析对合成工艺进行了优化,优化条件为:淀粉25 g,催化剂 0.75 g,2- 氯乙醇 10.0 g,NaOH 8.0 g,氯乙酸 10.5 g,溶剂含水量为 9 mL,羟乙基化反应时间为6 h。试验证明,相转移催化法制得的产品取代度高,稳定性好。
羧甲基-羟乙基淀粉 羟乙基化 相转移催化 取代度
变性淀粉是由天然淀粉与许多化学试剂作用生成的具有不同性质的产品,其性能比天然淀粉更为优良,被广泛应用于食品、纺织、造纸、医药、胶黏剂、铸造、石油开采等众多工业中[1]。羟乙基淀粉的醚键稳定,不易断裂,受电解质影响较小[2],广泛应用于造纸、医药、石油等领域;羧甲基淀粉在食品工业中广泛用作增稠剂、悬浮剂、稳定剂和黏合剂等[3]。但是单一变性淀粉本身存在一些不足,羟乙基淀粉的制备方法水媒法制备时间长,反应效率和取代度较低[4],而干法合成羟乙基淀粉虽然取代度高,但环氧试剂危险性大,合成条件苛刻,很难实现工业化[4];而羧甲基淀粉虽然合成条件安全,但是它不稳定,受电解质和pH的影响较大。针对这些不足,近年来很多学者对多重复合变性淀粉进行了研究[5-8],产品在性能上普遍优于单一变性淀粉,但是在工艺条件的研究方面还有待完善。
本研究以甲醇作为溶剂,通过引入相转移催化剂和醚化剂制备羟乙基淀粉,以期缩短合成羟乙基淀粉的时间,既克服水媒法制备时间长、产品取代度低的缺点,又能避免干法合成的危险性。然后通过羧甲基化对其进行二次改性,合成羧甲基-羟乙基淀粉,以实现两种变形淀粉的优势互补,提高产品的取代度和稳定性,扩大其应用范围。通过单因素分析和正交试验优化工艺条件,填补了相转移催化合成羧甲基-羟乙基淀粉的工艺研究的空白,对实现工业化生产和提高生产效率具有重要的现实意义。
1 材料与方法
1.1 材料与仪器
1.1.1 材料
玉米淀粉:市售;2-氯乙醇:天津市光复精细化工研究所;氯乙酸:天津市光复精细化工研究所;TBAB:国药集团化学试剂有限公司。
1.1.2 试验仪器
HH-S型水浴锅:巩义市英峪予华仪器厂;JJ-1精密增力电动搅拌器:常州国华电器有限公司;DZ-1A型电热恒温干燥箱:天津市泰斯特仪器有限公司;JA1003N型电子天平:上海精密科学仪器有限公司;Nexus傅里叶红外光谱仪:美国Thermo Nicolet公司。
1.2 羟乙基制备原理与方法
1.2.1 制备原理
采用甲醇溶剂法以2-氯乙醇为醚化剂制备羟乙基淀粉。将淀粉经过碱处理后,与醚化剂进行亲核取代反应,得到羟乙基淀粉。羟乙基化反应中,醚化剂不仅能与脱水葡萄糖单位中的3个羟基反应,还能和已取代的羟乙基反应,使一个葡萄糖单元可以与至少3个分子的醚化剂反应,得到大于理论上最大取代度的表观取代度。将淀粉分散在甲醇-水溶液中,碱化处理后加入氯乙醇及催化剂,在323 K时反应至结束,即生成HES:

1.2.2 制备方法
将25 g淀粉均匀分散于甲醇-水溶液中,置于250 mL三口烧瓶,在50℃恒温水浴中机械搅拌,加入适量的NaOH碱化30 min后,加入适量的氯乙醇和催化剂,反应6~14 h至反应结束,即制得羟乙基淀粉。
1.3 羧甲基-羟乙基淀粉制备原理与方法
1.3.1 制备原理
利用淀粉葡萄糖残基上的第六、第二和第三碳原子上的羟基所具有的醚化反应能力,使羟乙基淀粉和氯乙酸在碱性环境条件下发生双分子亲核取代反应。在碱处理过程中,氢氧化钠与羟乙基淀粉中羟基形成的活性中心越多,羧甲基取代效果越好,氯乙酸利用率越高。本试验采用湿法工艺进行羧甲基化反应:羟乙基淀粉直接与氯乙酸在碱性催化下反应生成了羧甲基-羟乙基复合变性淀粉:

1.3.2 制备方法
将1.2.2节制得的羟乙基淀粉产物冷却后加入70 mL甲醇和10 mL蒸馏水,用适量的NaOH进行碱处理,然后加入氯乙酸反应4 h。产物趁热用布氏漏斗抽滤,将滤渣用80%的甲醇水溶液洗涤2次,在50℃下干燥6 h即得产品。
1.4 摩尔取代度的测定
1.4.1 羟乙基摩尔取代度(MS)的测定
采用气相色谱法[9],以己二酸作催化剂,羟乙基淀粉于高温密闭条件下被氢碘酸(HI)水解,其羟乙基转化成碘乙烷,以内标法定量分析产生的碘乙烷,折算出羟乙基的含量,即可得出其摩尔取代度,从而对试验效果进行分析。反应原理式如下:
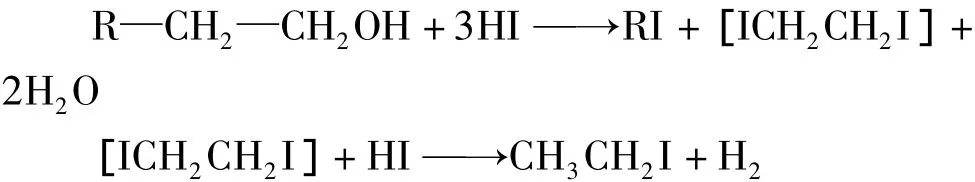
MS定义为碘乙烷克分子分数与淀粉中葡萄糖单元之比,其值由(1)与(2)式计算得出。


式中:45、156和162分别为乙氧基、碘乙烷和淀粉葡萄糖单元相对分子质量。
1.4.2 羧甲基摩尔取代度(DS)的测定
采用铜盐络合滴定法测定羧甲基取代度。基本原理是羧甲基淀粉与硫酸铜反应,生成的羧甲基淀粉铜盐沉淀易于过滤,对其滤液可用EDTA(乙二胺四乙酸二钠盐)滴定过量的铜,以PAN[1-(2-吡啶偶氮)-2-萘酚]为指示剂指示滴定终点。由EDTA对CuSO4溶液与对滤液滴定时消耗体积之差,即可求出试样消耗的铜含量,进而求出羧甲基官能团占试样质量的质量分数,其计算公式为:
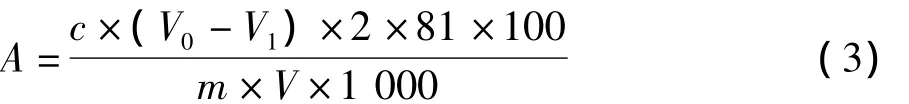
式中:A为羧甲基钠官能团占试样质量的质量分数/%;V1为滴定滤液所消耗EDTA溶液的体积/mL;V0为滴定硫酸铜溶液所消耗EDTA溶液的体积/mL;c为EDTA标准溶液的浓度/mol/L;m为称量固体样品的质量/g;V为吸取滤液体积与容量瓶容量之比值,常用50/250。
根据羧甲基钠官能团占试样质量的比例,可按下式计算羧甲基淀粉的取代度:
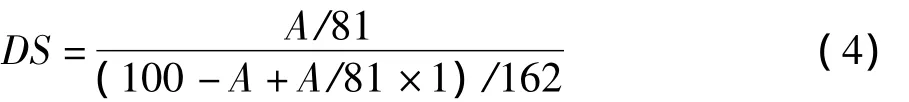
式中:162和81分别为淀粉葡萄糖单元和羧甲基钠官能团相对分子质量。
1.5 相转移催化剂的筛选
以4种典型的季铵盐和不同相对分子质量的聚乙二醇(PEG)分别作为催化剂进行羟乙基化反应,合成羟乙基淀粉,采用1.4.1节介绍的方法测定羟乙基淀粉的MS,比较这几种季铵盐和PEG的催化活性大小,筛选出最佳相转移催化剂。
1.6 羧甲基-羟乙基淀粉红外测定
采用傅立叶红外光谱仪进行结构表征,取适量充分干燥的样品,KBr压片法,扫描范围800~4 000 cm-1。
2 结果与讨论
2.1 相转移催化剂的选择
以4种典型的季铵盐:四正丁基溴化铵(TBAB)、四乙基溴化铵(TEAB)、四丁基氯化铵(TBAC)及十六烷基三甲基溴化铵(CTAB)和相对分子质量分别为200、400、600、800和1 000的 PEG 分别作为催化剂合成羟乙基淀粉,以MS为指标,比较这几种季铵盐和PEG的催化活性大小。其产物MS分别如表1。

表1 季铵盐和聚乙二醇催化产物的MS
由表1看出,4种季铵盐催化剂的催化效果都比较理想。其中TBAB的催化活性最大,而TEAB和TBAC作催化剂合成的羟乙基淀粉MS也比较高,这是由于它们的阳离子有对称结构,正电荷被屏蔽得更严密,形成的离子对Q+Y-在有机相中的分配系数更大,催化效果比CTAB这种结构不对称的催化剂好得多;TBAB的催化活性比TBAC好一些,这是由于含负离子Br-的催化剂比含负离子Cl-的催化剂更易于与亲和试剂结合[10]。对于PEG催化剂,当相对分子质量为400时,催化剂活性达到最大,由400到800时催化剂活性降低,在相对分子质量为1 000时催化活性再次升高。其中PEG400催化活性最高,这可能是由于PEG400形成更合适孔径的假环状结构与反应物阳离子结合,使亲核阴离子更“裸露”些,从而具有更高的反应活性[11]。而当聚乙二醇相对分子质量达到1 000时,可能是由于分子链更柔软,可以形成各种不同孔径的假环状结构,从而使催化活性变高。
综合上述活性分析,季铵盐类催化剂普遍比聚乙二醇类催化剂的催化活性高,季铵盐类又以TBAB的催化活性最高,因此选取TBAB作为PTC。
2.2 羧甲基-羟乙基淀粉制备单因素试验
2.2.1 甲醇溶剂含水量对MS的影响
淀粉25 g,催化剂 0.75 g,2- 氯乙醇 10.0 g,羟乙基化反应时间为6 h,不同溶剂含水量对MS的影响见图1。由图1可见,当溶剂含水量由6 mL增加到8 mL时,MS下降,当含水量为8 mL时MS最低,这是随着水量的增加,亲核体氯乙醇的水合程度加大,反应活性下降。当随后当水量从8 mL增加到9 mL时MS达到最大,此后开始下降。这是可能是因为水量较少时淀粉易糊化,增加水量使反应处于更稳定体系,故MS增大;水量超过9 mL时,催化剂在水相中的分布增大,催化效果下降。

图1 溶剂含水量对产品羟乙基摩尔取代度的影响
2.3.2 催化剂用量对MS的影响
淀粉25 g,2- 氯乙醇 10.0 g,溶剂含水量为9 mL,羟乙基化反应时间为6 h,不同催化剂用量对MS的影响见图2。由图2可见,起初MS随着催化剂用量的增加而升高,当TBAB用量为0.75 g时达到最大,但随着TBAB继续增加,MS开始下降,可能是降解反应或其他副反应速率显著上升。当TBAB用量大于10.0 g时,MS小幅上升,可能此时副反应速率略有降低。
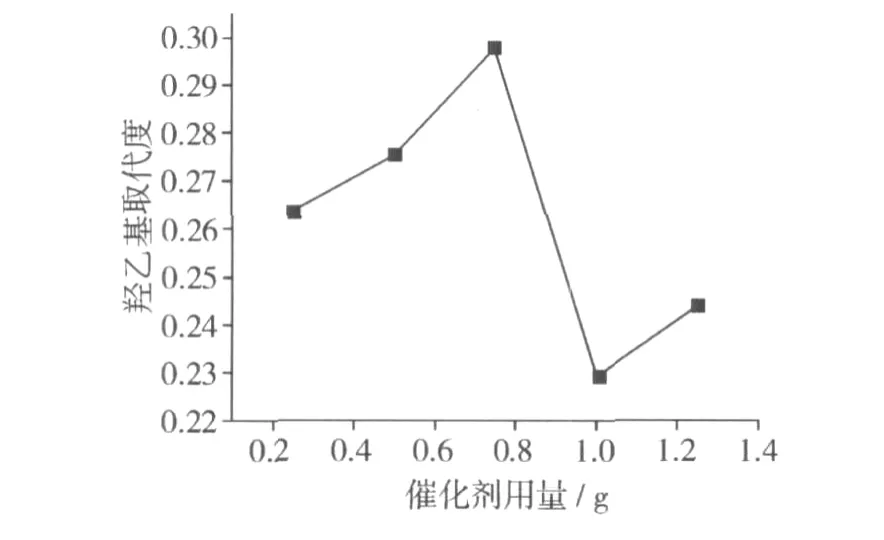
图2 催化剂用量对产品羟乙基摩尔取代度的影响
2.3.3 反应时间对MS的影响

图3 反应时间对产品羟乙基摩尔取代度的影响
淀粉25 g,催化剂0.75 g,2- 氯乙醇10.0 g,溶剂含水量为9 mL,不同反应时间对MS的影响见图3。由图3可见,随着反应时间的延长,MS没有明显变化。当反应时间为10h时,MS略有下降,可能是因为开始反应时,季铵盐的热稳定性不好,TBAB催化活性降低,取代度大小变化不明显,但是当反应时间达到10 h之后,季铵盐的热稳定状态变得稳定,延长时间,MS略微上升。因为反应时间对取代度影响不大,考虑生产效率,反应时间确定为6 h较为合适。
2.3.4 2-氯乙醇用量对MS的影响
淀粉25 g,催化剂0.75 g,溶剂含水量为9 mL,羟乙基化反应时间为6 h,不同2-氯乙醇用量对MS的影响见图4。由图4可见,随着2-氯乙醇用量的增加,MS不断增大,再增加2-氯乙醇用量,取代度几乎不变。因为反应试剂向淀粉内部的扩散速度随2-氯乙醇用量增大而增加,但扩散速度达到最大之后,继续增加2-氯乙醇用量,对反应效果基本没有影响。
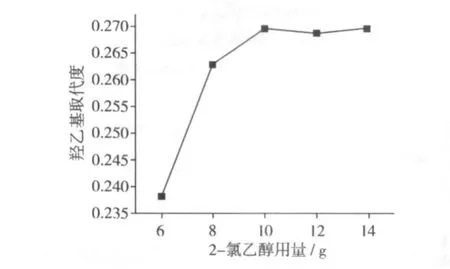
图4 2-氯乙醇用量对产品羟乙基取代度的影响
2.3.5 NaOH 用量对 DS 的影响
淀粉25 g,催化剂 0.75 g,2- 氯乙醇 10.0 g,溶剂含水量为9 mL,羟乙基化反应时间为6 h,氯乙酸10.5 g,不同NaOH用量对DS的影响见图5。图5可见,随着羧甲基化反应前预处理NaOH使用量的增加,碱处理淀粉生成的活性中心不断增加,DS不断上升,在用量为8.0~10.0 g时基本不变,但当 NaOH用量继续增加时,DS迅速下降,可能是因为pH过大导致淀粉糊化使反应无法正常进行。

图5 NaOH用量对产品羧甲基取代度的影响
2.3.6 氯乙酸用量对DS的影响
淀粉25 g,催化剂 0.75 g,2- 氯乙醇 10.0 g,溶剂含水量为9 mL,羟乙基化反应时间为6 h,NaOH 8.0 g,不同氯乙酸用量对DS的影响见图6。由图6可见,随着氯乙酸用量的增加,DS先上升后下降,当用量为10.5 g时达到最大。这说明在在一定范围内,氯乙酸用量的增加会使DS升高,产品溶胀速度加快,但用量继续增加酸度增加,不利于醚化反应的进行,反而使DS降低。

图6 氯乙酸用量对产品羧甲基取代度的影响
综合上述单因素试验可知:当溶剂含水量为9.0 mL,催化剂 TBAB 用量为 0.75 g,反应时间为6 h,2-氯乙醇用量为10.0 g时得到的羟乙基淀粉MS较高;当预处理羟乙基淀粉所用NaOH为8.0 g,氯乙酸为10.5 g时得到的羧甲基-羟乙基淀粉DS较高。
2.3 羧甲基-羟乙基淀粉红外分析
用傅里叶红外光谱仪对产品进行的红外表征见图7。在3 410 cm-1处为—OH的伸缩振动吸收峰,在866,758,717 cm-1处有—CH2—摇摆振动吸收峰,说明发生了羟乙基化反应;在1 650 cm-1处有C﹦O的伸缩振动吸收峰和2 930 cm-1处有—CH2—的伸缩振动吸收峰,1 080 cm-1处有—C—O—C—伸缩振动吸收峰,说明发生了羧甲基化反应[12]。

图7 羧甲基-羟乙基淀粉红外谱图
3 结论
本试验筛选出最佳相转移催化剂TBAB,缩短了羟乙基化的反应时间,避免了传统方法制备羟乙基淀粉的危险性。然后对其进行了二次改性,通过取代度测定与红外表征证明,合成出了取代度较高的羧甲基-羟乙基淀粉,实现了两种变性淀粉的优势互补;通过单因素试验对工艺进行优化,按质量比计算,得出了最佳优化条件为:淀粉25 g,溶剂含水量为9 mL,催化剂 0.75 g,2- 氯乙醇 10.0 g,NaOH 8.0 g,氯乙酸 10.5 g,羟乙基化反应时间为 6 h。试验表明:该工艺制得的羧甲基-羟乙基淀粉取代度高,配制水溶液稳定性好,不易分层。
[1]佘艳,张光旭,鄢烈祥,等.交联-甲基淀粉合成工艺可视化优化的研究[J].中国粮油学报,2009,4(24):62
[2]刘叶民,徐桂云,何蕾,等.羟乙基淀粉的羟乙基取代位置的研究[J].分析化学研究报告,2003,3:271-276
[3]林志荣,高玉群,陈莲英,等.羧甲基淀粉的制备和应用[J].现代食品科技,2004,12:181
[4]徐立宏,张本山,高大维,等.羟乙基淀粉的制备与应用[J].粮食与饲料工业,2001,11:41-43
[5]张力田.发展变性淀粉的生产和应用[J].淀粉和淀粉糖,1995(2):1-5
[6]武宗文,崔国士.高取代度羧甲基淀粉性能及应用研究[J].郑州粮食学院学报,1997,18(3):81-85
[7]张燕萍,周世英.羧丙基二淀粉磷酸酯的制备及应用[J].粮食与饲料工业,1998(12):40-42
[8]卢艳芬.几种变性淀粉基团的分析测定[J].湖南化工,1999(4):40-42
[9]Mourits,JMerkus,H de Galan L.Gas chromatographic determination of hydroxyethyl deriv-atives of glucose[J].Analytical Chemistry,1976,48(11):1557-1562
[10]Herriott A W,Picker D.Phase transfer catalysis.An evaluation of catalysis[J].Journal of the American chemical Society,1975,97(9):2345- 2349
[11]Saber Chatti,Michel Bortolussi,Andre Loupy.Cation and leaving group effect in isosorbide alkylation under microwave in phase transfer catalysis[J].Tetrahedron,2001,57(6):4365-4370
[12]赵文宽.仪器分析[M].北京:高等教育出版社,2001:158-160.
Synthetization of Carboxymethyl-hydroxyethyl Starch by Phase Transfer Catalysis and its Technical Optimization
Zhang Guangxu Hu Zhangyan You Yanqing Fang Yuan
(College of Chemical Engineering,Wuhan University of Tech-nology,Wuhan 430070)
As two important kinds of modified starch,carboxymethyl starch and hydroxyethyl starch are limited in their application because of their rigorous preparation process and unstability.In this paper,the hydroxyethyl starch was produced by a methanol solvent method.We selected tetrabutyl ammonium bromide(TBAB)as the phase transfer catalyzer(PTC)to synthesize hydroxyethyl starch with higher degree of substitution.Then,with chloroacetic acid as etherifying agent,we synthesized carboxymethyl- hydroxyethyl starch with good stability in a safe method.The single factor analysis was established to conduct process optimization.The optimization was as follow:starch:25 g,catalyst:0.75 g,2- chlorine ethanol:10.0 g,NaOH:8.0 g,chloroacetic acid:10.5 g,water content of solvent:9 mL,and hydroxyethylation reaction time:6 h.It was proved that the product prepared by this method had high degree of substitution and good stability.
carboxymethyl hydroxyethyl starch,hydroxyethylation,phase transfer catalyze,degree of substitution
TS231
A
1003-0174(2011)12-0034-05
2011-03-09
张光旭,男,1964年出生,教授,硕士生导师,催化剂与催化反应工程
胡张雁,男,1982年出生,硕士,催化剂与催化反应工程

