极性溶剂中微量环戊二烯的二聚反应
张荣娟,包宗宏,张展鹏
(南京工业大学 化学化工学院,江苏 南京 210009)
极性溶剂中微量环戊二烯的二聚反应
张荣娟,包宗宏,张展鹏
(南京工业大学 化学化工学院,江苏 南京 210009)
对微量环戊二烯(CPD)在极性溶剂二甲基甲酰胺(DMF)、甲基吡咯烷酮(NMP)和乙腈(ACN)中的二聚反应进行了研究,考察了反应温度、反应时间、溶剂中CPD初始含量对极性溶剂中微量CPD二聚反应的影响,讨论了极性溶剂的溶剂效应,并与非极性C5溶剂中常量CPD二聚反应过程进行了比较。实验结果表明,极性溶剂可以促进微量CPD二聚反应的进行,极性中等且结构简单的DMF对CPD二聚反应的促进作用最大,极性最强的NMP次之,极性最弱的ACN的促进作用最弱。在3种极性溶剂中,反应初始阶段CPD转化率和DCPD收率都随反应时间的延长、反应温度的升高和CPD初始含量的增加而增大;在105~125℃内,反应4 h后CPD的二聚反应趋于平衡。
环戊二烯;二聚反应;双环戊二烯;溶剂效应;碳五馏分;极性溶剂
溶剂性质对Diels-Alder反应有重要影响,溶剂分子和反应物分子相互作用会形成溶剂膜,改变反应物分子的自由能和电子结构,从而影响反应速率。选择合适的溶剂不仅可以加快反应速率,而且可以提高产物收率。因此,反应的溶剂效应备受关注[1-4]。
环戊二烯(CPD)是一种含有共轭双键的五元环,性质非常活泼,在室温下即可发生二聚反应生成双环戊二烯(DCPD)[5]。目前工业上在用C5原料生产聚合级异戊二烯(IP)的过程中,首先通过热二聚反应将C5原料中的CPD转化成沸点相对较高的DCPD,从而除去大部分CPD,然后再经萃取精馏、汽提和普通精馏等步骤制取 CPD含量小于lmg/kg的聚合级 IP[6-7]。进入萃取精馏塔的脱CPD后的 C5烃中约含有质量分数为 3%的CPD[8-9],因萃取精馏塔温度相对稍低,尽管用溶剂将CPD稀释到质量分数1%以下,但仍存在CPD的二聚反应,生成的DCPD在汽提塔底部高温下分解为CPD,其中部分CPD随再生的溶剂循环到萃取精馏塔顶部[10]。由于缺乏微量CPD在极性溶剂中二聚反应过程的动力学数据,在进行萃取精馏系统的工艺设计时,往往把它看成是一个简单的萃取精馏过程与溶剂再生过程,不考虑微量CPD在萃取精馏塔中的二聚与在汽提塔中的解聚现象,忽略微量CPD在两塔之间循环对萃取精馏过程的影响。研究微量CPD在萃取溶剂中的二聚反应,可更准确地调整工业萃取精馏塔的操作条件,以有效去除高纯度IP中存在的微量CPD,减少CPD的损耗。
本工作对微量CPD在极性溶剂二甲基甲酰胺(DMF)、乙腈(ACN)、N-甲基吡咯烷酮(NMP)中的二聚反应过程进行了研究,考察了反应温度、反应时间、溶剂中CPD的初始含量对二聚反应过程的影响,以便为工业上混合C5烃萃取精馏装置的工艺设计提供依据。
1 实验部分
1.1 试剂与仪器
CPD:由DCPD裂解分离得到,纯度大于等于99%;DMF:分析纯,上海久臆化学试剂有限公司; ACN(分析纯)、NMP(化学纯):上海凌峰化学试剂有限公司;正己烷:分析纯,上海试四赫维化工有限公司;邻二甲苯:化学纯,上海豪程化工股份有限公司。
实验用反应器为自制的直径 32 mm、体积250 m L的不锈钢反应釜,在顶端设有取样口和热电偶测量孔。
1.2 实验方法
[11]的方法将DCPD裂解为CPD;称取一定量的极性溶剂、CPD和内标物加入到反应釜内,通入氮气排除空气后密封,将反应釜置于恒温油浴中进行二聚反应;每隔一段时间,从反应釜内取0.4μL的试样,分析CPD和DCPD的含量。
1.3 分析方法
采用山东鲁南分析仪器厂SP-6890型气相色谱分析仪分析CPD和DCPD的含量;DMF和ACN中CPD和DCPD含量的色谱分析条件为:SE-30毛细管色谱柱,50 m×0.25 mm×0.5μm;汽化温度170℃,检测温度220℃,柱温采用二阶程序升温(40℃保持8 min,以20℃/m in的速率升至120℃保持10 min,再以20℃/min的速率升至180℃保持10 m in)。NMP中CPD和DCPD含量的色谱分析条件为:OV-1701毛细管色谱柱,30 m × 0.32 mm×0.33μm;汽化温度220℃,检测温度220℃,柱温采用一阶程序升温(40℃保持3 min,以20℃/m in的速率升至110℃保持10 m in)。
分别测定CPD和DCPD在不同溶剂中的校正因子,采用内标法定量。在DMF和ACN中,内标物为正己烷;在NMP中,内标物为邻二甲苯。
2 结果与讨论
2.1 反应温度的影响
分别考察了反应温度对不同极性溶剂中CPD二聚反应的影响,实验结果见图1和图2。
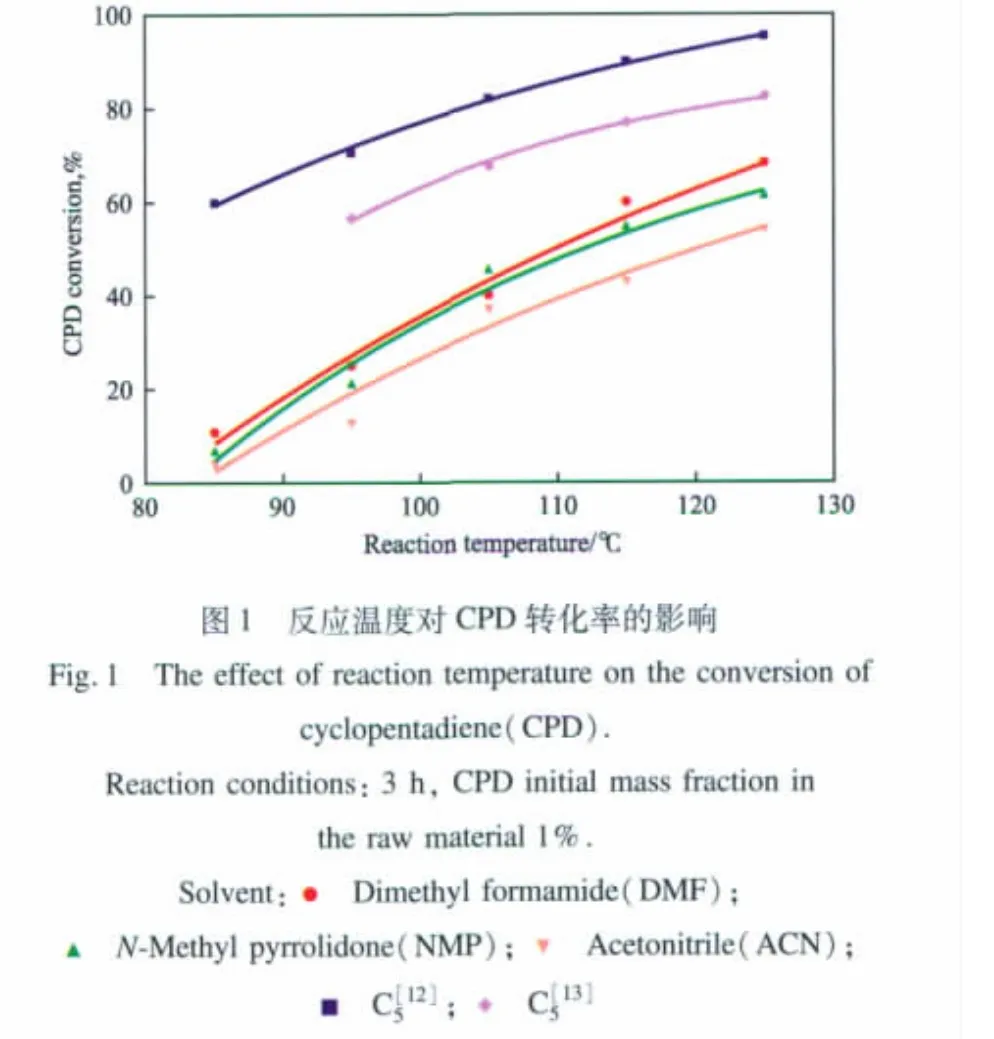

作为对照,图1和图2中给出了两组常量CPD在C5溶剂中二聚反应的文献数据[12-13]。其中,文献[12]的C5原料中CPD和DCPD的总质量分数约为16%,文献[13]的C5原料中CPD和DCPD的总质量分数约为10%。
由图1可见,反应温度一定时,在 C5溶剂中CPD的转化率均高于极性溶剂中CPD的转化率,且文献[12]中的CPD转化率高于文献[13],表明原料中CPD含量高是CPD转化率高的主要因素。在实验范围内,随反应温度的升高,4种溶剂中CPD转化率均增大;当反应温度超过115℃后,CPD转化率的增幅均减小。CPD的二聚反应是吸热反应[13],低温有利于平衡向正反应方向进行。因此,反应温度低于115℃时,CPD转化率增长较快;当反应温度超过115℃时,DCPD裂解反应加快,CPD转化率增幅减小。
由图1还可见,随反应温度的升高,极性溶剂中CPD转化率的增幅稍大于C5溶剂中的增幅。这是因为随反应温度的升高,C5溶剂中其他烯烃分子的运动加剧,这些分子的存在阻碍了CPD分子的相互碰撞,使CPD二聚反应受到阻碍,导致CPD转化率的增幅减缓。在3种极性溶剂中,除CPD和DCPD两种烯烃分子外,不存在其他烯烃分子,阻碍CPD二聚反应的因素少,因此,极性溶剂中CPD转化率的增幅比C5溶剂中的大。
一般情况下,对于结构类似的溶剂,极性强的溶剂有利于提高极性产物的收率[3]。在实验所用的3种溶剂中,NMP与DMF的极性高于ACN,因此NMP和DMF中的CPD转化率高于ACN中的CPD转化率,与图1中的实验结果一致。另一方面,NMP与DMF的偶极矩分别是13.64和12.88[14-15],NMP的极性高于DMF,但NMP中CPD的转化率却略低于DMF中CPD的转化率,这可能是因为NMP也是五元环分子,结构与CPD相似,CPD在NMP中反应时,溶剂分子对反应物分子的空间位阻较大,不利于CPD分子相互碰撞发生二聚反应。
由图2可见,C5溶剂中 DCPD收率在 115,120℃左右达到最大值,然后逐渐减小,这是由于C5溶剂中多种二烯烃与DCPD共聚反应加剧所致。在实验范围内,随反应温度的升高,3种极性溶剂中的DCPD收率均增大。其中,DMF中DCPD收率与反应温度近似呈线性关系,反应温度超过115℃后,NMP和ACN中DCPD收率的增幅趋缓。
在3种极性溶剂中,同一反应温度下,DCPD收率在DMF中最大,NMP中次之,ACN中最小。由图1可知,在DMF中更有利于CPD的二聚反应,因此DCPD收率最大;在NMP中DCPD的收率比在ACN中的大,这是由于NMP的极性比ACN的极性强所致。在ACN中,CPD转化率最小,因此DCPD收率的增幅也缓慢。
2.2 反应时间的影响
反应温度对不同极性溶剂中CPD二聚反应的影响见表1。为了对照,表1中给出了一组常量CPD在C5溶剂中二聚反应的文献数据[12]。

表1 反应时间对CPD转化率和DCPD收率的影响Table 1 The effects of reaction time on the CPD conversion and the DCPD yield
由表1可见,随反应时间的延长,3种极性溶剂中的CPD转化率和DCPD收率总体上逐渐增大。当反应温度和反应时间一定时,C5溶剂中的CPD转化率远高于极性溶剂中的CPD转化率,C5溶剂中多种二烯烃的存在导致CPD的消耗增大是C5溶剂中CPD转化率较高的主要因素。在不同反应温度下,反应2 h以后,C5溶剂中CPD转化率的增幅较小;但在极性溶剂中反应4 h以后,CPD转化率的增幅才稍有减缓。这是因为在极性溶剂中,反应4 h以后,二聚反应趋于平衡,但在C5溶剂中由于有多种二烯烃可与CPD进行反应,导致逆反应速率加快,反应平衡时间缩短。另外,在不同反应温度下,CPD转化率在NMP中随反应时间的延长而增大的幅度最大,ACN中的最小,这是由溶剂性质差异所致。
由表1还可见,在一定的反应温度和反应时间下,与极性溶剂相比,C5溶剂中的DCPD收率较高。随反应时间的延长,4种溶剂中DCPD收率都逐渐增大,但在极性溶剂中的增幅较大。这是因为在极性溶剂中,除DCPD分解外,不存在其他的DCPD消耗;而在C5溶剂中还含有许多其他烯烃,反应时间越长,副反应越多,DCPD消耗的就越多;且在极性溶剂中CPD转化率增幅较大,所以DCPD收率增幅较大。DCPD收率在ACN中基本呈线性关系,这与ACN的弱极性有关。
2.3 CPD初始含量的影响
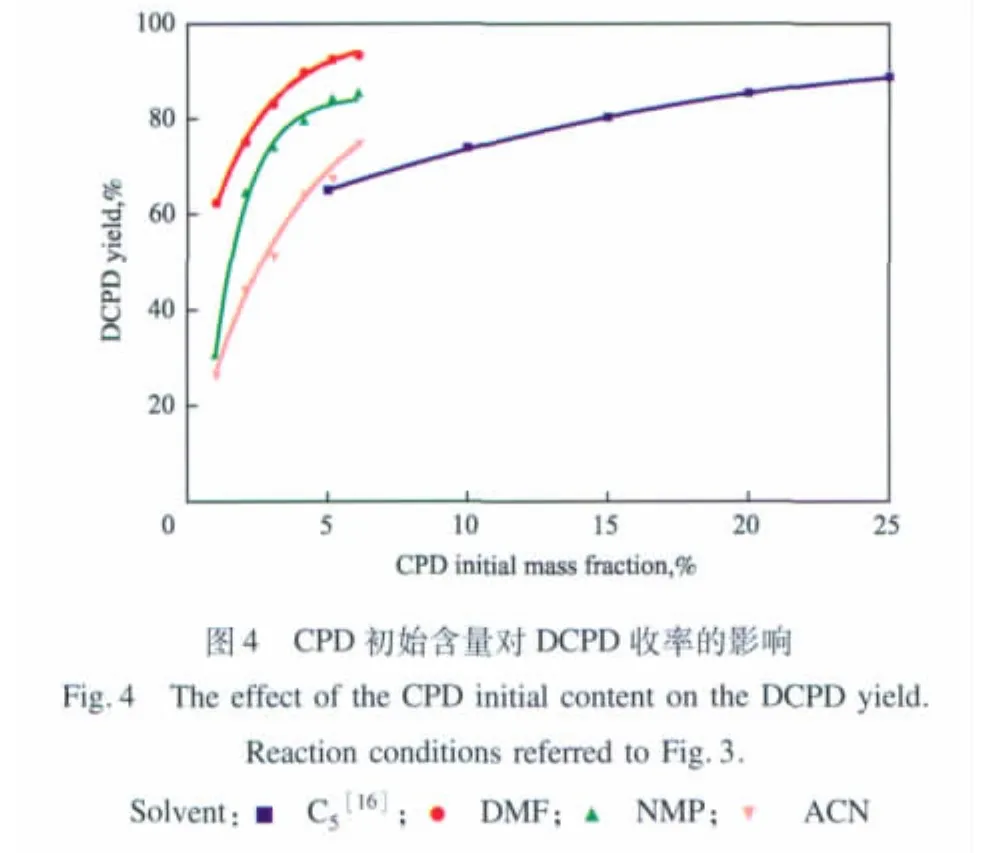
考察了极性溶剂中CPD初始含量对CPD转化率和DCPD收率的影响,实验结果见图3和图4。作为对照,图3和图4中给出了一组CPD在C5溶剂中二聚反应的文献数据[16]。
由图3可见,CPD初始含量一定时,与极性溶剂相比,C5溶剂中CPD的转化率较高。3种极性溶剂中,DMF中的CPD转化率最大,NMP中次之,ACN中最小,与图1中的变化趋势相同。随CPD初始含量的增加,4种溶剂中CPD的转化率均增大。这是因为CPD初始含量越大,反应过程中CPD分子相互碰撞的几率越大,反应速率就越快。但随CPD初始含量的增大,CPD转化率在极性溶剂中的增幅明显高于C5溶剂中的增幅。
由图4可见,当CPD初始含量相同时,极性溶剂中DCPD的收率高于C5溶剂中DCPD的收率。这是因为C5溶剂中除CPD的二聚反应外,还存在CPD,DCPD与其他烯烃的共聚反应,副反应的存在,使得DCPD收率相对降低;在极性溶剂中,因不存在其他烯烃与DCPD的副反应,因此DCPD收率较高。由图4还可见,随CPD初始含量的增加,4种溶剂中的DCPD收率都增大,但其增幅均逐渐减小。这是因为CPD二聚反应是可逆反应,反应达到平衡后,DCPD收率则不再随CPD含量的增大而增大。

3 结论
(1)通过研究微量 CPD在极性溶剂 DMF,NMP,ACN中的二聚反应发现,极性中等且结构简单的DMF对CPD二聚反应的促进作用最大,极性最强的NMP对二聚反应的促进作用次之,极性最弱的ACN对二聚反应的促进作用最弱。
(2)CPD二聚反应是一个可逆反应,在3种极性溶剂中,反应初始阶段CPD转化率和DCPD收率都随反应时间的延长、反应温度的升高和CPD初始含量的增加而增大;在105~125℃内,反应4 h后CPD二聚反应趋于平衡。
参考文献
[1] 黄蕾.溶剂效应对有机反应影响的分析[J].科技信息,2010,(13):158-159.
[2] Cativiela C,Dillet V,Garcia J,et al.Solvent Effects on Diels-Alder Reactions.A Semi-Empirical Study[J].J Mol Struct,1995,331(1-2):37-50.
[3] 熊中强,李宁涛,于艳军,等.Diels-Alder反应制备三环戊二烯的溶剂效应[J].化工生产与技术,2009,16(4):25-27.
[4] Karpyak N M,Makitra R G,Marshalok G A,et al.Solvent Effect on the Rate of Dimerization of Cyclopentadiene[J].JGen Chem,2005,75(11):1712-1716.
[5] 王秀敏,包宗宏.裂解C5馏分中二烯烃热二聚过程的研究[J].南京工业大学学报,2005,27(4):53-58.
[6] 张旭之,马润宇,王松汉,等.碳四碳五烯烃工艺学[M].北京:化学工业出版社,1998:609-630.
[7] 李东风,张祝蒙,杨元一.碳五与N-甲基吡咯烷酮常压汽液平衡数据的测定及关联[J].石油化工,2009,38(7):750-753.
[8] Susumu Takao,Kanagawa Ken,Takeo Koide,et al.Isoprene Purification Process:US,3510405[P].1970-05-05.
[9] 廖丽华,张祝蒙,程建民,等.加盐NMP法萃取精馏分离裂解碳五馏分[J].石油化工,2010,39(2):167-172.
[10] Arthur B H,Westfield N J,David C P,et al.Isoprene Purification Process:US,3231257[P].1966-01-18.
[11] 林璐璐,云志.裂解碳五常微量分析及双烯/顺酐反应动力学[D].南京:南京工业大学,2005.
[12] 赵春迎.裂解C5馏分综合利用及分离研究[D].兰州:兰州大学,2007.
[13] 李兴存,董燕敏,陈进富,等.热二聚法分离C5混合物中的环戊二烯[J].化学反应工程与工艺,2002,18(2):185-187.
[14] 李化昌,符斌.简明溶剂手册[M].北京:化学工业出版社,2009:308-309.
[15] 解一军,杨宇婴.溶剂应用手册[M].北京:化学工业出版社,2009:372-390.
[16] 刘家棋,王秀珍,张志鸿,等.裂解C5馏份热二聚制双环戊二烯[J].石油化工,1996,25(4):248-252.
Dimerization of Cyclopentadiene with Low Concentration in Polar-Solvents
Zhang Rongjuan,Bao Zonghong,Zhang Zhanpeng
(College of Chemistry and Chemical Engineering,Nanjing University of Technology,Nanjing Jiangsu 210009,China)
Dimerization of low concentration cyclopentadiene(CPD)in polar solvents of N-dimethylformamide(DMF),N-methyl-pyrrolidone(NMP)or acetonitrile(ACN)was studied.The effects of reaction temperature,reaction time and CPD initial concentration in the solution on the dimerization in the polar solvents were investigated.The experimental results were compared with the reference data aboutnormal concentration CPD dimerization in nonpolar C5solvent.The results showed that the polar solvents was in favor of the dimeriation of CPD.DMF with moderate polarity and simple structure could significantly promote the dimerization,on the contrary,the effect of ACN with the smallest polarity is the weakest.In the initial reaction stage,both the CPD conversion and the dicyclopentadiene yield in the three polar solvents separately increased with the prolongation of reaction time,the rise of reaction temperature and the increase of CPD initial concentration.Between 105℃and 125℃,the dimerization of CPD w ith low concentration was in equilibrium in the reaction 4 hours.
cyclopentadiene;dimerization reaction;dicyclopentadiene;solvent effect;C5fraction; polar solvent
1000-8144(2011)05-0511-05
TQ 203.3
A
2010-12-07;[修改稿日期]2011-01-11。
张荣娟(1984—),女,河南省南阳市人,硕士生,电话15996241465,电邮hnssq6@163.com。联系人:包宗宏,电话025-83587190,电邮zhbao@njut.edu.cn。
(编辑 李明辉)

