L-谷氨酸-5-甲酯金属化合物的合成、表征和生物活性
金龙飞,沈月松,吴勇飞,吴腊梅
(中南民族大学化学与材料科学学院,武汉430074)
L-谷氨酸-5-甲酯金属化合物的合成、表征和生物活性
金龙飞,沈月松,吴勇飞,吴腊梅
(中南民族大学化学与材料科学学院,武汉430074)
在仿自然的条件下,合成了L-谷氨酸-5-甲酯.对L-谷氨酸-5-甲酯晶体进行了X-射线单晶衍射测定.测量表明,L-谷氨酸-5-甲酯属单斜晶系,C2空间群,其中a=10.286(3)Å,b=4.6163(11)Å,c=17.111(4)Å;β=104.995(4)°.通过L-谷氨酸-5-甲酯与M gCl2·6H2O 和Ca(OH)2反应,分别合成得到了相应的金属化合物.用比色法测试了L-谷氨酸-5-甲酯对三磷酸腺苷二钠分解的催化活性,结果表明:L-谷氨酸-5-甲酯合镁和L-谷氨酸-5-甲酯合钙对三磷酸腺苷二钠的分解具有较好的活性.
L-谷氨酸衍生物;生物活性;三磷酸腺苷二钠
三磷酸腺苷既是一种重要的辅酶,又是体内能量的主要来源.由于谷氨酸残基是三磷酸腺苷分解酶和辅酶的结构特征之一,因此对谷氨酸的修饰以及配合物的研究,将有可能寻找到影响三磷酸腺苷活性的化合物或配合物.近20多年,氨基酸类产品应用大为广泛[1],其中对L-谷氨酸及其衍生物的研究则是热点方向之一[2,3],目前国内外相关研究报道层出不穷[4].通过扩展谷氨酸衍生物的修饰及其配合物的合成以研究对三磷酸腺苷分解的催化活性的研究,发现功能与结构的关系,为合成具有三磷酸腺苷分解酶和辅酶活性的模拟化合物提供指导作用,并有望合成活性更高的三磷酸腺苷分解酶和辅酶的模型化合物.由于三磷酸腺苷分解酶的结构及其催化机理极其复杂,所以设计高效专一的三磷酸腺苷分解酶模型化合物,具有重大的理论及实际意义.本论文基于自然温和条件,选择L-谷氨酸为原料合成L-谷氨酸-5-甲酯及其金属化合物,并拟测试其对三磷酸腺苷分解的生物活性,为进一步研究具有三磷酸腺苷分解酶和辅酶活性的模拟化合物打下较好基础.
1 实验部分
1.1 仪器和试剂
Perkin Elmer 2400 CHN型元素分析仪;FT-IR N EXU S智能型高分辨傅立叶红外光谱仪(KBr压片);UV-265可见紫外分光光度计(25℃,190~700 nm);X-4数字熔点仪.
L-谷氨酸、三羟基氨基甲烷、三磷酸腺苷二钠为生物试剂;其它试剂均为分析纯,未进一步提纯.
1.2 实验方法
1.2.1L-谷氨酸-5-甲酯的合成
L-谷氨酸-5-甲酯参照文献[5]法合成.取L-谷氨酸7.50 g(0.05 mol)置于烧瓶中,加入无水甲醇120 mL,边搅拌边加入3.70 mL 98% 浓H2SO4于25℃反应4~5 h.用三乙胺的甲醇溶液(V醇∶V胺=2∶1)调节至pH=8.0,置于冰箱中过夜.次日抽滤出固体,用95%甲醇进行重结晶,用无水甲醇洗涤.常温下真空干燥至恒重,纯品为白色晶状固体.产率93.8%.mp:169~ 170℃.A nal.,Found:C,45.02;H,6.89;N,8.71%.Calc:(C6H11NO4):C,44.72;H,6.88;N,8.69%.FT-IR(KBr pellet,ν/cm-1):3130~2598 m,1730 s,1611 s,1583 s,1355 m,2752~2 250 w,1080 m.将合成的L-谷氨酸-5-甲酯固体用50%的甲醇水溶液溶解后于室温下放置使溶剂慢慢挥发,7 d后溶液中析出可供测量的无色晶体.
1.2.2L-谷氨酸-5-甲酯合镁的合成
将0.32 g(2.00 mmol)L-谷氨酸-5-甲酯溶于15 mL水中,在室温下搅拌使其完全溶解,缓慢滴加5mL溶有0.21 g(1.05mmol)M gCl2·6H2O的水溶液,用0.10 mol/L N a2CO3溶液缓慢调节溶液至pH=6.0~7.0,溶液为无色.继续反应30 m in,反应完毕后减压蒸馏溶液至粘稠状,加入无水甲醇10~ 15 mL,溶液中出现白色沉淀物.过滤,用无水甲醇洗涤,干燥.产率:87.1%.mp>300℃.A nal.,Found:C,42.02;H,5.82;N,8.21%.Calc:(C12H20 M gN2O8):C,41.82;H,5.85;N,8.13%.FT-IR(KBr pellet,ν/cm-1):1727 s,1621 s,1566 s,1321 m,1053 m,568 m,482 m.
1.2.3L-谷氨酸-5-甲酯合钙的合成
将0.32 g(2.00mmol)L-谷氨酸-5-甲酯溶于15 mL水中,室温下搅拌使其完全溶解.用Ca(OH)2的水溶液缓慢调节至pH=7.0,溶液为无色.继续反应30m in,反应完毕后减压蒸馏溶液至粘稠状,加入无水甲醇10~15 mL,溶液中出现白色沉淀物.过滤,用无水甲醇洗涤,干燥.产率:72.1%.mp>300℃.A nal.,Found:C,39.95;H,5.63;N,7.83%.Calc:(C12H20CaN2O8):C,39.99;H,5.59;N,7.77%.F I-IR(KBr pellet,ν/cm-1):1724 s,1617 s,1569 s,1336 m,1041 m,576 m,485 m.
1.2.4L-谷氨酸-5-甲酯晶体结构的测定
取0.30 mm×0.30 mm×0.06 mm无色晶体置于Bruker SMART A PEX CCD X-射线单晶衍射仪上,在293(2)K,采用石墨单色化的M oKa射线 (λ=0.71073Å)作为衍射光源,扫描方式为Φ和ω,于2.46≤θ≤28.16收集得1287个衍射点,其中953个是独立点,R int值为0.0506.所有数据均采用SADABS multi-scan校正程序进行校正[6,7],其中,对满足I>2σ(I)的953个点进行结构解析.用直接法解得晶体结构.对所有非氢原子坐标,使用全距阵最小二乘法进行各项异性温度因子修正[7-9].对与N和C原子键合的H原子,采用骑跨式理论加氢,其中键长分别为0.89(NH3—H 原子)、0.98(CH—H 原子)和0.97Å(CH2—H 原子 ),Ueq(H)为1.2Ueq(母体原子)(—CH3和—NH3中H 原子,为1.5Ueq).最后精修结果为R1= 0.0506,w R2=0.1598(见表1).
1.2.5 催化三磷酸腺苷二钠分解的活性测试
催化三磷酸腺苷二钠分解的效果(活力大小)可用反应终止后反应液中无机磷(Pi)含量衡量[10-12].而无机磷可与硫酸钼酸铵反应生成有色化合物,因此无机磷含量可用比色法测定.
无机磷标准曲线的绘制:在均加有0.1 mL 20% 三氯酸(TCA)、0.3 mL H2O 的7支编号试管中分别加入0.1mL 的0、10、20、30、40、50、60mmol/L的N a2HPO3,再于各试管中加入2.5 mL硫酸钼酸铵-硫酸亚铁溶液,摇匀并于波长660 nm处测定吸收值OD.测量5次/样品.以测定的OD值为纵坐标,Pi浓度为横坐标作图,即得无机磷标准曲线.
化合物对三磷酸腺苷二钠分解活性的测定则通过测定混合体系的OD值后,比较无机磷标准曲线得相应的无机磷含量,即可判断出活性影响.具体操作:分别取反应介质0.4 mL于2支试管中,一支试管中依次加入0.4 mL化合物的溶液和1.0 mL溶剂,另支试管中直接加入1.4 mL溶剂(作为参照液).于室温下反应5 m in后于2支试管中分别加入0.2 mL 20%TCA中止反应.吸取上述反应液各0.5 mL,各加入2.5 mL硫酸钼酸铵-硫酸亚铁溶液.以参照液为对照并于660 nm处测定化合物溶液在的OD值.其中,反应溶液分别按下比例配制:
① 介质溶液:50 mmol/L三羟基氨基甲烷(T ris)-HCl(pH=8.80)+5 mmol/L三磷酸腺苷二钠+20 mmol/L N aCl+100 mmol/L CH3OH;
②10% 质量分数的硫酸钼酸铵溶液:10 g钼酸铵+100 mL 5 mol/L硫酸;
③硫酸钼酸铵-硫酸亚铁溶液:5 g硫酸亚铁+10 mL 10%硫酸钼酸铵溶液+87.5 mL蒸馏水;
④待测目标化合物溶液配制:将待测目标化合物配成质量浓度约16 g/L溶液.

表1 晶体学数据Tab.1 Crystallographic data
2 结果与讨论
2.1 合成和结构的光谱分析
L-谷氨酸-5-甲酯的合成采用了仿自然条件,产率达到93.8%;所得L-谷氨酸-5-甲酯易溶于水,难溶于甲醇、乙醇、乙醚、DM F、DM SO 等有机溶剂;1.0 mmol/L水溶液其pH≈4.元素分析的测量结果与理论计算结果基本相符.
在L-谷氨酸-5-甲酯红外光谱中,最显著特点为1730 cm-1处呈现一个新的强吸收峰,可指定为酯基中 νas(C=O)特征吸收峰[13].3130~ 2958 cm-1为 νas(NH+3)吸收峰,2752~ 2250 cm-1为 νs(NH+3)吸收峰,1611 cm-1为 νas(COO-)吸收峰,1355 cm-1为 νs(COO-)吸收峰,1080 cm-1为ν(C—N)吸收峰,1583 cm-1为 δas(NH+3)吸收峰,1412 cm-1为 δs(NH+3)吸收峰.上述吸收峰较之反应物L-谷氨酸的标准红外谱图,其变化不大,说明在生成物分子中形成内络盐部分的羧基和氨基依旧存在.
在钙和镁化合物的红外光谱中,1600 cm-1处均有 νas(COO-)吸收峰,1350 cm-1为 νs(COO-)吸收峰;与L-谷氨酸-5-甲酯中νas(COO-)、νs(COO-)谱峰相比,均发生了移动,表明羧基与金属离子的成键. 其中,Δν(COO-)≈250 cm-1,因此可认为化合物中羧基是以单齿配位模式与金属离子成键的[14-16].1040 cm-1处有ν(C—N)伸缩振动,与L-谷氨酸-5-甲酯中ν(C—N)伸缩振动约差40 cm-1;同时未见νas(NH+3)、νs(NH+3)、δas(NH+3)及δs(NH+3)吸收峰,说明氨基中氮原子也参加了成键.此外,可认为560 cm-1和465 cm-1处的吸收峰分别为ν(N—M)和ν(O—M)伸缩振动[17-18].推测化合物的结构见图1.元素分析数据也证明了该结构的可能性.
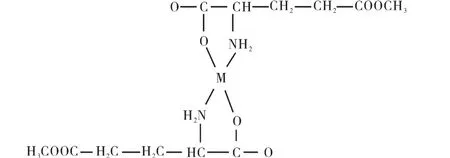
图1L-谷氨酸-5-甲酯金属化合物的可能结构Fig.1 Structures of metal complexes w ith 5-methyl-L-glutamate
2.2 晶体结构分析
L-谷氨酸-5-甲酯晶体属单斜晶系、C2空间群,a= 10.286(3)Å,b= 4.6163(11)Å,c=17.111(4) Å ;β=104.995(4)°.其独立单元结构见图2.其晶体结构中化合物分子以内盐形式存在,其键长、键角均在正常范围内(见表2).其扭转角Ψ1(N 1—C2—C1—O 2)=-34.1(3) °,Ψ2(N 1—C2—C1—O 2)=149.1(4) °,χ1(N 1—C2—C3—C4)=-56.2(4) °,χ2(C2—C3—C4—C5)=173.5(3) °,较之L-谷氨酸(Ψ1=-35 °, Ψ2=145 °, χ1= ±60 °,χ2=180°),有所改变.晶胞堆积见图3.在晶体结构中,分子间存在N—H…O氢键作用(见表3).化合物沿ob方向堆积,每6个分子通过8个N—H…O 或O…H—N 构成一个聚合单元.
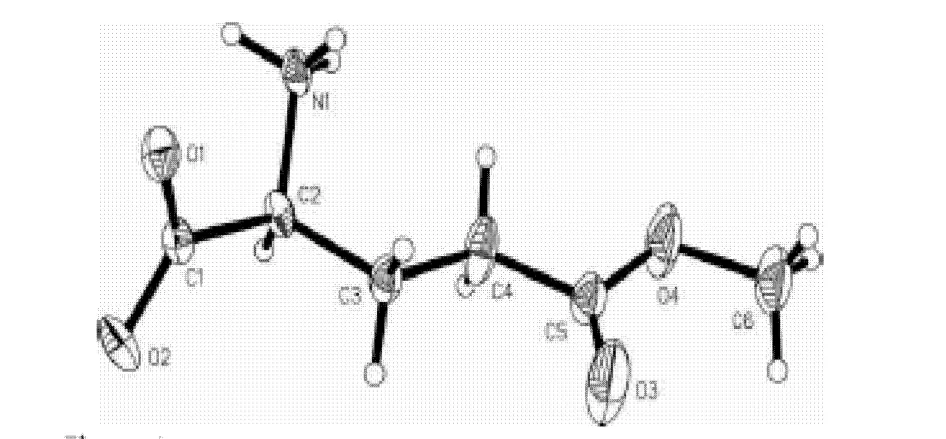
图2L-谷氨酸-5-甲酯结构Fig.2 Structure of 5-methyl-L-glutamate
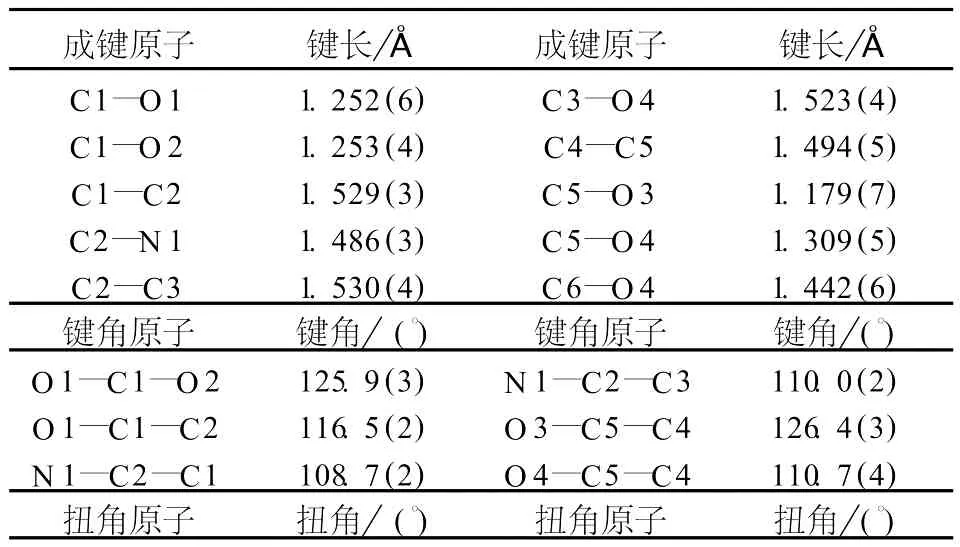
表2 选择的部分键长、键角和扭角Tab.2 Selected bond lengths,bond angle and torsion angles
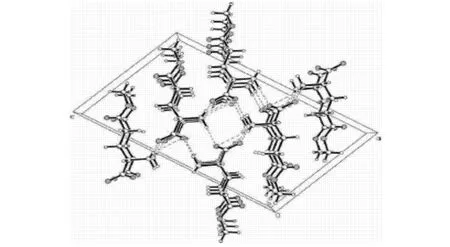
图3 晶胞堆积图Fig.3 Packing diagram in a unit cell
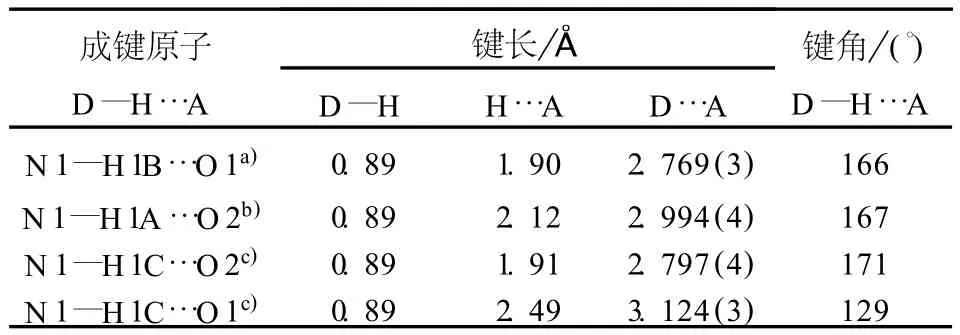
表3 氢键的键长和键角Tab.3 Hydrogen bond lengths and bond angles
2.3 对三磷酸腺苷二钠分解的影响
测定所得化合物体系的磷含量见表4.
L-谷氨酸-5-甲酯组成体系所测的分解无机磷含量为-1.507mmol.由于实验仪器及人为因素等可能产生的误差(如:若OD读数值误差±0.001,则经数据处理后对应的Pi含量误差为±1.012),则可认为经数据处理后对应的Pi含量存在误差±1.507.因此,室温下,可认定L-谷氨酸-5-甲酯对三磷酸腺苷二钠活性无影响.
由表4可知,L-谷氨酸-5-甲酯合镁和L-谷氨酸-5-甲酯合钙对三磷酸腺苷二钠的分解均有较好的活性,其活性L-谷氨酸-5-甲酯合镁>L-谷氨酸-5-甲酯合钙.
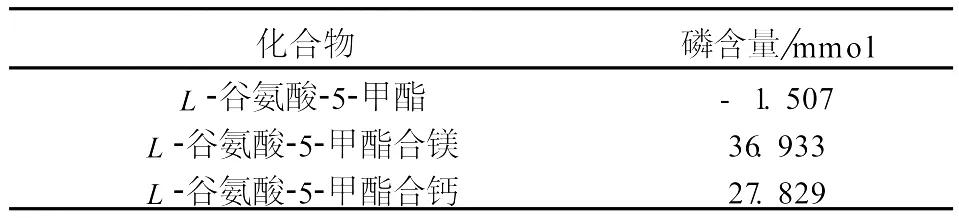
表4 化合物体系的磷含量Tab.4 Contents of phosphorus of system s w ith complexes
3 结语
以L-谷氨酸为原料,采用仿自然的条件,在甲醇溶剂中,加入硫酸为催化剂,合成得到L-谷氨酸-5-甲酯.测试表明,L-谷氨酸-5-甲酯分子中的羧基和氨基依旧保留着内络盐结构.L-谷氨酸-5-甲酯X-射线单晶衍射测定表明,L-谷氨酸-5-甲酯属单斜晶系C2空间群,其中a=10.286(3)Å,b=4.6163(11)Å,c= 17.111(4)Å;β= 104.995(4)°.L-谷氨酸-5-甲酯分别与M gCl2·6H2O 和Ca(OH)2反应,可合成得到相应的金属化合物.对合成所得的化合物,进行了三磷酸腺苷二钠分解的催化活性试验.比色法测试实验表明,在室温(25°C)和pH=8.80条件下,L-谷氨酸-5-甲酯对三磷酸腺苷二钠的分解几乎无影响;而L-谷氨酸-5-甲酯合镁和L-谷氨酸-5-甲酯合钙对三磷酸腺苷二钠的分解均产生较好的活性.
[1] 邹忠梅,喻长远.人体生命之源:氨基酸[M].北京:中国医药科技出版社,2000.
[2] Kurihara H,Hayakawa T,W atanabe H.Soil decontam inating method:JP,275741[P].2003-03-09.
[3] Ito S,M atsumoto K,Yamazaki Y,et al.A nt im icrobial composition:JP,11-302104[P].1999-02-11.
[4] 袁 瑾,钟惠民,李 聪.镍离子-氨基酸配合物的合成及其分析[J].氨基酸和生物资源,1995,17(3):40-42.
[5] 李为明,王小妹.L-谷氨酰胺制备研究[J].化工时刊,1999,9:16-19.
[6] Sheldrick GM.SHELXL 97.program for the refinementof crystal structure [M ].ttingen:U niversity ofttingen,1997.
[7] Sheldrick G M.SADABS[M].ttingen:U niversity ofttingen,1996.
[8] Bruker AXS Inc.SMART A PEX(V ersion 5.628),SA IN T+ (V ersion 6.45)andSHELXTL-N T(V ersion 6.12)[M].M adison:Bruker AXS Inc.,2001.
[9] Sheldrick GM.SHELXS97 and SHELXL 97[M].ttingen:U niversity ofttingen,1997.
[10] 张志良,瞿伟菁.植物生理学实验指导[M].3版.北京:高等教育出版社,2003:89-91.
[11] 薛应龙.植物生理学实验手册[M].上海:上海科学技术出版社,1985,111-112.
[12] 中国科学院上海植物生理研究所和上海市植物生理学会.现代生理学实验指南[M].北京:科学出版社,1999:104-106.
[13] 刘国湘,张新信,胡德荣,等.氨基酸酯化方法的比较及其红外光谱研究[J].氨基酸和生物资源,1995,17(3):36-38.
[14] 黄德如,汪仁庆.无机和配位化合物的红外和拉曼光谱[M].3版.北京:化学工业出版社,1986:235-239.
[15] 乐学义,杨 光,卢其明.[M n(H2O)(phen)2(PA c)](ClO4)的合成、红外光谱及晶体结构[J].无机化学学报,2002,18(4):427-430.
[16] 卢文贯,潘育方,彭翠红.配合物[Cu(HPHAC)2(py)2]的合成和晶体结构[J].无机化学学报,2005,21(5):721-724.
[17] 马卫兴,钱保华,高 健,等.配合物[Zn(tren)(HSSA)]的合成,晶体结构及表征[J].无机化学学报,2005,21(4):612-616.
[18] 祝心德,党元林,王成刚,等.2,4-二羟基苯甲酸缩硫脲及其配物的合成与生物活性研究[J].无机化学学报,1997,13(1):68-72.
Synthesis,Characterization and Biological Activity of M etal Complexes with 5-M ethyl-L-Glutamate
J in L ongf ei,S hen Yuesong,W u Yongf ei,W u L am ei
(College of Chem istry andM aterials Science,South-CentralU niversity for N ationalities,W uhan 430074,China)
U nder im itated natural conditionsin the im itation, 5-methyl-L-glutamate was prepared and characterized by elemental analysis and IR. The crystal structure was determ ined by single-crystal X-ray diffraction.The crystal is of monoclinic type,space groupC2 w itha=10.286(3)Å,b=4.6163(11)Å,c=17.111(4) Å , β= 104.995(4)°.Two complexes of Ca(Ⅱ )and M g(Ⅱ )w ith 5-methyl-L-glutamate were obtained by reating 5-methyl-L-glutamate w ithM gCl2·6H2O and Ca(OH)2,respectively.Spectrophotometrywas used to test for their activities on the hydrolysis of adenosine disodium triphosphate.The results show that the complexes of Ca(Ⅱ )andM g(Ⅱ )had good activity.
derivants ofL-glutam ic acid;biological activity;adenosine disodium triphosphate
O 723:Q 599
A
1672-4321(2011)01-0017-04
2010-12-13
金龙飞(1962-),男,博士,研究方向:化学生物学与药物化学;E-mail:longfei.jin@yahoo.com
湖北省自然科学基金重点资助项目(2008CDA 067)

