久效磷分子印迹传感器的电化学响应特性
连惠婷,陈娟娟,薛艳,刘斌
(华侨大学材料科学与工程学院,福建泉州 362021)
久效磷分子印迹传感器的电化学响应特性
连惠婷,陈娟娟,薛艳,刘斌
(华侨大学材料科学与工程学院,福建泉州 362021)
基于壳聚糖功能基体的电化学沉积,以久效磷为模板分子,在玻碳电极表面直接制备具有记忆功能的分子印迹电化学传感器.借助以氢键为主的弱的分子间作用力,实现久效磷在壳聚糖聚合基体内的印迹,而施加+0.6 V电压改变复合物成键的微环境可以实现洗脱.对分子印迹膜性质、洗脱方式等制备条件的考察,采用阳离子型电化学探针三氯化六铵合钌,研究分子印迹传感器对久效磷的电化学响应特性.结果表明,所制备的久效磷分子印迹电化学传感器具有较高的选择性,对久效磷的检测限可达0.1μmol·L-1.
分子印迹;传感器;电沉积;久效磷;壳聚糖
有机磷农药因其高效、量小,以及作用方式多、使用方便、半衰期短等优点成为一类广谱杀虫剂,而与此同时产生的环境问题也日益严重.因此,有机磷农药的残留分析受到了广泛关注[1].传统有机磷农残检测方法如光度法[2]、薄层层吸法[3]、气相色谱法[4]、液相色谱法[5]、生物测定法[6]、酶联免疫法[7]、气相色谱-质谱联用法[8]、液相色谱-质谱联用法[9]等普遍存在仪器贵,使用条件苛刻,不易携带等不足,在实际应用中受到很大的限制[10-11].近年发展出乙酰胆碱酯酶的酶抑制型传感器[12]和基于有机磷水解酶的电化学传感器[13]具有较高的选择性,但酶传感器要求制备和使用条件温和,在实际样品检测中受到一定程度的限制.因此,探索一种方便、省时、选择性好且稳定性高,适合于在线检测的的新方法成为当前该领域的热点.作为一项“量身定做”的技术,分子印迹技术(Molecule Imp rinting Technique, M IT)已经得到飞速发展.它可获得空间和结合位点上与模板分子完全匹配的聚合物,理论上对任何一个分子均可制备相应的分子印迹聚合物,具有预定选择性、专一性、高度稳定性[14].应用分子印迹聚合物(Molecularly Imp rinted Ploymer,M IP)取代天然物质作为传感元件,在保持传感器较高选择性和灵敏度的同时,其耐受性提高,寿命延长,在农残检测中具有潜在的优势[15].本文基于壳聚糖为功能基体的电化学沉积并结合分子印迹技术,制备了以久效磷(MCP)为模板的壳聚糖分子印迹电化学传感器.
1 实验部分
1.1 主要仪器与试剂
CH I630A型电化学工作站 (上海辰华仪器有限公司);三电极系统(分子印迹膜/玻碳电极(M IP/ GCE)为工作电极,铂丝电极为对电极,饱和甘汞电极为参比电极);磁力搅拌器(广东深圳天南地北有限公司);S-3500N型扫描电子显微镜 (日本 Hitachi公司).
壳聚糖(Chitosan,CTS,脱乙酰度≥90%,德国Sigma A ldrich有限公司);久效磷,敌百虫,氧化乐果,Ru(NH3)6Cl3(均为AR级,质量分数为99%,北京迪科马科技有限公司).采用含1.7 mmol·L-1Ru(NH3)6Cl3的0.1 mol·L-1KCl溶液为背景溶液;实验用水为M illi-Q型纯化水系统(美国M illipore公司)提供的超纯水.
1.2 久效磷分子印迹电化学传感器的制备
取一定量壳聚糖固体于稀HCl溶液中超声30 min,溶解后用NaOH溶液调节p H值至5.0;然后,逐滴加入以丙酮配制的久效磷溶液,形成含久效磷模板分子的质子化壳聚糖电化学沉积液.将三电极系统移入上述溶液中,在-1.5 V(vs.SCE,下同)下恒电位沉积5 min,取出后用水迅速淋洗并置于空气中晾干6 h.将此修饰电极浸于0.01 mol·L-1的 KCl溶液中,施加+0.6 V电压洗脱3次,每次3 min,以除去壳聚糖聚合物基体中的模板分子久效磷.最后用水冲洗,即可制成保留久效磷构型孔穴的久效磷分子印迹电化学传感器.
1.3 电化学实验
将M IP/GCE为工作电极的三电极体系移入背景溶液中,以微分脉冲伏安法记录Ru(NH3)6Cl3探针的伏安曲线.每次使用后,将电极浸于0.01 mol·L-1的KCl溶液中,施加+0.6 V电位处理3次,每次3 min,洗脱模板分子以便于重复使用.在相同条件下,使用不含久效磷的电化学沉积液制备非印迹电极(NM IP/GCE),并以此作对比实验.
2 结果与讨论
2.1 分子印迹膜的形成
壳聚糖是天然生物高分子甲壳素的衍生物,可溶于酸性水溶液.酸性壳聚糖为粘稠液体,在一定条件下能形成凝胶或薄膜,生物相容且无毒易改性.其中含有丰富的氨基,pKa值为6.3[16].当p H值低于pKa值时,大部分氨基被质子化,使壳聚糖成为一种水溶性的聚电解质;而当p H值大于pKa值时,氨基去质子化,壳聚糖变为不可溶.壳聚糖水凝胶可以通过 H2O还原消耗质子沉积到电极表面,与电极紧密结合并保持原有的性质[17-19].另外,壳聚糖表面丰富的氨基较易与含氢氧丰富的化合物形成分子间氢键[20],而久效磷分子上也含有丰富的氮、氢和氧元素,可能会与壳聚糖分子之间形成弱的分子间氢键.杨芸等[21]研究表明了,壳聚糖可以与久效磷形成复合物.实验选取壳聚糖作为聚合功能基体.
实验中的电沉积条件:沉积电位为-1.5 V,沉积时间为5 min,晾干时间为6 h.在含久效磷和不含久效磷的壳聚糖溶液中,电极以-1.5 V恒电位沉积5 min,其I-t曲线如图1所示.由图1可见,在沉积过程中,电流响应受到抑制,I-t曲线呈逐步下降趋势.说明膜的形成导致界面电子传导能力逐渐降低.此外,有无模板分子的存在,I-t曲线无明显不同,均光滑趋于平缓.因此可以推断电沉积过程中,非电化学活性的久效磷分子的电化学结构没有发生改变[22].
以循环伏安法对印迹传感器进行表征,以考察分子印迹膜的电化学响应特性,结果如图2所示.从图2可知,随着扫描次数的增多,探针分子的循环伏安响应曲线逐渐向外扩张,但当循环200圈时,曲线达到稳定而不再变化,这是膜在背景溶液中的稳定过程.图2显示,膜电极上探针分子的响应电流信号较裸电极上的明显降低,晾干后的印迹膜电极上的氧化还原电流信号比未经晾干的的降低也更明显.表明壳聚糖沉积在玻碳电极表面后,经过一定时间的晾干,聚合物膜在玻碳电极表面可能发生了一个重组过程,使网状膜变得更加有序均匀致密,探针分子的扩散受阻更大所致.
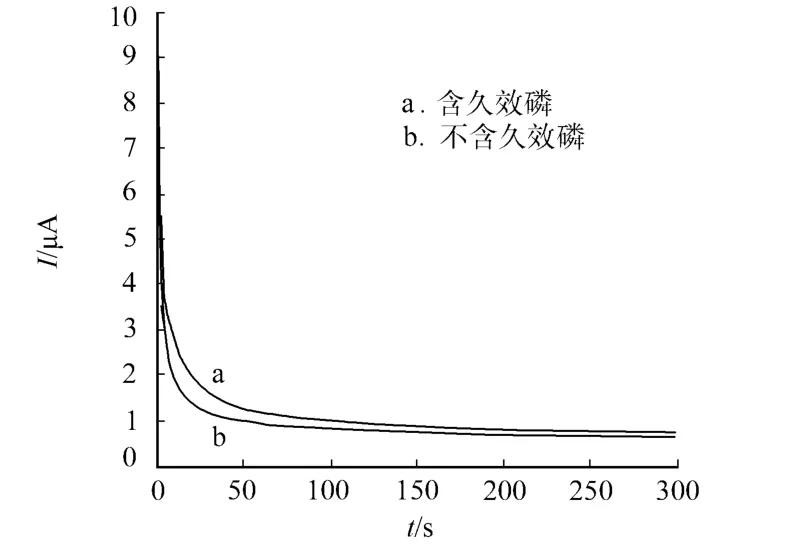
图1 电化学沉积i-t曲线Fig.1 Electrodeposition I-t curve
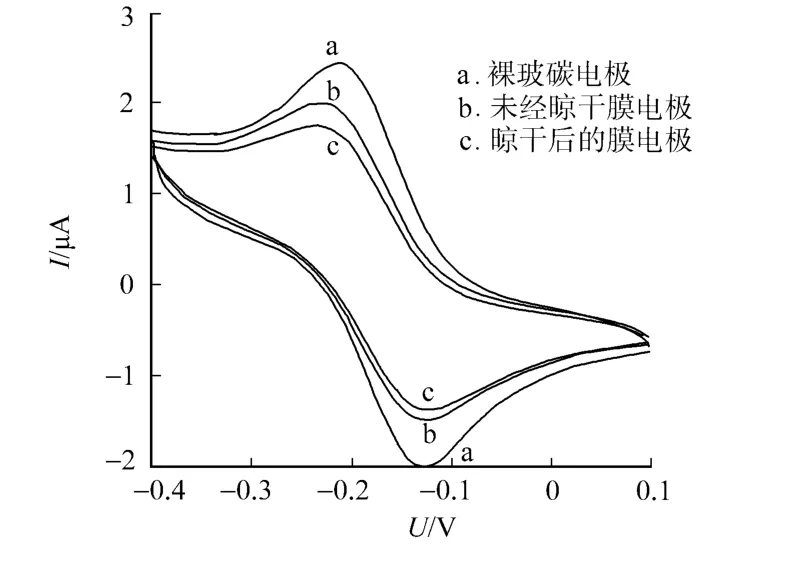
图2 电极的循环伏安图Fig.2 Cyclic voltammogram sof electrodes
利用扫描电镜(SEM)对工作电极的表观形态和表面结构进行显微观察,如图3所示.由图3(a)可见,表面未沉积任何物质的裸玻碳电极呈现出玻碳的黑色光泽,均匀而光滑,呈平面感;由图3(b)可以发现,电极表面立体感增强,颜色变浅,表面物质疏松,呈现出聚合物均匀的质感.充分说明,久效磷壳聚糖分子印迹膜可以均匀地电沉积到玻碳电极表面.

图3 电极的扫描电镜电镜图(5 000倍)Fig.3 SEM s of electrodes(5 000 times)
2.2 电位诱导洗脱模板分子
测试电位对壳聚糖久效磷之间结合力的影响,以探索洗脱模板分子的条件.实验结果表明,施加一定负电压对复合沉积层基本无影响.实验前后经电化学测试,循环伏安曲线和微分脉冲曲线基本无变化,可能是由于负电压下引发形成的聚合物对负电位稳定.但施加正电位时情况则不同,正电位可通过改变质子化壳聚糖与久效磷复合物内部的微环境而降低两者之间的结合力,迫使久效磷从大分子壳聚糖基体内部离开达到洗脱目的.
过低的正电位洗脱速度慢耗时长;过高电压则会使聚合膜与玻碳电极之间的结合受到损坏而导致膜脱离电极表面.实验结果显示,于工作电极上施加+0.6 V电压后,对于模板分子的洗脱效果最佳,当处理3次且每次3 min,微分脉冲伏安图基本不再变化,说明此时模板分子已基本洗脱完全.这可能是由于一定时间内,+0.6 V电压不足以破坏壳聚糖膜与玻碳电极之间结合性能,膜的性质不改变.
正电压改变印迹分子与基体之间的作用力后,中性的久效磷分子与水结合的驱动力显著大于其与质子化的壳聚糖的结合力.因此,久效磷分子溶入水中,实现模板分子的洗脱,壳聚糖基体中留下了与模板分子久效磷互补的孔穴.
久效磷分子印迹电化学传感器经吸附后及利用电位诱导法洗脱后的微分脉冲伏安曲线,如图4所示.由图4可见,每次洗脱后经微分脉冲伏安扫描,探针的还原峰基本回到同一个位置.表明,此电位诱导洗脱法用于模板分子的洗脱效果良好.

图4 久效磷分子印迹传感器的吸附洗脱Fig.4 Adsorption and elution of imp rinted sensor
2.3 分子印迹传感器的电化学响应特性
为了避免因质子化的壳聚糖分子吸附阴离子而对实验产生干扰,选择Ru(N H3)6Cl3用于电极表面状态的测试.电沉积层形成后,壳聚糖久效磷聚合膜与玻碳电极表面结合紧密,探针不容易通过聚合物膜到玻碳表面发生氧化还原反应,其法拉第电流很小[23].洗脱后,原久效磷模板分子在聚合物中占据的空间空出,探针分子则相对容易通过聚合物沉积层到达电极表面发生还原氧化反应.
当分子印迹传感器接触到含有久效磷的溶液时,久效磷又占据了一定量的孔穴,探针传质受阻.因此,电化学性质良好的氧化还原电化学探针可指示印迹膜对无电化学活性的模板分子的响应情况.通过记录印迹传感器对不同浓度目标分子发生识别时,探针分子的传质受到阻碍所导致的电流变化,从而实现印迹电化学传感器对模板分子的间接测定.
Ru(NH3)6Cl3探针在各工作电极上的循环伏安响应情况,如图5所示.图5中:曲线a为裸玻碳电极;曲线b为MCP-CS/GCE电极;曲线c为经+0.6 V电压处理3 min的MCP-CS/GCE电极;曲线d为经+0.6 V电压处理9 m in(3次,每次3 m in)的M IP/GCE电极.
从图5中曲线a可知,裸玻碳电极循环伏安曲线显示该电极可逆性良好.从图5中曲线b可知,电沉积MCP-CS后,探针分子不易通过相对致密的沉积层到达玻碳表面发生还原氧化反应,其法拉第电流降低;同时,从峰电位的偏移来看,电极可逆性变差.从图5中曲线c可知,洗脱模板分子后,膜内留有久效磷识别位点的孔穴,形成一定通道,探针分子较容易到达电极表面发生氧化还原反应,峰电流强度较之曲线b均增大.此时,氧化还原峰位置也会再次发生偏移,比未经洗脱电极的曲线b的可逆性稍增强,但还是比裸玻碳电极的曲线a的可逆性弱.直至洗脱完全,峰电位和峰电流均不再变化(图5中曲线d).探针在此印迹传感器上的电化学响应具有良好的可逆性,且其通道占据机理为印迹分子定量分析提供了基础.
把对照电极置于含久效磷的背景溶液中,经同样实验后引起的探针分子Ru(NH3)6Cl的氧化还原电流强度变化不明显.表明,对照电极上壳聚糖基体内未形成对久效磷的特别识别孔穴.
随着久效磷浓度(C)的增加,探针的还原峰电流值逐渐降低,峰电流与久效磷浓度在0.001~1.0 mmol·L-1的范围内有良好的线性关系,如图6所示.结果表明,其线性相关系数r为0.995 6,检测限为0.1μmol·L-1.
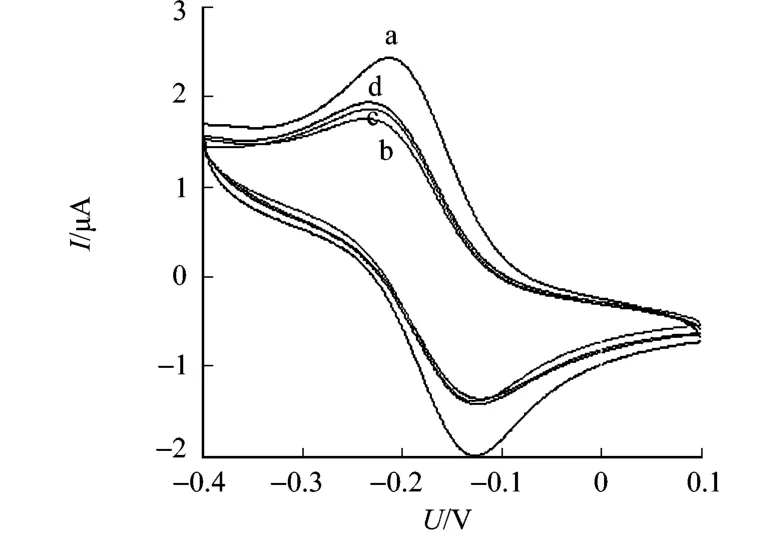
图5 探针在各电极上的循环伏安响应Fig.5 Cyclic voltammetric responses of probe at wo rking electrodes
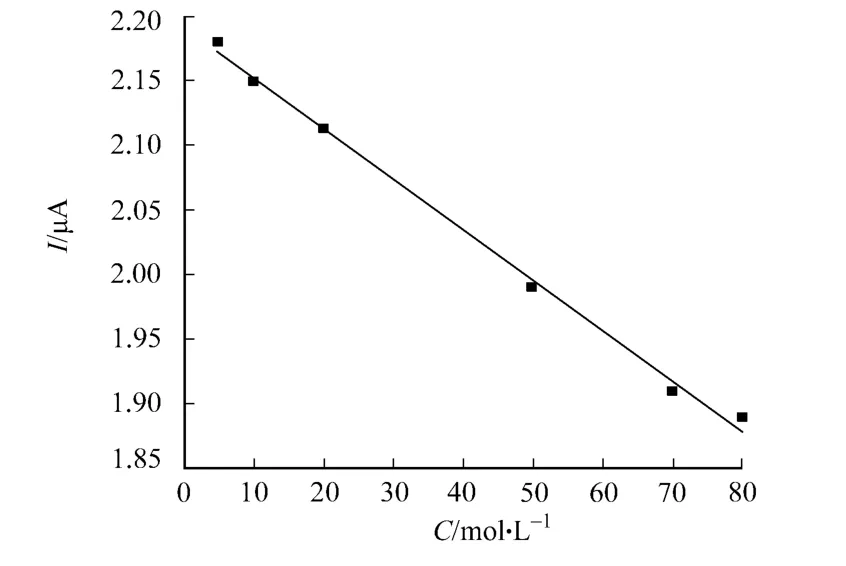
图6 印迹传感器对久效磷的响应的线性关系 Fig.6 linearity relationship of imp rinted senso r responding to MCP
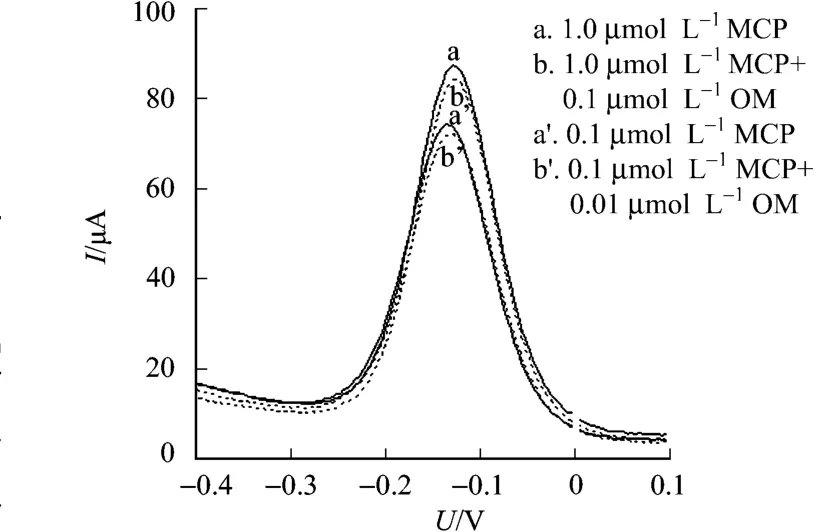
图7 氧化乐果对印迹传感器测定干扰情况Fig.7 Interference of OM for the determination of MCP at the M IP/GCE
2.4 分子印迹传感器的选择性
为了考察印迹膜内识别位点对模板分子是否具有特异选择性,选择与久效磷结构相似的氧化乐果(OM)和敌百虫(Tri),以丙酮配制成储备溶液,向背景溶液中注入该储备液溶液,分别记录氧化乐果和敌百虫浓度10倍于久效磷浓度的干扰情况.结果表明,与久效磷结构极相似的氧化乐果和敌百虫对分子印迹电化学传感器响应久效磷的干扰很小.
氧化乐果对印迹传感器测定的干扰,如图7所示.当加入10倍于被测目标分子浓度的氧化乐果后,其微分脉冲伏安曲线基本没有变化.对于1.0μmol·L-1MCP响应时的微分脉冲伏安曲线,与同时含有10.0μmol·L-1氧化乐果的微分脉冲伏安曲线之间出现的波动为6.18%;10倍浓度的氧化乐果对10.0μmol·L-1MCP测定的干扰波动仅为7.52%.敌百虫实验情况与此类似.说明,敌百虫在久效磷分子印迹电化学传感器对久效磷进行电化学响应时几乎没有干扰.
考察此分子印迹电化学传感器对不同形态久效磷分子响应情况.结果表明,以丙酮配制的久效磷加入壳聚糖溶液为电沉积液,所制备成的壳聚糖分子印迹电化学传感器对丙酮配制的久效磷有明显的吸附,而对以饱和KCl溶液阴离子化的久效磷无明显的吸附作用.这可能是弱极性溶剂丙酮可使久效磷分子保持较好的中性游离状态,由此直接电沉积并洗脱形成的分子印迹电化学传感器不易被对离子型久效磷具有特异性识别.说明,久效磷和壳聚糖之间是以氢键为主的弱作用力形成复合物.
2.5 分子印迹传感器吸附动力学
在p H值为7,温度为25℃下,分别考察非分子印迹电化学传感器与印迹电化学传感器对久效磷的吸附动力学曲线,结果如图8所示.
从图8可知,曲线在初始阶段上升比较快,约在60 min趋于饱和.由图8可判断等温线为Langmuir型,说明特异性识别只在因印迹而留下的固定数量的孔穴中和识别位点上进行.即使吸附久效磷的初始浓度不同,达到饱和状态吸附量基本相同,很好地证明了膜内识别位点数一定.
此外,从图8可知,非分子印迹电化学传感器对久效磷也有吸附,但比印迹传感器的对久效磷的吸附量小得多.这可能是由于非印迹膜仅是表层壳聚糖对久效磷的非选择性吸附,而印迹膜除表面吸附外,更多的是由于内部所形成的特异性识别位点对模板分子的结合所致.
2.6 分子印迹电化学传感器的重现性和稳定性
通过对一定浓度的久效磷溶液进行连续10次测定,结果表明传感器的相对标准偏差为3.3%,显示出良好的重现性.将传感器置于0.1 mol·L-1KCl溶液并于4℃冰箱中保存,一周后测定其对久效磷的响应性能.结果表明,信号能保持原有响应的92.0%,说明传感器用于测定的稳定性较好.
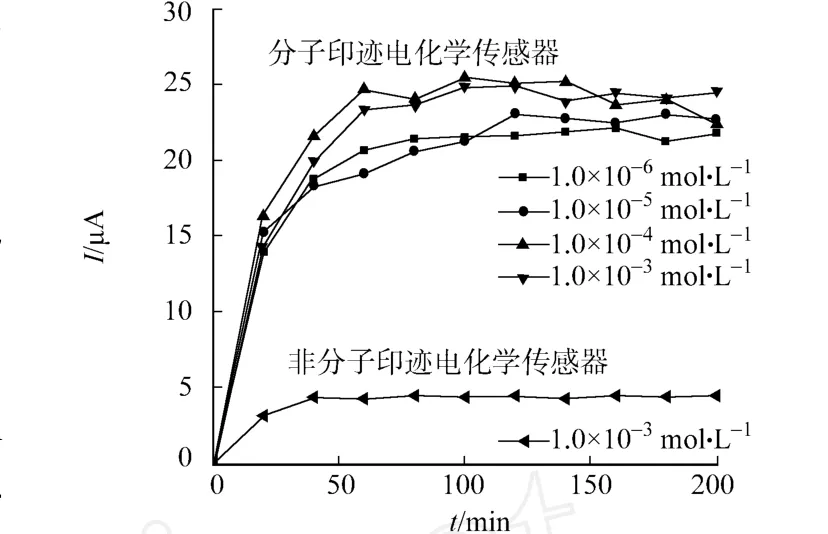
图8 传感器的吸附动力学曲线Fig.8 Adsorption kinetics of sensor
3 结束语
基于质子化壳聚糖在阴极的电化学沉积并结合分子印迹技术,直接在玻碳电极表面制备了可用于久效磷检测的壳聚糖分子印迹电化学传感器.借助以氢键为主的弱的分子间作用力实现久效磷了在壳聚糖聚合基体内的印迹;然后,通过施加+0.6 V电压改变复合物成键的微环境,可以实现洗脱.通过对分子印迹膜性质、洗脱方式等制备条件的考察,制备出的壳聚糖分子印迹电化学传感器的选择性良好.对不同农药的选择性高,对不同形态的目标分子久效磷也具有选择性.同时,此分子印迹传感器对模板分子久效磷的电化学响应特性良好,检测限可达0.1μmol·L-1.
[1]SCHON INGM J,KRAUSE R,BLOCK K.A dual amperometric/potentiometric FIA-based biosensor for the distinctive detection of o rganophospho rus pesticides[J].Sens Actuato rs(B),2003,95(1/2/3):291-296.
[2]RHOUA TIA,GEORGES I,MONTSERRA T C P.Selective spectrophotometric detection of insecticides using cholinesterases,phosphotriesterase and chemometric analysis[J].Enzyme and M icrob Technol,2010,46(3/4):212-216.
[3]CIESLA T,WA KSMUNDZKA-HAJNOS M.Two-dimensional thin-layer chromatography in the analysis of secondary plantmetabolites[J].J Chromatogr(A),2009,1216(7):1035-1052.
[4]RAMOSJ J,GONZALEZM J,RAMOSL.Comparison of gas chromatography-based approaches after fastminiaturised sample preparation for themonitoring of selected pesticide classes in fruits[J].JChromatogr(A),2009,1216 (43):7307-7313.
[5]WU Qiu-hua,CHANG Qing-yun,WU Chun-xia,et al.U ltrasound-assisted surfactant-enhanced emulsification microextraction for the determination of carbamate pesticides in water samp les by high performance liquid chromatography[J].J Chromatogr(A),2010,1217(11):1773-1778.
[6]MANSOUR SA,GAD M F.Risk assessment of pesticides and heavy metals contaminants in vegetables:A novel bioassay method using daphnia magna straus[J].Food Chem Toxicol,2010,48(1):377-389.
[7]Q IAN Guo-liang,WANG Li-min,WU Yun-ru,et al.A monoclonal antibody-based sensitive enzyme-linked immunosorbent assay(EL ISA)for the analysis of the o rganophospho rous pesticides chlorpyrifos-methyl in real samples[J].Food Chem,2009,117(2):364-370.
[8]RISSA TO SR,GALH IANE M S,ALM EIDA M V,et al.Multiresidue determination of pesticides in honey samples by gas chromatography-mass spectrometry and application in environmental contamination[J].Food Chem,2007, 101(4):1719-1726.
[9]林玉锁.农药环境污染的调查与诊断技术[M].北京:化学工业出版社,2003:5-8.
[10]M ICKOVA B,KOVALCZUK T,RAUCH P.Analytical performances of validated chemiluminescent enzyme immunoassays to detect N-methylcarbamate pesticides[J].Anal Chim Acta,2005,528(2):243-248.
[11]SETFORD SJ.Immunosensing in organic and mixed aqueous organic phase environments[J].Trends Anal Chem, 2000,19(5):330.
[12]刘淑娟,谭正初,沈国励,等.基于二氧化锆纳米粒子固定乙酰胆碱酯酶的甲基对硫磷传感器[J].传感器技术学报,2009,22(5):613-617.
[13]陈帆,陈欢林,何奕.有机磷水解酶传感器及其应用研究进展[J].传感器技术,2004,23(4):5-9.
[14]史瑞雪,郭成海,邹小红,等.分子印迹技术研究进展[J].化学进展,2002,14(3):182-191.
[15]PESAVENTO M,AGOSTINO GD,BIESUZ R.Molecularly imp rinted polymer-based sensors for amperometric determination of nonelectroactive substances[J].Electroanalysis,2009,21(3):604-611.
[16]Q IU Jian-ding,XIE Hui-ying,L IANGRu-ping.Preparation of porous chitosan/carbon nanotubes film modified electrode for biosensor application[J].M icrochim Acta,2008,162(1/2):57-64.
[17]WU Li-qun,LEE K,WANGXiang,et al.Chitosan-mediated and spatially selective electrodeposition of nanoscale particles[J].Langmuir,2005,21(8):3641-3646.
[18]LUO Xi-liang,XU Jing-juan,DU Ying,et al.A glucose biosenso r base on chitosan-glucose oxidase-gold nanoparticles biocomposite fo rmed by one-step electrodeposition[J].Anal Biochem,2004,334(2):284-289.
[19]ZANGM EISTER R A,PARK JJ,RUBLOFF GW.Electrochemical study of chitosan films deposited from solution at reducing potentials[J].Electrochim Acta,2006,51(25):5324-5333.
[20]刘斌,孙向英,徐金瑞.壳聚糖在分析化学中的应用[J].华侨大学学报:自然科学版,2003,24(3):225-233.
[21]杨芸,连惠婷,刘斌,等.敌百虫分子印迹聚合物的合成及其性能[J].华侨大学学报:自然科学版,2009,30(3): 284-288.
[22]马永飞,曲祥金,文仕云,等.分子印迹膜电化学传感器检测土壤中莠去津[J].化学研究与应用,2009,21(5):624 -629.
[23]刘志航,宦双燕,沈国励,等.以分子印迹电聚合膜为仿生受体检测辛可宁[J].高等学校化学学报,2005,26(6): 1049-1051.
(责任编辑:黄晓楠英文审校:陈国华)
Electrochemcial Characteristic of Monocrotophos Molecularly Imprinted Sensor
L IAN Hui-ting,CHEN Juan-juan,XUE Yan,L IU Bin
(College of Material Science and Engineering,Huaqiao University,Quanzhou 362021,China)
A molecularly imp rinted electrochemical sensor(M IP/GCE)of good memory capacity was developed.Using moncrotophos as temp latemolecule,the compound of chitosan and moncrotophos were direct synthesized onto the surface of glass carbon electrode basing on electrodeposition of function matrix chitosan with the aid of hydrogen bond between chitosan and moncrotophos,the imp rinted film was formed after the elution of moncrotophos from the co-deposited compound film by app lying+0.6 V on the electrode to change the combination microenvironment.Cationic probe Ruwas emp loyed to study the op timal conditions of film formation and the electrochemical performance of M IP/GCE on moncrotophos.Result show s,the monocrotophos molecularly imp rinted electrodeposition was of good selectivity and detection limit of 0.1μmol·L-1wasobtained.
molecularly imp rinted;senso r;electrodeposition;moncrotophos;chitosan
O 631;TP 212.2
A
1000-5013(2011)02-0182-06
2010-05-23
刘斌(1963-),男,教授,主要从事电化学传感器的研究.E-mail:bliu@hqu.edu.cn.
国家自然科学基金资助项目(20955001,20575023);福建省国际合作重点项目(2006I0021);福建省自然科学基金计划资助项目(D0710017,D0810016,U0850008)

