苯磺酰氯最佳合成工艺探讨*
王 琪,徐元萍,2,黄红缨
(1.江苏技术师范学院 化学与环境工程学院,江苏 常州 213001;2.江苏工业学院 化学化工学院,江苏 常州 213164)
科研与开发
苯磺酰氯最佳合成工艺探讨*
王 琪1,徐元萍1,2,黄红缨1
(1.江苏技术师范学院 化学与环境工程学院,江苏 常州 213001;2.江苏工业学院 化学化工学院,江苏 常州 213164)
本文以苯和氯磺酸为主要原料合成苯磺酰氯,改进现行的碱洗工艺为酸洗工艺,通过正交实验确定了最佳合成工艺条件,即原料配比n(氯磺酸)∶n(苯)=3.5∶1.0、反应时间2h、滴苯速度2h。改进工艺后原料利用率高,产品收率由60%提高到83%以上,同时可减少三废的排放。
苯磺酰氯;合成工艺;正交实验
Abstract:In this paper,benzenesulfonyl chloride was synthesized from benzene and chlorosulfonic acid,and the traditional caustic washing process was improved to the pickling process.Determined by orthogonal experiments,the best synthesis processwas:rawmaterial ratio of n(Chlorsulfuronacid∶n(benzene)=3.5∶1.0,reaction time was 2h,drip of benzene speed was 2h.The material availability was improved,The yield was raised from 60%to above 83%.Meanwhite thewasteswere reduced.
Key words:benzenesulfonyl chloride;synthesis process;orthogonal experiment
苯磺酰氯是一种用途广泛的化学中间体,用于制备磺酰胺及鉴定各种胺类[1]。工业苯磺酰氯的合成以苯和氯磺酸为原料,经磺化提纯而得。采用该路线制备苯磺酰氯的现行生产工艺为:在搅拌情况下,往氯磺酸中滴加苯,控制温度在25℃左右,反应完毕后,滴加碱洗,静置分层,然后吸取上层的水,下层用水洗,静置分层,将下层取出,为苯磺酰氯粗品,再进行减压蒸馏就得到苯磺酰氯成品。
此路线工艺简单,原料易得,但收率仅为40%~50%,且污染较为严重。
本文通过正交实验对最佳工艺条件进行了探讨,考察了原料配比、反应时间、滴苯速度对收率的影响,在反应后期滴加NaCl,反应结束后改原先的碱洗工艺为酸洗工艺。改进生产工艺后,提高了产品收率,降低生产成本,而且减少了三废的排放。
1 实验部分
1.1 苯磺酰氯的合成反应原理
将苯与氯磺酸反应,生成苯磺酰氯,反应方程式如下:

1.2 仪器及试剂
循环水式真空泵;烘箱;电动搅拌器等。
苯(A.R.永丰化学试剂厂);氯磺酸(上海亭新化工试剂厂);NaCl(原上海试剂四厂);H2SO4(丹阳永丰化学试剂厂),以上试剂均为分析纯。
1.3 苯磺酰氯制备
在装有电动搅拌器、温度计、球形冷凝管和恒压滴液漏斗的四口烧瓶中加入一定量的氯磺酸,通过恒压滴液漏斗,搅拌条件下滴加苯,温度在25℃左右。苯滴加完毕后,在25℃左右保温反应1~3h。反应结束后,向物料中加入一定量的NaCl,保温使其继续反应。
反应完毕后,将物料滴入H2SO4溶液中洗涤,控制温度小于30℃,然后转移至分液漏斗中静置30min。待上下分层,取上层溶液(上层液为苯磺酰氯,中间层液为副产物,下层液为含有硫酸盐的硫酸),用蒸馏水洗涤,静置过夜,取下层溶液(下层液为苯磺酰氯粗品)。
将所得苯磺酰氯粗品进行减压蒸馏,蒸出其中的水份等前馏份,取100℃[2]以上的馏分进行称重和分析,以计算产品收率。工艺流程见图1。
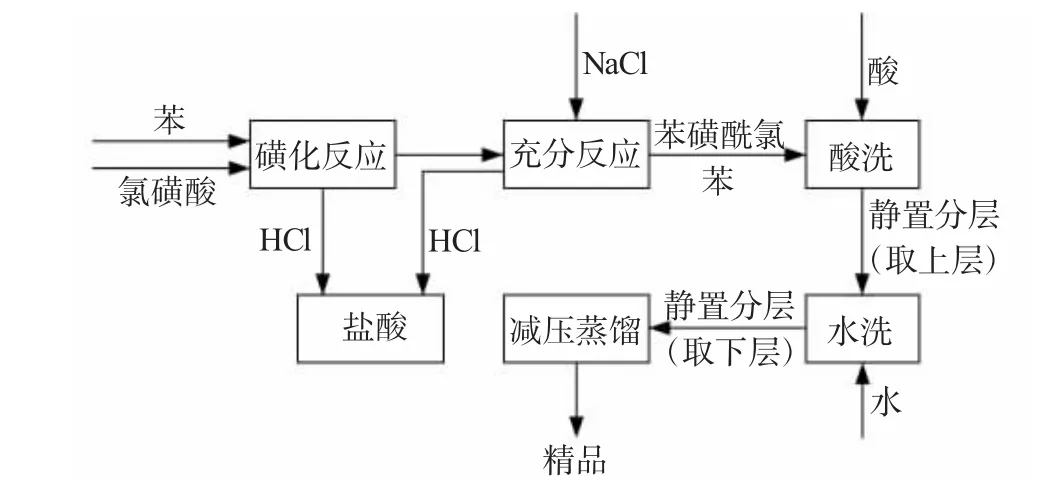
图1 工艺流程图Fig.1 Engineering flow sheet
2 结果与讨论
2.1 正交实验设计
综合分析工业生产条件,通过正交实验研究原料配比、反应时间和滴苯速度对反应产率的影响,以此来确定最佳工艺条件。正交实验因素水平表见表1。

表1正交实验水平表Tab.1 Orthogonal experimental level table
正交实验为四因素三水平,选用L9(34)正交表安排实验[3,4],见表 2。

表2正交实验表L9(34)Tab.2 Orthogonal table L9(34)
2.2 正交实验结果与讨论
应用表2的正交实验表,共进行9组实验,正交实验结果及分析见表3。

表3 正交实验结果与分析Tab.3 Results and analysis of orthogonal experiment
从表3可得出以下结论:
(1)各因素对磺化收率影响的顺序为:投料比>反应时间>滴苯速度,其中,投料比为显著因素,反应时间为一般因素,滴苯速度为不显著因素。
(2)最佳工艺条件为A2B3C2,见表4所示。

表4 最佳工艺条件Tab.4 The optimum conditions
(3)随着原料氯磺酸与苯的配比增加,收率也升高,但是从工业成本出发,将氯磺酸与苯的配比控制在3.5∶1。
(4)反应时间的影响 保温一定的时间,是为了使反应更彻底,让有机相与氯磺酸接触更充分,消除局部过热现象,提高冷却面的传热效率,使反应平稳完全地进行。保温反应的时间太短,搅拌不充分,物料不能充分混合,反应不完全;保温时间太长,会导致副反应的发生[5]。因此,反应时间一般控制在2h为宜。
(5)滴苯速度的影响 从理论上分析得知,放慢苯的加料速度,可以使反应体系中的苯含量相对减少,减少副产物二苯酚的形成[1],从而提高目标产物的收率。但通过正交实验发现,滴苯速度是一个不显著因素,因此,实验确定滴苯速度在2h左右为宜。
(6)磺化反应是一个放热反应,当温度过高时,会发生大量的副反应[1]。因此,该反应温度控制在25℃左右,不宜超过30℃。
(7)氯磺酸是一种强酸,遇水立即分解放出大量气体和热量,容易发生事故,因而生产中所有原料以及设备都必须干燥无水。在反应中会生成HCl气体,考虑到HCl气体极易溶于水。因此,反应中用循环水式真空泵对其抽负压,使生成的HCl气体溶于水中。在工业生产中,含酸水可循环使用,经分析其浓度达到要求后,可出售。
2.3 实验结果验证与讨论
我们在正交实验得出的最佳工艺条件的基础上又进行了一系列的验证实验。同时研究了NaCl用量、酸洗液的浓度等对苯磺酰氯产率的影响。
验证实验共进行了9组,结果见表5。
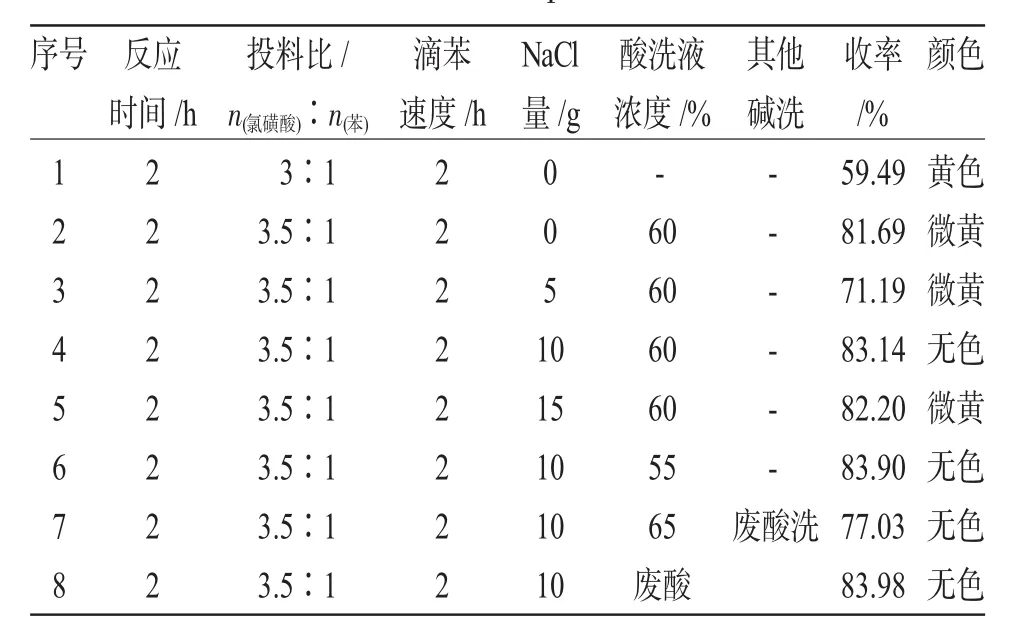
表5 验证实验结果Tab.5 Verified the experimental results
从表5中8组验证实验结果可得出以下结论:
(1)证实用酸洗比现行工业上所采用的碱洗工艺产率提高了二十多个百分点;酸洗液的浓度为60%或者用废酸洗涤效果是一样的;工业上可采用废酸循环使用。
(2)加入NaCl之后产率提高了约2%,这是因为NaCl会和一部分副产物反应,生成苯璜酰氯,这不仅减少了副产物的生成,而且还提高了产率。
(3)最佳工艺条件见表6。

表6 验证实验所得最佳工艺条件Tab.6 Verification experiment the optimum conditions obtained
3 结论
对于苯磺酰氯的合成,我们参考了工业生产的工艺条件,在现行工业生产的基础上考查了合成苯磺酰氯的反应条件——投料比、反应时间以及滴苯速度对产品收率的影响。在综合考虑这些因素的基础上通过一系列正交实验,得到了合成苯磺酰氯的最佳工艺条件,即:投料比 /n(氯磺酸)∶n(苯)为 3.5∶1、滴苯速度为2h、反应时间为2h。
另外,我们对现行工业生产工艺进行了一些改进:加入了NaCl以提高产率、改碱洗为酸洗工艺。通过实验得出加入NaCl能够提高产率2个百分点以上,同时确定了酸洗液的浓度为60%。
[1]陈爱英,张雨中.苯磺酰氯的制备[J].河北化工,2001,(2):27-28.
[2]《防火检查手册》编辑委员会.化学危险品手册[M].上海科学技术出版社,1983.1135.
[3]郝素娥,强亮生.精细有机合成单元反应与合成设计[M].哈尔滨工业大学出版社,2004.55-56.
[4]姚蒙正,等.精细化工产品合成原理[M].北京:中国石化出版社,2000.195-196.
[5]李培武,等.苯磺酰氯的生产工艺探讨[J].化学中间体,2002,18(19):30-32.
Optimal synthesis progress of benzene sulfonyl chloride*
WANG Qi1,XU Yuan-ping1,2,HUANG Hong-ying1
(1.College of Chemistry and Environmental Engineeing,Jiangsu Teachers′University,Changzhou 213001,China;
2.College of Chemistry and Chemical Engineering,Jiangsu University of Technology,Changzhou 213164,China)
TQ247.5
A
1002-1124(2011)03-0001-03
2010-12-28
江苏省高校科研成果产业化推进项目(JH09-16);江苏技术师范学院科研基金项目(KYY08018);江苏省贵金属深加工技术及其应用重点建设实验室开放课题(SYGK0711)
王 琪(1966-),女,硕士,山西太原人,副教授,主要从事精细化工产品研发和分析合作。

