初治涂阳肺结核患者服用固定剂量复合制剂与板式组合药的疗效比较
张斯钰 白丽琼 谭红专 唐益 谭振 肖涛 范江静 龚德华 万燕萍
结核病是严重危害人类健康的慢性传染病。直接面视下短程化疗(directly observed treatment strategy,DOTS)是世界卫生组织(WHO)向全球推行的治愈结核病患者和控制结核病流行的最有效策略,联合应用多种药物对结核病患者进行有效的短程化疗是现代结核病控制的首要技术措施。为了成功实施DOTS,WHO和国际防痨和肺部疾病联合委员会(the Union)一致推荐将固定剂量复合剂(fixeddose combination,FDC)代替单药制剂作为治疗结核病的基本药物[1]。目前,全球已有10多个结核病高负担国家采用了利福平、异烟肼(RH)二联FDC和(或)利福平、异烟肼、吡嗪酰胺(RHZ)三联FDC[2]。为探讨FDC在湖南省结核病防治规划中推广应用的可行性,本研究从细菌学和影像学两方面比较FDC与板式组合药对初治涂阳肺结核的疗效。
对象和方法
一、样本含量的估计
采取非连续变量样本估计方法,以严重不良反应停药率(P1)为6%估算,干预后停药率(P2)为 2%计算。根据 N=/(P1-P2)2(α=0.05,β=0.10,单侧检验,Zα=1.64,Zβ=1.28),得 N=407。
二、研究对象的纳入和分组
本研究选取湖南省湘潭县、宁乡县、平江县和益阳赫山区4所结核病防治机构为研究现场,在获得知情同意的情况下,以2008年6月至2009年4月连续确诊、登记且年龄在15~70岁的初治涂阳肺结核患者为研究对象。初治涂阳肺结核病例的诊断标准按照《中国结核病防治规划实施工作指南》执行。排除以下病例:(1)对药物过敏者;(2)心、肝、肾功能不全者;(3)有严重胃肠疾病者;(4)体质量低于30 kg者;(5)有精神疾患者;(6)聋哑和智力障碍者;(7)孕妇。
各研究现场利用随机数字表,分别将纳入的病例随机分配到FDC组和对照组。
本研究实际纳入534例初治涂阳肺结核患者,其中FDC组269例,对照组265例。
三、研究方法
(一)治疗方案
FDC组的治疗方案为2HRZE/4HR,采用浙江南洋药业有限公司生产的FDC,其中 H RZ为异福酰胺胶囊 ,每粒含 R 120mg、H 80mg、Z 250 mg(批号080101),E为上海医药(集团)有限公司信谊制药总厂生产的乙胺丁醇片,每片含量250 mg(批号071202);HR为异福胶囊,每粒含 R 150 mg、H 75 mg(批号 070901)。对照组的治疗方案为2H3R3Z3E3/4H3R3,强化期每板含 R:0.3 g×2片,H :0.3×2片,E:0.25 g×5片,Z:0.5 g×4片;继续期每板含 R:0.3 g×2片,H :0.3 g×2片。
(二)疗效判定
沿用1982年中华医学会结核病学分会修订的标准,评定不同阶段的X线胸片肺部病变情况,包括病灶[显著吸收(简称“显吸”)、吸收、不变和恶化] 和空洞(闭合、缩小、不变和增大)[3]。
四、统计学处理
采用Epidata 3.0建立数据库,采用SPSS 13.0进行资料分析,具体如下:疗效指标(如痰菌转阴率、治愈率等)的比较先用传统统计学检验分析其统计有效性,如果差异有统计学意义,则进一步用优效性检验,如果差异无统计学意义,则进一步用非劣效性检验[4];构成比的比较用卡方检验;等级资料用非参数检验。以P<0.05为有统计学意义。
结 果
一、可比性分析
FDC组和对照组的患者在性别、年龄、文化程度、职业、经济状况、医疗保险、BMI水平、病情等方面的差异均无统计学意义,提示2组对象有良好的可比性,详见表1。
二、疗效比较
(一)细菌学
2个月末,FDC组和对照组痰菌转阴数分别为257例(95.54%)和 246例(92.83%);疗程末,2组痰菌转阴数分别为 259例(96.28%)和 247例(93.21%)。统计学检验表明,FDC组和对照组在2个月末和疗程末的痰菌转阴率差异无统计学意义。非劣效性检验则表明,FDC组在2个月末和疗程末的痰菌转阴率均不劣于对照组(表2)。
(二)影像学
疗程结束时,FDC组的病灶显吸和吸收人数分别为111例和 122例,对照组分别为97例和124例,2组均没有出现病灶恶化的表现(表3)。非参数检验(Mann-Whitney U test)结果表明,2组患者病灶变化的差异无统计学意义(Z=-0.526,P>0.05)。FDC组和对照组的病灶吸收率分别为86.62%(233/269)和 83.40%(221/265)。χ2检验表明,2组病灶吸收率差异无统计学意义(χ2=1.087,P>0.05);非劣效性检验则表明,FDC组的病灶吸收率不劣于对照组(u=2.662,P<0.01)。
疗程结束时,FDC组的空洞闭合和缩小人数分别为21例和27例,对照组分别为13例和15例,2组均没有出现空洞增大的表现(表3)。非参数检验(Mann-Whitney U test)结果表明,2组患者空洞变化的差异无统计学意义(Z=-0.864,P>0.05)。FDC组和对照组的空洞缩小率分别为87.27%(48/55)和63.64%(28/44)。χ2检验和优效性检验均表明,FDC组的空洞缩小率高于对照组(统计学检验χ2=7.657,P<0.01;优效性检验u=2.770,P<0.01)。

表1 FDC组与对照组患者的一般情况比较
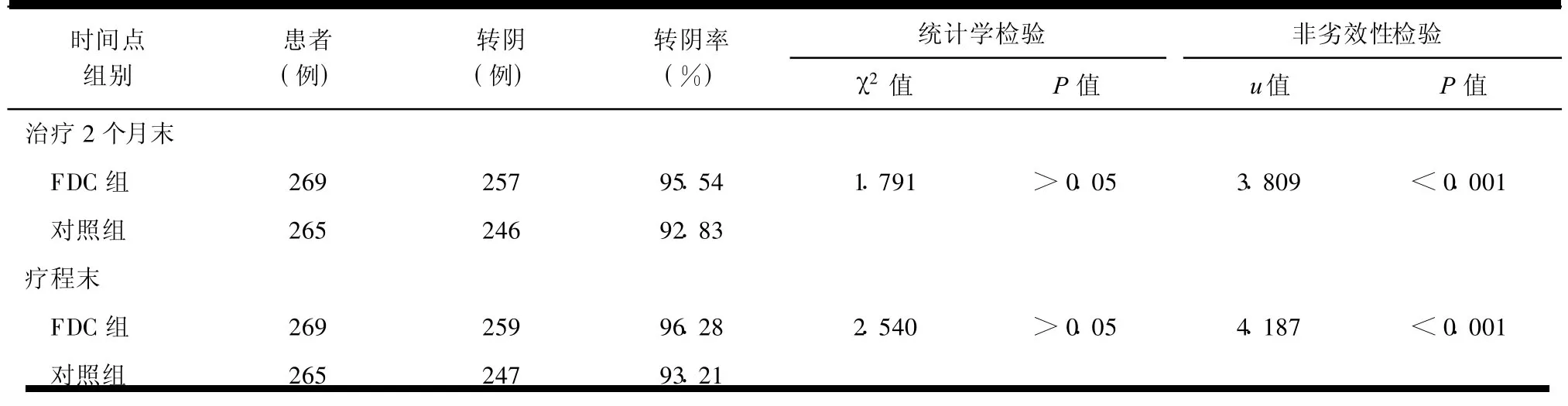
表2 两组患者2个月末、疗程末痰菌转阴情况

表3 2组患者疗程末病灶吸收情况(例)
讨 论
肺结核病化疗目的是杀灭病灶内的结核分枝杆菌,敏感病例经正规合理的化疗均有良好的疗效,而病灶则在痰菌消失后才逐步消失,且与病灶范围关系不大。因此,痰菌转阴率是评价疗效的最有效的指标,其中强化期(2个月末)痰菌转阴率可反映痰菌转阴的速度,疗程末的痰菌转阴率则表示化疗的近期疗效[3]。
本研究中FDC组和对照组的2个月末痰菌转阴率分别为 95.54%和 92.83%,治愈率分别为96.28%和93.21%,2组均未出现初治失败的病例。统计学检验表明FDC组2个月末痰菌转阴率和治愈率与对照组相比,差异均无统计学意义,非劣效性检验则表明FDC组2个月末痰菌转阴率和治愈率均不劣于对照组。因此,可以认为FDC和板式组合药对初治涂阳肺结核的疗效一样。与王健等[5-7]的研究结果一致,但是赵梅桂等[8-9]开展的社区对照试验却表明FDC组治愈率高于对照组。可能是由于以社区为基础的对照研究中,各社区间患者体质和结防人员业务能力等方面的差异均可导致疗效的差异,而研究者可能将这一差异误以为是药物引起的。与之相比,本研究在多个项目县(区)开展临床随机对照试验所得到的结果更具有外推性。因此,认为FDC与板式组合药对治疗初治涂阳肺结核是等效的,且痰菌转阴的速度没有差别。
FDC是多种抗结核药物的物理组合,各组成药物的分子结构并未发生改变。强化期联合使用异烟肼、利福平、吡嗪酰胺和乙胺丁醇可以尽快地杀死繁殖期菌群,使菌量急剧减少;继续期联合使用异烟肼、利福平则主要针对残留的少数代谢低下或半静止状态的结核分枝杆菌。有研究表明,2种药复合和3种药复合及其制剂在体内外均具有显著抗结核作用,并明显优于各配方中相应药物单独应用时的作用[10]。使用FDC制剂可以简化处方和服药,提高患者的服药依从性,有利于患者规律用药[11]。因此,国产FDC适合在湖南省结核病控制项目中推广使用。
[1] IUAT LD/WHO.The promise and reality of fixed-dose combinations with rifampicin.A joint statement of the International Union Against Tuberculosis and Lung Disease and the T uberculosis Prog ramme of the World Health Organization.T ubercle Lung Dis,1994,75:180-181.
[2] Norval PY,blomberg B,Kiter M E,et al.Estimate of the global market for rifampicin containing fixed-dose combination tablets.International Tuberculosis Lung Disease,1999,11,(3):S292-300.
[3] 马玙,朱莉贞,潘毓萱.结核病.北京:人民卫生出版社,2006.595-596.
[4] 谭红专.现代流行病学.2版.北京:人民卫生出版社,2008.217-218.
[5] 王健,赵锦,钟涛.国产固定剂量复合剂与板式组合药治疗肺结核临床近期效果评价.现代预防医学,2007,34(13):2590-2595.
[6] 谭卫国,杨应周,吴清芳,等.抗结核固定剂量复合剂与板式组合药治疗肺结核效果对比分析.中国防痨杂志,2007,29(2):117-121.
[7] 黄诚.抗结核固定剂量复合剂治疗肺结核疗效观察.江苏预防医学,2005,16(3):31-33.
[8] 赵梅桂,赵安贵,龙卫军,等.国产固定复合制剂肺宁/肺安治疗肺结核近期临床分析.实用预防医学,2006,13(4):874-875.
[9] 吴清芳,严薇荣,谭卫国,等.抗结核固定复合制剂与板式组合药化疗及管理的对照研究.中国医药卫生,2005,6(16):1-4.
[10] 李惠文,梁桂芳,赵伟杰,等.抗结核固定剂量复合制剂的抗结核活性研究.中国防痨杂志,2007,29(5):423-428.
[11] 张斯钰,白丽琼,谭红专,等.M orisky服药依从性量表在肺结核患者中的应用.中国防痨杂志,2010,32(9):527-530.

