吉非替尼致急性肺损伤
——附1例报道
倪莲芳 刘新民 高莉
吉非替尼是一种口服的表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor, EGFR-TKI),能与三磷酸腺苷(adenosine triphosphate, ATP)竞争酪氨酸激酶结构域中的ATP结合位点,抑制其磷酸化,从而阻断肿瘤细胞信号传导通路,抑制肿瘤细胞的生长、转移。作为第一个用于晚期非小细胞肺癌(non-small cell lung cancer, NSCLC)治疗的分子靶向药物,吉非替尼在亚裔、女性、非吸烟、腺癌等优势人群中的作用已经多个国际多中心临床试验证实。因其应用方便,副作用相对较小,对优势人群尤其是EGFR基因突变人群的有效率高,得到广大医生和NSCLC患者的认可。然而,随着临床的广泛应用,吉非替尼少见但极其严重的副作用急性肺损伤(acute lung injury, ALI)逐渐引起关注。现报道1例应用吉非替尼出现ALI的病例,以提高临床医生的认识。
1 临床资料
患者,男性,76岁,主诉发现肺部阴影2个月于2009年8月入院。2个月前患者因活动后气短于外院查CT肺血管成像(CT pulmonary angiography, CTPA)时发现左上肺团块影,1个月前查PET-CT提示左肺上叶尖段高代谢活性结节,考虑恶性病变。1个月前开始出现低热、四肢水肿症状,4年来体重下降15 kg。病程中无盗汗、胸痛、咯血症状,无宠物、鸟类接触史。既往:慢性阻塞性肺病史20余年,吸烟40余年,20支/天。入院体检:T 38oC,P 92次/分,R 18次/分,BP 120/60 mmHg。神志清,浅表淋巴结未及肿大,颈静脉怒张,桶状胸,双侧语颤减弱,左下肺叩诊浊音,左下肺呼吸音低,双肺未闻及明显干、湿啰音,心界不大,心律齐,各瓣膜听诊区未闻及杂音。腹部查体无异常,四肢可凹性水肿,双侧对称。可见杵状指。
入院后给予抗感染治疗,查血常规:WBC 6.01×109/L,NE 76.2%,HGB 104 g/L,PLT 272×109/L。尿便常规正常。肝肾功能无明显异常,ESR 66 mm/h,动脉血气(FiO221%)PH7.484,PCO234 mmHg,PO268.2 mmHg。胸部增强CT(图1A,图1B):左肺上叶尖后段不规则软组织密度占位,大小约4.8 cm ×4.5 cm×4.9 cm,病灶浅分叶,边缘不规则,与胸膜宽基底相连,平扫Ct值36 Hu,增强及延迟后Ct值71 Hu、70 Hu,强化不均匀,伴远段阻塞性肺炎,考虑周围型肺癌可能大;双肺慢支肺气肿改变,左下胸膜增厚,左侧少量胸腔积液。行CT引导下经皮肺穿刺,肺活检病理报告:左肺上叶穿刺少许肺组织,其内可见中分化腺癌浸润。全身浅表淋巴结B超示双侧腹股沟多发肿大淋巴结,呈靶环状。骨扫描:四肢长骨皮质血运丰富,代谢旺盛灶,结合临床符合肺性骨病表现,考虑肿瘤分期Ib期,T2aN0M0。肺功能:通气功能严重减退属阻塞型障碍,FEV1 46%,FEV1/FVC 42.46%,弥散功能严重减退,TLCO占预计值26.9%,TLCO/VA占预计值32.8%。心脏彩超:左心室整体收缩功能正常,LVEF>50%(simpson法)。
经积极抗感染治疗后,患者体温正常,喘憋有所好转,但一般情况差,肺功能严重减退,围手术期风险大,家属不同意手术治疗。患者体能状态评分(performance status, PS)3分,化疗耐受性差,获益可能性小,与患者家属商议后同意行靶向药物治疗(因活检肺组织少,未行EGFR基因突变检测)。患者于9月11日(图2A)始予吉非替尼(易瑞沙)250 mg/d口服。9月15日出现高热、喘憋,体温38oC-39.4oC,血气(FiO221%)PH7.48,PCO230.8 mmHg,PO257.9 mmHg。9月17日血常规:WBC 11.27×109/L,NE 82.6%,HB 104 g/L,PLT 258×109/L,胸片(图2B)示右上肺大片渗出,考虑不排除感染。予哌拉西林舒巴坦(一君)(9月17日-9月22日)抗感染无效,改用美罗培南(美平)(9月22日开始)联合替考拉宁(他格施)(9月24日开始)抗感染治疗,病情无明显好转。9月23日肺CT(图1C,图1D)示左上叶软组织肿块较前增大,右肺上叶间质病变伴渗出。痰培养阴性,降钙素原阴性,真菌G、G-M试验阴性,考虑不除外易瑞沙致急性肺损伤。于9月23日停用易瑞沙,继续抗感染治疗。因患者一般情况差,患者及家属不同意行气管镜检查以明确病因。9月27日胸片(图2C)示右肺上叶后段大片状影,提示病变仍进展,遂予甲基强的松龙80 mg/d静滴。次日体温正常,右肺啰音减少,动脉血气(FiO221%)PH7.471,PCO237.7 mmHg,PO263.5 mmHg。9月30日胸片(图2D)示右上叶后段大片状影明显吸收并密度减低,1周后(10月4日)改为强的松龙40 mg/d口服,每周减量5 mg,胸片提示右上叶后段大片状影基本吸收。
2 讨论
NSCLC约占肺癌总数的80%,由于缺乏有效的早期诊断方法,70%-80%的肺癌患者就诊时已为晚期,失去根治性手术切除机会。而针对晚期NSCLC,化疗新药的疗效似已达到平台期。分子靶向药物的出现为肺癌的治疗带来了新的希望和手段,以吉非替尼(易瑞沙)和厄罗替尼(特罗凯)为代表的TKI是目前被多国批准并被广泛应用于进展或难治性NSCLC的小分子靶向药物。事实上,对于不能耐受手术、放化疗的老年肺癌患者,靶向治疗常是适用的抗肿瘤方案。
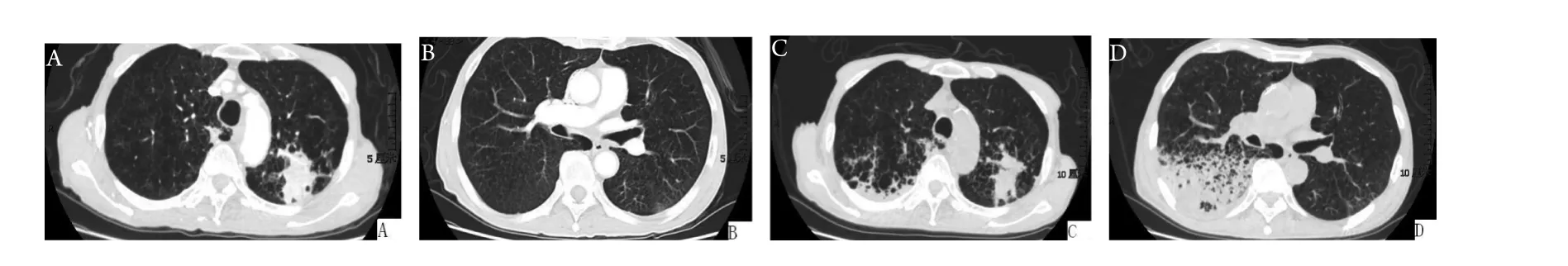
图1 应用吉非替尼前后肺CT变化。A和B:吉非替尼治疗前,左肺上叶尖后段不规则软组织占位;C和D:吉非替尼治疗后,右肺上叶间质病变伴渗出。Fig 1 Chest CT scan results comparison before and after gefitinib therapy. A and B: before gefitinib therapy; C and D:after gefitinib therapy.
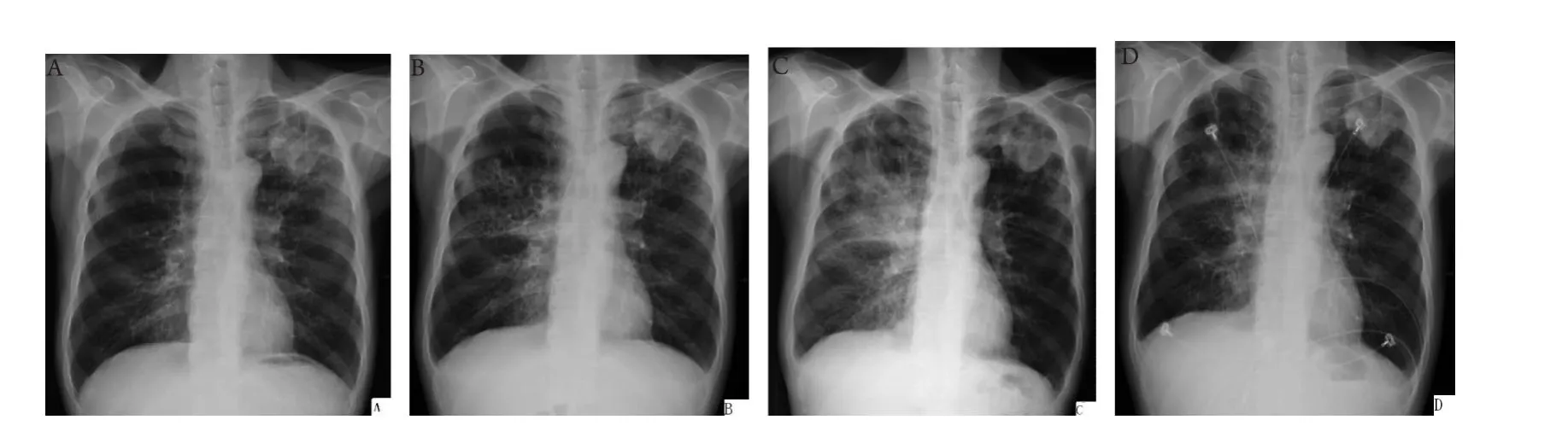
图2 用吉非替尼前后及用激素前后胸片变化。A:吉非替尼治疗前,左上肺团块影;B和C:吉非替尼治疗后,右上肺渗出;D:糖皮质激素治疗后,右上肺渗出明显吸收。Fig 2 Chest X-ray results comparison before and after gefitinib or glucocorticoids therapy. A: before gefitinib therapy; B and C: after gefitinib therapy; D: after glucocorticoids therapy.
吉非替尼于2002年首先在日本上市,2005年在中国上市,获批用于治疗既往接受过化疗的局部晚期或转移性NSCLC。最常见的不良反应为腹泻、皮疹、瘙痒、皮肤干燥和痤疮,一般发生于服药后1个月内,通常是可逆的[1]。随着临床的广泛应用,吉非替尼导致的肺损伤逐渐引起关注。日本学者Okamoto等[2]报道了首例因服用吉非替尼而导致严重间质性肺炎死亡的病例。患者给药8天后即出现呼吸困难,尽管给予大剂量类固醇激素治疗,仍然在给药13天后死亡。在日本吉非替尼引发间质性肺病(interstitial lung disease, ILD)的发生率较高,文献[3]报道发生率为3.2%-5.8%。在美国,接受吉非替尼治疗的患者ILD的发生率约为1%[4]。国内对于吉非替尼引发的ILD仅有个案报道,没有发病率的统计[5]。吉非替尼引发的ILD一旦发生,危险性大、死亡率高。文献[3]报道日本吉非替尼引发ILD的死亡率在30%-60%。
吉非替尼导致ALI的机制尚不明确。有专家[6]推测是因为对EGFR的抑制作用妨碍了肺部损伤的正常修复,从而加重了肺部损伤,并使免疫炎症反应失控,导致ALI的发生。也有报道[7]认为氧化应激参与了间质病的发生,研究发现吉非替尼引起的ILD患者血清中硫氧还蛋白水平增高,但具体机制还有待进一步研究。多项研究进行的多因素分析提示男性、既往有肺纤维化、PS评分差、有放疗史是ALI发生的独立影响因素[3],这可以为临床制定治疗决策提供一些参考。
吉非替尼引起的ALI的临床表现与其它急性肺损伤类似。一般在用药后4周内出现,表现为活动后气短、干咳,伴或不伴发热,停药后病情仍可进展。影像学表现为弥漫性间质病变或磨玻璃样改变。病理提示弥漫性肺泡损伤,肺泡上皮肿胀,肺泡间隔增厚,伴淋巴细胞、中性粒细胞、嗜酸性粒细胞浸润,伴或不伴透明膜形成。病原学检查阴性。血清学上可有LDH、KL-6、SP-D、SP-A升高。吉非替尼引起的ALI的治疗首先是停药,一般需要应用糖皮质激素,文献报道[8]一般用甲基强的松龙静脉点滴1 g/d,连续应用3天,继以强的松龙60 mg/d口服,每周减量10 mg,直至减停。一般数日内症状缓解,血气、影像学可以得到改善,表现为嗜酸细胞性肺炎者停药后即可好转[9]。本文病例在出现肺损伤给予停药后病情仍进展,给予甲基强的松龙静脉点滴80 mg/d,连续应用1周后影像学明显好转。可见,在激素的用量上可根据临床情况确定,以减少大量激素所带来的副作用。
对于很多晚期NSCLC患者,尤其是放化疗不能耐受或失效者,靶向治疗可能是唯一的抗肿瘤治疗方案,即使出现了严重的副作用,在对症处理好转后,仍存在进一步抗肿瘤治疗的问题。关于肺损伤后的再次用药,文献报道不多。Takamochi等[10]报道了1例56岁男性,肺腺癌IIIb期,吸烟,术后辅助化疗(卡铂+紫杉醇)2周期,17个月后出现全身(肺、骨、脑)转移,改用吉非替尼250 mg/d+全脑照射,14天后影像学提示肿瘤明显好转。但用药至45天,患者出现乏力、气短,影像学提示间质性肺浸润,考虑吉非替尼导致的ILD,予停药,并用甲基强的松龙1 g/d静滴,连续3天,后改为50 mg/d,每周减10 mg,1月后ILD好转。停药5月后肿瘤进展,再次用吉非替尼125 mg/d治疗仍有效,未再出现ILD。而Suzuki等[11]则报道1例再次用药后出现更严重ILD的病例。患者为59岁男性,肺腺癌IV期,吸烟,PS为1分,卡铂+紫杉醇一线化疗失败,改用吉非替尼250 mg/d二线治疗,用药后恶性胸水及血CEA均有改善,但23天后出现高热、气短,影像学提示ILD,停药并使用甲基强的松龙后ILD好转。但1月后肿瘤进展,再次用吉非替尼250 mg/d治疗,连用1周,歇2周,仍有效,第3个循环时再次出现ILD,且较前更重,但激素治疗仍有效。如何预测是否会再出现ILD,目前尚不清楚,需要有更多的临床观察来得出更进一步的结论。因此,笔者认为,当病情需要再次用药的时候,须充分与患者及家属交代再次发生ILD的可能性,否则应避免再次应用。
综上所述,吉非替尼引起的ALI一旦发生,往往较凶险,病死率高,应引起广大临床医生的重视。对于门诊处方吉非替尼,则应充分向患者交代风险,一旦出现相关呼吸系统症状,立即就医,及时行影像学检查,以期早期发现、诊断和及时处理,以减少死亡率。

