贲门癌合并2型糖尿病行Roux-en-Y手术治疗前后血糖变化的临床观察
于金海
早在二十世纪五十年代,欧美国家开始应用胃转流手术(Gastric Bypass,GBP)治疗病理性肥胖症[1],意外发现,肥胖合并2型糖尿病患者的血糖得到较好控制,约83%的患者血糖水平可以恢复正常[2],随着认识的深入及手术技术的进步,应用各种转流术治疗2型糖尿病已逐渐被国内外研究者接受,并应用于临床。吉林大学第一医院胃肠外科于2004年1月至2008年12月,共应用根治性全胃切除、Roux-en-Y吻合治疗贲门癌合并2型糖尿病患者32例,现将术前术后血糖及相关指标变化情况报告如下。
1 资料与方法
1.1 一般资料 本组患者32例,男25例,女7例,年龄43~72岁,平均55.8岁。所有患者均明确诊断为贲门癌合并2型糖尿病,患糖尿病时间0.5~9年,平均5.9年,BMI 22.6~28.2 kg/m2,平均24.3 kg/m2;合并脂肪肝10例,高血脂12例,高尿酸血症5例;在控制血糖所采取的措施中,单纯控制饮食,增加运动者5例;口服降糖药者10例,应用皮下注射胰岛素者17例,本组患者术前均给予胰岛素控制血糖,将空腹血糖控制在8 mmol/L以下,再行手术。
1.2 手术方法 本组患者均采用气管插管全麻,取上腹正中切口,根治性全胃切除按标准D2手术进行:全胃切除,清扫1、2、3、4、5、6、7、8、9、10、11、12 组淋巴结;术后消化道重建按Roux-en-Y方式吻合,应用强生直径25 mm圆型吻合器行食管空肠吻合,Roux袢40 cm,Y袢40 cm,吻合后缝闭肠系膜裂孔,结束手术。
1.3 术后营养支持与随访情况 本组患者术中均留置肠内营养管,置入空肠端侧吻合口以下20 cm,术后第1天给予全量静脉营养同时经鼻肠管给予葡萄糖氯化钠溶液500 ml,从第2天起减少静脉营养,增加肠内营养,至第3~4天应全量肠内养,应用胰岛素泵控制血糖在8~10 mmol/L,酌情掌握进食时间;血糖随访2年,测定术后不同时间的体重,BMI,空腹血糖,口服糖酌量试验,C肽,糖化血蛋白,胰岛功能,胰岛素抵抗指数(HOMA-ZR)=胰岛素水平(mU/L)空腹血糖(mmol/L)/22.5,合并症改善情况。
1.4 统计学方法 应用SPSS 10.0统计软件分析所有数据,所有数据均以±s,表示手术前后各项指标的比较采用配对t检查。
2 结果
2.1 术后恢复情况及并发症 本组32例患者,均行根治性全胃切除,Roux-en-Y吻合,手术时间130~240 min,平均155 min,术中失血量20~65(平均30.5)ml;术后进食时间5~9(平均6.2)d;术后住院时间7~21(平均8.5)d。术后1例患者出现食道空肠吻合口瘘,后经肠内营养支持于术后21 d全愈合,1例患者出现十二指肠列端瘘,经充分引流于术后14 d完全愈合,2例出现切口感染,经换药后,术后10 d完全愈合;出院后均恢复正常饮食,饮食量明显减少,约为原来的1/4~1/2,术后平均2周均正常生活工作。定期复查血常规,生化等项目均正常,未见贫血及营养不良。
2.2 术前、术后糖尿病相关化验指标对比 术后7 d开始,所有患者的降糖药物及胰岛素用量全部减少,至术后3个月,所有患者均停用降糖药物及胰岛素,血糖稳定,并逐渐下降至正常。
术后不同时间,所有患者的空腹血糖,餐后血糖,C肽,糖化血红蛋白,胰岛功能,胰岛素抵抗指数,均较术前明显改善,而BMI较术前无明显变化(详见表1)。
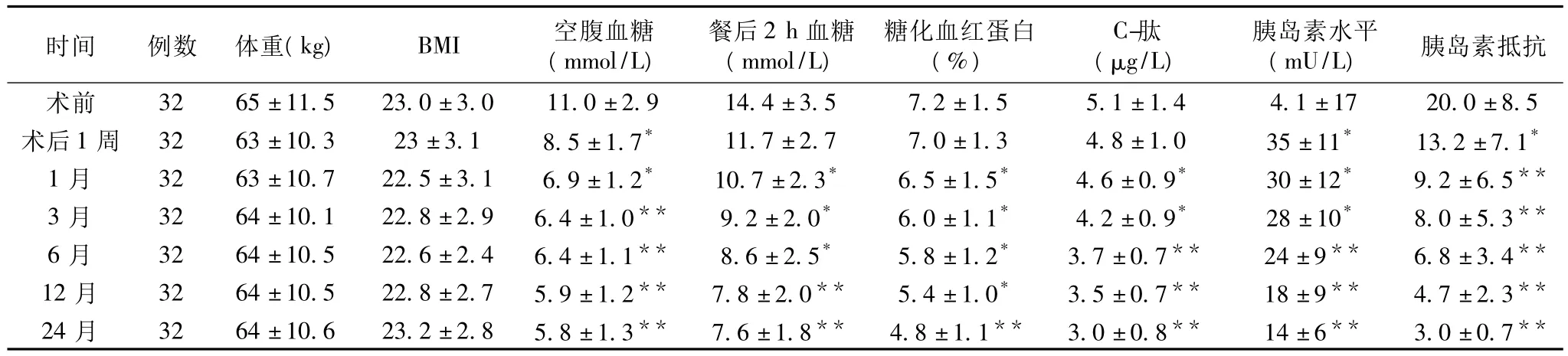
表1 2型糖尿病相关指标的变化
3 讨论
二十世纪中期,欧美等国家在对减肥手术进行术后随访、观察时发现,肥胖合并2型糖尿病的患者,术后早期血糖已开始下降[3],这种发现鼓励了外科医生进行更为系统的研究。国外学者通过大样本分析肥胖合并2型糖尿病的患者行不同减肥手术后的长期随访资料后,发现胃转流手术(GBP)各胆胰转流术(Biliopancreatic diversion,BPD)对并存的2型糖尿病治愈率达83% ~86%[4];而非转流的其他减肥手术,如可调节捆扎带胃缩小减容术,袖状胃切除术等,却达不到明显的治疗2型糖尿病的效果[5]。我国目前正在进行的多中心,大样本的RCT研究-胃癌合并2型糖尿病,行胃癌根治手术,不同消化道重建方式对患者术后血糖的影响,也已初步得出结论,即行毕II式和Roux-en-Y重建的患者,术后血糖明显降低或恢复正常,降糖药或胰岛素用量明显减少或已停用,而行毕I式重建的患者,术后血糖与术前比较无明显改变。上述所观察到的情况,与本研究所得出的结论是一致的。本研究经过2年的系统随访,观察到2型糖尿病患者,行Roux-en-Y消化道重建后,空腹血糖均恢复正常,术后胰岛素及降糖药均已停用,糖化血红蛋白术后也降至正常水平,胰岛素抵抗明显减轻。
2型糖尿病占糖尿病总数约85% ~90%,国内外的发病率逐年增加,全世界该疾病的患者已超过1.6亿[6],其并发症致残致死率高,严重危胁患者的生命、健康。传统观念认为,2型糖尿病系为内科疾病,治疗方法包括控制饮食,加强运动,口服降糖药,使用胰岛素等,但上述方法仅起到控制血糖的作用,不能使血糖永久恢复至正常水平[7]。基于前述的观察结果,国内外许多医疗机构试行开展了胃转流手术治疗2型糖尿病,治疗效果大多数较为理想。
研究认为2型糖尿病的发病机制之一在于“胰岛素抵抗”,即胰腺β细胞过度分泌导致疲劳,功能低下,或对血糖调节机制的反应迟钝,不能产生满足代谢需要的胰岛素,亦即胰岛素的产生量相对不足,形成高血糖状态,对β细胞造成经常性的或连续性的刺激,导致高胰岛素血症,久之诱使胰岛素靶器官、组织,如肝脏,肌肉,脂肪组织等的受体作用下调,胰岛素作用减弱,即形成胰岛素抵抗的血糖升高[8]。转流手术前,糖尿病患者的上消化道经食物刺激产生“胰岛素拮抗因子”,如十二指肠和空肠上段K细胞产生的抑胃肽(GIP),可刺激胰岛素的合成和释放,使胰岛素敏感性下降,从而形成胰岛素抵抗[9],行胃转流手术后,食物不再流经十二指肠及近端空肠,直接近入空肠远端,较早进入回肠,刺激回肠产生胰高血糖素样肽-1(Glucagon-Like Peptide-1,GLP-1),YY肽(PeptideYY,PYY)等,该类激素可促进胰岛素发挥作用,加速糖原合成及脂肪分解,抑制胃排空,产生胞胀感,增加胰岛素基因表达和胰岛素前体的合成,促进β细胞增殖、抑制其凋亡,进而达到降低改善胰岛素抵抗的作用[10,11]。
本项研究中,行根治性全胃切除,Roux-en-Y消化道重建,矿置了十二指肠及近段空肠,完全起到食物转流的作用,从而在根治胃癌的同时,也达到了治疗糖尿病的目的。但本研究缺乏对胃肠道相关激素水平的测定,在以后的临床观察及实验中,应进一步改善,以更好地阐述降糖机制。
[1]Scheen AJ.Treat of diabetes in patients with severe obesity.Biomed & Pharmactother,2000,54:74-79.
[2]Spivak H,Hewitt MF,Onn A,et al.Weight loss and improvement of obesity-related illness in 500 U.S.patients following laparoscopic adjustable gastric banding procedure.Am J Surg,2005,189:27-32.
[3]Huerta S,Kohan D,siddiqui A,et al.Assessment of comorbid conditions in veteran patient after Roux-en-Y gastric bypass.Am J Surg,2007,194:48-52.
[4]Polyzogopoulou EV,Kalfarentzos F,Vagenakis AG,et al.Restoration of euglycemia and normal acute insulin response to glucose in obese subjects with type 2 diabetes following bariatric surgery.Diabetes,2003,52:1098-103.
[5]Pories WJ,Swanson MS,Macdonald KG,et al.who would have thought it?An operation proves to be the most effective therapy for adult-onset diabetes mellitus.Ann Surg,1995,222:339-50.
[6]Rubino F,Gagner M,Gentileschi P,et al.The early effect of the Roux-en-Y gastric bypass on hormones involved in body weight regulation and glucose metabolism. Ann Surg,2004,240(2):236-242.
[7]Rubino F,Marescaux J.Effect of duodenal-jejunal exclusion in a non-obese animal model of type 2 diabetes:a new perspective for an old disease.Ann Surg,2004,239(1):1-11.
[8]Rubino F,Forgione A,Cummings D,et al.The mechanism of diabetes control after gastrointestinal bypass surgery reveal a role of the proximal small intestine in the pathophysiology of type 2 diabetes.Ann Surg,2006,244(5):741-749.
[9]Clements RH,Gonzalez QH,Long CI,et al.Hormonal changes after Roux-en-Y gastric bypass for morbid obesity and the control of type 2 diabetes mellitus.Am Surg,2004,70(1):1-5.
[10]David p,Daniel AL,Alejandro R,et al.The effects of duodenaljejunal exclusion on hormonal regulation of glucose metabolism in Goto-Kakizaki rats.Am J Surg,2007,194(2):221-224.

