浓缩丹参骨宝颗粒中水溶性有效成分的质量控制研究
蒋桂香 ,吕应年 ,范世锦 ,仲丽萍 ,崔 燎
1.广东双林生物制药有限公司,湛江市生物制药工程中心,广东湛江 524005;2.广东医学院,广东天然药物研究与开发重点实验室,广东湛江 524023
丹参为唇形科鼠尾草植物的干燥根部,丹参的有效成分包含脂溶性的蒽醌类成分和水溶性的酚酸类成分[1]。丹参中的有效成分能增加冠脉血流量,降血脂,抑制血栓形成,改善微循环[2-3],临床常用于心血管疾病的治疗,如市售的复方丹参片、丹参滴丸等。现代药理学研究发现,丹参水溶性活性成分具有抗骨质疏松的作用[4],其中,丹参素可有效预防糖皮质激素引起的大鼠骨质疏松,丹参素可增加大鼠成骨细胞的碱性磷酸酶(ALP)和骨钙素含量,提高成骨细胞(osteoblast,OB)体外矿化能力,使骨保护蛋白基因表达增多,在促使骨髓基质干细胞向成骨细胞分化的同时,抑制其向脂肪细胞分化[5]。丹参酚酸B具有相似的作用[6]。在上述药理学研究的基础上,本课题组研究了丹参水溶性成分用于治疗糖皮质激素型骨质疏松的新方法,开发成功抗骨质疏松的中药新药——丹参骨宝,其主要成分为丹参水溶性成分丹酚酸B、丹参素等[7]。该制剂的质量控制方法尚未建立。本文采用TLC法鉴别丹参骨宝颗粒中的丹参药材,采用HPLC法同时测定其中的丹参素和丹酚酸B的含量,建立了一种准确的含量测定方法,可有效控制丹参骨宝颗粒中有效成分的含量。
1 仪器和试药
LC1200型高效液相色谱,包括四元泵、DAD检测器、在线脱气机、LC1200中文工作站(美国安捷伦科技有限公司);AE204型十万分之一分析天平(瑞士梅特勒公司);MILLI—Q超纯水制备仪(美国密理博科技公司);四用紫外分析仪(上海顾村仪器厂);GF254预制薄层硅胶板(青岛海洋化工厂分厂);甲醇为色谱纯,其他试剂均为分析纯。
丹参素对照品、丹参酚酸B对照品(购自中国药品生物制品检定所);丹参骨宝颗粒(本室自制,规格为每袋3.0 g,批号分别为 091011、091012、091013)。
2 方法与结果
2.1 性状
本品为棕黄色颗粒,有独特香气味,规格为每袋3.0 g。
2.2 薄层色谱鉴别
采用TLC法[8]进行薄层色谱的鉴别。取本品1 g,加75%甲醇20 m1,超声20 min,滤过,滤液浓缩定容至5 ml,作为供试品溶液;取丹酚酸B对照品,加75%甲醇制成每毫升含2 mg的溶液,作为对照品溶液;取不含丹参的空白颗粒样品,同法制成缺丹参的阴性对照溶液。按照《中国药典》2010年版薄层色谱法(附录ⅥB)试验,吸取上述三种溶液各5 μl,分别点于同一硅胶GF254薄层板上,以甲苯-三氯甲烷-乙酸乙酯-甲醇-甲酸(2.0∶3.0∶4.0∶0.5∶2.0)为展开剂,展开,取出,晾干,置紫外光灯(254 nm)下检视。供试品TLC色谱中,在与丹参酚酸B对照品相应的位置上,显相同颜色的斑点,阴性样品无干扰。见图1。
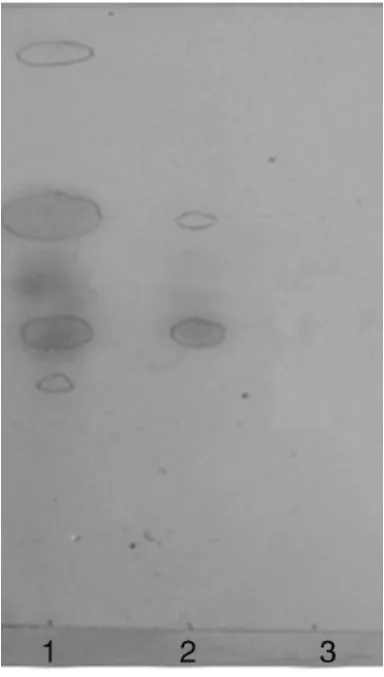
图1 供试品、丹酚酸B对照品、阴性对照溶液TLC色谱
2.3 含量测定
2.3.1 供试品溶液的制备 取研细的样品0.3 g,精密称定,加入20%甲醇25 ml,称重,超声10 min,放冷至室温,用流动相补足减失的重量,0.45 μm膜滤过,取续滤液,即得。
2.3.2 对照品溶液的制备 分别精密称取丹参素钠、丹酚酸B对照品适量,置于25 ml容量瓶中,用20%甲醇溶解并稀释至刻度,配制成浓度分别为152 μg/ml和292 μg/ml的对照品混合液。
2.3.3 色谱条件及系统适应性 色谱柱为Hypersil C18(4.6 mm×250 mm,5 μm);流动相为甲醇(A 相)-0.5%冰醋酸水溶液(V/V,B 相)进行线性梯度洗脱:0~9 min:10%A,9~20 min:10%A~60%A,20~30 min:60%A~10%A;检测波长为 281 nm;流速为1.0 ml/min;柱温为30℃。在上述色谱条件下,取对照品溶液、供试品溶液和阴性对照溶液各20 μl,分别进样,HPLC分析,记录色谱图。丹参素和丹参酚酸B的理论塔板数大于5000。试验结果表明,色谱系统适应性良好。阴性对照无显著色谱峰,表明空白溶剂不干扰样品的检测。见图2。
2.3.4 线性关系考察 精密量取对照品储备液0.2、0.4、0.8、1.0、1.2、1.6 ml,分别置于 10 ml量瓶中,加甲醇定容到刻度,摇匀即得系列浓度的对照品溶液。分别取配制好的各浓度对照品溶液20 μl,依次进样,记录峰面积积分值。以进样含量X(μg/ml)为横坐标,峰面积积分值Y为纵坐标,绘制标准曲线。经计算得丹参素的线性回归方程为Y=0.08452X+0.368(r=0.9996),丹参酚酸B的线性回归方程为Y=0.07857X+0.682(r=0.9998)。计算结果表明丹参素和丹参酚酸B分别在 3.0~24.0 μg/ml和 6.0~48.0 μg/ml范围内线性关系良好。
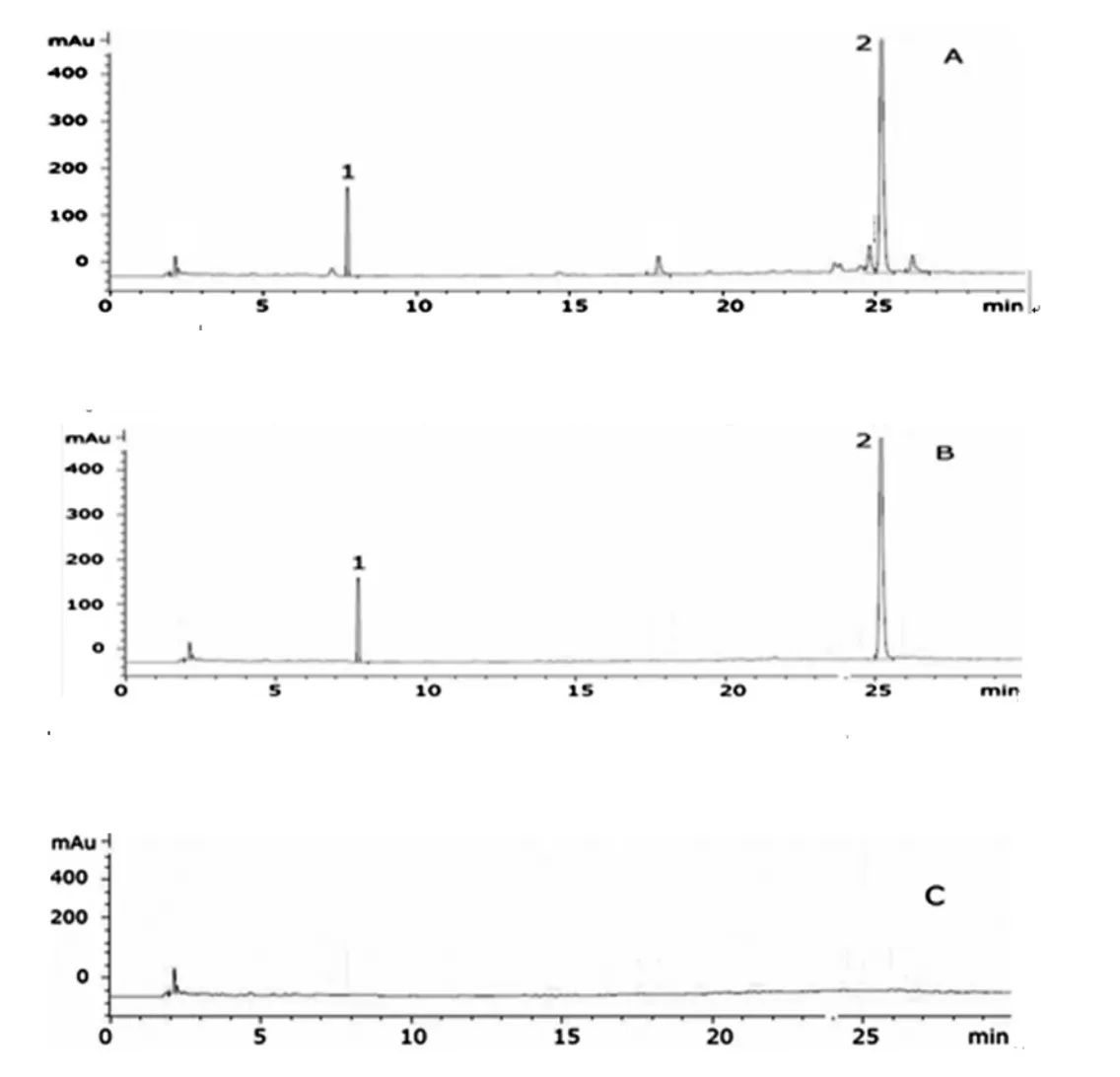
图2 供试品、对照品、阴性对照溶液高效液相色谱
2.3.5 精密度试验 精密吸取对照品溶液,按照上述色谱条件连续进样6次,每次进样量20 μl,以各药物成分峰面积计算RSD。计算得丹参素和丹参酚酸B的日内精密度RSD分别为1.20%和0.68%,表明试验方法精密度良好。
2.3.6 重复性试验 取同一批号的样品,按照供试品溶液配制方法,制备6份供试品溶液,按上述色谱条件进样分析,计算丹参素和丹参酚酸B的含量分别为0.26 μg/ml和5.63 μg/ml,RSD分别为1.60%和0.94%,表明该试验方法的重复性良好。
2.3.7 稳定性试验 取相同供试品溶液,分别在0、1、2、4、6 h进样测定丹参素和丹参酚酸B的峰面积,计算RSD。结果两种药物成分的RSD分别为1.30%和0.86%,表明供试品溶液在6 h内稳定。
2.3.8 加样回收率试验 精密称取已知含量的样品,配制成一定浓度的供试品溶液,分别加入丹参素和丹参酚酸B的对照品溶液,按上述色谱条件测定并计算回收率。见表1。
2.3.9 样品含量测定 取3个批号的样品,按照供试品溶液配制方法操作,进样20 μl,按色谱条件测定峰面积,外标法计算样品标示的百分含量。见表2。
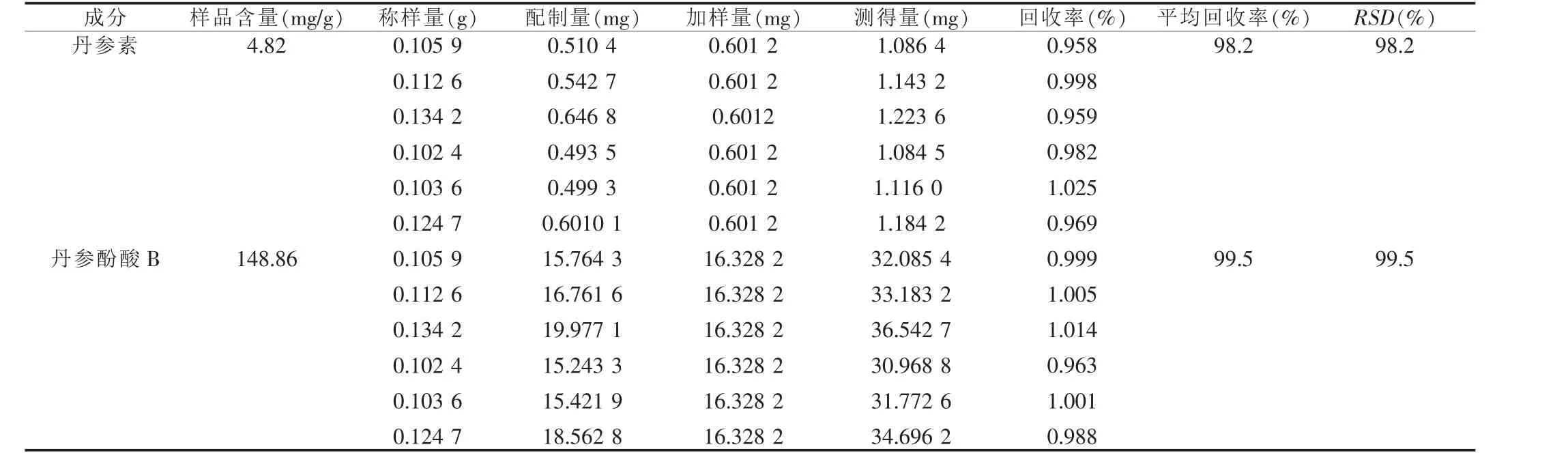
表1 加样回收率测定结果
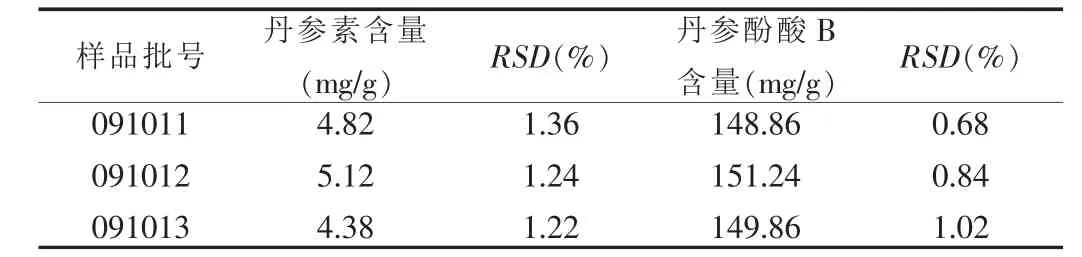
表2 样品含量测定结果(n=3)
3 讨论
在薄层色谱鉴别试验中,本文参照《中国药典》2010年版丹参的鉴别方法[8]进行。由于本品主要含丹参水溶性成分,不含丹参脂溶性成分(如丹参酮等),因此在此研究中将方法略作修改,药典中75%甲醇溶解改为20%甲醇,主要是增加水溶性成分的溶解度,提高测定的准确性。
在HPLC试验中,对药剂成分丹参素和丹参酚酸B做紫外光谱扫描发现,丹参素的最大吸收波长是281 nm,丹参酚酸B的最大吸收波长是286 nm。由于制剂中丹参素的含量较小,为提高准确性,选择测定波长为281 nm。结果表明在该条件下,两种有效成分的检测线性关系良好。
在HPLC试验中,由于样品物质丹参素和丹参酚酸B的化学结构中具有酸性羧基,在酸性流动相中色谱峰的对称性良好,峰形尖锐,有利于防止拖尾,经预试验在流动相中添加0.5%的冰醋酸能取得较好的峰形效果。
在本制剂中,丹参骨宝水溶性有效成分丹参素及丹参酚酸B的含量较高。丹参素是多羟基酚酸,在空气中加热易氧化,丹参酚酸B是由三分子的丹参素和一分子的咖啡酸结合而成,在有效成分提取、浓缩及制剂过程中,应严格控制各环节工艺参数,防止丹参酚酸B的分解以及丹参素的氧化,以保证制剂具有较高的水溶性活性成分含量。
[1]杜冠华,张均田.丹参现代研究概况与进展[J].医药导报,2004,23(7):355-359.
[2]肇毅,潘立勤.丹参促进创伤修复机制的研究现状[J].南京中医药大学学报,2000,16(4):253-254.
[3]张晓燕,吴铁,崔燎,等.丹参水提物对去卵巢大鼠牙槽骨骨量的影响[J].中成药,2007,29(2):268-270.
[4]Liao C,Yuyu L,Tie W.Osteogenic effects of D(+)β-3,4-dihydroxyphenyl lactic acid (salvianic acid A,SAA)on osteoblasts and bone marrow stromalcells ofintactand prednisone-treated rats [J].Acta Pharmacologica Sinica,2009,(30):321-332.
[5]邹丽宜,吴铁,崔燎.丹参抑制泼尼松大鼠骨质丢失[J].中成药,2006,28(4):537-539.
[6]孙宇,崔燎,吴铁.盐酸水提法制备丹参水溶性有效部位群及其对成骨细胞活性测定[J].中国药理学通报,2008,24(3):377-379.
[7]刘力名,吕应年,崔燎,等.正交设计-重复实验法优选丹参骨宝酸提取工艺的最佳条件[J].时珍国医国药,2010,21(2):282-283.
[8]国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010:255.

