MDEA-PZ复合胺溶液吸收烟气中CO2实验研究
,,, ,,,
(1.胜利油田勘察设计研究院有限公司,山东 东营 257026;2.青岛科技大学,山东 青岛 266042;3.中国石油大学(华东)化学工程学院,山东 东营 257061)
近年来,由于工业的急速发展和人口的迅猛增加,大气中CO2等温室气体的浓度远远超出自然生态系统所能承受的能力,产生了温室效应。CO2既是造成“温室效应”、导致地球气候变暖、破坏大气环境的主要污染物[1~3],同时又是一种重要的工业资源,广泛地应用于工业、农业、轻工、食品、医疗等领域,与人民生活密切相关[2~7]。随着能源的日益紧张和大气环境的恶化,富集并安全贮存燃料燃烧释放的CO2,将其作为“潜在的碳资源”加以开发利用,是一种迅速大量削减CO2排放量的有效手段[8]。
目前,化学吸收法已经成为烟气CO2回收的主要方法,尤其是烷基醇胺法脱除或回收CO2发展迅速[9]。工业上常用的烷基醇胺有乙醇胺(MEA)、二乙醇胺(DEA)、二异丙醇胺(DIPA)和N-甲基二乙醇胺(MDEA)等。其中MEA与CO2反应快,价廉易得,被广泛采用;MDEA具有较高的处理能力、较低的反应热和不腐蚀碳钢设备等优点,作为现代低能耗脱碳工艺而倍受重视,但因MDEA与CO2的反应速率较慢,其应用仍然受到限制[10]。因此,新型复合胺吸收液的筛选(复合胺法)又成为化学吸收法的研究热点[11]。
作者在此对MDEA-PZ复合胺溶液吸收烟气中CO2进行了实验研究,考察了相关因素对吸收效果的影响。
1 实验
1.1 试剂及仪器
MEA、DEA、MDEA、哌嗪(PZ)、Ca(OH)2,均为分析纯;医用蒸馏水。
转子流量计;智能电子皂膜流量计;单孔电热恒温水浴锅;氮气钢瓶;CO2钢瓶;雷磁PHS-3C型智能电子pH仪/电位(MV)仪。
1.2 方法
吸收实验装置见图1,再生实验装置见图2。
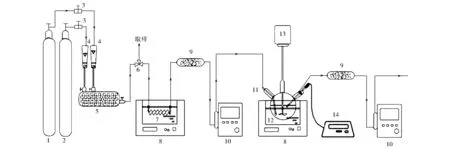
1.CO2钢瓶 2.N2钢瓶 3.气体阀门 4.气体流量计 5.气体混合缓冲瓶 6.三通阀 7.螺旋玻璃管 8.电热恒温水浴锅 9.气体干燥器 10.智能电子皂膜流量计 11.球形多孔反应探头 12.气液接触反应器 13.精密增力电动搅拌器 14.智能电子pH仪/电位仪
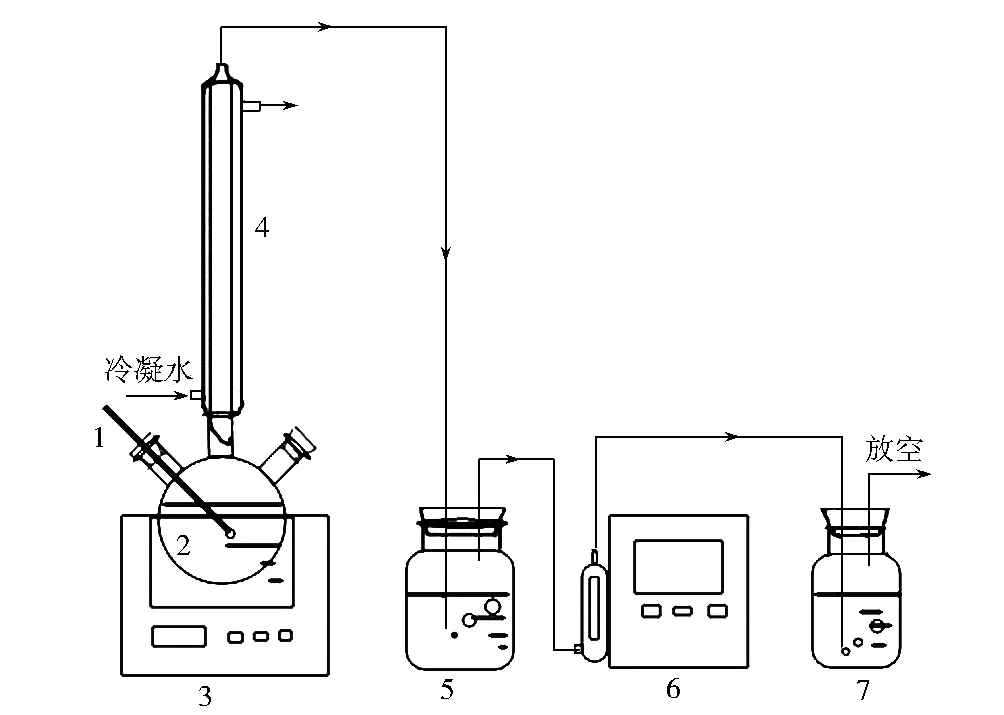
1.温度计 2.三口烧瓶 3.电热恒温油浴锅 4.冷凝管 5.浓硫酸洗气瓶 6.智能电子皂膜流量计 7.新制饱和氢氧化钙溶液
采用模拟烟道气(其中CO2体积分数为15%,N2体积分数为85%)进行吸收实验。打开CO2及N2减压阀,设定反应温度为40 ℃,用转子流量计和皂膜流量计对混合气进行标定,CO2和N2总流量稳定在4.33 mL·s-1。将球形多孔反应探头放入气液接触反应器(溶液体积为400 mL)中,同时开始计时,设定搅拌转速。每隔5 min记录一次数据(进出口气体流量、pH值、MV值)。当进气流量示数与出气流量示数低于5 mL·min-1时,反应达饱和,停止实验。
CO2吸收速率(每秒溶液吸收的CO2的物质的量)采用式(1)计算;用Matlab语言编程,计算测定的CO2吸收速率对时间的积分,得到CO2摩尔吸收容量。
n=PΔV/RT
(1)
式中:P为吸收系统内部压力,为常压,Pa;ΔV为皂膜流量计进口和出口示数之差,为被吸收的CO2体积,mL;n为吸收速率,mol·s-1;T为反应温度,℃;R为摩尔气体常数,8.314 J·K-1·mol-1。
吸收实验结束后,取下气液接触反应器,将其放入电热恒温油浴锅中,设定反应温度,进行CO2再生。利用皂膜流量计测定再生气产生速率,用饱和氢氧化钙溶液吸收再生气。当皂膜流量计测得的气体流量小于5 mL·min-1时,再生实验结束。再生实验中,富CO2吸收液通过加热再生解吸出CO2,重新成为贫液。加热再生得到的贫液的CO2饱和吸收量与新制二元复合胺溶液的CO2饱和吸收量之比即为二元复合胺体系的CO2吸收再生效率。
1.3 反应原理
三级胺没有多余的H原子,因此不会形成氨基甲酸根,其在吸收过程中扮演CO2水解时的催化剂,而使被吸收的CO2形成碳酸氢根离子。
MDEA水溶液中发生的反应如下[6,7]:
CO2与OH-的反应:
(2)
此反应进行得非常迅速。
CO2与MDEA的反应:
(3)
其中:R1、R2、R3为链烷醇基。
一般认为上述总反应可分两步进行,首先MDEA与CO2生成中间化合物:
(4)
然后中间化合物催化CO2水解:
(5)
其中:R1、R2=HOC2H4,R3=CH3。
哌嗪与CO2的反应机理与仲胺相似,但由于哌嗪分子的独特性(含有2个对称性亚氨基),在动力学和热力学上显示出优越的CO2吸收性能,与CO2反应十分迅速,且最大CO2吸收量比伯胺、仲胺的最大吸收量要大[9,10]。其反应如下:
(6)
(7)
(8)
(9)
-OOCN(C4H8)NCOO-+H2O
(10)
2 结果与讨论
2.1 MDEA-PZ复合胺溶液吸收CO2性能
在相同的实验条件下,考察对于总浓度为1 mol·L-1、不同摩尔配比(0.95∶0.05)~(0.5∶0.5)的MDEA-PZ复合胺溶液,吸收量、吸收速率与吸收时间、pH值、电位的关系。
2.1.1 吸收速率、吸收量与吸收时间的关系(图3、图4)

图3 吸收速率与吸收时间关系

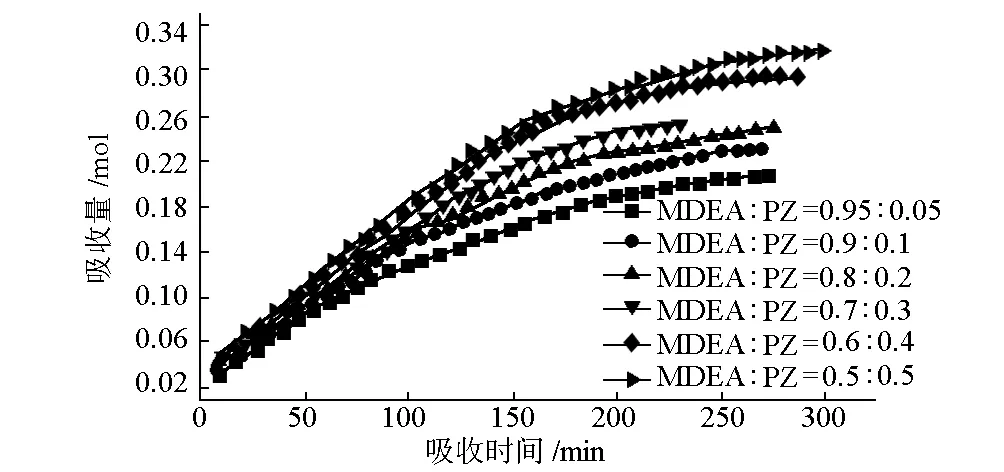
图4 吸收量与吸收时间关系
由图4可知,吸收的前50 min,各配比溶液吸收量基本相同;50 min后,随着二元复合体系中PZ浓度的增加,CO2吸收量不断增大;吸收280 min后体系基本达到饱和状态,其中摩尔配比为0.5∶0.5的复合胺溶液吸收量最大,为0.32 mol(合计0.8 mol·L-1)。
2.1.2 吸收速率、吸收量与pH值的关系(图5、图6)

图5 吸收速率与pH值关系
由图5可知,吸收速率随pH值的总体变化趋势相同,即随着pH值的降低,吸收速率减慢。当吸收液pH值相同时,不同配比复合胺溶液的吸收速率不同,其中摩尔配比为0.5∶0.5的复合胺溶液吸收速率最大,0.95∶0.05的最小。当吸收速率相同时,PZ浓度大的溶液其pH值大。由此可见,PZ浓度增加,加大了溶液的pH值、加快了吸收速率。

图6 吸收量与pH值关系
由图6可知,随着吸收的进行,pH值降低,吸收量升高。当pH值降到8.4左右时,吸收基本达到饱和,吸收量最多的为摩尔配比为0.5∶0.5的复合胺溶液,约0.32 mol(合计0.8 mol·L-1)。
2.1.3 吸收速率、吸收量与电位的关系(图7)

图7 吸收速率与电位关系
由图7可知,吸收速率随电位的总体变化趋势相同,起初溶液中OH-的浓度较高,吸收速率快,对应的溶液电位较低;随着吸收的进行,OH-不断消耗,溶液电位上升,吸收速率不断下降;当电位上升到-90 mV时,吸收基本达到饱和。

图8 吸收量与电位关系
由图8可知,随着吸收的进行,电位升高,吸收量变大;当电位上升到-90 mV时,吸收基本达到饱和,吸收量最多的一组为摩尔配比0.5∶0.5的复合胺溶液,吸收量约0.32 mol(合计0.8 mol·L-1)。
2.2 复合体系的交互作用
单组分MDEA体系、单组分PZ体系、二元复合体系中烟气CO2的吸收速率和吸收量与吸收时间的关系分别见图9、图10。

图9 吸收速率与吸收时间关系
由图9可知,吸收前80 min,二元复合体系的吸收速率要小于单组分PZ体系和单组分MDEA体系吸收速率之和;80 min后,二元复合体系的吸收速率要大于单组分PZ体系和单组分MDEA体系吸收速率之和。这说明二元复合体系中的两种组分之间存在正交互作用。
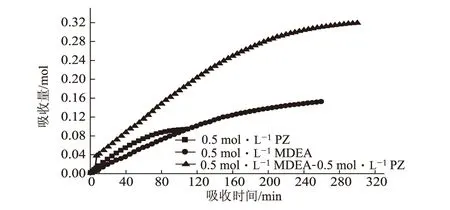
图10 吸收量与吸收时间关系
由图10可知,0.5 mol·L-1PZ体系的CO2饱和吸收量为0.10 mol、0.5 mol·L-1MDEA体系的CO2的饱和吸收量为0.152 mol、0.5 mol·L-1MDEA-0.5 mol·L-1PZ体系的CO2饱和吸收量为0.32 mol。单组分MDEA体系和单组分PZ体系的CO2饱和吸收量之和要小于二元复合体系,这也证实PZ、MDEA之间存在正交互作用。
2.3 再生性能(表1)

表1 MDEA-PZ复合胺溶液再生温度、pH值和再生率
由表1可见,对于MDEA-PZ体系,随着体系中PZ浓度的升高,CO2初始逸出温度先升高后降低。二元复合体系的CO2初始逸出温度均低于60 ℃,而再生温度基本都为103 ℃,0.5 mol·L-1MDEA-0.5 mol·L-1PZ再生温度最低,为102 ℃。同时可以看出,二元复合体系的再生温度高于单组分MDEA体系(101 ℃)、低于单组分PZ体系(104 ℃)。
由表1还可见,MDEA-PZ复合胺溶液摩尔配比为0.5∶0.5时,溶液的再生率最高,为88.61%,且此时再生pH值下降率最低,为11.39%;摩尔配比为0.7∶0.3时再生率最低,为83.91%。
3 结论
(1)在6种摩尔配比的MDEA-PZ体系中,0.5 mol·L-1MDEA-0.50 mol·L-1PZ吸收速率最快,吸收量最大,其最大吸收量为0.32 mol(合计0.8 mol·L-1)。
(2)0.5 mol·L-1MDEA-0.5 mol·L-1PZ二元复合体系的饱和吸收量大于单组分0.5 mol·L-1MDEA体系和0.5 mol·L-1PZ体系的饱和吸收量之和,说明MDEA-PZ复合体系的两种组分之间存在正交互作用。
(3)再生实验表明,0.5 mol·L-1MDEA-0.5 mol·L-1PZ复合体系的CO2初始逸出温度最低,为54 ℃;再生温度最低,为102℃;再生率最高,为88.61%;再生pH值下降率最低,为11.39%。
综合比较而言,0.50 mol·L-1MDEA-0.50 mol·L-1PZ复合胺溶液是烟气中CO2的最佳吸收剂。
[1] 李清方,陆诗建,张建,等.搅拌法对TEA溶液吸收和解吸CO2的实验研究[J].陕西科技大学学报,2009,27(4):48-51.
[2] 杨向平,陆诗建.回收烟气中二氧化碳用于强化采油技术进展及可行性分析[J].现代化工,2009,29(11):24-27.
[3] 陈泽焜.本菲尔脱碳工艺用新型活化剂ACT-1的开发与应用[J].中氮肥,1994,(6):9-13.
[4] 肖九高.烟道气中二氧化碳回收技术的研究[J].现代化工,2004,24(5):47-49.
[5] 陆诗建,李清方,张建,等.烯胺溶液吸收和解吸模拟烟气中二氧化碳实验研究[J].应用化工,2009,38(9):1245-1248.
[6] Gerald O.Carbon dioxide gets grounded[J].Chemical Engineering,2000,107(3):41-45.
[7] 杨向平,陆诗建,高仲峰,等.基于电位法和酸碱度法的醇胺溶液吸收二氧化碳[J].中国石油大学学报,2010,34(2):140-144.
[8] 彭彼得,朱世勇.复合催化热钾碱溶液与本菲尔溶液脱除CO2对比试验[J].化肥与催化,1990,(2):49-53.
[9] 夏明珠,严荷莲.二氧化碳的分离回收技术与综合利用[J].现代化工,1999,19(5):46-48.
[10] 费维扬,艾宁,陈健.温室气体CO2的捕集和分离[J].化工进展,2005,24(1):1-4.
[11] Parkinson G.Solid adsorbent scrubs CO2from flue-gas[J].Ch-emical Engineering,2000,107(2):21-24.

