放射性核素心室造影评价前壁心肌梗死后心力衰竭患者左室整体和局部功能
吴 迪
左室前壁心肌梗死(AM I)后,有一部分出现心功能障碍或心力衰竭,表现为心肌收缩不协调,收缩功能下降以及左室射血分数减少等。我们应用放射性核素心室造影 (RNVG)技术对不同纽约心脏病学会(NYHA)分级的左室前壁心肌梗死患者进行左室总体与局部收缩和舒张功能参数对比分析,以求对AMI造成的左室结构和功能的影响进行精确量化的深入研究和探索。本研究的目的是为了确定左室前壁AM I后的心力衰竭与RNVG心功能参数之间的精确关系。
方 法
1.病人选择
对照组:共15(男8,女 7)例,年龄(42±3)岁(38~61岁)。既往无高血压、冠心病、糖尿病和高脂血症等病史,体检和实验室检查均无阳性发现。
左室前壁AMI组:29(男26,女 3)例,年龄(51±2)岁(41~72岁),诊断按世界卫生组织(WHO)标准确立,全部为有Q波型AMI,在患者发病后3个月内病情相对稳定后进行RNVG,入院后根据临床NYHA分级又将患者分为2组:NYHAⅠ-Ⅱ级组17例,NYHA Ⅲ-Ⅳ级组12例。均以除外AMI造成的室壁瘤、室间隔穿孔、二尖瓣腱索断裂[1]。
2.放射性核素心室造影
使用日本ToshibaGCA-9013型SPECT,对每个患者进行常规多门电路平衡法RNVG,造影示踪剂为99mTc-RBC,采用体内标记法,剂量为740~925MBq。患者平卧于检查床上,取左前斜位30°~45°(以将左右心室影像最佳分隔为准)进行采集,放大倍数为2,矩阵为64×64,以病人心电图的R波作为触发信号进行采集,每个心动周期(R-R间期)分为32帧,共采集300~400个心动周期,将每个心动周期的信号进行叠加,最后获得一个清晰的心室心动周期的系列图像[2]。
原始资料采集后,调入专用计算机中进入心脏专用程序进行处理,在对原始资料进行时间和空间平滑后,经计算机处理获得多项心功能参数。
3.心脏功能参数
左室整体时间-放射性活度曲线分析,计算出左室总体功能参数。我们选择有代表性的参数,包括:①左室总体收缩功能参数:LVEF(左室射血分数,%);TPE(峰射血时间,ms);PER(峰射血率,%/s);1/3EF(前1/3射血分数,%);1/3ER(前1/3射血率,%/s);ESC(收缩未期计数量)。②左室总体舒张功能参数:TPF(峰充盈时间,ms);PFR(峰充盈率,%/s);1/3FF(前1/3充盈分数,%);1/3FR(前1/3充盈率,%/s);EDC(舒张未期计数量)。详见图1,3,5。
左室局部时间—放射性活度曲线分析,将左室以扇形等分为6个节段计算出各个节段的局部功能。包括:①左室局部收缩功能参数:LVREF(左室局部射血分数,%)。②左室局部舒张功能参数:LVR1/3FF(左室局部1/3充盈分数,%)。详见图2,4,6。
4.统计学处理
结 果
1.三组间总体收缩功能参数对比分析(表1)
表1 3组间左室总体收缩和舒张功能的比较()
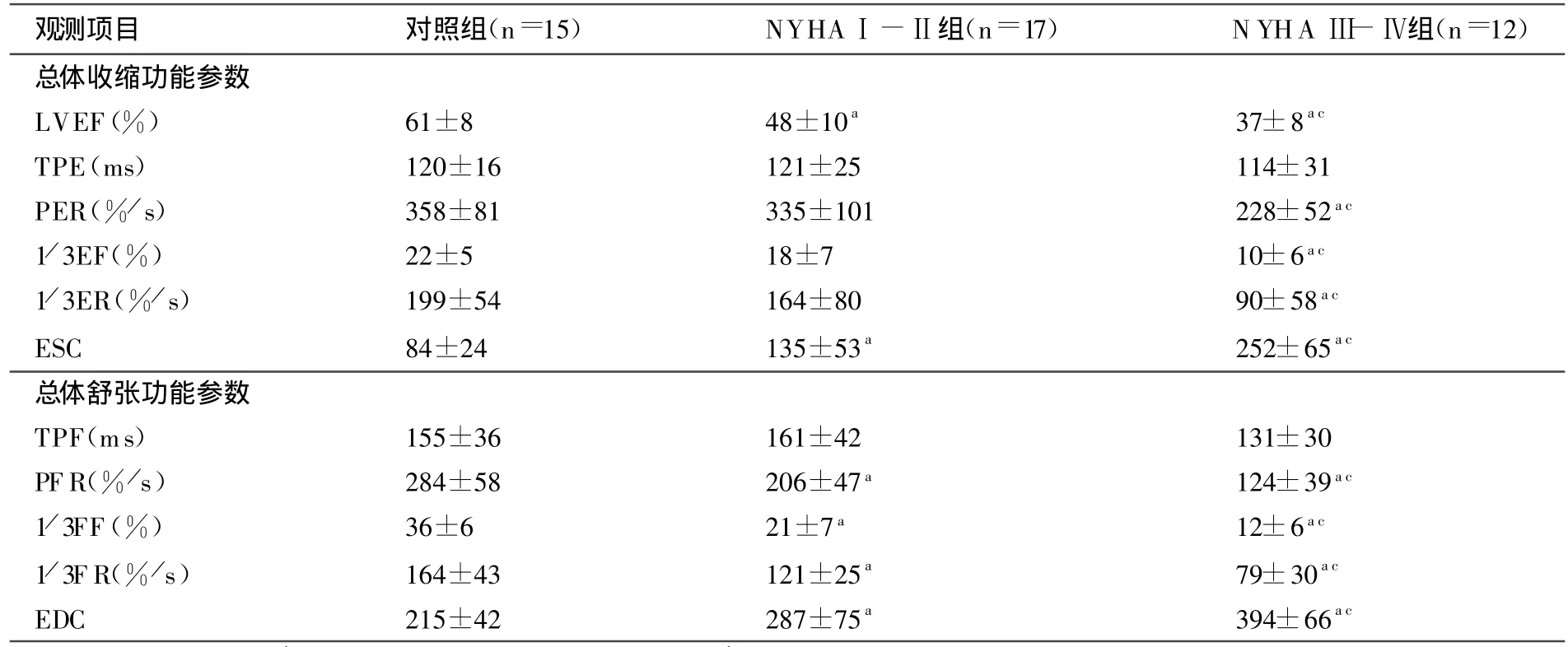
表1 3组间左室总体收缩和舒张功能的比较()
注:与对照组比较,aP<0.05。与NYHAⅠ-Ⅱ组比较,cP<0.05。
①LVEF:NYHAⅠ-Ⅱ组与对照组相比有显著下降(P<0.05);NYHAⅢ-Ⅳ组与对照组和NYHAⅠ-Ⅱ组相比,分别有显著下降(P<0.05)。②PER:1/3EF,1/3ER,NYHAⅠ-Ⅱ组与对照组相比无明显变化;NYHAⅢ-Ⅳ组与对照组和NYHAⅠ-Ⅱ组相比,分别有显著下降(P<0.05)。详见表1。
2.三组间总体舒张功能参数对比分析
①PF R:1/3FF,1/3FR,NYHAⅠ-Ⅱ组与对照组相比有显著下降(P<0.05);NYHAⅡ-Ⅲ组与对照组和NYHAⅠ-Ⅱ组相比,分别有显著下降 (P<0.05)。②EDC:NYHA Ⅰ-Ⅱ组与对照组相比有明显增大(P<0.05);NYHAⅢ-Ⅳ组与对照组和NYHA Ⅰ-Ⅱ相对比,分别有显著增大(P<0.05)。详见表1。
3.三组间局部收缩功能参数对比分析
LVREF,NYHA Ⅰ-Ⅱ组在4个节段 (侧壁下部、心尖部、间隔下部、间隔上部)与对照组相比有显著下降(P<0.05);NYHAⅢ-Ⅳ组在所有6个节段上与对照组和NYHAⅠ-Ⅱ组相比,分别有显著下降(P<0.05)。详见表 2。
4.三组间局部舒张功能参数对比分析
LVR1/3FF,NYHA Ⅰ-Ⅱ组在4个节段(侧壁下部,心尖部,间隔下部,间隔上部)与对照组相比有显著下降(P<0.05);NYHAⅢ-Ⅳ组在所有6个节段上与对照组和NYHAⅠ-Ⅱ组相比,分别有显著下降(P<0.05)。详见表2。
表2 3组间左室局部收缩和舒张功能比较()
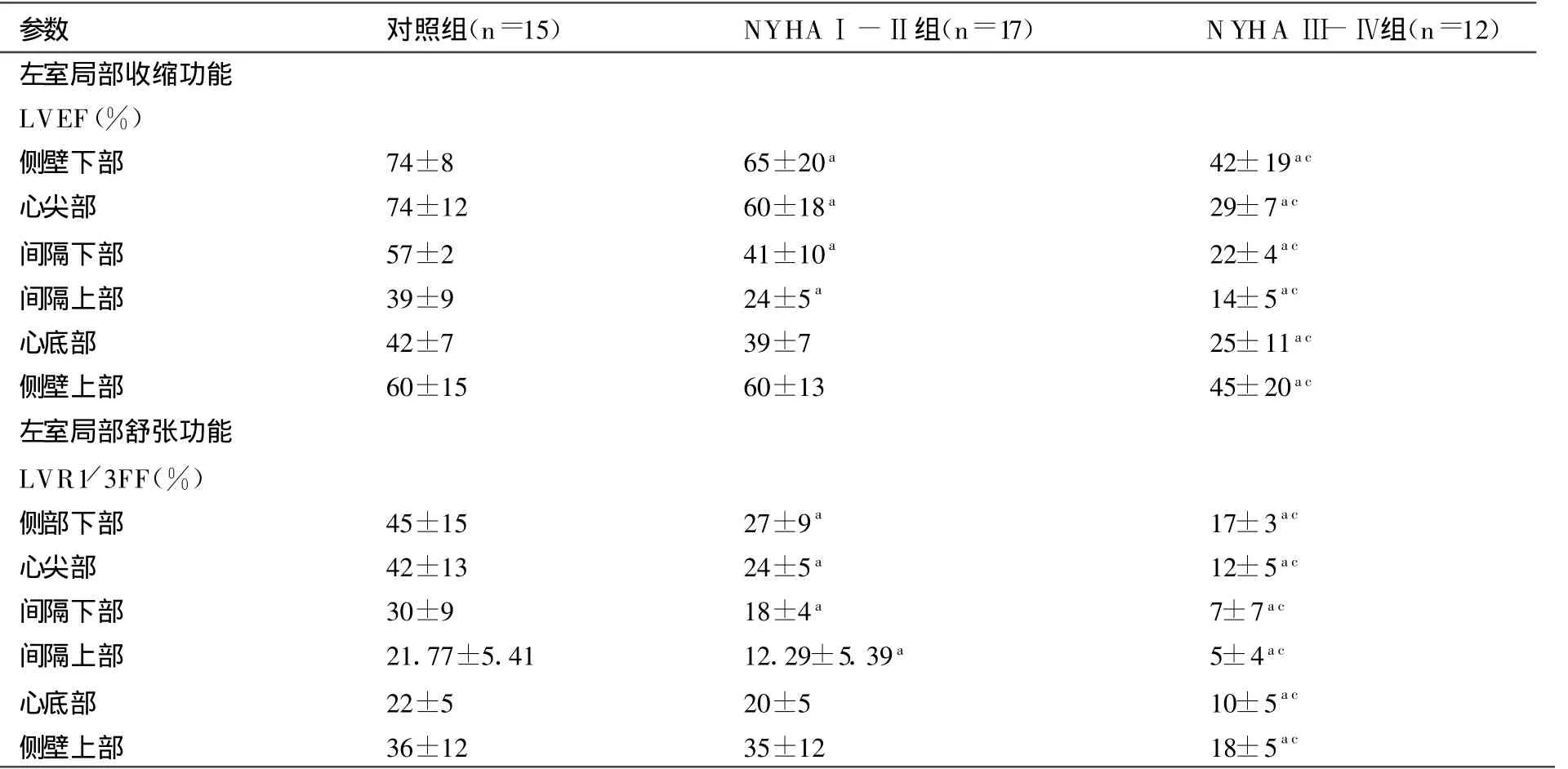
表2 3组间左室局部收缩和舒张功能比较()
注:与对照组比较,aP<0.05。与NYHAⅠ-Ⅱ组比较,cP<0.05。
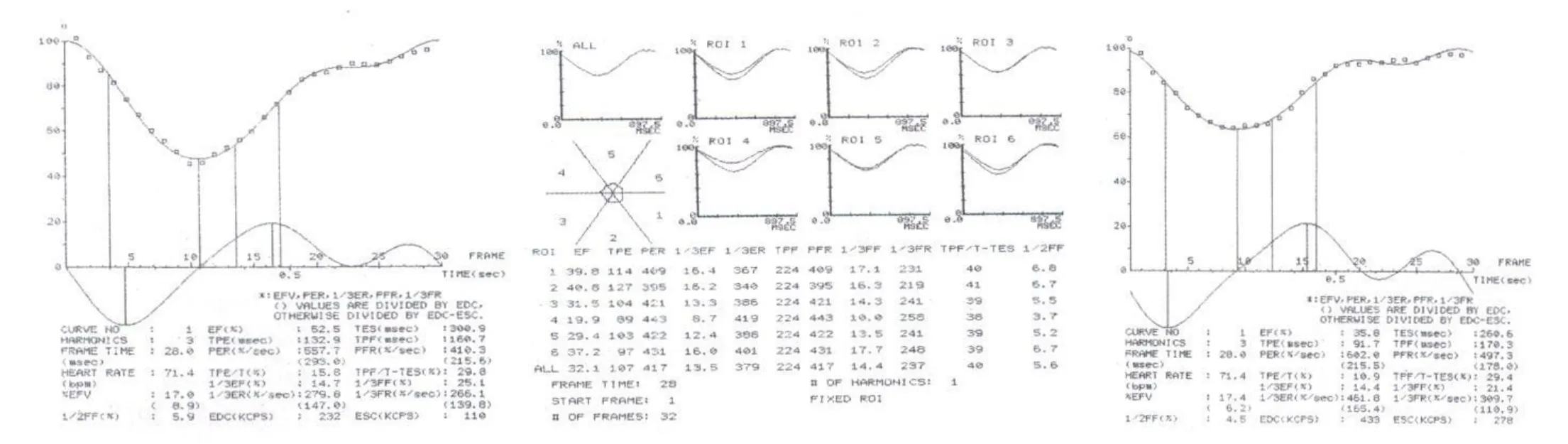
图1 对照组患者的左室整体时间-放射性曲线分析。图2 对照组患者的左室局部时间-放射性曲线分析。图3 NYHAⅠ-Ⅱ组患者的左室整体时间-放射性曲线分析。
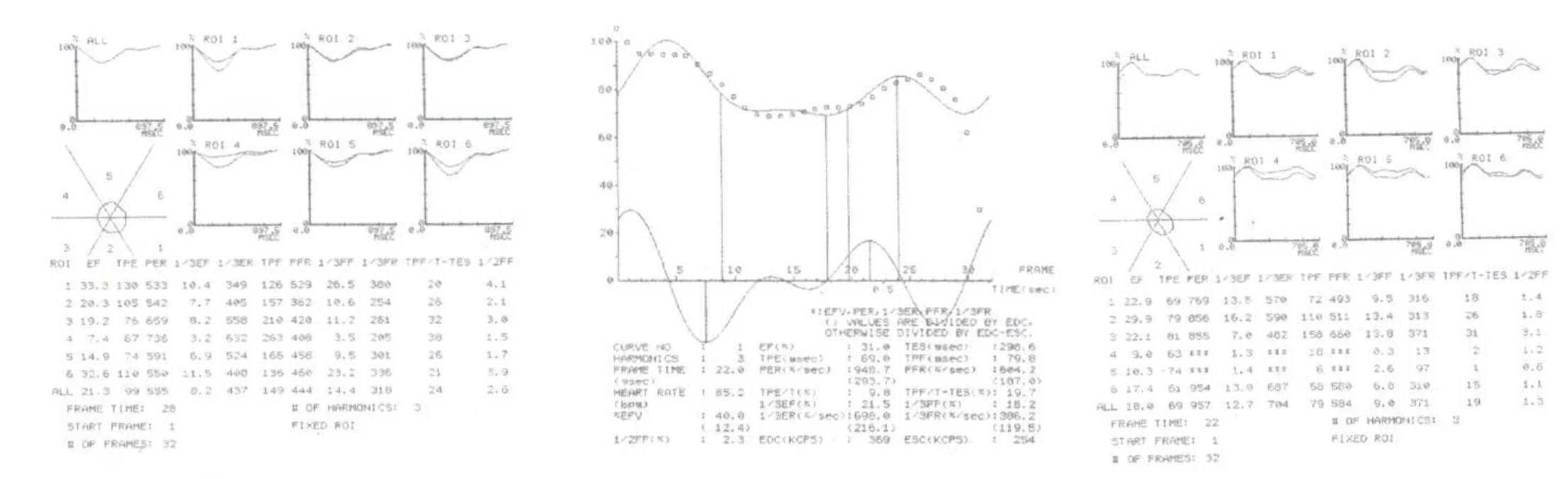
图4 NYHAⅠ-Ⅱ组患者的左室局部时间-放射性曲线分析。图5 NYHAⅢ-Ⅳ组患者的左室整体时间-放射性曲线分析。图6 NYHAⅢ-Ⅳ组患者的左室局部时间-放射性曲线分析。
讨 论
急性心肌梗死后出现心功能障碍乃至心力衰竭是非常严重的临床并发症。这类患者的临床预后极差,病死率很高。
急性心肌梗死后出现左心室重构塑是难以避免的,通常在梗死后数小时就发生。心肌坏死之后,心肌细胞崩解并且逐步吸收,同时成纤维细胞增生,胶原沉积纤维瘢痕出现。在左室腔内的压力作用下,梗死区室壁变薄,扩张,造成梗死扩展和左室扩大[3]。本研究发现,无论是代表左室收缩末容积的ESC还是代表舒张末容积的EDC,NYHAⅠ-Ⅱ组比对照均明显升高,而NYHA Ⅲ-Ⅳ组比对照组和NYHAⅠ-Ⅱ组分别进一步明显升高,从而也验证了上述观点。
由于严重缺血心肌能量供应发生障碍[4],致梗死周围的缺血区心肌收缩功能也严重受损。本研究发现,左室收缩功能的主要代表指标LVEF和LVREF,NYHAⅠ-Ⅱ组比对照组明显下降,而NYHAⅢ-Ⅳ组比对照组和NYHAⅠ-Ⅱ组也明显下降。
由于左室心肌舒张本身是一个耗能的过程,所以当心肌梗死时,梗死区和缺血区血液供应中断减小,心肌能量供应发生障碍,从而导致心肌舒张功能发生障碍。首先梗死区心肌坏死、炎症、水肿、胶原沉积和纤维化,使得该部位弹性下降,周围心肌组织受到瘢痕组织的牵拉,弹性也受到影响。这样左室总体和局部的顺应性就降低,引起左室扩张和左室舒张末压升高。另外由于左室舒张协调性的降低,引起左室舒张期压力下降速度的降低,使得左室充盈减少和充盈障碍[5]。本研究发现,在代表左室总体舒张功能参数PFR、1/3FF、1/3FR、中,NYHAⅠ-Ⅱ组比对照组明显下降,而NYHAⅢ-Ⅳ比对照组和NYHAⅠ-Ⅱ组有明显下降。
总之,引起急性心肌梗死后左室功能受损或心力衰竭的原因包括左室重塑、收缩功能下降、舒张功能障碍等。本文通过实际检测的患者多项心功能参数的统计分析,验证了急性心肌梗死后引起的左室功能受损或心力衰竭等一系列的心脏病理生理变化,为临床诊断和治疗提供了充分的证据。
1.Klocke FJ,Baird MG,Lorell BH,et al.ACC/AHA/ASNC guidelines for the clinical use of cardiac radionuclide imaging executive summary:a report of the American College of Cardiology/American Heart Heart Association Task Force on Practice Guidelines.Circulation,2003,108:1404-1418
2.DePuey EG,Garcia EV.Updated imaging guidelines for Nuclear Cardiology procedure.J Nucl Cardiol,2001,8:G1-G58
3.Pfeffer MA,Braunwald E:Ventricular remodeling after myocardial infraction:experimental observations and clinical implications.Criculation,1990,81:1161-1172
4.Bareiss P,Facello A,Constantinesco A,et al.Alterations in left ventricular diastolic function in chronic ischemic Heart Failure.Circulation,1990,81(SupplⅢ):Ⅲ 71-77
5.Browm EJ,Idoine J,Swinford RD,et al.Regional left ventricular filling:Does It reflect diastolic abnormalities in contiguous areas of myocardium.J Nucl Med,1989,30:165-173

