自体骨髓间充质干细胞移植对心肌梗死后心衰家兔炎性因子表达的影响
乔建晶 李树仁 胡 炜 王天红 刘东霞 荀丽颖 郝淸卿 吴 迪 董 洁 齐晓勇
(河北省人民医院,河北 石家庄 050051)
急性心肌梗死(AMI)往往伴随强烈的免疫炎症反应,是损伤部位修复机制的重要调控因素之一。免疫炎症反应过度激活将导致心肌进一步损伤,推动心室重塑的发生和发展〔1〕。多种抗炎药物已被用于AMI治疗,但临床研究尚未达到预期疗效。采用甲泼尼龙抑制心肌梗死后炎症反应,但患者心律失常发生率增加,梗死面积扩大,甚至增加心脏破裂的发生率。非甾体类抗炎药物治疗AMI的相关研究也与预期不符。两项大的临床试验RENAISSANCE和RECOVER结果显示:重组TNF受体融合蛋白依那西普(Etanercept)对心力衰竭患者的住院率和病死率无明显改善。实验研究显示BMSCs移植可以抑制AMI后免疫炎症反应,延缓心肌梗死后心室重塑〔2,3〕,可能与调节相关炎性细胞因子的表达有关。本实验观察BMSCs移植对心肌梗死后心衰家兔炎性细胞因子表达的影响,以揭示其治疗心肌梗死的机制。
1 材料与方法
1.1 动物及分组 河北医科大学实验动物中心提供(许可证号:SCXK冀2008-1-003)5月龄健康雄性新西兰白兔34只,体重1.8~2.3 kg,随机分为假手术组、AMI后心衰模型组、BMSCs移植组。组间体重无显著差异。
1.2 主要试剂 胎牛血清(美国hyclone公司);低糖DMEM培养基(美国 hyclone公司);Percoll原液(美国Pharmacia公司);DAPI(瑞士Roche公司);5-氮胞苷(美国SIGMA公司)。
1.3 BMSCs的分离、培养、诱导及标记 在股骨处穿刺抽取3~5 ml骨髓,用Percoll分离液(密度1.073 g/ml)分离骨髓单个核细胞,将分离的细胞悬液置于含10%胎牛血清的 DMEM培养基中,放入37℃,5%CO2饱和湿度孵箱中培养。3~5 d首次换液,以后每3或4天换液1次,14~21 d细胞生长融合80%以上后,以0.25%胰蛋白酶消化,按1∶2比例传代培养。于移植前1天用含5-氮胞苷(10μmol/L)诱导培养基继续培养24 h。移植前 2 h用含二脒基苯基吲哚(DAPI)(浓度50μg/ml)标记培养基培养2 h。最后收集1×107BMSCs,用DMEM浓缩至1 ml,置于冰上(不超过1 h),移植备用。
1.4 兔AMI后心衰模型的建立 称重后,兔仰卧于手术台,经耳缘静脉注射3%戊巴比妥钠1 ml/kg麻醉,剪除胸毛、消毒铺无菌洞巾,沿胸骨正中线第2,3肋间稍偏左做长约3 cm切口,分离肋间肌、剪断肋骨、剪开心包暴露心脏,用6/0医用无损伤缝线穿过左冠状动脉前降支深部,小心打结并观察心电图动态变化。心电图可见相应导联ST段抬高,同时肉眼观察结扎区域心肌变白为结扎成功,逐层关胸,缝合切口。术后3 d肌注青霉素80万U预防感染。术前及术后2 h记录体表心电图。1.5 细胞移植 AMI术后14 d,仍以3%戊巴比妥钠1 ml/kg耳缘静脉麻醉兔二次开胸,再次行胸骨左侧切口打开胸腔,暴露心脏,选取心肌梗死周边区域4个注射点,BMSCs组注射BMSCs悬液,AMI后心衰模型组注射 PBS液。每点注射0.25 ml,注射位置以6/0手术线标记。术后独笼精心饲养。
1.6 超声心动图左心功能测定 采用美国惠普公司5500型彩色多普勒超声心动图仪在术前、心梗后7 d、细胞移植后28 d分别由同一专科医生进行超声心动图检测。重点测算左室舒张末内径(EDD)、左室射血分数(EF)、短轴缩短率(FS),取3次测量平均值,由超声心动图医生进行操作。
1.7 取材 各组动物饲养至细胞移植后4 w,在全身麻醉下再次开胸,心内注射10%氯化钾2 ml使心脏停搏于舒张期,迅速取下心脏,冰盐水冲洗干净,在相应梗死周边区切取标本,置入液氮罐冷冻保存备用。
1.8 ELISA法测血清炎性因子 分别于术前、心梗后7 d、细胞移植后28 d(处死前)经耳缘静脉抽血2~3 ml,避免溶血,抗凝剂用EDTA,2 000 r/min离心8 min,取上清-20℃保存,采用双抗体夹心ELISA法检测血清IL-6、TNF-α、CRP的浓度。试剂盒由美国ADL公司提供,严格按照试剂盒说明书操作。
1.9 实时定量PCR法检测心肌组织NF-κB、IL-6、TNF-αmRNA表达 将心肌组织按RNA试剂盒(Invitrogen公司产品)说明书提取RNA。42℃反转录(反转录试剂盒:Promega,USA)50 min,95℃ 5 min灭活反转录酶。Syber Green荧光定量PCR检测(Hot Start Fluorescent PCR Core Reagent Kits,ABI)。仪器型号:ABI 7300 Real-Time PCR System,美国ABI公司。PCR热循环参数:96℃ 4 min,然后三步反应:94℃ 30 s,58℃ 30 s,72℃30 s,40个循环,于每个循环的第3步即:72℃ 30 s收集荧光信号。实时荧光定量PCR结果分析:扩增完毕后,进入结果分析界面,以GAPDH为内参照基因,与对照组相比,得到目的基因表达的相对定量值(RQ值),将RQ值用于统计分析。引物序列:兔 NF-κB,121 bp,上游引物 5'-TACGGCTTCCCACACTATGG-3',下游引物 5'-TCACAACATCCAGGGTCAGT-3';兔 IL-6,79 bp,上游引物 5'-GCCTGCTGAGAATCACTTCG-3',下游引物5'-TCGTCACTCCTGAACTTGGC-3';兔 TNF-α,148 bp,上游引物5'-AGTAGCAAACCCGCAAGTG-3', 下 游 引 物 5'-GCTGAAGAGAACCTGGGAGT-3';兔 GAPDH,92 bp,上游引物 5'-CAAGAAGGTGGTGAAGCAGG-3',下 游 引 物 5'-CACTGTTGAAGTCGCAGGAG-3'。
1.10 统计学处理 采用SPSS13.0统计软件包,计量资料以x±s表示。多组资料之间的比较采用单因素方差分析,多组间均数对比采用q检验。
2 结果
2.1 BMSCs形态观察 大部分BMSCs于12 h贴壁,72 h可见贴壁生长以分散、克隆集落方式增殖,少量细胞拉长呈纺锤形紧贴培养瓶底部生长繁殖。5~7 d后细胞开始快速增殖,集落逐渐增大。11~14 d细胞集落间出现相互融合,细胞铺满单层,呈旋涡状排列。大部分呈长梭形,少数三角形、多角形。密集处中心的细胞由多边形转变为梭形。胞核较大,多为卵圆形,也有圆形、不规则形,其中可见处于分裂期的核仁,胞体肥大,胞质丰富,大多数细胞有伪足。见图1。
2.2 荧光显微镜下观察DAPI标记的BMSCs 经DAPI标记2 h后,在荧光显微镜下可观察到DAPI标记的BMSCs。细胞移植28 d后,处死家兔后,取梗死周边区域心肌组织,经冰冻切片机切片后,在荧光显微镜下可观察到的经DAPI标记的移植BMSCs。见图 2。
2.3 家兔心功能检测结果 术前各组EDD、EF、FS均无显著差异。AMI后心衰模型制作7 d,AMI后心衰模型组、BMSCs组EF值比正常对照组显著降低(P<0.05);AMI后心衰模型组和BMSCs组EF值差异不显著。细胞移植后28 d,正常对照组、BMSCs组EDD均明显低于AMI后心衰模型组(P<0.05),EF及FS均明显高于AMI后心衰模型组(P<0.05)。差异有统计学意义,见表1。
2.4 血清炎性因子检测结果 术前各组炎性因子无显著差异。术后7 d,与正常对照组相比AMI后心衰模型组、BMSCs组的血清 IL-6、TNF-α、CRP的浓度均显著增加(P <0.05),但AMI后心衰模型组和BMSCs组之间差异不显著。细胞移植后28 d,BMSCs组血清 IL-6、TNF-α、CRP 的浓度比 AMI后心衰模型组显著降低(P<0.05);正常对照组略低于BMSCs组,但无显著差异。见表2。
2.5 心肌组织炎性因子PCR检测结果 细胞移植后28 d,BMSCs组梗死边缘区心肌组织IL-6、TNF-αmRNA表达比AMI后心衰模型组显著降低(P<0.05)。见表3。
2.6 心肌组织NF-κB的PCR检测结果 与正常组相比AMI后心衰模型组、BMSCs组的心肌梗死边缘区的NF-κB均显著增加(P<0.05),BMSCs组比AMI后心衰模型组显著降低(P<0.05)。见表3。

表1 兔心功能测定(x ± s,n=8)

表2 兔血清炎性因子测定结果(x ± s,n=8)

表3 兔移植28 d心肌组织炎性因子PCR检测RQ值(x ± s,n=8)

图1 BMSCs 20 d(×200)
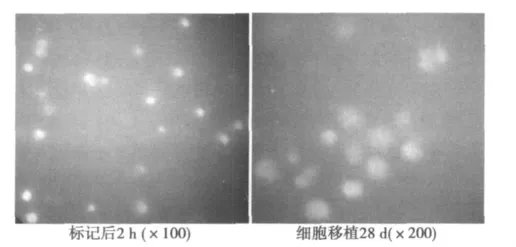
图2 DAPI标记后2 h及细胞移植28 d后心肌组织BMSCs
2.7 心功能与心肌组织炎性因子及NF-кB的相关性 细胞移植后28 d时,EF与血清炎性因子呈负相关(CRP:r=-0.605,P=0.002,Y=93.959 -4.344X;TNF-α:r= -0.425,P=0.039,Y=85.346-0.122X;IL-6:r= -0.475,P=0.025,Y=86.967 -0.085X);与心肌组织炎性因子呈负相关(TNF-α:r=-0.592,P=0.002,Y=71.206 - 2.887X;IL-6:r= -0.512,P=0.011,Y=70.392-1.509X);与心肌组织 NF-κB呈负相关(r=-0.866,P=0.001,Y=71.621-10.039X)。其中 Y 代表 LVEF值,X代表各个炎性因子。
3 讨论
骨髓干细胞用于心肌梗死治疗研究已经成为心血管疾病领域的研究热点。动物研究几乎一致显示骨髓干细胞可以明显改善梗死心脏心功能,抑制心室重塑〔4,5〕,相关的临床研究也得到了类似的结果〔6〕。但由于目前临床研究的样本量较小,另外无法完全做到随机对照,再加上目前干细胞治疗心肌梗死的确切机制并不清楚,因此骨髓干细胞到底能否治疗心肌梗死尚未得到完全肯定。目前认为其机制可能与心肌和血管再生、抑制心肌细胞凋亡以及旁分泌机制有关〔7〕。BMSCs治疗AMI的机制较复杂,除了目前的几种机制外,可能存在有其他未知机制。本研究结果显示:BMSCs移植可以抑制NF-κB表达,下调炎性细胞因子(TNF-α、IL-6和CRP)的表达,可以明显改善心肌梗死后心功能,延缓心肌梗死后向心力衰竭方向的进展。BMSCs具有独特的免疫学特性,移植到机体后可以调节受体的免疫炎症反应〔8〕。由于心肌梗死后伴随的免疫炎症反应在随后的梗死后心室重构过程中起着重要的推动作用〔9〕。故可以认为心肌梗死后减轻免疫炎症反应可以抑制心室重构,改善心功能。心肌梗死后伴随一定程度的免疫炎症反应,而且免疫炎症反应在心室重构进展中起着重要的推动作用,心肌梗死后调节免疫炎症反应可能成为抑制心室重塑的新靶点。NF-κB是与炎症反应有关的即早基因的表达调控关键因子之一。NF-κB与抑制蛋白I-κB结合在胞浆中呈非活化状态,在刺激因子作用下,与I-κB解离而活化,并迅速核移位,与特异性κB结合而启动靶基因转录,分泌白细胞介素、肿瘤坏死因子、细胞黏附分子、干扰素等炎性介质,产生急性炎症反应。NF-κB能在转录水平激活炎性细胞因子,而某些细胞因子如TNF-α、IL-6又可进一步激活 NF-κB,如此循环产生放大作用〔10〕。本研究发现,BMSCs移植后,可显著降低梗死边缘区NF-κB的表达,进而调控炎症反应有关的即早基因的表达,下调了炎性因子TNF-α、IL-6和CRP的表达,减轻炎症反应对心肌的损伤,从而减轻心肌梗死后心室重塑。
TNF-α和IL-6作为促炎细胞因子对心肌细胞具有毒性作用,可以抑制心肌收缩功能,诱导心肌细胞凋亡,推动心室重构的进展〔11〕。正常心肌组织很少表达TNF-α和IL-6,而心肌缺血损伤可迅速激发TNF-α和IL-6的高水平表达。动物实验也证实抑制TNF-α的活性可以明显减小心肌梗死面积,改善心功能〔12〕。因此,抑制TNF-α和IL-6的表达有助于延缓心肌梗死后心室重构。本实验结果显示细胞移植后4 w时,AMI后心衰模型组促炎因子TNF-α和IL-6在梗死区存活心肌内表达明显增加,而BMSCs移植组明显降低促炎因子TNF-α和IL-6的表达。从而在一定程度上抑制炎症反应,延缓心肌梗死后家兔心室重塑,延缓向心力衰竭的发展。
CRP是由白细胞介素-6及TNF等细胞因子诱导的在肝脏合成的一种急性时相反应蛋白。机体在感染、组织损伤等应激情况下会产生急性时相反应,此时IL-6,TNF等细胞因子分泌增多,肝脏合成的CRP明显增加。CRP在正常人群含量极低,其水平增高被认为机体内存在炎症反应。采用高灵敏度的系统来检测CRP已经被多项前瞻性研究证实是未来发生心血管事件的预测指标。本实验研究发现BMSCs可以减少CRP的合成,减轻炎症反应。本研究结果提示BMSCs可能通过抑制NF-κB活性而下调炎性细胞因子(CRP、TNF-α和 IL-6)表达,从而也阻断了NF-κB与炎性细胞因子的相互激活和促进,从而减轻炎症反应,减轻心肌梗死后左室重塑,延缓心肌梗死后向心力衰竭的进展。因此作者推测BMSCs治疗心肌梗死可能部分归功于免疫炎症调节机制,BMSCs移植有望成为心肌梗死后免疫调节治疗的策略之一。
BMSCs移植后通过免疫调节发挥作用〔13〕。BMSCs表达的表面分子可以与T细胞发生相互作用,调节T细胞的生物活性,通过这种免疫调节作用,一方面可以逃避免疫反应对其自身的破坏,另一方面也可以减轻周围组织中的免疫反应强度,从而在一定程度上保护组织功能。BMSCs的免疫调节作用机制复杂,可能与多种因素有关〔14〕。(1)本身低免疫原性,MSCs表达中等水平的MHC-Ⅰ类分子,从而能被NK细胞赦免;不表达MHC-Ⅱ类分子,故能逃避异原性CD4+T细胞的识别。同时它不表达FAS配体或共刺激分子,因而不能诱导效应T细胞反应;(2)通过分泌可溶性细胞因子(如肝细胞生长因子和TGF-α),与T细胞直接接触诱导T细胞活化受阻;通过PGE2和吲哚胺2,3双加氧酶介导活化NK细胞增殖受抑〔15〕;(3)改变T细胞和DC的表型、功能,研究发现MLR中加入BMSCs后Treg明显增加;人BMSCs通过细胞间接触可将APC转化为半成熟的抑制型DC而诱导外周耐受。另外BMSCs在体外能明显抑制CD8+T细胞增殖,同时减低Thl而增加Th2。
由于骨髓干细胞移植可能通过定向分化、融合、旁分泌、抑制免疫炎症反应等作用方式影响梗死区心肌再生和血管形成,因而是一种有前途的研究方向。到目前为止,国内外研究由于移植的细胞类型,途径,病例数,无严格对照,随访时间少等诸多原因目前仍存在许多尚待解决的问题。比如是否需要采用动员方案及最佳动员时机,移植细胞是否需要纯化,细胞移植的最佳时间点,最佳移植途径,最佳移植数量,以及是否存在成瘤现象;缺乏干细胞治疗的长期资料,细胞移植治疗的具体机制等。另外,植入缺血心肌内的BMSCs生存能力差,这也大大限制了它们的修复能力。怎样有效提高移植细胞的存活,还需继续努力研究和探索。这些问题都需要我们在进一步的研究实践中逐渐解决。随着科技的发展和社会的进步,细胞移植无疑对缺血性心脏病的治疗提供了新的手段,并将会产生广阔的应用前景。
1 Maekawa Y,Mizue N,Chan A,et al.Survival and cardiac remodeling after myocardial infarction are critically dependent on the host innate immune interleukin-1 receptor-associated kinase-4 signaling〔J〕.Circulation,2009;120:1401-14.
2 Mann DL,McMurray JJ,Packer M,et al.Targeted anticytokine therapy in patients with chronic heart failure:results of the Randomized Etanercept Worldwide Evaluation(RENEWAL)〔J〕.Circulation,2004;109:1594-602.
3 Du YY,Zhou SH,Zhou T,et al.Immuno-inflammatory regulation effect of mesenchymal stem cell transplantation in a rat model of myocardial infarction〔J〕.Cytotherapy,2008;10(5):469-78.
4 Li SR,Qi XY,Hu FL,et al.Mechanisms of improvement of left ventricle remodeling by transplanting two kinds of autologous bone marrow stem cells〔J〕.Chin Med J,2008;121(23):2403-6.
5 李树仁,齐晓勇,张建清,等.经冠脉自体骨髓干细胞移植改善左室重构机制的研究〔J〕.中国老年学杂志,2007;27(21):2057-62.
6 Mohyeddin-Bonab M,Mohamad-Hassani MR,Alimoghaddam K,et al.Autologous in vitro expanded mesenchymal stem cell therapy for human old myocardial infarction〔J〕.Arch Iran Med,2007;10:467-73.
7 Schuleri KH,Boyle AJ,Hare JM.Mesenchymal stem cells for cardiac regenerative therapy〔J〕.Handb Exp Pharmacol,2007;180:195-218.
8 Fibbe WE,Nauta AJ,Roelofs H.Modulation of immune responses by mesenchymal stem cells〔J〕.Ann N Y Acad Sci,2007;1106:272-8.
9 Liao YH,Cheng X.Autoimmunity in myocardial infarction〔J〕.Int JCardiol,2006;112:21-6.
10 Bradham WS,Moe G,Wendt KA,et al.TNF-α and myocardial matrix metalloproteinases in heart failure relationship to LV remodeling〔J〕.Am JPhysiol Heart Circ Physiol,2002;282(4):1288-95.
11 Nian M,Lee P,Khaper N,et al.Inflammatory cytokines and postmyocardial infarction remodeling〔J〕.Circ Res,2004;94(12):1543-53.
12 Sugano M,Tsuchida K,Hata T,et al.In vivo transfer of soluble TNF-alpha receptor 1 gene improves cardiac function and reduces infarct size after myocardial infarction in rats〔J〕.Faseb J,2004;18(7):911-3.
13 Maitra B,Szekely E,Gjini K,et al.Human mesenchymal stem cells support unrelated donor hematopoietic stem cells and suppress T-cell activation〔J〕.JBone Marrow Transplant,2004;33(6):597-604.
14 Nauta AJ,Fibbe WE.Immunomodulatory properties of mesenchymal stromal cells〔J〕.Blood,2007;110:3499-506.
15 Grazia MS,Andrea CB,Heba A,et al.Mesenchymal stem cells inhibit natural killer-cell proliferation,cytotoxicity,and cytokine production:role of indoleamine 2,3-dioxygenase and prostaglandin E2〔J〕.Blood,2008;111:1327-33.

