浸渍活性炭吸附低浓度PH3动力学
王学谦,宁平
(昆明理工大学 环境科学与工程学院,云南 昆明,650093)
黄磷尾气、密闭电石炉尾气等工业废气中富含CO,是优质的有机化工原料气,但其中存在的主要杂质磷、硫、氰限制了该气体作为一碳化工原料气的使用[1-2]。要利用其中的高浓度 CO作为原料气生产甲醇、二甲醚等高附加值产品,就必须对尾气中的 PH3等有害杂质进行深度处理。密闭电石炉每生产1 t电石副产炉气约400 m3,其中,CO的体积分数高达80%~85%。但现有大多数的电石生产企业都未处理和回收利用电石炉尾气,而以送火炬燃烧方式排放,既浪费大量有用的资源和能源,又造成严重的环境空气污染,像密闭电石炉尾气这样富含CO的宝贵资源,至今没有得到资源回收利用,其限制因素就在于密闭电石炉尾气由于有害杂质PH3,H2S和HCN等的存在,这些有害杂质尤其是尾气中磷的存在,致使羰基合成催化剂中毒[3]。国家电石行业准入条件已规定密闭电石炉气必须净化综合利用。目前,国内外对低浓度PH3的净化方法主要有吸附法和化学吸收法[4-5]。化学吸收法以化学氧化吸收法为主,主要利用次磷酸钠、高锰酸钾、硫酸、过氧化氢等与PH3进行化学反应,从而实现PH3的净化,但化学氧化吸收法存在二次污染问题,氧化剂消耗量大且氧化剂难于回收[6-8]。吸附法中较典型的是浸渍活性炭催化氧化法,该法主要通过负载HCl和铜等活性组分[9-15],使还原态的 PH3被催化氧化而后吸附在活性炭表面、达到深度去除的目的,这是一种有效可行的方法。本文作者以PH3为研究对象,研究了在微氧含量(≤1%)条件下PH3在浸渍活性炭上的吸附平衡和吸附动力学行为,试图为研究工业气氛中PH3的迁移转化规律及浸渍活性炭在典型工业废气处理中的应用提供理论依据。
1 实验
1.1 实验材料和仪器
活性炭采用河南长葛活性炭厂生产活性炭,活性炭的物性参数如表1所示,将10 g 活性炭均匀分散到50 mL含0.1 mol/L醋酸铜的溶液中,浸渍24 h[9-10],然后进行真空过滤。活性炭在120 ℃下干燥12 h,再在350 ℃温度下对浸渍活性炭焙烧6 h制得。

表1 活性炭的物性参数Table 1 Parameters of activated carbon
PH3的分析采用气相色谱-火焰光度法测定。气相色谱型号为:岛津 GC-14C(带火焰光度检测器),聚四氟乙烯填充柱。色谱工作条件为:N2和 H2流速为40 mL/min,色谱柱温为50 ℃,检测器温度为200 ℃,检出限为0.01 mg/m3。
1.2 实验方法
实验采用动态配气的方法,钢瓶中是实验要求浓度的PH3与氮气的混合气体,和微量空气在混合器中混合均匀后,以0.3 L/min的流速进入吸附床层单元,空气在进入混合器之前用 CaCl2干燥管干燥,以除去空气中的水分。吸附反应在一个直径为 9 mm、高为60 mm的不锈钢圆柱状反应器中进行。
用气相色谱仪测定进出口气体PH3浓度,获得各个温度下不同进口浓度的穿透曲线;然后对穿透曲线按式(1)积分可得对应的吸附容量[15];以平衡质量浓度ρe为横坐标,饱和吸附容量qe为纵坐标作图,即可得一定温度下PH3的吸附等温线;以时间t为横坐标,t时刻对应吸附量q为纵坐标作图,便可得吸附速率曲线。
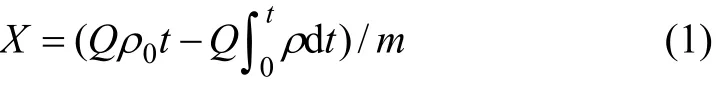
式中:X为吸附容量,g/g;Q为气体流量,m3/min;t为吸附时间,min;ρ0为吸附柱入口质量浓度,mg/m3;ρ为吸附柱出口质量浓度,mg/m3;m为吸附剂质量,g。
2 结果与讨论
在本研究的前期工作中,已经发现改性活性炭上PH3的脱除是催化氧化脱磷过程。PH3在活性炭上先被氧化成H3PO4和P4O10(P2O5),然后吸附在活性炭上[10]。
在醋酸铜改性活性炭上,存在着含氧官能团和CuO在活性炭表面形成的络合物 CuOx-AC等活性中心。CuOx-AC是醋酸铜在高温煅烧后,铜盐被还原与活性炭表面基团生成的络合物。上述官能团对催化剂脱磷起重要作用。脱磷过程是个催化氧化过程,反应产物中的氧不是直接来自气相中的氧,而是来自金属氧化物中的晶格氧,气相中的氧只是用来补充催化剂在反应中消耗的晶格氧。催化氧化脱磷过程反应如下:
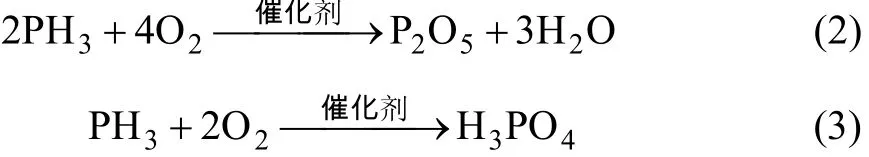
2.1 吸附等温线
当氧体积分数为1%时,在20,40,60,80和95℃的PH3吸附等温线[16-17]如图1所示。
经过PH3吸附等温线用Langmuir和Freundlich吸附等温方程进行对比描述,发现Freundlich吸附等温方程具有较好的相关性,因此,选用Freundlich等温方程进行拟合,见表2。
由表2的Freundlich吸附等温方程可知:不同温度下吸附等温方程参数 1/n均在 0.1~0.5之间,说明PH3在浸渍活性炭上易被吸附。

图1 PH3吸附等温线Fig.1 PH3 adsorption isotherms
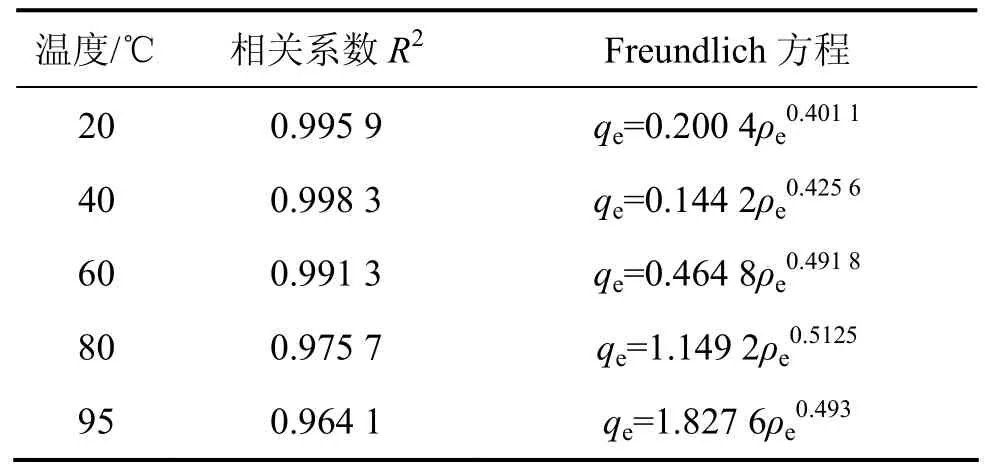
表2 Freundlich方程拟合PH3在浸渍活性炭上吸附等温线方程Table 2 Freundlich adsorption equations for adsorption of PH3 on impregnated activated carbon
从吸附等温线可以看出:在20~40 ℃范围内吸附容量随温度的升高而减少,在60~95 ℃范围内吸附容量随温度的升高而增加;PH3在低温范围(20~40 ℃)属典型的物理吸附,在此温度下,外界不能为化学反应提供足够的活化能,化学反应无法有效进行,因此,主要是靠 PH3分子在吸附剂微孔表面上的吸着作用,分子吸着固定在吸附剂表面上后,势能降低,对外界放出热量,所以,这一过程是一个放热过程,也就是低温有利于吸附。PH3在高温范围(60~95 ℃)的吸附属化学吸附,PH3在吸附剂上发生的热化学反应方程式按式(3)及(4)进行,PH3在60~95 ℃有利于吸附,这与吸附等温线的变化规律相吻合。
2.2 吸附动力学
经过对实验数据的动力学试算比较,发现只有班厄姆吸附速率方程的拟合相关性最好,因此,确定选用班厄姆(Bangham)吸附速率方程对吸附速率曲线进行拟合。
班厄姆公式可写成如下形式:
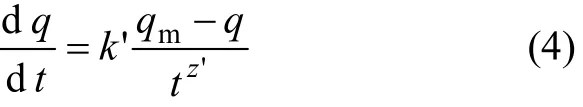
积分式为:
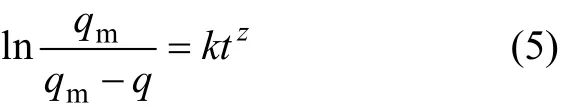
经整理后得:
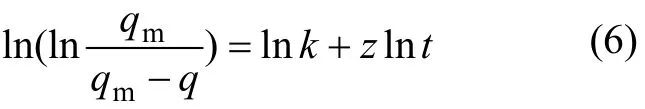
式中:q为吸附容量,g/g;qm为平衡吸附量,g/g;t为时间,h;k和z为常数。
利用ln{ln[qm/(qm-q)]}对ln t作图可得一条直线,并可由直线的斜率和截距求出式中的常数。氧体积分数为1% PH3的吸附速率曲线如图2所示。利用班厄姆公式对PH3在吸附剂上的吸附速率曲线进行拟合,作ln t关系曲线,PH3吸附的班厄姆拟合曲线见图 3;由此求取反应速率等参数,得到用于描述不同温度下PH3在浸渍活性炭上吸附的班厄姆吸附动力学方程,见表3。
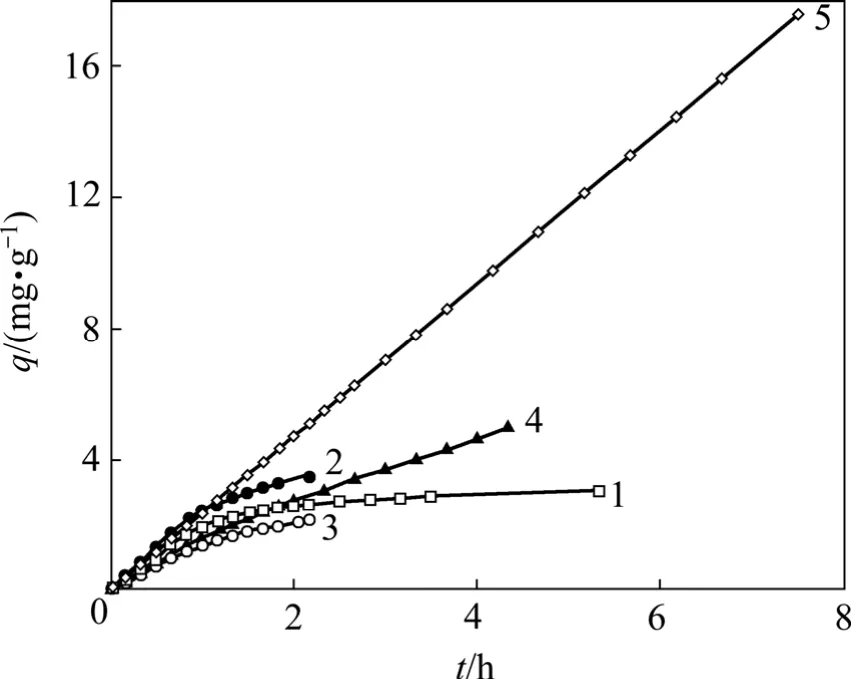
图2 PH3在浸渍活性炭上的吸附速率曲线Fig.2 Adsorption rate curves of PH3 on impregnated activated carbon
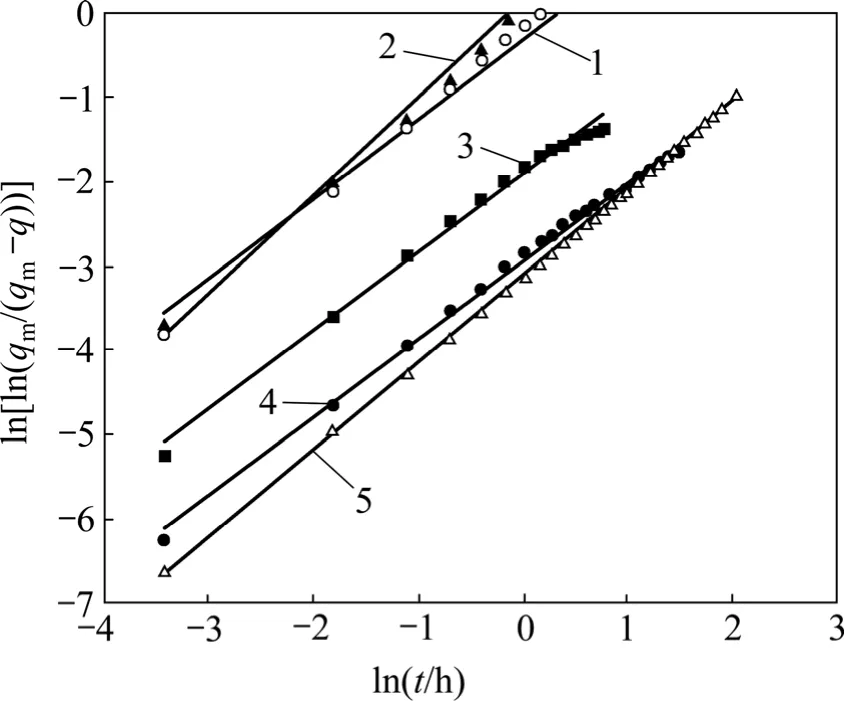
图3 PH3在浸渍活性炭上吸附的班厄姆吸附动力学曲线Fig.3 Bangham kinetic curves of PH3 adsorption on impregnated activated carbon
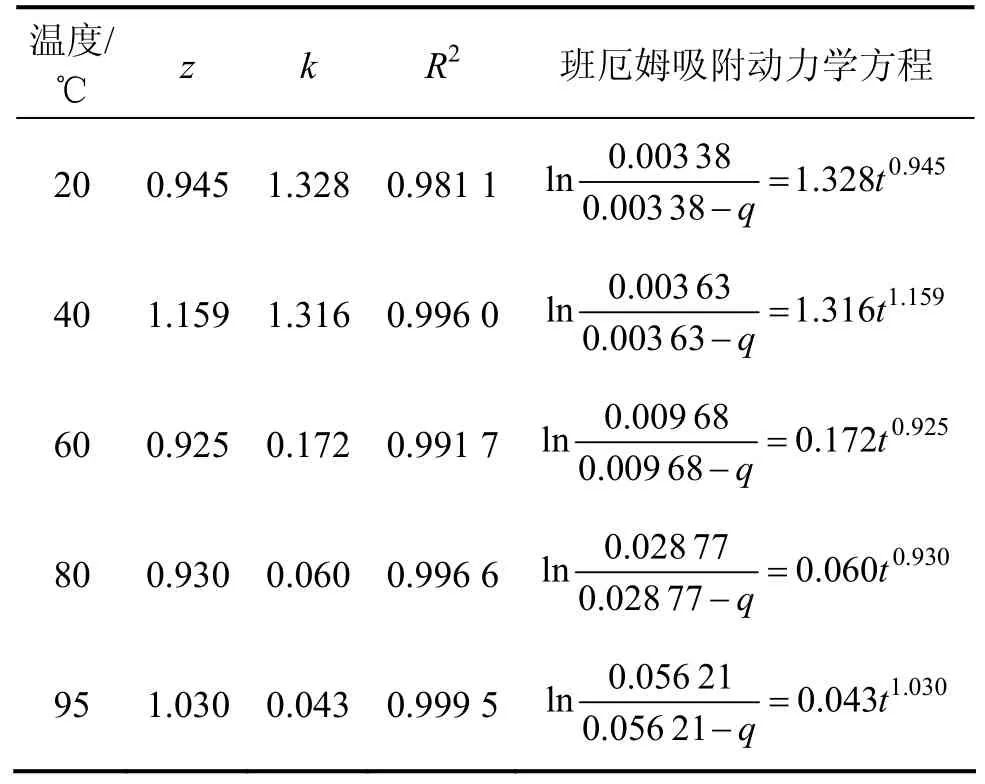
表3 不同温度下的班厄姆吸附动力学方程Table 3 Bangham kinetic equation on different temperature
从表3可以看出:班厄姆吸附动力学方程对PH3在上浸渍活性炭上的吸附拟合相关性较好,可以得到理想的吸附速率方程。
3 结论
(1) 在氧体积分数为1%时微氧条件下,PH3在浸渍活性炭上的吸附可用 Freundlich等温方程进行描述,Freundlich等温方程具有较好的相关性。
(2) 温度对 PH3在浸渍活性炭上的吸附等温线的影响可分为2个阶段:在20~40 ℃低温范围内,以物理吸附为主,物理吸附是个放热过程,温度越低越有利于吸附;高温范围内(60~95 ℃)是以化学吸附为主的反应过程,温度越高越有利于吸附。
(3) 在氧体积分数为1%时微氧条件下,PH3在浸渍活性炭上的吸附符合班厄姆吸附动力学方程。通过实验获得了用于描述不同温度下PH3在浸渍活性炭上吸附的班厄姆吸附动力学方程。
[1] 宁平, 王学谦, 吴满昌, 等. 黄磷尾气碱洗—催化氧化净化[J].化学工程, 2004, 10(5): 61-65.NING Ping, WANG Xue-qian, WU Man-chang, et al. Purifying yellow phosphorus tail gas by caustic washing—Catalytic oxidation[J]. Chemical Engineering, 2004, 10(5): 61-65.
[2] 熊辉, 杨晓利, 李光兴. 次氢酸钠氧化脱除黄磷尾气中的硫、磷杂质[J]. 化工环保, 2002, 22(31): 161-164.XIONG Hui, YANG Xiao-li, LI Guang-xing. Removal of sulfur and phosphorus from tail gas in yellow phosphorus production by sodium hypochlorite oxidation process[J]. Environmental Protection of Chemical Industry, 2002, 22(31): 161-164.
[3] 宁平, Bart H J, 王学谦, 等. 催化净化氧化黄磷尾气中的磷和硫[J]. 中国工程科学, 2005, 7(6): 27-35.NING Ping, Bart H J, WANG Xue-qian, et al. Removal of P4,PH3and H2S from yellow phosphoric tail gas by a catalyticoxidation process[J]. Engineering Science, 2005, 7(6):27-35.
[4] Li W C, Bai H L, Hsu J N, et al. Metal loaded zeolite adsorbents for phosphine removal[J]. Industrial & Engineering Chemistry Research, 2008, 47(5): 1501-1505.
[5] 宁平, 易玉敏, 瞿广飞, 等. PdCI2-CuCI2液相催化氧化净化黄磷尾气中 PH3[J]. 中南大学学报: 自然科学版, 2009, 40(2):340-345.NING Ping, YI Yu-min, QU Guang-fei, et al. Catalytic oxidation PH3in yellow phosphoric tail gas with PdCl2and CuCl2solution[J]. Journal of Central South University: Science and Technology, 2009, 40(2): 340-345.
[6] 瞿广飞, 宁平, 李军燕. 磷化氢液相催化氧化净化催化剂的初筛[J]. 环境工程, 2007, 25(5): 70-71, 75.QU Guan-fei, NING ping, LI Jun-yan. Screening of catalysts for phosphine catalytic oxidation in aqueous solution[J].Environmental Engineering, 2007, 25(5): 70-71, 75.
[7] 张玉, 宁平, 瞿广飞. 磷化氢净化技术进展[J]. 四川化工,2005, 8(5): 16-24.ZHANG Yu, NING Ping, QU Guang-fei. Research progress of removal of PH3[J]. Sicuan Chemical Industry, 2005, 8(5): 16-24.
[8] 王成俊, 郭爱红, 王福生, 等. 次磷酸钠工业生产过程中 PH3尾气处理技术[J]. 天津化工, 2003, 17(5): 37-38.WANG Cheng-jun, GUO Ai-hong, WANG Fu-sheng, et al.Treatmental technology of PH3waste gas in the process of industrial sodium hypophosphite production[J]. Tianjin Chemical Industry, 2003, 17(5): 37-38.
[9] 宁平, 潘克昌, 谢有畅, 等. 黄磷尾气固定床催化氧化净化的方法: 中国, CN1398658A[P]. 2003-02-26.NING Ping, PANG Ke-chang, XIE You-chang, et al. Catalytic oxidation of yellow phosphoric tail gas using fixed bed: China,CN 1398658A[P]. 2003-02-26.
[10] Wang X Q, Ning P, Shi Y, et al. Adsorption of low concentration phosphine in yellowphosphorus off-gas by impregnated activated carbon[J]. Journal of Hazardous Materials, 2009, 171: 588-593
[11] Cal M P, Strickle B W, Lizzio A A, High temperature hydrogen sulfide adsorption on activated carbon Ⅰ: Effects of gas composition and metal addition[J]. Carbon, 2000, 38(13):1757-1765.
[12] Bagreev A, Bandosz T J. A role of sodium hydroxide in the process of hydrogen sulfide adsorption/oxidation on caustic:Impregnated activated carbons[J]. Industrial & Engineering Chemistry Research, 2002, 41(4): 672-679.
[13] Bagreev A, Menendez J A, Dukhno I, et al. Bituminous coal-based activated carbons modified with nitrogen as adsorbents of hydrogen sulfide[J]. Carbon, 2004, 42(3):469-476.
[14] Adib F, Bagreev A, Bandosz T J. Adsorption/oxidation of hydrogen sulfide on nitrogen: Containing activated carbons[J].Langmuir, 2000, 16(4): 1980-1986.
[15] Wang L, Cao B, Wang S D, et al. H2S catalytic oxidation on impregnated activated carbon: Experiment and modeling[J].Chemical Engineering Journal, 2006, 118(3): 133-139.
[16] Huang C C, Chen C H, Chu S M. Effect of moisture on H2S adsorption by copper impregnated activated carbon[J]. Journal of Hazardous Materials, 2006, 136: 866-873.
[17] 金一中, 徐灏, 谢裕坛. 活性炭吸附苯、甲苯废气的研究[J].高校化学工程学报, 2004, 18(2): 258-263.JIN Yi-zhong, XU Hao, XIE Yu-tan. Adsorption of benzene and toluene vapour on activated carbon[J]. Journal of Chemical Engineering of Chinese University, 2004, 18(2): 258-263.

