阿德福韦酯联合拉米夫定治疗HBeAg阳性慢性乙肝疗效观察
权耀生
山西省汾阳医院,山西 汾阳 032200
慢性乙型病毒性肝炎是由乙肝病毒 (HBV)引起的一种严重慢性疾病,它极大地危害着人类的健康,抗病毒治疗是控制该病情的关键,更是阻止肝硬化及肝癌发生的有效方法[1],核甘类药物如拉米夫定 (LAM)、阿德福韦酯(ADV)、替米夫定、恩替卡韦等治疗慢性乙肝疗效已得到人们的认可,但长期应用由于乙肝病毒变异而可能导致治疗失败。近年来,我们采用了ADV联合LAM治疗HBeAg阳性慢性乙肝取得较好的疗效,现报告如下。
1 资料与方法
1.1 病例选择
2009年2月-2010年5月我院门诊和住院治疗的HBeAg阳性慢性乙肝患者90例,诊断全部符合2008年西安会议修订的病毒性肝炎防治方案[2]诊断标准,三组病例在治疗52周期间均未接受免疫调节剂及抗病毒治疗,HB-sAg、HBeAg均阳性,HBV-DNA定量 (实时荧光定量PCR)HBV-DNA>10copies/ml,并排除其他肝炎病毒重叠感染。将所选病例随机分为A.B.C三组,A组30例、B组30例,C组30例,三组患者的年龄、性别、病程、肝功能及病毒学等指标差异无统计学意义 (P>0.05),具有可比性。
1.2 方法
1.2.1 分组与治疗 三组均在应用如葡醛内酯、甘草酸二胺等保肝药物治疗的同时,A组:单用ADV(正大天晴公司,商品名名正)10mg/d,B组:单用LAM100 mg/d(葛兰素史可公司,商品名贺普丁),C组:ADV 10mg/d联合LAM100 mg/d。
1.2.2 观察指标与检测 患者治疗前及治疗后4、12、26、38、52周检测 HBV-DNA、HBV标志物、肝功能、肾功能,血磷改变并记录患者症状、体征变化及不良事件的发生率。HBV-DNA定量检测用荧光定量PCR方法,所用仪器为美国ABI公司的PE5700,试剂盒由中山大学达安基因有限公司提供;HBV标志物检测用酶联免疫吸附法,试剂盒由上海科华实业有限公司提供;肝、肾功能采用日立7600全自动生化分析仪及配套试剂检测。
表1 3组患者治疗前后ALT检测结果 (U·L-1,)

表1 3组患者治疗前后ALT检测结果 (U·L-1,)
?
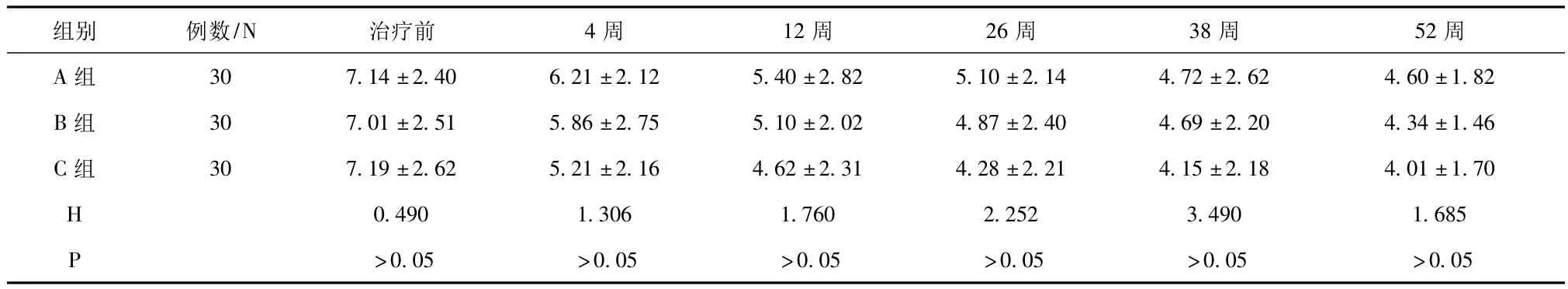
表2 3组患者治疗前后HBV DNA检测结果 (M+QR,log10copies·m-1)
1.2.3 统计学方法
应用SPSS11.5软件进行统计学分析,计量资料表1,采用以表示。表2,采用中位数±四分位数间距 (M±OR)表示。
2 结果
2.1 3组患者治疗前后ALT、HBV DNA检测结果
3组患者治疗后与治疗前比较:同组ALT水平均显著下降,组间ALT下降水平比较无统计学意义 (P>0.05)。3组患者HBV-DNA中位数水平较基线值分别下降2.54、2.67、3.18log10 copies·ml-1,详见表 1、表 2。
治疗前3组间比较F=2.010,P>0.05;同组不同时点与治疗前比较F=116.065,P<0..01;不同时点与组间交互作用F=0.522,P>0.05;与同组治疗前检查结果比较:*P<0.01。
治疗52周时3组HBV-DNA达到检测水平以下 (<500 copies·mL)的百分率分别为50.0%(15/30)、53.3%(16/30)、及80%(24/30),C组与A组及B组比较均有显著差异 (χ2值分别为5.93及4.8,P值均<0.05)。
2.2 联合治疗对HBAg阴率的影响
三组治疗4、12、26、38周HBeAg转阴率比较无统计学意义 (P>0.05),52周时C组明显大于A、B两组 (P<0.0)。结果见表3。

表3 3组患者HBeAg转阴率比较[n(%)]
2.3 联合治疗对HBeAg/抗一HBe血清转换率的影响
HBeAg/抗-HBe血清转换率C组最高,3组比较差异无统计学意义 (P>0.05)结果见表4。

表4 三组患者各观察时间点HBeAg/抗-HBeAb血清转换比较[n(%)]
2.4 3组患者不良反应及基因型耐药率比较
B组有1例患者治疗44周时出现rtM204V+rtL180M变异,HBV-DNA反弹,肝功能损害加重,经加用ADV、保肝等对症、支持治疗后好转出院。3组患者治疗52周时,A、B、C组患者的基因型耐药率分别为0、23.3% (7/30)、0(χ2=15.18,P<0.05),C组耐药率明显低于 B组。A,B、C组患者在治疗过程中未出现药物相关的肾功能损害和血磷改变。
3 讨论
慢性乙型病毒性肝炎是由乙型肝炎病毒 (HBV)引起的一种严重危害人类健康的疾病,容易进展为肝硬化和肝癌。目前公认抗病毒治疗是慢性乙型肝炎治疗的关键,更是阻止肝硬化及肝癌发生的有效途径。LAM与ADV均是有效治疗慢性乙肝的核苷类药物,自临床应用以来均收到了较好效果,但两药各有自己的优缺点。LAM具有较强的抑制乙肝病毒作用,疗效确实,但病毒耐药变异率高,应用1年的耐药率高达24%,且平均每年增加15%~20%。服用4~5年后,将有70%~80%的患者发生耐药。耐药后可发生病毒学反弹,肝脏功能再次受到损伤,转氨酶升高,目前已有LAM耐药后发生病情加重甚至导致重型肝炎而死亡的报告。而ADV早期效果好,后期效力不足,耐药发生率较低,服用1年为0%,服用2年为3%,服用3、4、5年分别为11%、18%、29%。但它最大的缺点是抗乙肝病毒的强度不如LAM、替比夫定和恩替卡韦。使用早期 (3个月以内)效果不错,但若长期使用,当病毒载量降至一定程度后,迟迟不发生病毒转阴,有些病例转阴后几个月,病毒再次转阳,化验乙肝病毒变异指标,各个位点并未出现阳性。为此,我们采用两种药联合应用抗乙肝病毒治疗,二药联合治疗利用了LAM的快速高效,及ADV的低耐药,机制互补,在HBV-DNA、HBeAg阴转率方面明显优于A、B两组,差异均有统计学意义 (P<0.01)。肝功能ALT下降水平,C组高于 A、B两组,但无统计学意义 (P>0.05),患者基因型耐药率比较。治疗52周时,A、B、C组患者的基因型耐药率分别为0、23.3% (7/30)、0(χ2=15.18,P<0.05),C组耐药率明显低于B组。结果证实二药联合治疗,既可降低LAM的耐药水平,发挥LAM的高持续应答及长期稳定病情效果,又弥补了ADV后期效力不足的缺点,因此,我们认为ADV与LAM联合治疗疗效高,并且持久稳定,值得推广,至于长期联合治疗是否会出现多重耐药,有待于进一步观察。
[1]卢平宣.慢性乙型肝炎抗病毒治疗的现状与进展[J].内科.2008,3(2):246-248.
[2]中华医学会肝病学分会,中华医学会感染病学分会.病毒性肝炎防治方案[J].中华传染病杂志,2001,19(1):56.

