不同骨科植入物对放射治疗的影响
倪昕晔 汤晓斌 林 涛 宋浩磊 孙苏平 陈 达*
1(南京航空航天大学核科学与工程系,南京 210016)
2(南京医科大学附属常州第二人民医院,常州 213003)
引言
恶性骨肿瘤手术后有较高的复发率,20世纪70年代以前恶性骨肿瘤的治疗以截肢术为主,手术后5年生存率为10% ~20%。自20世纪90年代以来,结合化疗和放射治疗的应用,恶性骨肿瘤的综合保肢术得以发展,患者5年生存率上升为50% ~80%[1],约50% ~80%的癌症患者死前发生了骨转移[2],Sakaura报道全椎体肿瘤即使行全脊椎大块切除,术后复发率仍很高,故术后应辅助放疗、化疗或免疫治疗,以消灭残存的瘤细胞[3]。
随着三维实形放射治疗、调强放射治疗、图像引导放射治疗技术的应用,对加速器输出的剂量计算精度的要求也越来越高。目前,常用的骨科体内植入物为不锈钢及钛合金两种,其密度大于人体组织,放射治疗当射线穿过金属材料时会有较大程度的衰减,从而影响肿瘤的放射剂量。临床研究表明,剂量±5%的变化就会引起无并发症的肿瘤控制概率的显著改变,肿瘤治疗剂量若有近10%的增加,肿瘤控制概率几乎有5倍的增加[4]。放射治疗的基本目标是最大限度地将放射线的剂量集中到病变(靶区)内,杀灭肿瘤细胞,而使周围正常组织和器官少受或免受不必要的照射[5-6]。因此,不锈钢及钛基合金植入物时植入物周围肿瘤部位进行的放射治疗造成了较大的影响。
由于碳的原子序数为6,密度较低与人体相近,所以X射线在碳材料中的衰减系数远低于金属材料。在X射线波长为0.154 2 nm的条件下,碳材料质量衰减系数为 5.50,而 Co、Cr、Ti分别为 354、259、204。因此,碳相对于金属对射线剂量的影响小很多。
放射治疗的流程是:用普通模拟定位机或 CT模拟定位机来找出肿瘤的位置,再用计划系统根据肿瘤吸收剂量来计算射线的剂量分布,最后在直线加速器上执行治疗计划。本研究分析商用的不锈钢植入物、钛基合金植入物以及自制的碳纤维植入物在放射诊断中的影像学区别及对放射治疗剂量的影响,从而分析碳纤维组成的骨科植入物在放射治疗中的应用前景。
1 材料与方法
采用3种不同材质骨科植入物(不锈钢植入物、钛基合金植入物以及自制的碳纤维植入物),通过手术先后植入同一只家猪的同一只后腿。在普通模拟定位机上进行普通模拟定位,观察植入物固定位置是否一致,得到普通模拟定位图像,即二维影像;通过模拟定位CT室的移动激光灯,借助3个金属定位小球对猪腿的位置进行固定,以保证猪大腿扫描位置的一致,再进行CT扫描模拟定位,从而得到三维影像。通过观察二维和三维影像,分析不同材质骨科植入物对放射影像的影响。
把CT模拟定位图像传输至放射治疗计划系统来进行治疗计划设计,比较剂量分布,分析不同材质植入物对放射治疗剂量的影响。放射治疗计划系统设计计划的具体参数如下:射野对整个大腿骨进行适形治疗,单个照射野,X射线,能量为6 MV,加速器角度为0°,准直器角度为0°,加速器输出量为200 MU,计算网格为0.3 cm×0.3 cm×0.3 cm,剂量计算方法采用叠代算法(superposition)。
在本研究中,使用的3种不同材质骨科植入物如下:不锈钢植入物为国产,常用的是316 L(美标,国标为00Cr17Ni14Mo2),主要成分为铁、铬、镍,以及少量的氮、锰、硅、硫、钼等,拥有良好的机械性,在体内较易腐蚀,因此常作暂时性的内置物;钛基合金植入物为国产,含有铝(Al)和钒(V),耐腐蚀性好;碳纤维植入物为南京航空航天大学材料科学与技术学院自制,是被高温石墨化处理过的2.5维PAN基的碳/碳复合材料。3种植入物的厚度都为0.4 cm,不锈钢植入物、钛基合金植入物、碳纤维植入物宽度分别为 1.3、1.5、1.5 cm,长度分别为12.5、14.0、14.0 cm,如图 1 所示。
在本研究中使用的主要设备如下:普通模拟定位机是荷兰核通公司生产的Simulix-HQ型模拟定位机,CT模拟定位机是德国西门子公司生产的SOMATOM Definition双源256排CT,放射治疗计划系统是美国CMS公司的 XIO 4.40计划系统,计划系统模拟的直线加速器是德国西门子公司的PRIMUS-PLUS加速器。

图1 不同材料的骨科植入物(从上到下依次为不锈钢、钛基合金、碳纤维)Fig.1 Orthopedic implants of different materials(stainless steel,titanium alloy,carbon fiber from top to bottom)
2 结果
首先,在普通模拟定位机上拍摄未进行手术的模拟定位片,如图2所示。然后,分别拍摄植入不锈钢、钛基合金、碳纤维植入物的模拟定位片,如图3~图5所示。可以观察到不锈钢、钛基合金植入物清晰地显示在模拟定位片上,挡住了后面的骨组织,而植入碳纤维植入物的模拟定位片与未植入植入物的模拟定位片相比,骨组织的分辨率没有受到影响。比较CT模拟定位片(见图6~图9),不锈钢植入物的周围有较大伪影,钛基合金植入物的周围伪影小,碳纤维植入物的周围无伪影。
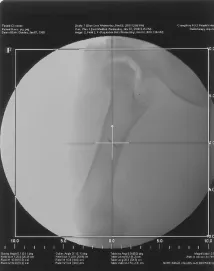
图2 无植入物的模拟定位片Fig.2 Simulation film of no implant
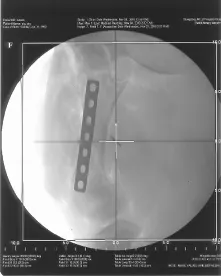
图3 不锈钢植入物的模拟定位片Fig.3 Simulation film of stainless steel implant
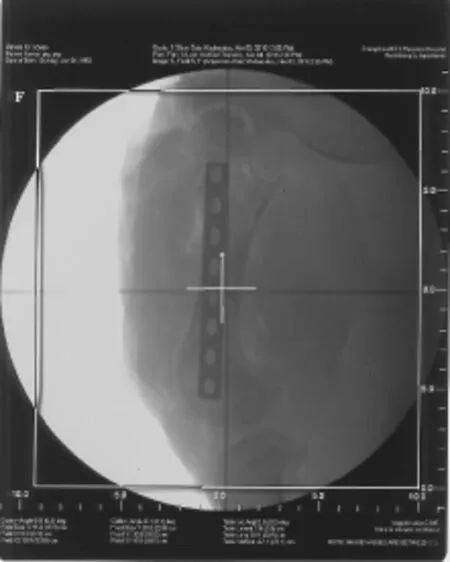
图4 钛基合金植入物的模拟定位片Fig.4 Simulation film of titanium alloy implant
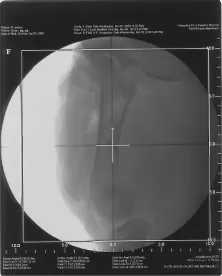
图5 碳纤维植入物的模拟定位片Fig.5 Simulation film of carbon fiber alloy implant
通过计划系统对无植入物、植入不锈钢、植入钛基合金、植入碳纤维进行计划设计,结果如图6~图8所示。由于射线入射组织表面处有一定的倾斜,因此等剂量线也有一定的倾斜(见图6),60%的等剂量线能到达组织底部。植入不同的植入物后,等剂量线发生了变化:由图7可见,不锈钢对射线的阻挡作用最大,等剂量线上扬幅度最大,特别是钢板下方的等剂量线往上隆起,60%的等剂量线不能到达组织底部;由图8可见,钛基合金对射线的阻挡作用较大,等剂量线上扬幅度较大,钛基合金下方的等剂量线往上微隆起,60%的等剂量线不能到达组织底部;由图9可见,碳纤维对射线的几乎无阻挡作用,等剂量线与没有植入物的等剂量线一致(见图6),60%的等剂量线能到达组织底部。通过点剂量比较射线分别穿过等厚(0.4 cm)的正常组织、不锈钢、钛基合金、碳纤维原射线分别衰减1.6%、5.7%、4.5%、1.6%,不锈钢对射线的阻挡作用最大。

图6 无植入物时的剂量分布Fig.6 Dose distribution of no implant
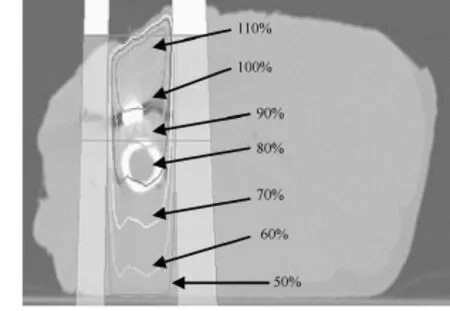
图7 植入不锈钢植入物的剂量分布Fig.7 Dose distribution of stainless steel implant
3 讨论
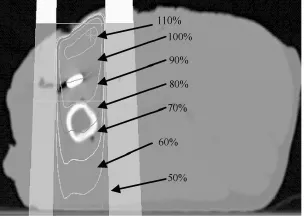
图8 植入钛基合金植入物的剂量分布Fig.8 Dose distribution of titanium implant
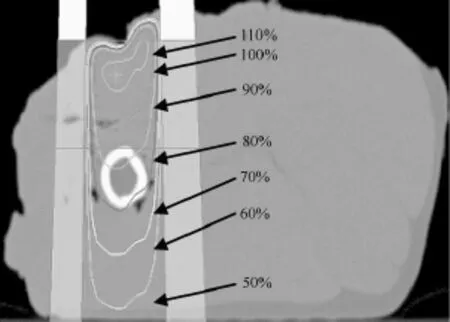
图9 植入碳纤维植入物的剂量分布Fig.9 Dose distribution of carbon fiber implant
从实验结果分析看,无论是诊断级别的 X线(KV级)还是治疗级别的 X线(MV级),碳纤维植入物对于射线几乎无衰减,主要原因是碳的原子序数较低,射线与其作用效果与人体相当。在诊断过程中,碳纤维植入物对图像质量没有影响,在三维影像中不会在植入物周围产生伪影,在二维影像中对植入物组织不会造成遮挡作用。
在放射治疗过程中,可以不用考虑碳纤维植入物因射线的衰减而导致骨肿瘤放射剂量不足。在植入不锈钢植入物、钛基合金植入物后进行骨肿瘤放射治疗时,应加大照射量来满足肿瘤剂量的要求,而没有植入物遮挡的骨肿瘤和正常组织会受到过量照射。在射线照射金属时,金属表面会产生剂量增加的现象[7],会增加放射治疗剂量的不均匀性。在放射治疗的过程中,碳纤维植入物与不锈钢植入物、钛基合金植入物相比有明显优势。
碳及其复合材料在骨科领域有较好的应用前景[8-9],碳材料通常是被用做医学金属植入材料的涂层,很少用做整体的植入体或骨固定材料,用作整体的骨科植入体或骨固定材料还没有在临床应用。虽然碳纤维植入物具有比强度大、比模量高、抗疲劳性能好、可设计性强、破损安全性能好、生物相容性好等优点[10-11],但要成为临床实用骨科植入物需克服如下问题[12]:碳纤维材料植入人体后会与周围软组织或骨组织发生摩擦,碳颗粒容易脱落;碳纤维材料为黑色,与人体骨颜色相差较大;需对材料表面改性,使其有一定的生物活性;会出现疲劳性问题;等等。
4 结论
通过研究得到如下结果:碳纤维骨科植入物相对于另外两种植入物(不锈钢植入物、钛基合金植入物),在放射治疗的模拟定位及放射治疗中有着不可比拟的优势,碳纤维骨科植入物在放射治疗应用中有很好的应用前景。
到目前为止,还没有商用碳纤维骨科植入物在临床使用。为此,推动医用碳纤维材料的研究和发展,对提高人类的健康水平和生活质量具有重要的意义。
[1]胡永成,马宏庆.全国骨转移瘤治疗专题座谈会会议纪要[J].中华骨科杂志,2003,23(6)323-325.
[2]袁文,贾连顺,肖建如,等.带锁钢板在颈椎肿瘤手术中的应用[J].临床骨科杂志,2000,3(4):254-256.
[3]Sakaura H,Hosono N,Mukai Y,et al.Outcome of total en bloc spondylectomy for solitary metastasis of the thoracolumbar spine[J].J Spinal Disord Tech,2004,17(4):297 - 300.
[4]ICRU Report No.24.Determination of absorbed dose in a patient irradiated by beams of X or γ rays in radiotherapy procedures[S].USA,Washington DC:,1976.
[5]胡逸民.肿瘤放射物理学[M].北京:原子能出版社,1999:544-549.
[6]Mesbahi A,Nejad FS.Dose attenuation effect of hip prostheses in a 9 MV photon beam:commercial treatment planning system versus Monte Carlo calculations[J].Radiat Med,2007,25(10):529-535.
[7]倪昕晔,汤晓斌,刘云鹏,等.背向散射因子在放射治疗中的作用[J].辐射防护,2011,31(1):30 -34.
[8]Shimmin A, Beaulé PE, Campbell P. Metal-on-metalhip resurfacing arthroplasty[J].J Bone Joint Surg Am,2008,90(3):637-654.
[9]王亮,胡明,陈明钊,等.碳一钛组合式人工股骨头的应用前景[J].中国组织工程研究与临床康复,2009,22(13):4309-4312.
[10]Meier R,Schulz M,Krimmer H,et al.Proximal interphalangeal joint replacement with pyrolytic carbon prostheses[J].Oper Orthop Traumat,2007,19(1):1 -15.
[11]Montezuma SR,Loewenstein J,Scholz C,et al.Biocompatibility of materials implanted into the subretinal space of Yucatan pigs[J].Invest Ophthalmol Vis Sci,2006,47(8):3514 -3522.
[12]Meister K,Cobb A,Bentley G.Treatment of painful articular cartilage defects of the patella by carbon fibre Implants[J].J bone joint Surg Br,1998,80(6):965 -970.

