消乳散结胶囊提取工艺中芍药苷转移率探究
史亚军,唐志书,宋忠兴,杨明
消乳散结胶囊为国家药品监督管理局药品标准[WS-11331(ZD-1331)-2002]收载品种,处方由香附、全蝎、牡丹皮、柴胡、当归、玄参、白芍等 16 味药材组成,具有疏肝解郁,化痰散结,活血止痛之功效,临床用于肝郁气滞,痰瘀凝聚所致的乳腺增生,乳房胀痛等。原生产工艺是将香附、全蝎、牡丹皮 3 味粉碎成细粉;柴胡、当归、玄参、丹参、土贝母 5 味以 60%乙醇提取,其余白芍等加水提取后与前述两部分提取物混合制粒后制成胶囊。在生产过程中发现其芍药苷转移率较低,且质量标准中芍药苷的含量限度也很低,而芍药苷作为该制剂中明确的有效成分,其含量对疗效的发挥有着重要的作用。本文拟对其制备过程中各工序产物的芍药苷含量进行测定,从而寻找影响转移率的因素,为本品的进一步开发研究和提高质量标准做出有益探索,也为其他中成药的二次开发提供借鉴。
1 材料与方法
1.1 材料与仪器
Waters 600E 高效液相色谱仪、Waters 600 泵、Waters 2487 紫外检测器及 Millennium32 色谱工作站为美国Waters 公司产品;供试药材均由咸阳市药材公司提供,经陕西中医学院中药鉴定教研室胡本祥教授鉴定,均符合药典相关标准;乙腈为色谱纯;其他试剂均为分析纯;水为双蒸水;芍药苷对照品由中国药品生物制品检定所提供,批号为110736-200423。
1.2 方法
1.2.1 根据制备工艺获得各工序产物 处方中共有 16 味药材,按制备工艺,香附、全蝎、牡丹皮 3 味,粉碎成细粉,备用;柴胡、当归、玄参、丹参、土贝母 5 味,加 60%乙醇回流提取 2 次,每次 1.5 h,滤过,滤液减压回收乙醇,得清膏①备用;将白芍等 8 味药材加水煎煮 2 次,第1 次1.5 h,第2 次 1 h,滤过,合并为滤液②,减压浓缩至相对密度为1.08~1.10(60℃)的清膏③,加乙醇使含醇量达 50%,冷藏 24 h,滤过,得滤液④;滤液④减压回收乙醇,加入清膏①,并继续浓缩为相对密度 1.32~1.35(60℃)的稠膏⑤;减压干燥,粉碎,与牡丹皮等 3 味中药的细粉混匀,得干浸膏⑥;加入淀粉,混匀,装入胶囊,即得成品。
1.2.2 含量测定 高效液相法对白芍和牡丹皮药材中芍药苷含量进行测定,再分别测定水提取液②、清膏③、水提醇沉液④、醇提清膏①、水提醇沉清膏浓缩后所得稠膏⑤、与药材细粉混合后的干浸膏⑥和成品中芍药苷的含量。
1.2.2.1 色谱条件 色谱柱 Kromosil ODSC18(5 μm,4.6mm×200mm),乙腈:0.1%磷酸(11∶89)为流动相,检测波长为230 nm,柱温:室温。
1.2.2.2 对照品溶液的制备 取芍药苷对照品适量,加甲醇制成 0.062 mg/ml 的溶液,作为对照品。
1.2.2.3 供试品溶液的制备
⑴药材供试品溶液制备:取白芍和牡丹皮药材粉 0.1 g,精密称定,置 50 ml 容量瓶中,加稀乙醇35 ml,超声处理30min,放冷,加稀乙醇至刻度,摇匀,滤过,取续滤液作为供试品溶液。
⑵煎煮液(滤液②)、浓缩液(清膏③)、醇沉液(滤液④)、稠膏(⑤)供试品溶液的制备:精密吸取煎煮液 20 ml、清膏 2 ml、醇沉液 2 ml,精密称取稠膏 0.8 g,分别置 50 ml容量瓶中,各加稀乙醇 35 ml,超声处理 15min,放冷,加稀乙醇至刻度,摇匀,滤过,取续滤液作为供试品溶液。
⑶干浸膏(⑥)、成品供试品溶液的制备:精密称取干浸膏 0.5 g、胶囊内容物 0.9 g,分别置具塞锥形瓶中,各精密加甲醇 20 ml,密塞,称定重量,超声处理 30min,取出,放冷,再称定重量,用甲醇补足减失重量,摇匀,滤过,取续滤液作为供试品溶液。
1.2.2.4 标准曲线及线性范围 分别精密吸取对照品溶液(浓度 0.062 mg/ml)4、8、12、16、20 μl,按上述色谱条件测定峰面积,以峰面积对芍药苷含量进行回归,计算的回归方程为:A = 1894198C + 2975,相关系数 r = 0.9999,表明芍药苷在 0.248~1.240 μg 范围内线性关系良好。
1.2.2.5 方法学研究 按上述方法进行测定,精密度实验RSD 为1.56%,重复性实验 RSD 为1.10%,稳定性实验在 8 h 内其 RSD 为0.86%,芍药苷的平均回收率为98.36%、RSD 为1.07%,表明本方法精密度、重复性、稳定性和回收率均符合要求。
1.2.2.6 样品测定 分别精密吸取芍药苷对照品溶液10 μl、白芍、牡丹皮药材供试液 10 μl、煎煮液、浓缩液、醇沉液、稠膏供试品溶液 5 μl,干浸膏、成品供试品溶液10 μl,按 1.2.2.1色谱条件测定芍药苷含量。
2 结果
测定原料及各阶段产物中芍药苷含量,计算芍药苷在各工序的转移率,结果见表1。
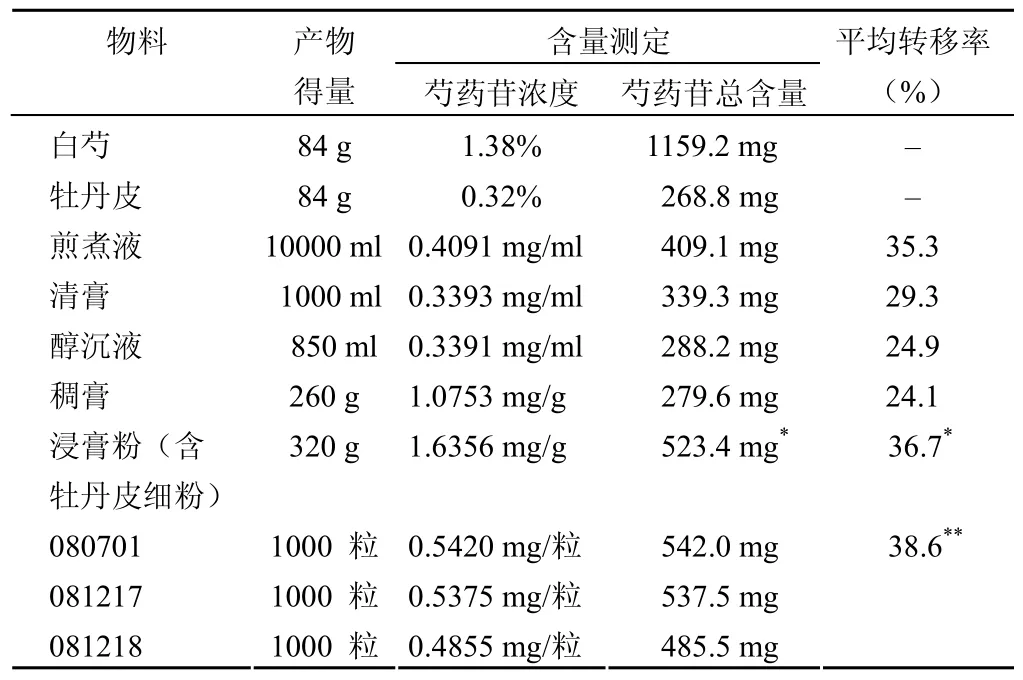
表1 样品中芍药苷含量测定及转移率结果(n = 3)
3 讨论
芍药苷在固体状态下受温度、时间的影响较小,但在溶液中稳定性较差,有研究表明其水溶液在 95℃保存3.5 d,结果含量较保温前下降了 60%[1],说明芍药苷对热的稳定性与含水率有关。在制剂生产过程中,芍药苷始终处于含水的状态下,而芍药苷本身结构中含有苯甲酸酯键,在有水的条件下受热易分解或受其他成分的干扰,从而含量降低。在本品制备工艺中白芍采用水煎煮提取,芍药苷的提取率为35.3%;浓缩至清膏时芍药苷仅保留原药材的 29.3%;醇沉并回收乙醇后芍药苷仅保留原药材的 24.9%;继续浓缩至稠膏时芍药苷仅保留原药材的 24.1%,加入牡丹皮细粉后,芍药苷含量增加了 87.2%,使得成品转移率为36.7%。数据分析结果提示,本品在制备过程中应尽可能采取减压低温提取浓缩干燥,并尽量缩短受热时间。
尽管成品中白芍提取转移率偏低(24%),但由于牡丹皮细粉的加入,使 3 批成品中芍药苷平均含量在0.5217 mg/粒。牡丹皮药材在 2005 版药典中并未规定芍药苷的含量,根据文献[2-3],牡丹皮来源广泛,其中芍药苷的含量差异较大,含量范围为0.2%~2.0%。牡丹皮由于粉碎后直接加入,转移率按照 90%计算,结合药典中白芍的最低含量和本实验研究结论,建议适当提高本品质量标准中的含量限度至 0.4 mg/粒(原标准为0.2 mg/粒)。
提取液、清膏、稠膏等液体物料在供试品制备时采用稀乙醇作为提取溶剂,是因为在进行工艺含量测定方法学研究时进行了回收率实验,实验结果表明,用甲醇稀释溶解时回收率无法达到要求(90%~110%),而用稀乙醇回收率较高,原因可能是甲醇的加入使提取液产生了较为严重的醇沉现象,沉淀过程中包裹部分芍药苷,通过超声也不能完全提取,因此采用稀乙醇作为提取溶剂,提取率符合要求。而在干浸膏和成品等固体进行含量测定时,采用了质量标准中的供试品制备方法,其回收率是符合要求的,且以甲醇为溶剂制备的供试品溶液的杂质峰较稀乙醇少,因此在固体样品供试品制备中采用了甲醇作为提取溶剂。
现代研究表明,芍药苷有一定降血糖、免疫调节和抗肿瘤作用[4],对消乳散结胶囊的功能主治有一定的支持作用,应该为本制剂的主要有效成分,因此应该尽可能提高其转移率以保证制剂疗效。目前在进行中成药二次开发的过程中,许多制剂的前处理对有效成分的转移率都有一定影响。现代中药制剂是在传统汤剂基础上发展起来的,传统汤剂煎煮后即可服用,且煎煮时间较短,并无纯化、浓缩、干燥等工序。而现代中药制剂提取时间较长,还要经历浓缩干燥等过程,对有效成分可能产生影响,使得多数中成药作用弱于汤剂。因此,在进行中药新药和现有中成药二次开发的过程中,应在尊重中药传统提取方法的基础上,充分考虑有效成分的转移率来进行工艺革新和改进。
[1]Yan XL, Zhang JJ, Li XY, et al.The content stability influence of temperature on paeoniflorin from radix paeoniae alba, adix paeoniae alba extract and Qianqingkun granule.Chin Traditional Herbal Drugs,2003, 34(2):131-133.(in Chinese)闫兴丽, 张建军, 李小燕, 等.温度对白芍药材、白芍提取物及乾坤清颗粒成品中芍药苷含量稳定性的影响.中草药, 2003,34(2):131- 133.
[2]Zhang LJ, Tu WQ, Qu LB, et al.Determination of paeonol and paeoniflorin in cortex moutan from various habitats by HPLC.J Xinyang Normal Univ (Nat Sciee Ed), 2007, 20(2):223-225, 251.(in Chinese)张留记, 屠万倩, 屈凌波, 等.不同产地牡丹皮中丹皮酚和芍药甙含量的 HPLC法测定.信阳师范学院学报(自然科学版), 2007,20(2):223-225, 251.
[3]Wang ZJ, Tang LY, He Y, et al.Determinat the paeoniflorin of cortex moutan by HPLC.Chin J Exp Traditional Med Formulae, 2006,12(8):12-13.(in Chinese)王祝举, 唐力英, 赫炎, 等.高效液相色谱法测定牡丹皮中芍药苷的含量.中国实验方剂学杂志, 2006, 12(8):12-13.
[4]Hu N, Xu HY, Chen ZW, et al.The advance of pharmacology research paeoniflorin.J Qiqihar Medl Coll, 2007, 28(9):1093-1095.(in Chinese)胡南, 许惠玉, 陈志伟, 等.芍药苷的药理学研究进展.齐齐哈尔医学院学报, 2007, 28(9):1093-1095.

