拟均相两段工艺氧化法制备双醛淀粉
刘晓庚,刘 峰,储著龙,李凤月,彭冬梅,孙 明,毕文柯,陈雨梦
拟均相两段工艺氧化法制备双醛淀粉
刘晓庚,刘 峰,储著龙,李凤月,彭冬梅,孙 明,毕文柯,陈雨梦
(南京财经大学食品科学与工程学院,江苏 南京 210003)
以绿豆淀粉为原料,NaIO4为氧化剂的拟均相两段工艺制备双醛淀粉(dialdehyde starch,DAS),考察预处理阶段中温度、酶处理、超声活化和氧化阶段中反应温度、反应时间、pH值、投料比、NaIO4浓度、淀粉乳浓度、相转移催化剂对制备双醛淀粉的影响,前段的预处理采用超声活化处理,后段的氧化工艺考察相转移催化剂的影响,并用正交法对制备双醛淀粉的工艺进行优化。结果表明:在以醛基含量为考察指标,预处理时不宜用酶,处理温度50~60℃,经30℃、40W、40kHz超声活化淀粉乳30min能有效提高淀粉与NaIO4的氧化反应活性,制得高醛基含量的DAS。相转移催化剂对提高产品醛基含量有一定作用。经正交试验优化得到的最佳条件为:以十六烷基三甲基氯化铵为相转移催化剂、反应时间2h、反应温度40℃、n(NaIO4):n(淀粉) =1.0:1.0、NaIO4浓度0.5mol/L、淀粉乳质量分数10%、体系pH2,在此条件下,制得的DAS双醛含量为96.81%。经光谱和理化性能等指标的检测证实所得的DAS与文献报道的DAS相符合。
淀粉;拟均相;NaIO4氧化;超声活化;相转移催化剂;制备;双醛淀粉
淀粉是目前世界上应用广且储藏量大的可食性碳水化合物,也是最为重要的食物或饲料资源。淀粉的改性研究历来是广大科技工作者关注的热点。双醛淀粉(dialdehyde starch,DAS)是一种含大量有效活性醛基的氧化变性淀粉,其主要结构是水合半醛醇和分子内及分子间的半缩醛,被认为是一种极具潜力和发展前途的生物基产品和重要的化工原料。由美国农业部北方研究所于上世纪50年代开发,很快规模化工业生产,目前仅日、美、欧发布的专利己近300件[1],且DAS应用领域不断拓展,至今DAS仍是世界淀粉研究的热点之一。我国DAS研发及应用工作起步虽晚,但发展迅速,已成为国际研究DAS的重要成员[2]。本课题组在调研的基础上[1-17],发现DAS的制备大多在30~50℃的非均相体系中完成[1,2,4-7,10],所制得的DAS醛基含量和活性受到限制,产品的应用也受到限制。拟均相能提高体系的分散性和反应的均匀性[10],超声活化能明显提高反应活性[11],本实验探讨超声活化拟均相两段法的氧化法制备DAS,旨在开发实用的DAS制备工艺,同时提高氧化反应速度及改善产品的性能。
1 材料与方法
1.1 材料、试剂与仪器
绿豆淀粉(经重铬酸钾氧化法[3]测得淀粉含量98.30%)山东金城股份有限公司;α-淀粉酶(酶活力3000~5000U)无锡酶制剂公司;高碘酸钠、聚乙二醇和硫酸等化学试剂均为分析纯或化学纯;实验用水为蒸馏水。
HH-2型恒温水浴锅 国华电器有限公司;2K-82A型真空干燥箱 上海实验仪器厂有限公司;KQ2200DB型数控超声器 昆山市超声仪器有限公司;UV-1102紫外-可见分光光度计 上海天美科学仪器有限公司;Nicolet 5700 FT红外光谱仪 美国Thermo Electron 公司;BS224S电子分析天平 北京赛多利斯仪器系统有限公司;XP-700E偏光显微镜;WZZ-2B型自动旋光仪;PHS-3C型pH计;NDJ-79型旋转黏度计;反应装置按文献[4]自制。
1.2 方法
1.2.1 双醛淀粉的制备
用NaIO4与淀粉反应,淀粉分子中葡萄糖单体的C2和C3碳原子上的羟基可选择性地被IO4-氧化成醛基使环形分子开裂。其反应式为:

取一定量淀粉放入准备好的蒸馏水,在搅拌下加入一定量淀粉酶,于50~60℃水浴振荡器中恒温一段时间使其成乳液后冷却,即得拟均相淀粉,然后于(30±5)℃、40W、40kHz条件下超声活化15~30min;将50.0mL一定浓度的NaIO4置于按文献[4]搭装的反应器中,搅拌后加0.1mol/L H2SO4调节溶液pH值,然后将配制好的淀粉乳液连续滴加到反应器,在一定的温度条件下反应;反应结束后,将混合物抽滤,滤饼用水反复洗涤至无I离子(用AgNO3检测),再用丙酮洗涤数次,以防止干燥后结块;真空干燥至质量恒定,得白色双醛淀粉,取样分析醛基含量。滤液和洗液合并后送至电解装置,氧化回收I。以产物中醛基含量为考察指标,考察各因素对制备过程的影响。
1.2.2 双醛淀粉的检测
1.2.2.1 IR和UV光谱测定
用KBr压片法于红外光谱仪上分别测得原淀粉和两种(超声活化和未经超声活化)自制DAS的IR谱图。用20℃条件下的原淀粉和两种自制DAS饱和水溶液于紫外-可见分光光度计上测得其UV光谱图(以蒸馏水为空白)。
1.2.2.2 双醛淀粉中醛基测定
双醛淀粉中醛基的测定采用文献[5]中碱消耗法测定。
1.2.2.3 碘酸和高碘酸测定
HIO4与淀粉反应后,其产物中碘酸和高碘酸含量,用依次滴定法进行分析测定[6]。
1.2.2.4 其他指标测定
DAS的偏光性用偏光显微镜观测;旋光性用自动旋光仪测定;pH值采用pH计测定;黏度用旋转黏度仪测定;DAS与I2的反应性、糊化度和外观的测定按文献[7]的方法进行,溶胀度、溶解性分别按文献[8-9]方法进行。
2 结果与分析
2.1 双醛淀粉的制备
2.1.1 预处理阶段的影响及其分析
为使反应进行得快速又彻底,要对淀粉进行预处理以使其尽可能均匀分散于反应体系中达到拟均相体系。谭义秋等[10]采用机械活化拟均相法,本课题组在总结文献[10]研究的基础上探讨了α-淀粉酶、唾液酶的预处理实验,以及根据超声活化原理[11]设计超声活化预处理实验,结果是酶处理对提高产物DAS中的醛基含量几乎无贡献,反而使醛含量下降和出现5%左右的羧基。原因可能是在酶作用下部分淀粉降解为单糖或双糖,而这样的糖易氧化成酸,因此,不宜采用酶预处理。但据文献[12-13]报道,酶法或酶-化学法在低温短时氧化下能制得低黏度高黏结力的氧化淀粉。然而超声活化对提高产物DAS中的醛基含量却有明显促进作用,实验得到的最佳结果表明:在前期预处理温度不超过其糊化温度时(实验测得以50~60℃为宜)振荡约1h,然后于(30± 5)℃、40W、40kHz条件下超声活化15~30min,能使DAS的醛基含量提高15%~20%,而且稳定性好。
2.1.2 氧化阶段的影响及其分析
2.1.2.1 反应温度的影响
固定其他条件,在温度为20、30、40、50℃和60℃时制备DAS,结果见图1。
从图1可知,在温度<40℃时,提高温度有助于提高产物中醛基含量,到40℃时达到最高,随后随着温度升高产物中醛基含量缓缓下降。原因主要是反应温度过高DAS的醛基会被过氧化成酸[14-15],另外淀粉在温度较高(>60℃)下会水解或糊化,导致被氧化成其他物质或难以氧化。但温度过低,难以得到醛基含量高的DAS,因此氧化反应温度以40℃为宜。
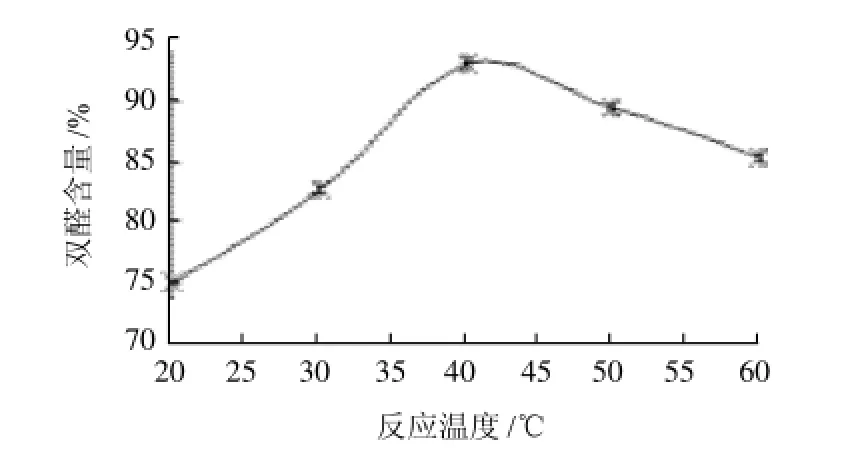
图1 反应温度对DAS醛基含量的影响Fig.1 Effect of reaction temperature on the content of aldehyde groups in DAS
2.1.2.2 pH值的影响
固定其他条件,在反应pH值分别为1.0、1.5、2.0、3.0、4.0和6.0时制备DAS,结果见图2。
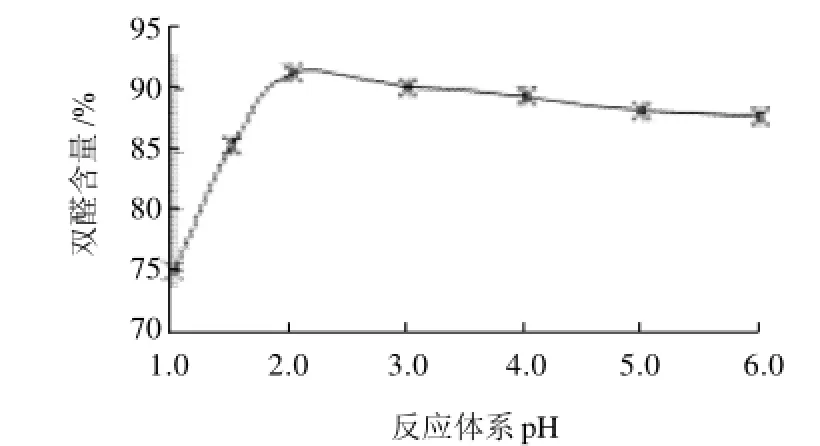
图2 pH值对DAS醛基含量的影响Fig.2 Effect of pH on the content of aldehyde groups in DAS
从图2可知,在pH<2时,醛基含量随pH值增大而迅速增加,至pH2时达到最大,随后醛基含量随pH值增大而缓降。原因是在高酸性或高碱性下,DAS分子内或分子间的醛基与羟基发生缩醛或半缩醛交联反应程度大大增强,使醛基含量降低;另外氧化剂在高酸性或高碱性下的氧化能力和氧化效果均变差。因此控制pH值为2。
2.1.2.3 反应时间的影响
其他条件固定,反应体系的反应时间分别为0.5、1.0、2.0、3.0h和4.0h时制备DAS,结果见图3。由图3可以看出,反应时间在0.5~2.0h,产物中醛基含量增幅较大,随后醛基含量基本趋于稳定。原因是随反应的进行,反应物逐渐减少,生成物不断增加,所以产物中醛基增加,而当反应接近或达到平衡时,生成物几乎不再增加,因此醛基含量趋于稳定不变。因此反应时间控制为2.0h。

图3 反应时间对DAS醛基含量的影响Fig.3 Effect of reaction time on the content of aldehyde groups in DAS
2.1.2.4 投料比的影响
其他条件固定,控制NaIO4与淀粉的物质的量的比值分别为0.8:1.0、0.9:1.0、1.0:1.0、1.1:1.0、1.2:1.0时制备DAS,结果见图4。
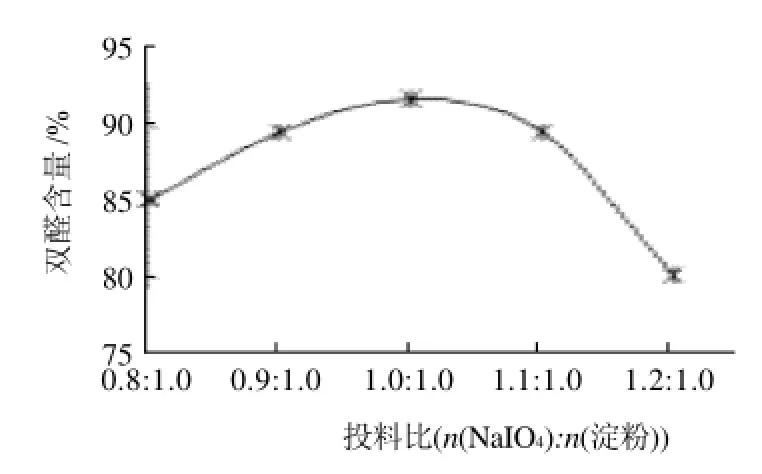
图4 投料比对DAS醛基含量的影响Fig.4 Effect of NaIO4/starch ratio on the content of aldehyde groups in DAS
从图4可以看出,n(NaIO4):n(淀粉)≤1时,随比值增大有利于DAS醛基含量提高;当n(NaIO4):n(淀粉)>1时,再增加n(NaIO4):n(淀粉)比值,会使醛基含量降低。原因是实验中固定反应体系溶液总体积,随n(NaIO4):n(淀粉)值的增大,NaIO4浓度提高,而NaIO4浓度最佳在0.4~0.6mol/L[16],浓度过高会使醛基过度氧化成羧酸,过低又会氧化不完全。所以应控制n(NaIO4): n(淀粉)=1.0:1.0。另外,淀粉乳的质量分数对DAS醛基含量也有影响,通过实验,结果表明淀粉乳质量分数以10%为宜,这与文献[17]的结果相一致。
2.1.2.5 相转移催化剂的影响
在其他条件固定,于反应的淀粉乳液中加入一定量的相转移催化剂,然后滴加NaIO4制备DAS,实验结果见图5。
由图5可知,在考察的十二烷基三甲基氯化铵、十二烷基三甲基溴化铵、十六烷基三甲基氯化铵3种季铵盐型和聚醚型的聚乙二醇(相对分子质量600~4000)的相转移催化剂中,季铵盐型的催化效果优于聚醚型的聚乙二醇(600~4000),而且季铵盐型的催化效果顺序是十六烷基三甲基氯化铵>十二烷基三甲基氯化铵>十二烷基三甲基溴化铵。因此实验选用十六烷基三甲基氯化铵为相转移催化剂,用量为0.015~0.040mol/L。另外,用未预处理的淀粉以十六烷基三甲基氯化铵为相转移催化剂制得的DAS醛基含量低于90%。
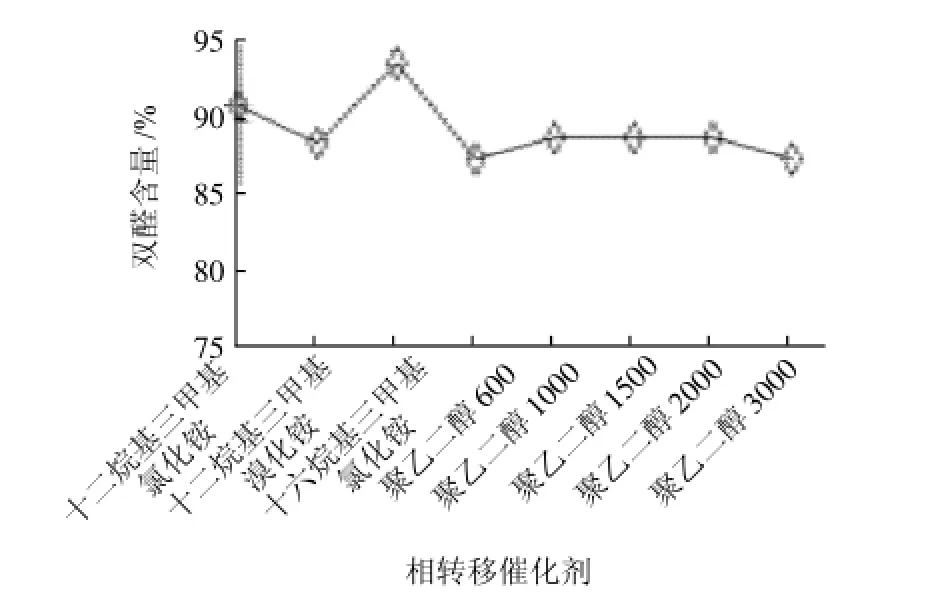
图5 相转移催化剂的影响Fig.5 Effect of phase transfer catalyst on the content of aldehyde groups in DAS
2.1.3 氧化反应工艺条件优化正交试验

表1 氧化反应制备DAS工艺条件L9(34)正交试验因素及水平Table 1 Factors and levels in orthogonal array design
根据单因素试验结果,固定反应液的体积(250mL)设计四因素三水平正交优化试验。因素水平见表1,按1.2.1 节方法进行DAS制备,正交试验结果见表2。

表2 正交试验结果Table 2 Results of orthogonal array design expriments
由表2极差分析可知,各因素对产物双醛含量的影响大小为B>A>C>D,即反应温度>反应时间>pH值>n(NaIO4):n(淀粉),可见反应温度影响最大,n(NaIO4):n(淀粉)的影响最小;最佳条件为反应温度40℃、反应时间2h、pH2、n(NaIO4):n(淀粉)=1.0:1.0。
2.1.4 最优组合验证实验
在最佳条件A1B2C1D2进行DAS制备实验,结果DAS中双醛含量为96.81%,与优化理论(Y优=Y平均+w1,优+w2,优+w3,优+w4,优)计算值Y优=97.87%相一致,说明本实验设计科学可靠。
2.2 DAS产品质量的检测
2.2.1 光谱测定
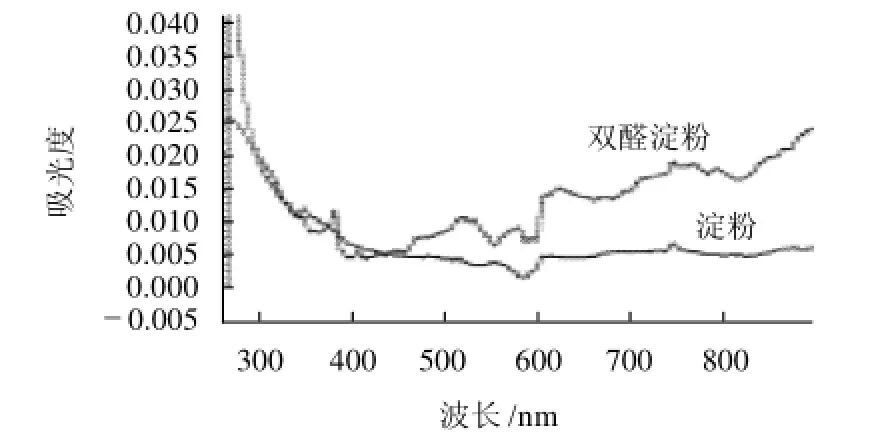
图6 原淀粉和自制双醛淀粉的紫外可见光谱图Fig.6 UV-Vis spectra of native starch and DAS
由图6 UV吸收光谱实验结果表明:原淀粉与DAS的图谱在同一波长下,自制DAS的吸收明显较原淀粉大,原因是DAS在冷水中的溶解度远大于原淀粉;原淀粉与自制DAS的UV吸收光谱最大区别是在波长550~600nm,原料淀粉呈凹形且吸收谷在580nm处吸收最小,而DAS则呈凸形且吸收峰在580nm处吸收最大。这一结果与来国莉等[18]的报道一致。说明所制产品为双醛淀粉。

图7 原淀粉和自制双醛淀粉的红外光谱图Fig.7 Infrared spectra of native starch and DAS
由图7可知,由于淀粉被氧化后,在淀粉糖环上的C2、C3处形成了双醛,所以DAS中除了保留在3431cm-1处—OH伸缩振动宽强吸收峰、2936cm-1处出现明显的饱和烃C—H伸缩振动吸收峰及990~1160cm-1处的C—O伸缩振动吸收带等淀粉特征峰外,还在1722cm-1处出现了醛基的C=O特征吸收峰,而在1160cm-1处羟基的C—O吸收峰都减弱;另外,由于被超声活化后的氧化度更高,因此超声活化制备的DAS在1722cm-1处的C=O和1160cm-1处的C—O吸收峰比未经超声活化制备的DAS更强。可见超声活化对NaIO4氧化法制DAS有促进作用。

表3 DAS品质质量的检测结果Table 3 Evaluation results of DAS quality
2.2.2 DAS的质量检测
从表3可知,所得的DAS产品的质量指标与文献报道值是相符的,同时还可以看出DAS的性能与原料淀粉发生了巨大变化,这从一个侧面进一步说明所制得的产品为DAS。
3 结论与讨论
用拟均相两段工艺的NaIO4氧化绿豆淀粉制备DAS可行,但前段的预处理不宜用酶,而用超声活化效果较好,预处理温度为50~60℃,这样既易得到分散均匀的淀粉乳,又不分解破坏淀粉。
实验得到温度30℃超声活化30min能非常有效地提高淀粉与NaIO4的氧化反应活性,可在较短时间内制备高醛基含量的DAS。其原因是超声空化作用破坏了淀粉紧密的颗粒表面及结晶结构,产生晶格缺陷,结晶度下降,削弱了氢键结合力,激活了活性基团,使反应活化点增多,同时也减弱了反应试剂的内扩散阻力,提高传质速率,促使氧化剂能顺利渗透到淀粉团粒内部参与反应。
后段的氧化工艺考察了相转移催化剂对DAS制备的影响,经试验得到十六烷基三甲基氯化铵为相转移催化剂有良好效果。经试验优化得到的最佳条件为以十六烷基三甲基氯化铵为相转移催化剂、反应时间2h、反应温度40℃、n(NaIO4):n(淀粉)=1.0:1.0、NaIO4浓度0.5mol/L、淀粉乳的质量分数10%、体系pH2,在此条件下制得的DAS双醛含量96.81%。反应所制得产品经UV和IR光谱测定具有醛基的特征,而且经外观、偏光性、与I2的反应性、黏度和溶解性等的检测结果也证实其与文献报道的DAS的性能指标相一致,所以所制备的确实是DAS。
由于十六烷基三甲基氯化铵会对HIO4的电解再生回收循环利用有一定的不良影响,因此对HIO4的电解再生回收循环利用方法的改进有待进一步研究。另外,如何使DAS的制备能保持优越的重现性和稳定性,也值得进一步研究。
[1]殷强峰. 双醛淀粉Schiff碱衍生物的合成与应用[D]. 大连: 大连理工大学, 2008.
[2]YU Jiugao, CHANG P R, MA Xiaofei. The preparation and properties of dialdehyde starch and thermoplastic dialdehyde starch[J]. Carbohydrate Polymers, 2010, 79(2): 296-300.
[3]黄本立, 程兰英. 重铬酸钾氧化法快速测定淀粉的初步研究: 一[J].食品工业科技, 1984(1): 7-12.
[4]蓝平, 廖安平, 谢涛, 等. 高碘酸氧化木薯淀粉制备双醛淀粉的研究[J]. 广西民族学院学报: 自然科学版, 2002, 8(4): 33-35.
[5]任与伟, 翟丽霞. 双醛淀粉的制备与含量测定[J]. 中国医院药学杂志, 1983, 3(10): 24-25.
[6]魏健美, 陈建新, 赵崇涛, 等. 碘酸与高碘酸依次测定法的研究[J].福建师范大学学报: 自然科学版, 1994, 10(3): 59-63.
[7]张友松. 变性淀粉生产与应用手册[M]. 北京: 中国轻工业出版社, 1999.
[8]GB/T 14797.3—2008 浓缩天然胶乳: 硫化胶乳: 溶胀度的测定[S].
[9]国家药典委员会. 中华人民共和国药典: 二部[S]. 2010版. 北京: 中国医药科技出版社, 2010.
[10]谭义秋, 黄祖强, 农克良. 机械活化木薯淀粉制备双醛淀粉的研究[J]. 精细化工, 2010, 27(3): 273-279.
[11]刘晓庚. 超声化学及其在粮油食品工业中应用[J]. 粮食与油脂, 2001 (7): 9-11.
[12]任便利, 陈均志, 叶林宇. 酶-化学法制取氧化淀粉[J]. 粮食与饲料工业, 2005(11): 21-22.
[13]曾洁, 高海燕, 李新华. 酶解对氧化淀粉应用性质的影响[J]. 食品工业科技, 2003, 24(12): 29-31.
[14]SLOAN J W, HOFREITER B T, MELLIES R T, et al. Properties of periodate oxidized starch[J]. Industrial and Engineering Chem, 1956, 48 (7): 1165-1172.
[15]ANDERSON D M W, GREENWOOD C T, HIRST E J. Physicochemical studies on starch. PartⅡ. The oxidation of starches by potassium metaperiodate[J]. J Chem Soc, 1955, 74: 225-231.
[16]柯伟, 陈宇春. 甘薯淀粉制备双醛淀粉的试验[J]. 福建林业科技, 1997, 24(2): 94-96.
[17]蓝平, 蓝丽红, 廖安平, 等. 高碘酸钠氧化木薯淀粉制备双醛淀粉工艺研究[J]. 食品工业, 2008(6): 23-25.
[18]来国莉, 付丽红, 于乐山. 亚硫酸品红分光光度法测定双醛淀粉含量的研究[J]. 中国皮革, 2006, 35(7): 13-16.
Preparation of Dialdehyde Starch by Homogeneous Oxidation
LIU Xiao-geng,LIU Feng,CHU Zhu-long,LI Feng-yue,PEN Dong-mei,SUN Ming,BI Wen-ke,CHEN Yu-meng
(College of Food Science and Engineering, Nanjing University of Finance and Economics, Nanjing 210003, China)
The preparation of dialdehyde starch (DAS) from mung bean starch was achieved by homogeneous sodium periodate oxidation. The effects of pre-treatment temperature, enzymatic treatment, ultrasonic activation in the pre-treatment stage and reaction temperature, reaction time, pH, sodium periodate/starch ratio and phase transfer catalysts in the oxidation stage on the preparation of dialdehyde were investigated. Ultrasonic activation and phase transfer catalysis were first studied in this study. Orthogonal test was applied to explore the optimal preparation conditions of DAS. Results indicated that ultrasonic activation of starch at 30 ℃ for 30 min was beneficial to improve reaction activation and the application of enzyme was not suitable in the pre-treatment stage. The optimal pre-treatment temperature was 50-60 ℃. In addition, phase transfer catalysis was also beneficial to improve the content of aldehyde group in final products. The optimal experiment conditions were cetyltrimethyl ammonium chloride (CETAC) as the phase transfer catalyst, reaction temperature of 40 ℃, reaction time of 2 h, pH 2, NaIO4/starch ratio of 1.0:1.0, NaIO4 concentration of 0.5 mol/L, and starch concentration of 10%. The obtained final products were white and the content of aldehyde group in final products was up to 96.81%. The spectral and physicochemical properties of DAS were consistent with previous reports.
starch;homogeneous;NaIO4oxidation;ultrasonic activation;phase transfer catalyst;preparation;dialdehyde starch
TS236.9
A
1002-6630(2011)04-0049-05
2010-07-18
刘晓庚(1962—),男,教授,硕士,研究方向为食品化学和应用化学。E-mail:lxg_6288@163.com

